إمكانية الوصول إلى الكروماتين وتعبير MicroRNA في الخلايا السلفية النيفرون أثناء نمو الكلى
Mar 11, 2022
لمزيد من المعلومات: ali.ma@wecistanche.com
أندرو كلوجستون1,2,3، أندرو بودنار2,3، ديبورا مالطا سيركويرا2,3يو لينغ فوا2,5,6، أليسا لولر8,9,10كريستي بوغز7أندرياس بفينينج8,10جاكلين هو2,3*ودينيس كوستكا1,4*
1قسم علم الأحياء التنموي ، كلية الطب بجامعة بيتسبرغ ، بيتسبرغ ، بنسلفانيا ، الولايات المتحدة الأمريكية2مركز أبحاث رانجوس ، مستشفى UPMC للأطفال في بيتسبرغ ، بيتسبرغ ، بنسلفانيا ، الولايات المتحدة الأمريكية3قسم طب الأطفال ، قسم أمراض الكلى ، كلية الطب بجامعة بيتسبرغ ، بنسلفانيا ، الولايات المتحدة الأمريكية4قسم علم الأحياء والأنظمة الحاسوبية ومركز بيتسبرغ للبيولوجيا التطورية والطب ، كلية الطب بجامعة بيتسبرغ ، بيتسبرغ ، بنسلفانيا ، الولايات المتحدة الأمريكية5قسم الطب الوراثي والجيني ، قسم طب الأطفال ، مستشفى UPMC للأطفال في بيتسبرغ ، بيتسبرغ ، بنسلفانيا ، الولايات المتحدة الأمريكية6قسم علم الأمراض ، مختبر الوراثة البيوكيميائية السريرية ، مستشفى UPMC للأطفال في بيتسبرغ ، بيتسبرغ ، بنسلفانيا ، الولايات المتحدة الأمريكية7قسم طب الأطفال ، قسم أمراض الجهاز الهضمي والكبد والتغذية ، كلية الطب بجامعة بيتسبرغ ، بيتسبرغ ، بنسلفانيا ، الولايات المتحدة الأمريكية.8علم الأحياء الحسابي،9العلوم البيولوجية ، و10معهد علم الأعصاب ، جامعة كارنيجي ميلون ، بيتسبرغ ، بنسلفانيا ، الولايات المتحدة الأمريكية
الملخص
تنشأ نيفرون الثدييات من عدد سكانخلايا سلف النيفرون، والتغييرات في نسخ هذه الخلايا تساهم في وقف تكوّن الكلية ، وهو محدد مهم لعدد النيفرون. لتوصيف تعبير microRNA (ميرنا) وتحديد المناطق التنظيمية المفترضة لرابطة الدول المستقلة ، قمنا بجمع خلايا سلف النيفرون من الماوسالكلىفي اليوم الجنيني 14.5 واليوم صفر بعد الولادة ومعايرة تعبير RNA الصغير والكروماتين الذي يمكن الوصول إليه عبر transposase. اكتشفنا تعبيرًا عن 1،104 miRNA (114 مع تغييرات التعبير) ، و 46374 منطقة يمكن الوصول إليها من الكروماتين (2،103 مع تغييرات يتعذر الوصول إليها). على مستوى الجينوم ، تسلط بياناتنا الضوء على عمليات مثل التمايز الخلوي ، وترحيل الخلايا ، وتفاعلات المصفوفة خارج الخلية ، ومسارات الإشارات التنموية. علاوة على ذلك ، قاموا بتحديد العناصر التنظيمية الجديدة المرشحة لرابطة الدول المستقلة لـ Eya1 و Pax8 ، وكلاهما من الجينات له دور في تمايز الخلايا السلفية النيفرون. أخيرًا ، نربط miRNAs المتغيرة للتعبير ، بما في ذلك let -7-5 p و miR -125 b -5 p و miR -181 a -2-3 p و miR {{ 20}} p ، مع عناصر تنظيمية رابطة الدول المستقلة المرشحة والجينات المستهدفة. تسلط هذه التحليلات الضوء على مواضع تنظيمية جديدة مفترضة لـ mRNA في أسلاف النيفرون.
مقدمة
الوحدة الوظيفيةالكلىهو النيفرون ، الذي يعمل على تصفية الفضلات والحفاظ على التوازن الطبيعي للماء والقاعدة الحمضية والإلكتروليتات في الجسم. يختلف عدد النيفرون بشكل كبير في البشر (عادةً ما بين مائتي ألف وأكثر من مليون نيفرون (Hughson et al. ، 2003)) ويتم إنشاؤه قبل الولادة في البشر (تقريبًا يوم ما بعد الولادة 2-3 في الفئران (Hartman et al. ، 2007 ؛ Hinchliffe وآخرون ، 1991)). لا يمكن أن تتجدد النيفرون بعد الولادة ، ويرتبط انخفاض منح النيفرون بزيادة خطر الإصابة بأمراض الكلى المزمنة وارتفاع ضغط الدم (بيرترام وآخرون ، 2011). يتم تحديد عدد النيفرون ، بدوره ، إلى حد كبير من خلال مجموعة من الخلايا تسمىخلايا سلف النيفرون(سيبريان وآخرون ، 2014 ب). في المراحل الأخيرة منالكلىفي التطور ، تزيد أسلاف النيفرون من ميلهم إلى التمايز ، مما يؤدي إلى استنفاد سكانهم تدريجيًا ويمثل التوقف النهائي لتكوين الكلية (Hartman et al. ، 2007 ؛ Rumballe et al. ، 2011 ؛ Volovelsky et al. ، 2018). إن فهم الآليات التي تنظم وقف تكوّن الكلية له آثار مهمة على تحديد موهبة النيفرون وخطر الإصابة بأمراض الكلى اللاحقة.
أثناءالكلىالتنمية ، التجديد الذاتي Cited1 plus / Six2 plus nephron يتم تحفيزها لتصبح أولية مذكورة 1- / Six2 plus ، ثم تفرق في Wnt 4- معبرة عن الحويصلات الكلوية استجابة لـ Wnt9b / -catenin (McMahon وآخرون ، 2016 ؛ Rumballe وآخرون ، 2011). تتضمن التغييرات النسخية الجوهرية في أسلاف النيفرون المبكرة مقابل المتأخرة الجينات والمسارات التي تؤثر على شيخوخة الخلايا الجذعية ، على وجه الخصوص ، mTor وهامارتين القامع (S. Chen et al. ، 2015 ؛ Volovelsky et al. ، 2018). في الواقع ، يُعتقد أن هامارتين يزيل حساسية أسلاف النيفرون لإشارات التجديد الذاتي ، وبهذه الطريقة يساهم في وقف تكوّن الكلية (S. Chen et al.، 2015). بما يتفق مع الفكرة القائلة بأن أسلاف النيفرون الأوائل لديهم ميل أكبر للتجديد الذاتي ، فإن الملاحظة التي تفيد بأن إمكانية الوصول إلى الكروماتين يتم إثرائها لمواقع الربط لعوامل نسخ خلايا سلف النيفرون الأساسية ، بما في ذلك Six2 و Wt1 عند مقارنتها بأسلاف النيفرون المتأخرة (Hilliard et al. ، 2019). وقد ثبت أن عوامل النسخ هذه تربط تسلسل المحسن الموجود في "النقاط الساخنة التنظيمية" في الجينوم (O'Brien et al. ، 2018). يحدث تحريض أسلاف النيفرون بسبب ارتفاع مستويات الكاتينين ، مما يؤدي إلى تنشيط مجمعات Lef1 / Tcf7 في الجينات المهيأة لتنشيط برنامج استحداث الكلية (Park et al. ، 2012) ، وقد تم اقتراحه على أنه معقد مع Tcf7l1 و Tcf7l2 لإنشاء وصيانة حلقات الكروماتين التنظيمية التي تسهل تنشيط الجينات (Guo et al. ، 2021).

انقر لمسحوق Cistanche tubulosa لعلاج أمراض الكلى
أوضحت الدراسات الحديثة أن الرنا الميكروي (ميرنا) في تنظيم وقف تكوّن الكلية. miRNA عبارة عن جزيئات RNA قصيرة غير مشفرة تستهدف نسخ messenger-RNA (mRNA) لتقليل الترجمة أو التدهور المعزز عبر مجمع الإسكات الناجم عن RNA (RISC) (Bartel ، 2009). يعتبر البروتين Lin28b مثبطًا معروفًا لعائلة Let -7 من miRNAs (Heo et al. ، 2008). ينخفض تعبير Lin28b في أسلاف النيفرون مع استمرار تكوّن الكلية ، ويتزامن هذا مع زيادة في التعبير عن عائلة -7 miRNA (Yermalovich et al. ، 2019). علاوة على ذلك ، ينتج عن الحث الشرطي لتعبير Lin28b في سلالة Wt 1- قمع let -7 miRNA ، وهو ما يكفي لإطالة تولد الكلية (Yermalovich et al.، 2019). من غير المعروف ما إذا كانت miRNAs الأخرى تنظم توقيت تكوين الكلية. بالإضافة إلى ذلك ، في حين تم تحديد المعززات التي تنظم تعبير الحمض النووي الريبي الطويل غير المشفر أثناء تكوّن الكلية (Nishikawa et al. ، 2019) ، لم يظهر أي منها لتنظيم تعبير ميرنا في أسلاف النيفرون.
في هذه الدراسة ، سعينا إلى تحديد ميرنا الجديد في وقت واحد والذي يساهم في وقف تكوّن الكلية ، جنبًا إلى جنب مع الميزات التنظيمية المحتملة لرابطة الدول المستقلة. لذلك ، لملاحظة التغييرات في تعبير miRNA وإمكانية الوصول إلى الكروماتين بين اليوم الجنيني 14.5 (E14.5) واليوم صفر بعد الولادة (P 0) ، أنتجنا مجموعات بيانات متطابقة mRNA-seq و ATAC-seq من أساسي وغير ممر.خلايا سلف النيفرونفي هاتين الفترتين. حددنا 114 miRNAs التي يتم التعبير عنها تفاضليًا فيخلايا سلف النيفرونبين هاتين النقطتين الزمنيتين ، بالإضافة إلى 2103 منطقة من إمكانية الوصول إلى الكروماتين المتغيرة والتي نطلق عليها المناطق التي يمكن الوصول إليها تفاضليًا (DARs). تشير تحليلات التخصيب للأهداف الجينية المتوقعة لتغيير الميرنا بشكل كبير وكذلك بين المواقع الجينومية لـ DARs إلى مسارات تؤثر على تمايز الخلايا الظهارية ، وترحيل الخلايا ، وتفاعلات المصفوفة خارج الخلية ، ومسارات الإشارات التنموية الرئيسية مثل إشارات Wnt و Notch و TGF- . نلاحظ تغييرات كبيرة في إمكانية الوصول في الكروماتين ونقدم خطوطًا متعددة من الأدلة التي تشير إلى تورط منطقتين جينوميتين كمعززات مفترضة للجينات Eya1 و Pax8 في خلايا سلف النيفرون. أخيرًا ، حددنا إمكانية الوصول المتسقة للكروماتين وتغييرات تعبير miRNA لـ 33 زوجًا من miRNAs و DARs ، بما في ذلك let -7-5 p، miR -125 b -5 p، miR -181 a { {11}} p و miR -9-3 p والجينات المستهدفة المفترضة المعبر عنها في أسلاف النيفرون لـ miRNAs المعبر عنها تفاضليًا.
نتائج
عزل مجموعات الخلايا السلفية للنيفرون من E14.5 و P 0الكلى
الخلايا السلفية النيفرونتم عزلها عن طريق الاختيار الإيجابي لـ Itg 8 عند E14.5 أو عند P 0 ، وتم تقسيم كل عينة لأداء mRNA-seq و ATAC-seq ومراقبة الجودة (الشكل التكميلي 1 AB). أكد PCR الكمي (qRT-PCR) أن جينات علامة السلف النيفرون Six2 و Cited1 (Huang et al. ، 2016) يتم التعبير عنها بشكل كبير في عينات السلف النيفرون المعزولة بالنسبة إلى الكلالكلى، أكثر من علامات أنواع الخلايا الأخرى (بما في ذلك برعم الحالب (كالب) (سيبريان وآخرون ، 2 {{1 {16}}} 14 أ) ، الخلايا البطانية (البقان) (كوباياشي وآخرون ، 2008) ، السدى الكلوي (Pdgfr) (S. Chen et al. ، 2015) والحويصلة الكلوية (Lhx1) (Brunskill وآخرون ، 2014) (الشكل التكميلي 1 C). فيما يتعلق بالجنس ، تراوحت القمامة المستخدمة لعينات E14.5 من 27 في المائة إلى 50 في المائة من الإناث ، وتراوحت المواليد لعينات P0 من 31 في المائة إلى 75 في المائة من الإناث. في المتوسط ، كانت عينات E14.5 من الإناث بنسبة 38 في المائة ، وعينات P0 كانت 49 في المائة من الإناث (الشكل التكميلي 1 د). سمحت لنا مجموعات الخلايا السلفية النيفرون المتطابقة بالتحليلإمكانية الوصول إلى الكروماتينوتعبير RNA الصغير في نفس مراحل التطوير عند نقطتين زمنيتين (E14.5 و P 0).
تمتلك أسلاف النيفرون المبكرة والمتأخرة ملفات تعريف نسخ ميرنا متميزة
اكتشف تسلسل الحمض النووي الريبي الصغير 1،1 0 4 نسخًا معروفة من miRNA وحدد 114 miRNAs التي تُظهر تغيرًا كبيرًا في التعبير بين عينات E14.5 و P {{1 0} (معدل الاكتشاف الخاطئ ( FDR)=0. 0 5 ؛ الجدول الإضافي 1). يُظهر نصف miRNA المعبر عنه تفاضليًا تعبيرًا متزايدًا عند P 0 مقارنةً بـ E14.5 ، ويبرز تحليل المكون الرئيسي تجانسًا أكبر في تعبير miRNA بين عينات E14.5 مقارنةً بـ P 0 (الشكل 1 أ). يكشف التجميع الهرمي عن مجموعة واضحة من miRNAs في تلك التي تزيد من وتناقص التعبير بين E14.5 و P 0 ، على التوالي (الشكل 1 ب). يعتبر أعضاء عائلة Let -7 من miRNAs من بين أكثر الكائنات المجهرية التي تم الكشف عنها بشكل كبير ، ونلاحظ أن جميع أفراد العائلة الذين لديهم تغييرات ملحوظة يظهرون تعبيرًا متزايدًا في P0 (البيانات غير معروضة). يتماشى هذا مع النتائج التي توضح أن تقليل تعبير Lin28b يؤدي إلى زيادة كبيرة في تعبير العائلة -7 على مدار عملية تكوّن الكلية (Yermalovich et al.، 2019). تشتمل miRNAs الأخرى ذات التعبير الأعلى بشكل ملحوظ عند P0 على miR -429-3 p ، أحد أفراد عائلة miR -200 المعروف بتأثيرها في تمايز خلايا podocyte (Z. Li et al. ، 2016) ، وكلاهما miR {{30 }} a -5 p and miR -125 b -5 p. من المعروف أن الاثنين الأخيرين يقمعان نصوص Lin28 في بيئات خلوية مختلفة (Chaudhuri et al. ، 2012 ؛ Potenza et al. ، 2017). تتضمن miRNA مع تعبير أقل بشكل ملحوظ في P0 تكوين الأوعية (S. Wang et al. ، 2008) وتعزيز الانتشار (Schober et al. ، 2014) miR -126.
تمكّن أداة DIANA miRPath من تحليل مسار KEGG لـ miRNA استنادًا إلى أهداف الجينات الخاصة بكل منها ، كما هو متوقع بواسطة micro T-CDS (Vlachos et al.، 2 0 15). نجد أن miRNA مع أكبر التغييرات في التعبير بين E14.5 و P 0 (لأعلى أو لأسفل) هي تلك التي تنظم المسارات ذات الأدوار الرئيسية في تكوين الكلية (الشكل 1C ، الشكل التكميلي 2). على سبيل المثال ، يتم إفراز Tgf- عن طريق الخلايا اللحمية المحيطة لتعزيز تمايز سلف النيفرون (Rowan et al.، 2 {{5 0}} 18) ، ونلاحظ انخفاض التعبير بين السلف النيفرون miRNA الذي يستهدف المؤثرات النهائية لـ "مسار إشارات TGF" (مسار KEGG mmu04350 ، قيمة p 1.45e - 6). يؤثر "مسار إشارات MAPK" (mmu04010) على تنظيم وتهيئة أسلاف النيفرون للتمايز ، وينظم تفاعلهم مع المصفوفة خارج الخلية (ECM) عبر Itg 8 (Ihermann-Hella et al. ، 2018). نلاحظ عددًا كبيرًا من miRNAs المنظمة لأعلى ولأسفل والتي تستهدف جينات مختلفة في مسار إشارات MAPK (قيم p 3.5e - 6 و 3.0 e - 4 للقوائم الأعلى والأسفل ، على التوالي) . أخيرًا ، يعد مسار KEGG "تفاعل مستقبل المصفوفة خارج الخلية (ECM)" (mmu04512) هو المسار الأكثر إثراءً الذي تم تحديده بشكل ملحوظ ، ويتم استهداف الجينات المكونة له بشكل أكبر بكثير بواسطة miRNA التي تزيد في التعبير بمرور الوقت (قيمة p 7.4e { {32}} بين زيادة miRNA مقابل 1.1e -2 بين المتناقصين). يتم استهداف الجينات المرتبطة بـ ECM بواسطة بعض الجينات الأكثر تعبيرًا عن جزيئات miRNA التي نكتشفها والتي تزيد بشكل ملحوظ ، بما في ذلك miR -196 a -5 p، miR -148 a -3 p، miR -125 -5 ص ، وليكن -7 و -5 ص. على وجه الخصوص ، فإن miR -196 a -5 p هي أعلى miRNA معبرًا عنه في عيناتنا ، وتلاحظ زيادة بمقدار 8- أضعاف بين E14.5 و P0. نصوص الجينات التي كانت الأهداف المتوقعة لـ miRNA (باستخدام TargetScan (Agarwal et al. ، 2015)) مع زيادة التعبير في P0 تشمل Bach2 ، وهو رابط جزيئي مقترح بين مسارات MAPK / AP1 و Six2 / -catenin للتجديد الذاتي والتمايز في أسلاف النيفرون ، على التوالي (Hilliard et al. ، 2019).
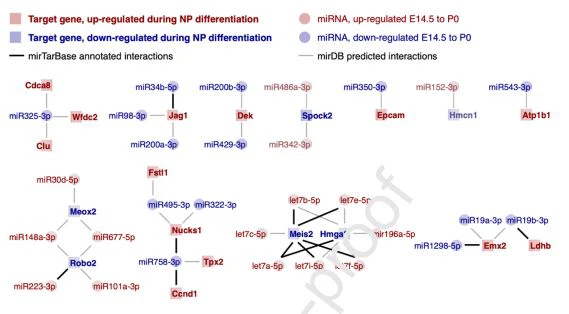
لتحديد الأهداف المفترضة لـ miRNAs المعبر عنها تفاضليًا في أسلاف النيفرون ، استخدمنا التعليقات التوضيحية الحسابية لـ miRNAs المتوفرة في miRDB (Y. Chen & Wang ، 2 0 20) ، وتفاعلات miRNA-mRNA التجريبية المشروحة من قاعدة الهاون (HY Huang et al. ، 2020) ، بالاقتران مع مجموعة بيانات تسلسل الحمض النووي الريبي أحادية الخلية E14.5 التي تم إنشاؤها مسبقًا (Bais et al. ، 2020). وهكذا ، أنشأنا قائمة بتفاعلات miRNA-mRNA المحتملة بناءً على التعبير التفاضلي للمير بين E14.5 و P0 في أسلاف النيفرون مع تغيير مناظر في التعبير الجيني المستهدف بين أسلاف النيفرون المُستعد للتجديد الذاتي ، وكذلك معبيًا و التفريق بين أسلاف النيفرون (الشكل 2). يشير تحليلنا إلى أن Meis2 و Hmga2 أهداف محتملة لعائلة let -7 من miRNAs في أسلاف النيفرون (الشكل 2) ، مع انخفاض التعبير عن Meis2 و Hmga2 المرتبط بزيادة التعبير عن أفراد عائلة let -7 في التمايز أو الشيخوخة أسلاف النيفرون. يتم التعبير عن عامل النسخ Meis2 بقوة في أسلاف النيفرون والسدى الكلوي أثناءالكلى(Lam et al.، 2014) ، ويرتبط بتنظيم تكاثر الخلايا في سياقات أخرى (Abruzzese et al. ، 2019). Hmga2 هو بروتين مرتبط بالكروماتين غير الهيستوني ، ويتم التعبير عنه بدرجة عالية في الخلايا الجذعية ، وقد ارتبط بمجموعة متنوعة من أورام اللحمة المتوسطة (Fusco & Fedele ، 2007 ؛ Lam et al. ، 2014). وبالمثل ، هناك زيادة في تعبير Jag1 مرتبط بتناقص تعبير miR -34 b -5 p و miR -983 p و miR -200 a -3 p في التفاضل أو أسلاف النيفرون الشيخوخة (الشكل 2). Jag1 هو رابط رئيسي في إشارات Notch يزداد تعبيره مع تمايز أسلاف النيفرون (Chung et al. ، 2016). جميع أهداف miRNA المتوقعة أو المشروحة للجينات مع تغيرات التعبير بين أسلاف النيفرون المتجدد ذاتيًا والمُفرق والمتفرق متاح في تكميلي.
الشكل 1. التغييرات الجوهرية في تعبير miRNA بين أسلاف النيفرون E14.5 و P 0. أ) يُظهر تحليل المكون الرئيسي أن النقطة الزمنية التنموية هي مساهم رئيسي في اختلاف تعبير ميرنا. ب) خريطة الحرارة تصور التعبير النسبي لجميع ميرنا المتغيرة بشكل كبير. الأعمدة التي تحتوي على عينات E14.5 على اليسار موضحة باللون الأخضر الفاتح ، والأعمدة التي تحتوي على نماذج P 0 على اليمين موضحة باللون الأخضر الداكن. ج) تخصيب الجينات من مسارات KEGG المحددة بين أهداف الجينات المتوقعة لميرنا المنظم لأعلى ولأسفل (الأشرطة الحمراء والزرقاء ، على التوالي). الحد الأدنى للقيمة الاحتمالية المضمنة هو 1e -5.

الشكل 2. تفاعلات ميرنا-مرنا مع دور محتمل في شيخوخة الخلايا السلفية النيفرون والتمايز. يتم عرض ميرنا (دوائر) ومرنا (المربعات). تظهر miRNAs مع زيادة التعبير بين E14.5 و P 0 باللون الأحمر ، وتظهر miRNAs التي تنخفض باللون الأزرق. الجينات المستهدفة المشروحة (من mirDB و mir TarBase) مع زيادة التعبير بين التجديد الذاتي أو التجهيز أو التمايزخلايا سلف النيفرون(Bais et al. ، 2020) باللون الأحمر ، mRNA مع انخفاض التعبير باللون الأزرق. تم حذف الحواف من mirDB و mirTarDB غير المتوافقة مع تغييرات التعبير المرصودة ولكن تم تضمينها في الجدول التكميلي 2.
تمتلك أسلاف النيفرون المبكرة والمتأخرة بيئات كروماتين مميزة
سمحت لنا بيانات ATAC-seq المأخوذة من أسلاف النيفرون E14.5 و P 0 بتحديد 46374 منطقة من الكروماتين الذي يمكن الوصول إليه (بمعدل اكتشاف غير قابل للاختزال (Boleu et al.، 2 0 15) عتبة {{ 22}}. 1 ، انظر (الشكل التكميلي 3 C ، الجدول التكميلي 3) ، مجتمعة عبر العينات والنقاط الزمنية. نلاحظ أن بياناتنا تتوافق مع إرشادات ATAC-seq لمشروع ENCODE (ENCODE ، nd) (الشكل التكميلي 3 أ ، B) وأننا نلاحظ زيادة معدلات الحفظ بين قمم IDR مما هو موضح في عناصر التحكم العشوائية (الشكل التكميلي 3 D). من بين IDRs التي أبلغنا عنها ، يحتوي 3576 على معززات موثقة في VISTA (Visel et al. ، 2007) و / أو FANTOM5 (de Rie et al. ، 2017) قواعد بيانات مُحسِّن ، و 13495 تحتوي على تسلسلات DNA مع أدوار تنظيمية متوقعة في أنسجة فأر أو نوع خلية واحد على الأقل وفقًا لـ EnhancerAtlas 2.0 (Gao & Qian ، 2020).
كشف تحليل المكون الرئيسي (المعدل للاختلافات بين الجنسين) عن تجميع واضح للعينات حسب النقطة الزمنية التنموية (الشكل 3 أ). لتحديد المواقع الجينية مع التغييرات في إمكانية الوصول إلى الكروماتين ، قمنا بمقارنة إشارة ATAC-seq بين عينات E14.5 و P 0. لاحظنا 2،1 0 3 DARs ، والتحكم في FDR بنسبة 1 0 في المائة. من بين هؤلاء 1323 (55 في المائة) أظهروا زيادة في إمكانية الوصول عند P0 مقارنة بـ E14.5 ، وكشف التجميع الهرمي عن تمييز واضح بين DARs التي تفتح وتغلق بين E14.5 و P0 ، على التوالي (الشكل 3 ب).
تم تحديد آثار أقدام عامل النسخ باستخدام HINT ومطابقتها مع بروتينات ربط الحمض النووي باستخدام أشكال من قاعدة بيانات HOCOMOCO 11 (Kulakovskiy et al. ، 2 0 18). من بين 431 نموذجًا تم اختبارها ، تظهر DARs التي تحتوي على آثار أقدام للعديد من بروتينات عامل النسخ المرتبطة بتكوين الكلية زيادة في إمكانية الوصول بين E14.5 و P 0. من بين آثار الأقدام الموجودة في DARs التي تزيد من إمكانية الوصول في المتوسط ، تنتمي الستة الأوائل إلى آثار أقدام عامل النسخ المتطابقة مع Pax8 ({{1 0}. 15) ، Six2 (0. 14) ، Cebpd (0. 13) ، ستة 4 (0. 13) ، يونيو (0.12) ، فوس (0.11). تتضمن آثار الأقدام الموضحة في DAR إغلاق عوامل النسخ E2F2 و E2F4 ، والتي من المعروف أنها تؤثر على تقدم دورة الخلية (Gaudet et al. ، 2011) وتعزز تكاثر الخلايا (D. Wang et al. ، 2000) في السياقات الخلوية الأخرى (الشكل التكميلي) 4).
لتقييم السياق البيولوجي لفتح وإغلاق DARs ، استخدمنا أداة إثراء المناطق الجينومية للتعليقات التوضيحية (GREAT) (McLean et al. ، 2010) لتسليط الضوء على مجموعات الجينات مع إثراء مناطق الكروماتين المتغيرة المرتبطة. باستخدام هذا النهج ، نحدد العمليات البيولوجية لعلم الجينات (GO) المرتبطة ارتباطًا وثيقًا بتطوير السلف النيفرون: على وجه الخصوص ، فإن العملية الأكثر إثراءً بين فتح DARs هي "تنظيم تمايز الخلايا الظهارية" (GO: 0030856 ، قيمة Q ذات الحدين {{3) }}. 5e -5) ، و "التنظيم الإيجابي لتمايز الخلايا الظهارية" (GO: 0030858 ، قيمة Q ذات الحدين=5 e -3) من بين أفضل 10 أكثر ثراءً ( الشكل التكميلي 5). كلاهما يتفق مع زيادة في ميل أسلاف النيفرون للخضوع للتحولات من اللحمة المتوسطة إلى الظهارية (MET) عندما يتمايزون (S. Chen et al. ، 2015). تشمل المسارات المخصّصة الأخرى "التنظيم الإيجابي لمسار إشارات الشق" (GO: 0045747 ، قيمة Q ذات الحدين=2 e -5) ، والتي تتوافق مع الدور الذي تلعبه إشارات Notch في تعزيز تمايز سلف النيفرون ( Chung et al. ، 2016). لم يكشف إغلاق 10،083 DARs الذي تم اكتشافه عن مصطلحات GO المهمة بناءً على معايير GREAT الافتراضية للأهمية (انظر الشكل التكميلي 5).
الشكل 3. الاختلافات في إمكانية الوصول إلى الكروماتين تميز E14.5 مقابل P 0خلايا سلف النيفرون.A) تحليل المكون الرئيسي لعينات ATAC-seq يسلط الضوء على النقاط الزمنية التطورية كمصدر رئيسي للتباين. ب) خريطة الحرارة تظهر تغيرات كبيرة في مناطق IDR عبر عينات ATAC-seq. تم وضع تعليقات توضيحية على عينات / أعمدة E14.5 باللون الأخضر الفاتح ، وتم توضيح عينات / أعمدة P 0 باللون الأخضر الداكن. ج) GO مصطلحات العملية البيولوجية المخصبة للمناطق الجينومية التي تفتح بين E14.5 و P 0 وفقًا لـ GREAT ، مرتبة حسب القيمة P ذات الحدين ، FDR أقل من أو يساوي 0. 001.

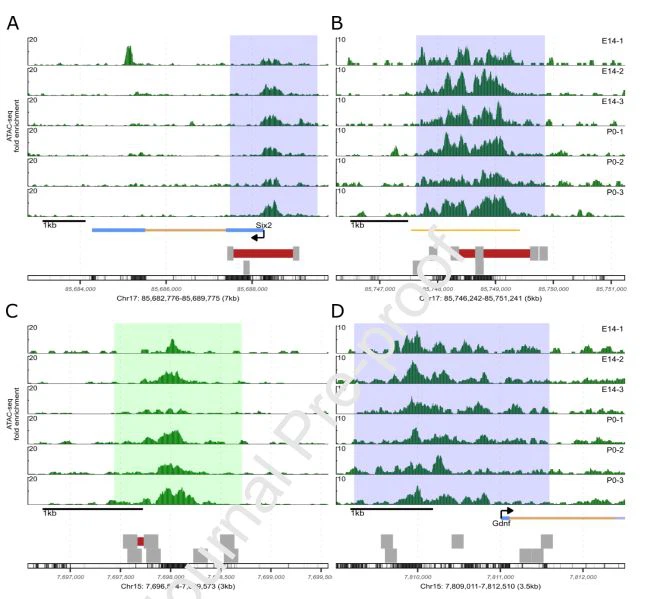
بعد ذلك ، استكشفناإمكانية الوصول إلى الكروماتينفي مناطق الجينوم التي تحتوي على محفزات ومعززات للجينات ذات الأدوار المنشورة في تمايز خلايا السلف النيفرون. من بين هؤلاء ، يعد عامل النسخ Six2 أمرًا بالغ الأهمية للحفاظ على تعدد القدراتخلايا سلف النيفرون(Self et al. ، 2006) ، وفي جميع العينات ، لاحظنا وجود كروماتين يمكن الوصول إليه يحيط بمحفزه ومُحسِّن Six2 معروف بحوالي 50 كيلو بايت من موقع بدء النسخ Six2 (TSS) (O'Brien et al. ، 2018) (الشكل 4 أ ، ب ، مناطق مظللة باللون الأزرق). نلاحظ أيضًا مناطق الكروماتين التي يمكن الوصول إليها على المروج والمحسن المنشور للبروتين Gdnf (الشكل 4D ، E) ، والذي يفرزه أسلاف النيفرون لتعزيز تفرّع برعم الحالب (Sanchez et al. ، 1996 ؛ Vega et al. ، 1996 ). يقع هذا المُحسِّن على حوالي 113 كيلو بايت في الجزء العلوي من محفز الجينات ومن المعروف أنه يستجيب لإشارات Wnt في سياق تطوير أسلاف النيفرون (Park et al. ، 2012). بينما لا يتغير مروج Gdnf بشكل كبير بمرور الوقت ، فإن المُحسِّن المشروح يزيد بشكل كبير من عدم إمكانية الوصول. نلاحظ أيضًا مناطق الكروماتين التي يمكن الوصول إليها والتي تحيط بمُحسِّن منشور نشط في أسلاف النيفرون لـ Eya1 التي تقع بحوالي 325 كيلو بايت في الجزء العلوي من TSS للجين (Park et al. ، 2012) (الشكل التكميلي 6). Eya1 هو عامل نسخ يتفاعل مع Six2 للحفاظ على تعدد القدرات في سلف النيفرون (J. Xu et al. ، 2014).
نلاحظ العديد من DARs التي لا تتداخل مع الميزات التنظيمية المعروفة ولكنها تشمل المناطق التي يُتوقع أن يكون لها نشاط مُحسِّن لجينات معينة في مجموعة متنوعة من أنواع خلايا الماوس كما هو موضح في EnhancerAtlas 2. 0 (Gao & Qian، 2020). بالإضافة إلى المُحسِّن المنشور لـ Eya1 (Park et al. ، 2012) (الشكل التكميلي 6) ، يشمل DAR الختامي في أحد إنترونات Eya1 (الشكل 5 أ-ب) منطقة يُتوقع أن يكون لها نشاط مُحسِّن على جين Eya1 في الماوس السلف العصبي والخلايا السلفية المحببة أحادية الخلية (Gao & Qian ، 2020). تماشياً مع انخفاض نشاط المُحسِّن ، لاحظنا سابقًا أن التعبير عن Eya1 قد انخفض في التمييز بين أسلاف النيفرون باستخدام بيانات E14.5 scRNA-seq (الشكل التكميلي 7) (Bais et al. ، 2020). يتوافق هذا مع بيانات ChIP-seq المنشورة في سلالات النيفرون الأولية E16.5 التي تظهر نقصًا في علامة المحسن النشط ، H3K27ac ، ونقص الارتباط من Ctnnb1 و Lef1 و Six2 و Tcf7 (الشكل 5) (Guo et al. . ، 2021). يحتوي هذا المُحسِّن المحتمل أيضًا على آثار أقدام لعامل النسخ لـ Hoxd10 في ذروته ، وهو عامل نسخ ضروري للتمييز والتكامل بين أسلاف النيفرون أثناء التحولات اللحمية إلى الظهارية (MET) (Yallowitz et al. ، 2011).
تتداخل DAR التي تزيد من عدم إمكانية الوصول إلى الكروموسوم 24 مع منطقة الكروماتين مع نشاط مُحسِّن متوقع لعامل النسخ Pax8 في الخلايا المستزرعة من كلى الفأر والظهارة المعوية والرحم (Gao & Qian، 2020). Pax8 زائدة جزئيًا عن Pax2 ، ولكن مطلوب واحد على الأقل من عاملي النسخ هذين في أسلاف النيفرون من أجلالكلىالتنمية (Bouchard et al.، 2002؛ Narlis et al.، 2007). لاحظنا سابقًا أن تعبير Pax8 يزيد في تمايز وتمايز أسلاف النيفرون (الشكل التكميلي 7) ، ونلاحظ زيادة كبيرة في إمكانية الوصول في DAR الذي يشمل هذه الميزة التنظيمية. ترتبط هذه المنطقة أيضًا بعلامة مُحسِّن نشطة ، H3K27ac ، وربط Ctnnb1 و Lef1 و Six2 و Tcf7 في بيانات ChIP-seq المنشورة من أسلاف النيفرون الأولية E16.5 (الشكل 5) (Guo et al. ، 2021). نلاحظ عددًا من آثار أقدام عامل النسخ التي تقع ضمن ذروة إمكانية الوصول المحفوظة للغاية في DAR ، بما في ذلك اثنتان لـ Sall1 ، وهو عامل نووي معروف بتأثيره على تكوين الكلية (Kanda et al. ، 2014) ، وسبعة آثار أقدام مجمعة بشكل وثيق لإصبع الزنك المرتبط بـ MYC بروتين (Maz) ، وهو عامل نسخ ثبت أن له تأثيرات تعتمد على الجرعةالكلىالتطور في البشر والفئران (Haller et al. ، 2018). يحتوي الجدول التكميلي 3 على قائمة كاملة بالمناطق التي يمكن الوصول إليها والتي نجدها بالإضافة إلى إحصائيات إمكانية الوصول التفاضلية الخاصة بها ، والتعليقات التوضيحية للجينات ، والإكسونات ، والمروجين التي تتداخل معها ، وقوائم آثار عامل النسخ المرتبطة بتكوين الكلية الرئيسية التي تم تحديدها.
الشكل 4. ملامح ATAC-seq في مواقع تنظيمية معروفة ومفترضة. لكل لوحة من أعلى إلى أسفل ، تشير الأوجه إلى إثراء أضعافإمكانية الوصول إلى الكروماتينفي عينات E14.5 و P 0 ، مع تحديد IDRs و DAR على أنهما تمييزات باللون الأزرق (IDR غير متغير) والأخضر (فتح DAR). والأحمر (إغلاق DAR). يصور الوجه التالي التعليقات التوضيحية الجينية والمواقع الجينية (باللون الرمادي) والمناطق الخالية من النوكليوزوم (باللون الأحمر) المقاسة في عينات مجمعة E14.5 و P 0 ، و PhastCon6 0 درجات الحفظ (يشير اللون الأسود إلى 1 {{ 12}} 0٪ حفظ ، أبيض 0٪ محفوظ أ) محفز وجسم جيني لعامل النسخ Six2. ب) مُحسِّن لـ Six2 تم نشره بواسطة Park et. آل. ج) مُحسِّن يمكن الوصول إليه تفاضليًا لـ Gdnf مع زيادة إمكانية الوصول عند P0. د) المروج لـ Gdnf.
الشكل 5. DARs تتداخل مع معززات جديدة محتملة للجينات المرتبطة بتكوين الكلية. A و C) تصور الألواح خريطة للمنطقة 1 ميغا بايت المحيطة بجين مهم ، مع جينات ترميز البروتين باللون الأخضر والتفاعل المُحسِّن / المروج المقترح كحلقة سوداء . B و D) من أعلى إلى أسفل ، تصور اللوحات إثراء أضعافإمكانية الوصول إلى الكروماتينتم القياس في عينات E14.5 و P 0 ، مع تمييز IDR باللون الأخضر (الفتح) والأحمر (الإغلاق) ، متبوعًا بقياسات ChIP-seq في هذه المناطق التي تم قياسها بواسطة Guo et. آل. في السلف النيفرون الأوليالخلايا(جو وآخرون ، 2 0 21). تصور اللوحة الثالثة التعليقات التوضيحية للجينات (باللون الأزرق) والعناصر التنظيمية المتوقعة من Enhancer Atlas 2.0 (باللون الأحمر) ، وتشير اللوحة الرابعة إلى آثار أقدام عامل النسخ المحددة في بيانات ATAC-seq. تُصوِّر اللوحة الخامسة النيوكليوسومات (باللون الرمادي) و NFRs (باللون الأحمر) ، وتشير اللوحة السفلية إلى الحفظ. أ) منطقة 1 ميغا بايت تحتوي على الجسم الجيني لـ Eya1 ومحسن Eya1 محتمل حوالي 325 كيلو بايت في المنبع. ب) منطقة 4.5 كيلو بايت تحتوي على محسن Eya1 المحتمل. ج) منطقة 1 ميجابايت تحتوي على موضع الجين Pax8 ومحسن متوقع. د) منطقة 4.5 كيلو بايت تحتوي على المُحسِّن المتوقع وتداخله DAR.

تساعد المجالات المرتبطة طوبولوجيًا في تحديد علاقات المُحسِّن المحتمل - علاقات ميرنا
المجالات المرتبطة طوبولوجيًا (TADs) هي مناطق على نطاق واسع من تنظيم الكروماتين عالي الترتيب الذي ينتج عن تعبئة الكروماتين في النواة في مساحة ثلاثية الأبعاد (Dixon et al. ، 2012) ، وتقتصر تفاعلات المحسن والمروج عادةً على عناصر داخل نفس TAD (Symmons et al. ، 2014). قمنا بتقريب TADs من أسلاف النيفرون باستخدام التعليقات التوضيحية الناتجة عن الخلايا الجذعية الجنينية للفأر (ESCs) (Y. Wang et al. ، 2018). لفحص مناطق تنظيم رابطة الدول المستقلة المحتملة لـ miRNA ، قمنا بربط التغييرات فيإمكانية الوصول إلى الكروماتينمع ميرنا المعبر عنه تفاضليًا داخل نفس TAD. بشكل عام ، توجد 42778 منطقة فريدة يمكن الوصول إليها (حوالي 92 بالمائة) داخل TADs المشروحة ، ومن هذه المناطق الثلاث 0 ، 626 (حوالي 72 بالمائة) لا تتداخل مع مروج معروف. وهذا يشمل 2103 سندات ، مع 1180 و 923 فتح وإغلاق بمرور الوقت ، على التوالي. تشترك خمسة عشر DARs افتتاحية في TAD مع واحد أو أكثر من miRNAs مع تعبير متزايد بين E14.5 و P0 ، وتسعة DARs إغلاق تشترك في TAD مع واحد أو أكثر من miRNA مع تعبير منخفض. يلخص الشكل 6 هذا النهج ويوضح المسافات بين DARs و miRNA المطابق لها ، والتي تتراوح من 27 كيلو بايت إلى أكثر من 1 ميجا بايت (المتوسط: 447 كيلو بايت). يوضح الجدول 1 مجموعات من العلاقات المحتملة بين DAR و miRNA ، مع قائمة DAR واحدة لكل ميرنا متطابق.
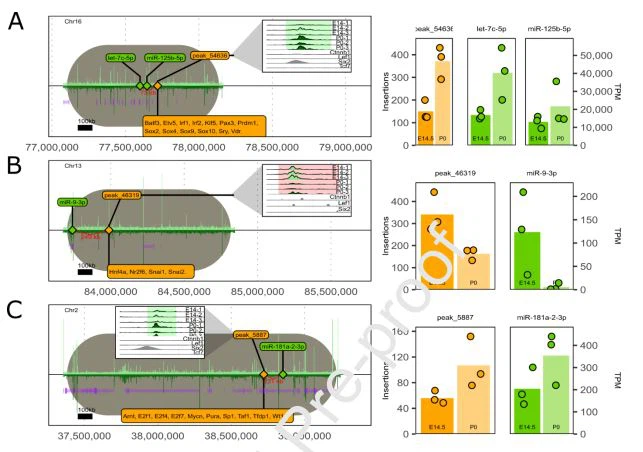
من بين أزواج مُحسِّن ميرنا المشروحة ، نلاحظ ثلاثة منها ذات أهمية خاصة. أولاً ، تم تحديد DAR الافتتاحي 120 كيلو بايت مع المصب من let -7 c -5 p و 73 كيلو بايت أسفل مجرى miR -125 b -5 p ، والذي يرتبط بـ Six2 موقع ملزم في مجموعة بيانات سلف النيفرون E16.5 المنشورة مسبقًا ChIP-seq (الشكل 7 أ) (Guo et al. ، 2021). لنفترض أن -7 c -5 p هي واحدة من أعظم ما نكتشفه -7 miRNAs ، ومن المعروف أيضًا أن عائلة let -7 تقمع Lin28btranscripts (Slack & Ruvkun، 1997 ؛ Zhu et al. ، 2011). نلاحظ أنه تم تحديد Hmga2 و Meis2 أيضًا كأهداف جديدة محتملة لعائلة Let -7 في أسلاف النيفرون (الشكل 2). تم أيضًا عرض miR -125 b -5 p لقمع نصوص Lin28 في أنواع الخلايا المكونة للدم والسلف (Chaudhuri et al. ، 2012). ثانيًا ، إن miR -9-3 p هو المكمل العكسي لـ miR -9-5 p ، وهو miRNA الذي ثبت مؤخرًا أنه يحمي منالكلىالتليف عن طريق استهداف المسارات الأيضية (Fierro ‐ Fernández et al.، 2 0 20). اكتشفنا انخفاضًا أكبر من 10- أضعاف في نصوص miR -9-3 بين أسلاف النيفرون E14.5 و P0 ، وقد حددنا عنصرًا تنظيميًا محتملاً على بعد حوالي 249 كيلوبايت (الشكل 7 ب). نلاحظ آثار أقدام عامل النسخ لـ Snai1 و Snai2 في DAR المرتبط ، والتي ثبت أنها تعزز التحولات الظهارية إلى اللحمة المتوسطة (EMT) (Sundararajan et al. ، 2019). أخيرًا ، قمنا بمطابقة miR -181 a -2-3 p مع موضع محتمل بين جينات رابطة الدول المستقلة التنظيمي 131 كيلو بايت على الكروموسوم 2 ، حيث نلاحظ أثر عامل النسخ لعامل النسخ Wt1 ، وهو منظم رئيسي لسلف النيفرون البقاء على قيد الحياة (Kreidberg et al. ، 1993) ، و Six2 ملزم في مجموعة بيانات سلف النيفرون E16.5 المنشورة (الشكل 7C)) (Guo et al. ، 2021).
الجدول 1. يتغير تعبير miRNA ، المطابق لواحد أو أكثر من DAR في نفس TAD.

الشكل 6. العثور على مُحسِّن المرشح - أزواج ميرنا المستهدفة. ب) المواقع الجينومية لكل ميرنا المفحوصة بالنسبة لمحسن مرشحها (شريط عمودي برتقالي). يظهر مقياس تغيير طية log2 الخاصة بهم على المحور y ، ويتم تمييز miRNA مع زيادة التعبير أو تناقصه باللونين الأخضر والأحمر ، على التوالي.

الشكل 7. أربعة محسنات محتملة - أزواج ميرنا المستهدفة. يتم تمييز الإعلانات باللون الرمادي ، محاذاة بنقاط البداية ، ورسمت في نفس المقياس لتوضيح الحجم النسبي. تظهر الجينات المعروفة من Ensembl باللون الأرجواني ، بينما تشير المناطق الداكنة إلى exons. يتم عرض إمكانية الوصول النسبية في E14.5 و P 0 كمخططات شريطية أعلى وأسفل الخط الأسود الأفقي ، على التوالي ، وكذلك في المخططات الداخلية التي توضح تراكم البيانات في DAR المحدد جنبًا إلى جنب مع بيانات ChIP-seq المنشورة بواسطة Guo et . آل. (Guo et al.، 2021). يتم سرد آثار أقدام عامل النسخ التي تم تحديدها بواسطة HINT في اللافتات البرتقالية. تشير المخططات الشريطية في لوحات منفصلة على اليمين إلى تعبير miRNA (أخضر) وأحداث إدراج Tn5 الطبيعية في مناطق المُحسِّن المقترحة (برتقالية). أ) يتم التعبير عن اسم let -7 فرد العائلة -7 c -5 p بشدة فيخلايا سلف النيفرونويقابل "ذروة _54636" 119 كيلو بايت في منطقة بين الجينات. ب) يتم مطابقة miR -9-3 p مع 249 كيلوبايت. ج) miR -181 a 2-3 يقع على بعد 131 كيلو بايت من "الذروة _5887" ، وهو محسن جيني محتمل.
مناقشة
في هذه الدراسة ، سعينا إلى تحديد ميرنا الجديد في وقت واحد والذي يساهم في وقف تكوّن الكلية ، جنبًا إلى جنب مع الميزات التنظيمية المحتملة لرابطة الدول المستقلة. حددنا 114 miRNAs التي يتم التعبير عنها تفاضليًا في خلايا سلف النيفرون ، بالإضافة إلى 2،1 0 3 DARs ، في E14.5 مقارنة بـ P0الكلى. نلاحظ ميزات متعددة تتوقع معززات افتراضية جديدة للجينات Eya1 و Pax8 فيخلايا سلف النيفرون. أخيرًا ، حددنا الاتساقإمكانية الوصول إلى الكروماتينوتغيير تعبير miRNA لـ 33 زوجًا من miRNAs و DARs ، بما في ذلك let -7-5 p و miR -125 b -5 p و miR -181 a -2-3 p و miR -9-3 p ، والجينات المستهدفة المفترضة المعبر عنها في أسلاف النيفرون لـ miRNAs المعبر عنها تفاضليًا. تُظهر بياناتنا معًا أن التغييرات الجوهرية في أسلاف النيفرون وتعتمد على مرحلة تكوين الكلية تنعكس في بيئة الكروماتين للخلية السلفية وفي نسخة ميرنا الخاصة بها.
من بين التغييرات التي نلاحظها في نسخة miRNA سلف النيفرون ، نلاحظ زيادات كبيرة في التعبير عبر عائلة {0} مع تقدم عمر السلف. يتوافق هذا مع التقارير السابقة: يعتبر بروتين Lin28b ومجموعة -7 من miRNAs متعارضين بشكل متبادل ويشكلان مفتاحًا ثنائي الاستقرار يتحكم في التعبير -7 في الثدييات (Zhu et al.، 2011) وفي أسلاف النيفرون ، فإن التحول نحو تعبير السماح -7 المتزايد يؤثر بشكل مباشر على توقيت وقف تكوّن الكلية (Yermalovich et al. ، 2019). نلاحظ أيضًا زيادة التعبير عن miR -125 b -5 p ، والذي يُعرف أيضًا بقمع التعبير عن Lin28b في السياقات الخلوية الأخرى (Chaudhuri et al.، 2012؛ Potenza et al.، 2017). تعد عائلة let -7 و miR -125 b -5 p من بين 114 miRNA يتم التعبير عنها تفاضليًا بين E14.5 و P0 في أسلاف النيفرون ، مما يشير إلى دور miRNAs في تطوير سلف النيفرون لا يقتصر على السماح لـ -7 / Lin28b. على سبيل المثال ، تشتمل miRNAs التي تنخفض في التعبير على عضوين من عائلة miR -200 ، والتي تم الإبلاغ عن أنها تلعب دورًا في تمايز خلايا podocyte (Z. Li et al. ، 2016): miR -200 ب -3 ص و ميل -429-3 ص. علاوة على ذلك ، نلاحظ انخفاضًا في التعبير عن miR -126 a 5p ، والذي يُعرف بأنه يعزز تكوين الأوعية (Schober et al. ، 2014 ؛ S. Wang et al. ، 2008). قد يعكس هذا النسب اللحمية المتوسطة الشائعة من أسلاف الأوعية الدموية والنيفرون ، والتزام مجموعة فرعية من هذه الخلايا لتصبح أسلاف النيفرون.
تُظهر تحليلات المسار للأهداف الجينية المتوقعة لتغيير miRNAs باستخدام DIANA miRPath (Vlachos et al. ، 2015) إثراء MAPK و TGF- إشارات ، وكلاهما المنظمان الرئيسيان لأسلاف النيفرون (Hilliard et al. ، 2019 ؛ Ihermann-Hella et al. ، 2018 ). يتم أيضًا تمثيل العديد من مسارات KEGG الأخرى بين الأهداف الجينية المتوقعة لـ miRNAs المنتظمة ، بما في ذلك المسارات المتعلقة بالمصفوفة خارج الخلية ، والهيكل الخلوي الأكتيني ، والالتصاق البؤري: جميع الجوانب الحاسمة للهجرة الخلوية ، والتمايز ، والتفرع ، والتعلق ، والاستقطاب ، والانتشار (روزاريو وديسيموني ، 2010). يتم استهداف الجينات المرتبطة بـ ECM من قبل بعض miRNAs الأكثر تعبيرًا والتي تزداد بشكل ملحوظ التي نكتشفها ، بما في ذلك أعلى نسخة تم التعبير عنها نكتشفها: miR -196 a -5 p. من المعروف أن miR -196 a -5 p تستهدف Col1a1 ، و Col1a2 ، و Col3a1 - وهي جينات يتم تنظيمها في أسلاف النيفرون التي تعاني من نقص في Pax 2- والتي تخضع للتبديل في السدى الكلوي (Naiman et آل ، 2017). وبالتالي ، فإن زيادة التعبير miR -196 -5 قد يكون لها دور في تعزيز حدود النسب مع تقدم الأسلاف في العمر. علاوة على ذلك ، نحدد تفاعلات مستهدفة جديدة محتملة للـ miRNA-mRNA والتي قد تساهم في وقف تكوّن الكلية ، بما في ذلك التنظيم الأعلى لعائلة let -7 التي قد تستهدف Hmga2 و Meis2 (المرتبط بتكاثر الخلايا) (Abruzzese et al . ، 2019 ؛ Fusco & Fedele ، 2007 ؛ Lam et al. ، 2014 ؛ Mugford et al. ، 2009) مع تقدم عمر أسلاف النيفرون. Hmga2 ليس له دور معروف فيالكلىتطوير. ومع ذلك ، يُعتقد أن Meis2 له تداخل وظيفي مع عامل النسخ ذي الصلة Meis1 ، المعروف أنه مطلوب لتطور الكلى (Hisa et al. ، 2004). نلاحظ أيضًا التنظيم السلبي لـ miRs (miR -34 b -5 p و miR -983 p و miR -200 a -3 p) التي قد تستهدف Jag1 ، المعروف عنه أنه منظم ومهم في تمايز النيفرون (Chung et al. ، 2016).
جنبًا إلى جنب مع نسخة ميرنا المتغيرة ، قمنا بقياس التغيرات في بيئة الكروماتين لخلية سلف النيفرون بين E14.5 و P 0 في نفس الوقت. نصف اثنين من المعززات الجديدة المفترضة لـ Eya1 و Pax8 ، بناءً على (1) قربهما من معززات الجينات هذه ، (2) التغييرات الخاصة بكل منهما فيإمكانية الوصول إلى الكروماتينأثناء التطور بما يتماشى مع تغير التعبير الجيني للوقت الكاذب أثناء التمايز ، (3) آثار أقدامالكلىعوامل النسخ التنموي ، (4) حفظ التسلسل ، (5) دليل على وظيفة المُحسِّن في الأنسجة / أنواع الخلايا الأخرى من Enhancer Atlas2. 0 (Gao & Qian ، 2020) ، و (6) بيانات ChIP-seq في E16 .5 سلالات النيفرون لعلامة المعززات النشطة (H3K27ac) وربط عامل النسخ لـ Ctnnb1 و Lef1 و Six2 و Tcf7. نلاحظ انخفاضًا في إمكانية الوصول إلى الكروماتين لمُحسِّن Eya1 ، وهو ما يتوافق مع دور Eya1 في تعزيز تعدد قدرات سلف النيفرون ومع التقارير التي تفيد بأن فقدان Eya1 يؤدي إلى الاندمال الظهاري المبكر للسكان السلف (J. Xu et al. ، 2014 ؛ PX Xu وآخرون ، 1999). يساهم Pax8 و homolog Pax2 الخاص به في مواصفات النسب لأسلاف النيفرون (Bouchard et al. ، 2002) ، ولن تخضع أسلاف النيفرون التي لا تحتوي على واحد على الأقل من هذه الجينات (Narlis et al. ، 2007). تتسق إمكانية الوصول المتزايدة إلى الكروماتين التي اكتشفناها لمحسن Pax8 المفترض مع زيادة تعبير Pax8 في الظهارة الكلوية حيث تفرق النيفرون.
كشف تحليل الإثراء (McLean et al. ، 2010) لـ DARs عن "تنظيم التمايز الظهاري" باعتباره المصطلح الأكثر إثراء بين مناطق الكروماتين المفتوحة ، مما يشير إلى أن DARs التي نكتشفها قد تحتوي على ميزات تنظيمية تقود أو تستجيب لإشارات للتمييز وتطويرخلايا سلف النيفرونفي أنواع الخلايا الظهارية. تعد إشارات الشق من بين مصطلحات GO الأكثر إثراءً التي تم تحديدها بين فتح DARs ، وفي أسلاف النيفرون ، يُعرف هذا المسار بقمع تعبير Six2 وتعزيز تمايز خلايا السلف النيفرون (Chung et al. ، 2016). من بين الجينات المتورطة في هذا المسار هو Jag1 ، وهو رابط رئيسي في إشارات Notch تم الإبلاغ عن ارتباط تعبيره عكسيًا بتعبير Six2 و Hes1 (Chung et al. ، 2016). نلاحظ أن Jag1 هو هدف توضيحي لثلاثة miRNAs مع زيادة التعبير (miR34b -5 p و miR 98-3 p و miR200a -3 p ، الشكل 2). أخيرًا ، نلاحظ إثراء الجينات المرتبطة بإعادة تشكيل الأوعية الدموية وتشكلها في فتح DAR ، على الرغم من أن هذا يبدو أنه نتيجة للجينات المشتركة بين هذه المسارات التنموية وتمايز الخلايا الظهارية ، بما في ذلك Jag1 و Eya1 و Hes1 و Foxc1 و Hey2.
تغييرات فيإمكانية الوصول إلى الكروماتينضمنخلايا سلف النيفرونتم قياسها في دراسات سابقة (Guo et al. ، 2021 ؛ Hilliard et al. ، 2019).
بشكل عام ، تتوافق نتائجنا مع هذه الدراسات السابقة ، مع التركيز على الجينات المرتبطة بـ Notchsignaling و Pax 8-. على وجه الخصوص ، على الرغم من وجود بعض الاختلافات التجريبية في هذه الدراسات السابقة عند مقارنتها بهذا التقرير. من المحتمل أن يتم الخلط بين عزل أسلاف النيفرون التي تعبر عن GFP باستخدام خلية نشطة مضان من ستة 2- فأر مراسل التحوير الجيني من خلال اكتشاف أن هذا الأليل لديه انخفاض في عدد النيفرون بنسبة 45 بالمائة تقريبًا (Hilliard et al. ، 2019 ؛ Volovelsky وآخرون ، 2018). بالإضافة إلى ذلك ، تم إثبات أن أسلاف النيفرون المستزرعة (التي نمت بجرعة منخفضة أو عالية من CHIR) لديها نسخ مميزة من أسلاف النيفرون الأولية ، مما يشير إلى أن إمكانية الوصول إلى الكروماتين الخاصة بهم ستكون مختلفة أيضًا (Guo et al. ، 2021 ؛ Hilliard et al. ، 2019). نظرًا لأن الهدف من دراستنا هو فهم كيفية تأثير التغييرات في منظر الكروماتين على تعبير ميرنا في وقت مبكر مقابل أسلاف النيفرون المتأخرة ، كان من الضروري تحليل أسلاف النيفرون الأولية.

الكستانش أفضل للكلى
من خلال الجمع بين هذه التغييرات الملحوظة في بيئة الكروماتين مع التغييرات المتطابقة في تعبير ميرنا ، فإننا نشير إلى العديد من أزواج محسن ميرنا المفترضة الجديدة في وقف تكوين الكلية لمزيد من الدراسة. إن miRNAs miR -125 a -5 p ودع -7 c -5 p ، على سبيل المثال ، نرى زيادة ملحوظة في التعبير بين E14.5 و P 0 ، ويتم تلخيص ذلك من خلال زيادة عدم إمكانية الوصول إلى DAR (chr16: 77،719، 058 77، 720،407) في نفس TAD. يرتبط DAR أيضًا بموقع ربط Six2 (Guo et al. ، 2021) ، وقد يشير إلى مُحسِّن يؤثر على تعبير miR -125 a -5 p and / or let {{18} } c -5 p ، والتي بدورها يمكن أن تعزز التمايز من خلال قمع Lin28b. وبالمثل ، نلاحظ وجود مُحسِّن محتمل لـ miR 181a ، المعروف بقدرته على تعديل تعبير الرينين لدى البشر (Marques et al. ، 2015) وقد تم اعتباره هدفًا علاجيًا لتقليل السمية الكلوية نظرًا لقدرته على قمع BIRC6 وموت الخلايا المبرمج (Liu et آل ، 2018). أخيرًا ، نلاحظ DAR إغلاقًا مرتبطًا بـ miR -9-3 p والذي يحتوي على آثار أقدام لعامل النسخ للبروتينات المستجيبة للإشارات Wnt Snai1 و Snai2.miR -9-3 p's المكمّل العكسي ، miR -9-5 p ، من المعروف أنه يحمي منالكلىثبت أن التليف (Fierro ‐ Fernández et al. ، 2020) و Snai1 و Snai2 يعززان الورم الخبيث السرطاني في خلايا سرطان جلد الفأر (Olmeda et al. ، 2008) ولتعزيز التحولات الظهارية إلى اللحمية المتوسطة (EMT) في مرضى السرطان (Sundararajan et al.، 2019) ، بينما من المعروف أن miR -9 يعزز تكوين الأوعية وهجرة الخلايا البطانية للورم (Zhuang et al.، 2012). قد توجد آلية تؤدي فيها زيادة إشارات Wnt إلى تقليل التعبير عن Snai1 و Snai2 ، مما يقلل بدوره تعبير miR -9-3 لدعم تمايز السلف النيفرون.
حددت دراستنا بشكل شامل التغييرات في منظر الكروماتين ونسخة ميرنا لأسلاف النيفرون أثناء التطور الجنيني ، وقد حددنا المناطق المنظمة لرابطة الدول المستقلة و miRNA التي قد تلعب دورًا في وقف تكوّن الكلية. توفر تحليلات الإثراء لكل من بيانات mRNA-seq و ATAC-seq أدلة جذابة حول الآليات التي قد تكون متورطة ، مثل المسارات التي تنظم تمايز سلف النيفرون ، بما في ذلك Notch و TGF-. لقد أبلغنا أيضًا عن عنصرين تنظيميين مفترضين جديدين لـ Eya1 و Pax8 ، الجينات المعروفة بأهميتها فيالكلىالتطوير ، والتسلسلات التنظيمية المحتملة لميرنا الرئيسي المتورط في وقف تكوّن الكلية.
طُرق
سلالات الفأر
تم الحصول على قرص Wildtype CD -1 من الإناث الحوامل المتزاوجات مع مرور الوقت من Charles River Laboratories، Inc. (Wilmington، MA، USA، RRID: MGI: 5659424) والكلىتم جمعها من الفضلات في اليوم الجنيني E14.5 أو P 0. تم إيواء جميع الحيوانات في vivarium في مركز Rangos Research في مستشفى UPMC للأطفال في بيتسبرغ (بيتسبرغ ، بنسلفانيا ، الولايات المتحدة الأمريكية) وتم إجراء جميع التجارب على الحيوانات وفقًا لسياسات لجنة رعاية الحيوان المؤسسية واستخدامها في جامعة بيتسبرغ. تم تحديد جنس كل جنين أو جرو عن طريق إجراء تفاعل البوليميراز المتسلسل على الحمض النووي الجيني المعزول من قصاصات الذيل باستخدام الاشعال التالية لجين كروموسوم Y Sry: SryF 5ʹ-GATGATTTGAGTGGAAATGTGAGGTA-3ʹ و SryR 5ʹ-CTTATGTTTATAGGCATGCATGCAT} ' تم نشره مسبقًا (McFarlane et al. ، 2013).
تسلسل الحمض النووي الريبي الصغير والتحليل
مجموع الحمض النووي الريبي المعزول منخلايا سلف النيفرونتم تقديم المتبقي بعد إزالة جزء الخلية من سلسلة ATAC إلى مركز تسلسل العلوم الصحية في مستشفى UPMC للأطفال في بيتسبرغ لإعداد المكتبة باستخدام مجموعة إعداد مكتبة QIAseq miRNA (Qiagen 3315 {{1 {18}}} 2). تم إجراء التسلسل أحادي الطرف لمكتبات mRNA-seq على Illumina NextSeq5 0 0 ، وتم ترتيب المكتبات على عمق يقارب 50 مليون قراءة أحادية النهاية لكل مكتبة. تمت محاذاة القراءات المتسلسلة بعد ذلك مع جينوم الماوس mm10 باستخدام حزمة Rsubread (Liao et al. ، 2019) (الإصدار 2.0.1) ، وتم التعليق عليها بـ miRNA المعروفة المدرجة في miRBase (الإصدار 22) (Kozomara & Griffiths-Jones ، 2014) مع وظيفة featureCounts الخاصة بحزمة Rsubread. تم قياس التعبير التفاضلي للميرنا المعروف باستخدام حزمة DESeq2 R (الإصدار 1.26.0) (Love et al. ، 2014). تم تضمين جزء القراءات المتوافقة المشروحة على ميرنا المعروف وكذلك جزء الأجنة الأنثوية لكل عينة كعوامل مساعدة في نموذج الاختبار المقدم إلى DESeq2. تم بعد ذلك تحديد miRNA المعبر عنه تفاضليًا أثناء التحكم في معدل الاكتشاف الخاطئ عند 5 بالمائة ، وتم تحديد اتجاه التغيير (زيادة مقابل تناقص) بناءً على قيمة تغيير الطيات ("زيادة" تشير إلى تعبير أعلى عند P0 مقارنة بـ E14.5) . تم حساب إثراء المسارات التنظيمية بين الأهداف الجينية المتوقعة لـ miRNA مع زيادة وتناقص التعبير بشكل ملحوظ باستخدام أدوات DIANA miRPath الإصدار 3.0 (Vlachos et al. ، 2015). تم استرداد النصوص المستهدفة المتوقعة لـ miRNA من مستودعات TargetScan (Agarwal et al. ، 2015) و miRDB (Y. Chen & Wang ، 2020).
عزل سلف النيفرون
الكلىتم تشريحها من أجنة {0}} E14.5 أجنة أو صغار P0 ، واعتبرت كل فضلات عينة واحدة. تم استخدام كلية واحدة لكل عينة لعزل الحمض النووي الريبي الكلي لاستخدامها "كعنصر تحكم كامل في الكلى" في التحليلات اللاحقة (انظر أدناه). تم جمع ما مجموعه ثلاث عينات في كل نقطة زمنية. تم بعد ذلك عزل الخلايا القشرية من كل عينة باستخدام فرز الخلايا المنشط مغناطيسيًا (MACS) كما تم نشره مسبقًا (Brown et al. ، 2011). لفترة وجيزة ، خضعت الكلى لعملية الهضم الجزئي باستخدام 2 ملي مولار كولاجيناز أ (روش 11088793001) و 3.5 ملي مولار بنكرياتين (سيجما P1625) في محلول ملحي بالفوسفات (PBS) لمدة 15 دقيقة عند 37 درجة. تم إيقاف تفاعل الهضم باستخدام مصل بقري جنيني بارد 100 ٪ (FBS) ، وتم جمع معلق الخلية وتعليقه في محلول ملحي بارد من Dulbecco مع الفوسفات (DPBS) مع 1 ملي مولار من مثبط البروتياز فينيل ميثيل سلفونيل (PMSF) (Sigma-Aldrich 10837091001). تم غسل الخلايا وإعادة تعليقها في مخزن مؤقت للعزل المثلج يتكون من 2 في المائة من FBS في برنامج تلفزيوني ، ثم تم تحضينها بخرز مغناطيسي (مجموعة Dynabeads FlowComp Flexi ، ThermoFisher 11061D) تم تحويلها إلى أجسام مضادة لـ Integrin alpha 8 (Itg 8 ، R&D Systems AF4076) باستخدام DSB-X Biotin Protein Labeling Kit (ThermoFisher D -20655). تم عزل أسلاف النيفرون المرتبطة بهذه الخرزات كما تم نشرها مسبقًا (Hemker et al. ، 2020) وتم تجميعها عبر الكلى لكل عينة. تمت معالجة قسمة من 50 ، 000 من الخلايا السلفية النيفرون على الفور من خلالإمكانية الوصول إلى الكروماتينبروتوكول إعداد المكتبة (انظر أدناه) ، وتم استخراج الحمض النووي الريبي الكلي من تعليق الخلية المتبقية باستخدام Qiagen miRNeasy Mini Kit (Qiagen 217004).
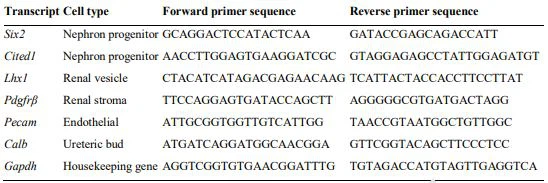
لتأكيد تخصيبخلايا سلف النيفرونبالنسبة لأنواع الخلايا الأخرى ، تم عزل الحمض النووي الريبي الكلي من أسلاف النيفرون وكذلك من الكلالكلى(التحكم الكامل في الكلى ، انظر أعلاه) ، والنسخ العكسي الكمي PCR (qRT-PCR) للعلامات التالية: البقان وكالب اللذان يميزان الحويصلة الكلوية (Brunskill et al. ، 2014) ، السدى الكلوي (S. Chen et al. ، 2015) ، البطانية (Kobayashi et al. ، 2008) ، وبرعم الحالب (Cebrian et al. ، 2014a ) الخلايا ، على التوالي ؛ انظر أيضًا الشكل التكميلي 1. تم استخدام Gapdh (Barber et al. ، 2005) كجين التدبير المنزلي وتم حساب القياس النسبي عبر طريقة 2- ΔΔCt (Livak & Schmittgen ، 2001). تم تضمين الاشعال لهذه النصوص في الجدول 2.
الجدول 2. الاشعال RT-PCR.
إمكانية الوصول إلى الكروماتينإعداد المكتبة
حوالي 50 ، 000خلايا سلف النيفرونتم استخدامها لإنشاء كل مكتبة تسلسل لـ ATAC-seq باستخدام مجموعة Nextera DNA Flex Library Prep Kit (Illumina FC -121-1030) مع التعديلات وفقًا لطريقة منشورة مسبقًا (Buenrostro et al. ، 2 0 13). باختصار ، تم تعليق الخلايا في محلول تحلل غير أيوني بارد مثلج يتكون من 10 ملي مولار تريس ، 10 ملي مول كلوريد الصوديوم ، 3 ملي مولار MgCl2 ، 1 ملي مولار PMSF مثبط البروتياز ، و 0.05 بالمائة Triton X -100 بالحجم لمدة 10 دقائق لخلية ليز الأغشية مع ترك الأغشية النووية سليمة. تم تعليق نوى سلف النيفرون السليمة في مخزن مؤقت للتبديل يحتوي على إنزيم الترانسبوساز وحضنت عند درجة 37 لمدة 30 دقيقة. تمت تنقية الحمض النووي الجيني المجاني الذي تم إصداره من خلال عملية التحويل باستخدام مجموعة MinElute PCR Purification (Qiagen 28004) ثم فهرستها باستخدام بادئات فهرسة أمامية (i7) وعكس (i5) من Nextera Index Kit (Illumina FC -121-1011). تم تحقيق ربط الفهرس وتضخيم الشظايا باستخدام برنامج التدوير الحراري لتضخيم PCR للطريقة.
لتحديد العدد الأمثل لدورات التضخيم المطلوبة لمكتبة ATAC-seq ، تم إجراء تفاعل جانبي qPCR باستخدام SsoAdvanced SYBR Supermix (BioRad 1725274) و 96- جهاز Cycler الحراري C100 (Bio-Rad) لحساب التطبيع قيمة المراسل (Rn) لكل دورة. تم تحديد رقم الدورة التي وصل فيها التفاعل إلى ثلث الحد الأقصى من التألق الخاص به على أنه العدد الأمثل لدورات التضخيم المتبقية ، وتعرض الحجم المتبقي لتفاعل تحويل ATAC-seq المفهرس لهذا العدد من الدورات الإضافية في التضخيم النهائي برنامج. تمت تنقية المكتبات النهائية باستخدام حبات مغناطيسية Ampure XP (Beckman Coulter A63881).
إمكانية الوصول إلى الكروماتينالتسلسل
تم إجراء التسلسل المزدوج لمكتبة ATAC-seq على Illumina NextSeq5 0 0 بواسطة مركز تسلسل العلوم الصحية في مستشفى UPMC للأطفال في بيتسبرغ ، مع مضاعفة تركيزات المكتبة من المتوقع أن ينتج عنها 90 مليون قراءة ثنائية النهاية لكل عينة . تم خفض جودة القراءات باستخدام TrimGalore (BabrahamLab ، 2014) (الإصدار 0.4.3) في وضع "-- المقترن" ومع الإعدادات الافتراضية بخلاف ذلك. تمت محاذاة القراءات مع جينوم mm10 (Church et al. ، 2011) باستخدام Bowtie2 (Langmead et al. ، 2009) (الإصدار 2.3.1) مع الإعدادات "-- local -q -X 2000 --" م ". تم وضع علامة على القراءات الناتجة عن نسخ PCR لنفس جزء الحمض النووي باستخدام وظيفة MarkDuplicates (الإصدار 2.10.9) من Picard Tools (الإصدار 2.10.9) مع الإعدادات الافتراضية. تم تعيين القراءات التي تم تعيينها بشكل غامض لأكثر من موقع واحد في الجينوم بشكل عشوائي إلى أحد هذه المواقع إذا كان هناك أقل من أربعة احتمالات ، وتم حذفها بطريقة أخرى (ENCODE ، nd) (باستخدام برنامج Python النصي المتاح على https: // github. com / kundajelab / atac _ dnase _ pipelines (Lee، 2017) بالإعدادات "-- paired-end -k"). تم استخدام Samtools (H. Li et al. ، 2009) (الإصدار 1.3.1) لتصفية القراءات المكررة وغير المعينة واليتامى والميتوكوندريا ، وكذلك فرز وفهرسة ملفات BAM. اتبعت مراقبة جودة بيانات ATAC-seq إرشادات ATAC-seq الخاصة بمشروع ENCODE (ENCODE ، nd) ، وتم أخذ عينات من مكتبات العينات بشكل عشوائي بحيث تحتوي كل منها على 31 مليون قراءة ثنائية النهاية من أجل تطبيع الاختلافات في أحجام المكتبات.

يمكن أن يمنع القسطرة من عدوى الكلى
تحديد مناطق الكروماتين التي يمكن الوصول إليها
تم تحويل ملفات BAM التي تحتوي على قراءات ATAC-seq التي تمت تصفيتها إلى تنسيق BED بنهاية مزدوجة باستخدام Bedtools '(Quinlan & Hall، 2 0 1 {{2 0}} (الإصدار 2.26.0)' تم تفجيرها 'وظيفة مع الإعدادات "- bed pe -mate1". تم تحديد مناطق الكروماتين الذي يمكن الوصول إليه باستخدام أداة التحليل المستند إلى النموذج لـ ChIP-seq (MACS2 ، الإصدار 2.1.1.20160309) خوارزمية استدعاء الذروة الواسعة (Zhang et al. ، 2008) ، مع الإعدادات "-- تنسيق BEDPE {{ 18}} g mm -p 0. 01 -- wide -- shift 37 -- text size 75 -- keep-dup all -- model ". لتحديد المناطق التي يمكن الوصول إليها عالية الثقة ، تم إجراء مقارنات بين الزوجين (لكل مجموعة من التكرارات من نقطة زمنية معينة) وتم حساب معدل الاكتشاف غير القابل للإنتاج (IDR) (Q. Li et al. ، 2011) باستخدام وسيلة متاحة للجمهور. تنفيذ Python (GitHub https://github.com/nboley/idr) (Boleu et al. ، 2015) مع الإعدادات "-- الذروة العريضة لنوع ملف الإدخال -- الترتيب p.value {{ 35}} soft-IDR-threshold 0. 1 -- سرير نوع ملف الإخراج ". على وجه التحديد ، بالنسبة لكل نقطة زمنية ، تم إرسال ملف BED متسلسل لجميع المناطق التي يمكن الوصول إليها من خلال وسيطة "-- قائمة الذروة" لكل مقارنة (على سبيل المثال ، عند مقارنة عينتين من طراز E14.5 ، فإن جميع القمم العريضة لـ E14.5 بين جميع مكررات الثلاثة المستخدمة). تم دمج مناطق إمكانية الوصول التي كانت متسقة بواسطة IDR في مقارنات مكررة ثنائية الزوج على الأقل (بحد أدنى 20 بالمائة من التداخل) في مجموعة موحدة من المناطق التي يمكن الوصول إليها عالية الثقة ("مناطق IDR").
التغييرات في مناطق الكروماتين التي يمكن الوصول إليها
تم تحديد إمكانية الوصول لكل منطقة IDR داخل عينة معينة من خلال حساب عدد أحداث التحويل التي تحدث أثناء تطبيع محتوى GC المتسلسل عبر العينات. تم تحقيق ذلك باستخدام برنامج نصي مخصص (متوفر في مستودع البرامج المصاحب ، انظر البيانات التكميلية). تم بعد ذلك تحديد التغييرات في إمكانية الوصول هذه من خلال مقارنة هذه القيم عبر النقاط الزمنية باستخدام حزمة برامج Limma-voom (الإصدار 3.42.2) (Ritchie et al.، 2 0 0 6). لحساب جنس الجنين ، تم تضمين جزء الأجنة الأنثوية في كل عينة كعامل مساعد في النماذج الخطية المستخدمة لتحليل إمكانية الوصول التفاضلي ، وتمت إزالته كتأثير دفعي في التصورات باستخدام وظيفة إزالة تأثير دفعة حزمة Limma. تم اعتبار مناطق الكروماتين التي يمكن الوصول إليها بشكل تفاضلي (DARs) مفتوحة بشكل كبير (زيادة إمكانية الوصول بين E14.5 و P 0) أو إغلاق (انخفاض إمكانية الوصول بين E14.5 و P0) عند التحكم في معدل الاكتشاف الخاطئ عند 10 بالمائة . تم تحديد تحليلات الإثراء الوظيفي لفتح وإغلاق المناطق الجينومية من خلال تقديم الإحداثيات ذات الصلة إلى أداة إثراء المناطق الجينومية للتعليقات التوضيحية (GREAT ، متاح على http://great.stanford.edu/public/html/) (McLean et al. ، 2010 ). تم استرجاع التعليقات التوضيحية للمعززات المعروفة والمتوقعة من مستودعات FANTOM5 (Andersson et al. ، 2014) و VISTA (Visel et al. ، 2007) و EnhancerAtlas 2.0 (Gao & Qian ، 2020).
آثار أقدام عامل النسخ
تم تحديد آثار أقدام عامل النسخ من خلال تجميع جميع ملفات BAM من نفس النقطة الزمنية ، ثم تشغيل برنامج تحديد بصمة TF Footprints (HINT) المستند إلى Regulatory Genomics Toolbox (HINT) (الإصدار 0. 12.3) ، وتحديداً نموذج البصمة لـ ATAC -seq data (متوفرة على www.regulatory-genomics.org) (Z. Li et al.، 2 0 18). تم تشغيل هذا البرنامج بإعدادات "بصمة التلميح الأيمن -- الكائن=ملم 10 -- على التوالي -- بنهاية مقترنة". تم بعد ذلك شرح آثار الأقدام بأشكال ربط الماوس المعروفة من قاعدة بيانات HOCOMOCO 11 (Kulakovskiy et al. ، 2018) باستخدام وظيفة مطابقة نموذج HINT مع الإعدادات "تحليل الشكل الأيمن الذي يطابق -- الكائن الحي=mm10". تم استبعاد آثار الأقدام مع درجات HINT أقل من 10. أخيرًا ، تم قياس أنماط النشاط التفاضلي بين آثار الأقدام المتطابقة باستخدام الوظيفة التفاضلية لبرنامج RGT-HINT ، مع إعدادات "تفاضل التلميح الأيمن -- الكائن=ملم 10 -- قبل الميلاد {{27} } NC 12 -- ملفات تعريف الإخراج ". تم تحديد مستويات النشاط المتغيرة بشكل كبير على أساس قطع قيمة p 0.05 (طريقة فريدمان-نيمني).

يمكن أن يحسن القسطرة وظائف الكلى
التكوين النووي
تم تجميع القراءات المحاذية من نفس النقطة الزمنية في ملف BAM واحد ، وتم استخدام حزمة NucleoATAC (الإصدار 0. 3.4) لتحديد الأنماط في أطوال القراءة التي توحي بكل من الثنائيات النووية المرتبطة والمناطق الخالية من النوكليوزوم ( NFRs) (شيب وآخرون ، 2015). تم تنفيذ هذا البرنامج باستخدام الإعدادات الافتراضية. تم شرح النيوكليوسومات على أنها منطقة 146 نقطة أساس تتمحور حول كل منها يسمى ثنائي النواة.
تعبير الحمض النووي الريبي أحادي الخلية
تمت معالجة بيانات التعبير الجيني أحادي الخلية لمخطوطة سابقة (BioRxiv https://www.biorxiv.org/content/10.1101/2020.09.16.300293v1) (Bais et al. ، 2020) ، وتم استرجاعها من Gene Expression Omnibus (GEOID GSE158166). تتضمن البيانات المُعالجة المُدمجة في الشكل التكميلي 7 أنواع الخلايا ، ومستويات التعبير الجيني ، وحفلات الزفاف منخفضة الأبعاد (tSNE) ، وشروح الزمان الكاذبة المتعلقة بالمسار المحدد بين مجموعات التكاثر والتمييز بين أسلاف النيفرون. تم الوصول إلى البيانات وتنظيمها باستخدام حزمة SingleCellExperiment R (Lun & Risso ، 2019).
تفاعلات ميرنا-مرنا في شيخوخة الخلايا السلفية النيفرون والتمايز
جينات ذات تعبير متغير بين التجديد الذاتي والاستعداد والتمييزخلايا سلف النيفرونتم الحصول عليها من الجدولين التكميليين 3 و 4 اللذين نشرهما Bais et al .. (FDR< 0.1="" for="" all="" genes,="" 99="" genes="" total).="" mirtarbase="" v8.0="" for="" the="" mouse="" was="" downloaded="" (https://mirtarbase.cuhk.edu.cn/~mirtarbase/mirtarbase_2022/cache/download/8.0/mmu_mt="" i.xls)="" while="" mirdb="" version="" 6.0="" predictions="" were="" obtained="" from="" the="" mid="" b="" website="" (y.="" chen="" &="" wang,="" 2020);="" high-quality="" mirna-to-target-gene="" predicted="" interactions="" with="" a="" minimum="" score="" of="" 90="" were="" considered.="" annotated="" mir="" target="" genes="" and="" differentially="" expressed="" genes="" were="" then="" intersected="" using="" the="" r="" programming="" environment="" to="" generate="" figure="" 2="" and="" supplemental="" table="">
تسلسل الكروماتين المناعي في أسلاف النيفرون الأولية
تم استرداد بيانات تسلسل الكروماتين المناعي (ChIP-seq) لربط -catenin و Lef1 و Six2 و Tcf7 في أسلاف النيفرون الأولية من ملفات BedGraph داخل مستودع GEO (GSE131119) لـ Guo et al. ، 2021. تم حساب متوسط قيم إشارة إثراء الطية عبر عينات مكررة.
فحص العناصر التنظيمية التي تؤثر على تعبير ميرنا
للكشف عن معززات محتملة لـ miRNA ، قمنا بتعليق miRNA و DARs مع المجالات المرتبطة طوبولوجيًا (TADs) التي توجد فيها على أساس التعليقات التوضيحية mm10 من الخلايا الجذعية الجنينية للفأر ، والتي تم تنزيلها من مستعرض الجينوم ثلاثي الأبعاد (متاح على http: // 3dgenome fsm.northwestern.edu /) (Y. Wang et al. ، 2018). مناطقإمكانية الوصول إلى الكروماتينو miRNA كانت تعتبر من المعززات المرشحة - أزواج miRNA إذا كانت تشغل نفس TAD وأظهرت تغييرات متسقة في إمكانية الوصول والتعبير (زيادة إمكانية الوصول مع زيادة تعبير miRNA والعكس بالعكس). تم اعتبار DARs "ميزات تنظيمية" ممكنة فقط إذا لم تتداخل مع مروج معروف أو نهاية exon. تم إعطاء الأولوية للأزواج المحتملة من miRNA والعناصر التنظيمية المفترضة إذا كانت 1) تقع ضمن نفس TAD و 2) شهدت تغيرات كبيرة بين E14.5 و P 0 (زيادة تعبير miRNA وزيادة إمكانية الوصول إلى منطقة IDR ، والعكس صحيح) .
شكر وتقدير
ساهم شيلبي حمكر وأبها بايس في التصميم التجريبي. تم إجراء التسلسل لـ ATAC-seq و mRNA-seq بواسطة مركز تسلسل العلوم الصحية في مستشفى UPMC للأطفال في بيتسبرغ.
تضارب المصالح
أعلن أي تضارب المصالح
التمويل
تم دعم AC من خلال منح من المعهد الوطني للسكري والجهاز الهضمي والكلىالأمراض التابعة للمعهد الوطني للصحة (T32DK 061296-17). تم دعم DK من خلال منح من المعهد الوطني للعلوم الطبية العامة التابع للمعهد الوطني للصحة (R01GM115836). تم دعم JH من خلال منح من المعهد الوطني للسكري وأمراض الجهاز الهضمي والكلى تحت المعهد الوطني للصحة (R01DK103776 و 125015). تم دعم DMC من قبل شبكة دراسة المتلازمة الكلوية (NEPTUNE) جائزة التطوير الوظيفي وزمالة ما بعد الدكتوراه في مستشفى الأطفال في مستشفى بيتسبرغ الاستشاري للأبحاث. تم دعم YP من خلال منح من مستشفى UPMC للأطفال في بيتسبرغ واتحاد أمراض الميتوكوندريا في أمريكا الشمالية.

توافر البيانات
تم استرداد معززات الماوس المتوقعة من FANTOM5 (DOI: 10.1038 / nature12787 ؛ الملف متاح هنا) و Vista (DOI: 10.1093 / var / gkl822 ؛ الملف متاح هنا) و EnhancerAtlas (DOI: 10.1093 / var / gkz980 ؛ ملفات الماوس متوفرة هنا) قواعد بيانات. تم تنزيل جينوم الماوس mm10 وشروحه عبر مشروع جينومات Illumina (متاح هنا). تم استرداد ملف over-chain لرفع إحداثيات mm9 إلى mm10 من مستعرض جينوم UCSC (DOI: 10.1101 / gr.229102 ؛ الملف متاح هنا). تم استرداد التعليقات التوضيحية لـ TAD من الخلايا الجذعية الجنينية للفأر من متصفح الجينوم ثلاثي الأبعاد (DOI: 10.1186 / s 13059-018-1519-9 ، الملف متاح هنا). تم استرداد أهداف نسخة miRNA المتوقعة من TargetScan (DOI: 10.7554 / eLife.05005 ، الملف متاح هنا) ، ومن الإصدار 6 miRDB (DOI: 10.1093 / var / gkz757 ، الملف متاح هنا). تتوفر بيانات ATAC-seq بما في ذلك مواقع IDR / DAR والشروح ونتائج الإثراء التفاضلي على GEO (GSE168339) ، وكذلك بيانات mRNA-seq بما في ذلك التعليقات التوضيحية ونتائج التعبير التفاضلي (GSE168342). يتوفر كود الكمبيوتر المستخدم لمعالجة البيانات وتحليلها ، ولإنشاء الأرقام على https://bitbucket.org/clugstonA/mirna_enhancers
فهرس
Abruzzese، MP، Bilotta، MT، Fionda، C.، Zingoni، A.، Soriani، A.، Petrucci، MT، Ricciardi، MR، Molfetta، R.، Paolini، R.، Santoni، A.، & Cippitelli، M (2019). عامل النسخ المثلي MEIS2 هو منظم لبقاء الخلايا السرطانية ونشاط IMiDs في المايلوما المتعددة: التحوير بواسطة مثبطات البروتين Bromodomain و Extra-Terminal (BET). موت الخلايا والمرض ، 10 (4). https://doi.org/10.1038/s41419-019-1562-9
Agarwal، V.، Bell، GW، Nam، JW، & Bartel، DP (2015). التنبؤ بالمواقع المستهدفة الفعالة للـ microRNA في mRNAs الثدييات. إلييف. https://doi.org/10.7554/eLife.05005
Andersson، R.، Gebhard، C.، Miguel-Escalada، I.، Hoof، I.، Bornholdt، J.، Boyd، M.، Chen، Y.، Zhao، X.، Schmidl، C.، Suzuki، T . ، Ntini ، E. ، Arner ، E. ، Valen ، E. ، Li ، K. ، Schwarzfischer ، L. ، Glatz ، D. ، Raithel ، J. ، Lilje ، B. ، Rapin ، N. ،… Sandelin ، أ (2014). أطلس من المعززات النشطة عبر أنواع الخلايا البشرية والأنسجة. الطبيعة، 507 (7493) ، 455-461. https://doi.org/10.1038/nature12787
بابراهام لاب. (2014). تقليم وافر. في المعلوماتية الحيوية. http://www.bioinformatics.babraham.ac.uk/projects/trim_galore
Bais، AS، Cerqueira، DM، Clugston، AS، Ho، J.، & Kostka، D. (2020). يكشف تسلسل الحمض النووي الريبي أحادي الخلية عن نشاط دورة الخلية التفاضلية في مجموعات الخلايا الرئيسية أثناء تكوّن الكلية. بيوركسيف. https://doi.org/https://doi.org/10.1101/2020.09.16.300293
Barber، RD، Harmer، DW، Coleman، RA، & Clark، BJ (2005). GAPDH كجينة تدبير منزلي: تحليل تعبير GAPDH mRNA في لوحة من 72 نسيجًا بشريًا. علم الجينوم الفسيولوجي. https://doi.org/10.1152/physiolgenomics.00025.2005
بارتل ، موانئ دبي (2009). التعرف على الهدف MicroRNA والوظائف التنظيمية. الخلية ، 136 (2) ، 215-233. https://doi.org/10.1016/j.cell.2009.01.002.MicroRNA
بيرترام ، جي إف ، دوغلاس دينتون ، آر إن ، ضيوف ، بي ، هيغسون ، دكتوراه في الطب ، وهوي ، WE (2011). رقم النيفرون البشري: الآثار المترتبة على الصحة والمرض. طب كلى الأطفال ، 26 (9) ، 1529-1533. https://doi.org/10.1007/s00467-011-1843-8
Boleu، N.، Kundaje، A.، Bickel، PJ، & Li، Q. (2 0 15). معدل الاكتشاف غير القابل للإنتاج (2.0.3). https://github.com/nboley/idr
بوشار ، إم ، سوابني ، أ ، ماندلر ، إم ، نيو بيسر ، أ ، وبوسلينجر ، إم. (2002). مواصفات النسب الكلوية بواسطة Pax2 و Pax8. الجينات والتنمية. https://doi.org/10.1101/gad.240102
..............
من: المجلة التجريبية
2021 تم النشر بواسطة Elsevier Inc.
