تحفز التركيزات المنخفضة من الباراكوات التنشيط المبكر للكيناز الخاضع للتنظيم خارج الخلية والبروتين كيناز B و C-Jun N-terminal Kinase 1/2 Pathways: دور C-Jun N-Terminal Kinase في موت الخلايا الناجم عن الباراكوات
Mar 07, 2022
جهة الاتصال: Audrey Hu Whatsapp / hp: 0086 13880143964 البريد الإلكتروني:audrey.hu@wecistanche.com
ميريا نيسو سانتانو ، جوزيه إم موراين ، لورديس غارسيا-روبيو ، آنا غوميز-مارتين ، روزا أ.
الملخص:
الباراكوات هو مبيد أعشاب ينطوي على مخاطر محتملة للتسبب في داء باركنسون بسبب السمية العصبية المثبتة وتشابه بنيوي قوي مع 1- methyl -4- phenylpyridinium (MPP plus) ، وهو سم عصبي معروف يسبب متلازمة إكلينيكية مشابهة إلىمرض الشلل الرعاش(PD). ومع ذلك ، لا يُعرف في الوقت الحاضر سوى القليل جدًا عن مسارات الإشارات التي ينشطها الباراكوات في أي نظام خلوي. في هذه الدراسة ، قمنا بالتحقيق في تأثير الباراكوات على تنشيط الكينازات 1 و 2 المنظمة للإشارة خارج الخلية (ERK1 / 2) ، و c-Jun N-terminal kinase (JNK) ، وبروتين كيناز B (PKB) في خلايا E18. حفزت التركيزات المنخفضة من الباراكوات زيادات مبكرة جدًا في الفسفرة ERK1 / 2 و JNK1 / 2 و PKB. مثبطات فوسفاتيديلينوسيتول 3- كيناز (PI -3 ك) wortmannin و LY 294002 (2- (4- مورفولينيل) -8- فينيل -4 H {{ 19}} benzopyran -4- 1) منع الزيادات المبكرة التي يسببها الباراكوات في فسفرة PKB. علاوة على ذلك ، كانت الزيادات المبكرة بوساطة الباراكوات في تنشيط ERK1 / 2 حساسة لمثبط البروتين كيناز كيناز 1 (MEK1) المنشط بالميتوجين PD 98059 (2 # -amino -3 # - methoxyflavone) ، في حين كانت استجابات JNK1 / 2 تم حظره بواسطة مثبط JNK1 / 2 SP 600125 (anthra [1-9- cd] pyrazol -6 (2H) -one). لم تؤثر المعالجة المسبقة بـ wortmannin ، LY 294002 ، أو PD 98059 على موت خلايا الباراكوات في خلايا E18. في المقابل ، قلل SP 600125 بشكل ملحوظ من موت الخلايا الناجم عن الباراكوات في خلايا E18. في الختام ، لقد أظهرنا أن التركيزات المنخفضة من الباراكوات تحفز الزيادات القوية المبكرة جدًا في الفسفرة ERK1 / 2 و JNK1 / 2 و PKB في خلايا E18. علاوة على ذلك ، تشير البيانات المقدمة إلى أن تثبيط مسار JNK1 / 2 يحمي خلايا E18 من موت الخلايا الناجم عن الباراكوات ويدعم حقيقة أن تثبيط التنشيط المبكر لـ JNK1 / 2 يمكن أن يشكل استراتيجية محتملة في علاج PD. الكلمات المفتاحية: باراكوات؛ تركيزات منخفضة JNK. موت الخلية شلل الرعاش.

عشب مضاد لمرض باركنسون:cistanche
المقدمة
مرض باركنسون (PD)هو اضطراب تنكس عصبي يتميز بموت الخلايا العصبية الدوبامينية في الجزء الفرعي من القسطنطينية السوداء بالتزامن مع شوائب داخل الهيولى تعرف باسم أجسام ليوي (Olanow and Tatton ، 1999). 5-10 في المائة فقط من مرضى شلل الرعاش لديهم شكل عائلي من هذا المرض مع وضع وراثي جسمي سائد في الوراثة (جاسر ، 2001). تعتبر العوامل الوراثية مهمة في المرضى الصغار ، ولكن من غير المحتمل أن تلعب دورًا رئيسيًا في شلل الرعاش المتقطع الأكثر شيوعًا. على النقيض من ذلك ، تشير الدراسات الوبائية إلى العديد من العوامل البيئية التي تزيد من خطر الإصابة بالشلل الدماغي (مرض الشلل الرعاش). وشملت هذه مبيدات الآفات ومبيدات الأعشاب والمواد الكيميائية الصناعية والزراعة والعيش في بيئة ريفية (Cory-Slechta et al.، 2005؛ Gasser، 2001؛ Landrigan et al.، 2005؛ Tanner and BenShlomo، 1999). تتعلق الحجة الأكثر إقناعًا لدعم عامل بيئي في PD باكتشاف التأثيرات البيولوجية لـ MPTP (1- ميثيل -4- فينيل -1 ، 2،3 ، 6- tetrarchy-dropyridine). ينتج هذا السم للجهاز العصبي المركزي متلازمة مشابهة سريريًا وتشريحًا لـ PD (Kopin and Markey ، 1988 ؛ Langston et al. ، 1983). بهذا المعنى ، تم اقتراح مبيد الأعشاب باراكوات المستخدم على نطاق واسع (1،1 # -dimethyl -4، 4 # -bypiridinium) كعامل خطر مفترض بناءً على كل من التناظر الهيكلي لـ MPPþ ، المستقلب النشط لـ MPTP ( Tanner and Langston ، 1990) ، وحول تقارير مرض باركنسون المرتبطة بالتعرض للعامل (Hertzman et al. ، 1990 ؛ Hubble et al. ، 1993 ؛ Jimenez-Jimenezet al. ، 1992 ؛ Liou et al. ، 1997 ؛ Wang et آل ، 1992). ومع ذلك ، في حين أن مسارات الإشارات المشاركة في موت خلايا MPP معروفة جيدًا (Halvorsen et al. ، 2002 ؛ Gomez-Santos et al. ، 2002 ؛ Gonzalez-Polo et al. ، 2003) ، لا يُعرف سوى القليل جدًا عن مسارات الإشارة النشطة. بواسطة الباراكوات (Cheng et al.، 2003؛ Chun et al.، 2001؛ Peng et al.، 2004) على أي حال ، لا توجد دراسات حول الأحداث المبكرة التي لوحظت بعد التعرض لتركيزات منخفضة من الباراكوات.
يمكن للعديد من المنبهات ، بما في ذلك MPPþ والباراكوات ، تنشيط مجموعة من شلالات الإشارات داخل الخلايا التي ترتبط ارتباطًا وثيقًا بكل من مسارات موت الخلايا وبقاء الخلية. على سبيل المثال ، MPPþ (Gomez-Santos et al. ، 2002 ؛ Halvorsen et al. ، 2002) ينشط أعضاء عائلة بروتين كيناز (MAPK) وبروتين كيناز B (PKB). يتم تنشيط أفراد عائلة TheMAPK بواسطة MPPþ أو الباراكوات بما في ذلك كينازات تنظيم الإشارات خارج الخلية 1 و 2 (ERK1 / 2) ، و kinases c-Jun N-terminal (JNK1 و JNK2) ، و p38 MAPK. ومن المقبول عمومًا أن ERK1 / 2 يعزز تنشيط PKB بقاء الخلية عن طريق تنشيط مسارات الإشارات المضادة للاستماتة ، في حين يرتبط تنشيط JNK1 / 2 و p38 MAPK بموت الخلايا العصبية (Harper and LoGrasso ، 2001 ؛ Shin et al. ، 2001 ؛ Xia et al. ، 1995) . تنشيط مسار فوسفاتيديلينوسيتول 3- كيناز (PI -3 K) / مسار PKB يساهم في بقاء الخلايا العصبية (شين وآخرون ، 2001). على وجه الخصوص ، يمكن أن يلعب تنشيط مسار JNK1 / 2 دورًا مهمًا في MPP سمية الباراكوات (Cassarino et al. ، 2000 ؛ Halvorsen et al. ، 2002 ؛ Peng et al. ، 2004) وبالتالي في العمليات الخلوية التي تتأثر في PD(مرض الشلل الرعاش).

cistanche الأعشاب: مكافحة مرض باركنسون
المواد والأساليب
خط الخلية والثقافة.
تم استخدام الأرومات العصبية في دماغ الفئران التي تم تخليدها تلقائيًا ، خلايا E18 ، في هذه الدراسة. تم الحصول على خط الخلايا E18 عن طريق الخلود التلقائي من ثقافات 18- قشور دماغية لجنين يبلغ من العمر يوم واحد وتم توفيرها من قبل الدكتور أ. مونيوز (Instituto de InvestigacionesBiome´dicas ، CSIC ، مدريد ، إسبانيا) . تمثل خلايا E18 الخلايا العصبية البدائية التي تعبر عن NF 68 والعلامة العصبية البدائية nestin ولكنها تفتقر إلى علامة الخلايا النجمية ، البروتين الحمضي الليفي الدبقي. بعد تحريض التمايز الجزئي باستخدام dibutyryl-cAMP ، تعبر الخلايا عن علامات عصبية إضافية مثل NF 145 و NF 220 و enolase الخاص بالخلايا العصبية (Mun˜oz ، الاتصال الشخصي). نمت الخلايا في Hanks 'F -12 (Hyclone ، Brevieres ، فرنسا) واستكملت بنسبة 10 بالمائة FCS (Hyclone) ، الستربتومايسين (100 مجم / مل) ، والبنسلين (100 وحدة / مل). تم زرع الخلايا في 5 3 10 5 في قارورة نسيج نسيجية تبلغ مساحتها 75- سم 2 (TPP ، Trasadingen ، سويسرا) وتم تحضينها عند 37 درجة مئوية في جو هواء بنسبة 5 بالمائة من ثاني أكسيد الكربون / 95 بالمائة. تم تمرير الثقافات مرة واحدة في الأسبوع عن طريق التربسين باستخدام محلول التربسين- EDTA (Hyclone).
علاجات الخلايا.
تم تجريب الخلايا المتكدسة (حوالي 80 بالمائة) في قوارير زراعة الأنسجة 75- سم 2 وبذرها في أطباق زراعة الأنسجة بتركيز 5 3104 من الخلايا / سم 2. وبعد أربع وعشرين ساعة ، تم شفط الوسيط واستبداله بوسط جديد بمفرده أو وسط يحتوي على التركيزات المحددة من الباراكوات. في تجارب أخرى ، تراكيز مختلفة من مثبطات كيناز (LY 294002 ، وورتمانين ، SP 600125 ، و PD(مرض الشلل الرعاش)98 0 59 ، جميعها من Tocris ، بريستول ، المملكة المتحدة) تمت إضافتها قبل 30 دقيقة من التعرض للباراكوات. عندما تم إذابة مثبطات كيناز في ثنائي ميثيل سلفوكسيد ، تم إجراء الضوابط بأعلى تركيز مستخدم (0.2 بالمائة حجم / حجم). لم تؤثر إضافة ثنائي ميثيل سلفوكسيد على قيم صلاحية لوحات التحكم.
فحص جدوى الخلية
تم تحديد صلاحية الخلية بواسطة مقايسة MTT اللونية (Mosmann ، 1983). في الخلايا القابلة للحياة ، يمكن لإنزيم نازعة هيدروجين إنزيم الميتوكوندريا استقلاب MTT في صبغة فورمازان التي تمتص الضوء عند 57 0 نانومتر. لهذه التجارب ، تم استخدام 24- لوحات اختبار جيدة. في نهاية كل علاج ، تمت إضافة 1 0 0 لتر من MTT المحضر بتركيز 5 مجم / مل في برنامج تلفزيوني إلى كل طبق. بعد 3 ساعات من الحضانة ، تم صب المادة ، وتم إذابة رواسب الفورمازان باستخدام الأيزوبروبانول الحمضي (0.04 - 0.1 N HCl في الأيزوبروبانول المطلق). تم قياس امتصاص الصبغة المحولة بطول موجة يبلغ 570 نانومتر مع طرح خلفي عند 630-690 نانومتر. تم ضبط امتصاص الثقافات غير المعالجة بنسبة 100 في المائة.
لتأكيد النتائج التي تم الحصول عليها عن طريق مقايسة MTT ، تم أيضًا تقييم موت الخلايا عن طريق قياس إطلاق إنزيم اللاكتات ديهيدروجينيز (LDH) إلى وسط الثقافة باستخدام مجموعة مقايسة LDH اللونية (Roche ، Indianapolis ، IN) وفقًا لتعليمات الشركة الصانعة . تم تعريف تسرب LDH على أنه نسبة نشاط LDH في وسط الثقافة إلى إجمالي النشاط لكل بئر (3100). تم الحصول على بيانات قابلة للمقارنة باستخدام كلتا الطريقتين.
تحضير المستخلصات الخلوية وتحليل اللطخة الغربية.
بعد المعالجات التجريبية ، تم شطف الخلايا (المزروعة في أطباق 60- مم) مرتين باستخدام برنامج تلفزيوني بارد وإزالتها عن طريق الكشط ثم طردها عند 900 3 جم لمدة 5 دقائق عند 4 درجات مئوية. تحتوي على 50 ملي مولار HEPES ، ودرجة الحموضة 7.5 ، و 300 ملي كلوريد الصوديوم ، و 1 في المائة تريتون X -100 ، و 2 ملي مولتر EDTA ، و 5 ملي مولار MgCl2 ، و 25 ملي مولار NaF ، و 1mMNa3VO4 ، وكوكتيل مثبط البروتياز (Sigma ، St Louis ، MO). تم الطرد المركزي للخلايا عند 13 ، 000 3 جم لمدة 5 دقائق عند 4 درجة مئوية ، تم تخزين المواد الطافية عند 80 درجة مئوية حتى التحليل بواسطة لطخة ويسترن. تم قياس تركيز البروتين وفقًا لـ Bradford (1976) باستخدام BSA كمعيار.
تم حل كميات متساوية من البروتينات (1 0 LG لكل حالة) في 12 بالمائة من الرحلان الكهربائي للهلام SDS ونقلها إلى أغشية PVDF وفقًا للطرق التقليدية المعدلة جزئيًا (Fuentes et al. ، 2000). باختصار ، تم نقل البروتينات (250 مللي أمبير لمدة 60 دقيقة) إلى أغشية PVDF باستخدام جهاز Mini Trans-Blot Cell (Bio-Rad ، Hercules ، CA). يتضمن إجراء الكشف المناعي نقل الغشاء وإغلاقه (60 دقيقة في درجة حرارة الغرفة) باستخدام TTBS (10 ملي مولار تريس / حمض الهيدروكلوريك ، ودرجة الحموضة 7.5 ، و 150 ملي مول كلوريد الصوديوم ، و 0.2 بالمائة توين -20) التي تحتوي على 10 بالمائة من الحليب المجفف الخالي من الدسم. تم تحضين الأغشية بعد ذلك لمدة 60 دقيقة في درجة حرارة الغرفة باستخدام أجسام مضادة أولية متعددة النسيلة للأرانب (جميعها من Cell Signaling ، Beverly ، MA ، المخفف 1: 1000) في TTBS 10 بالمائة من الحليب المجفف الخالي من الدسم أو 5 بالمائة BSA. بعد الغسيل (لمدة دقيقتين 5- باستخدام TTBS) ، تم تحضين الأغشية (60 دقيقة عند درجة حرارة الغرفة) بأجسام مضادة ثانوية مضادة للأرانب مقترنة بالبيروكسيديز (1: 5000 في TTBS مع 10 بالمائة من الحليب المجفف الخالي من الدسم). بعد الغسيل (لمدة 5- دقيقتين و 10- دقيقة) ، تم تصور اكتشاف الأجسام المضادة المرتبطة بواسطة التلألؤ الكيميائي باستخدام كاشف ECL-plus (Amersham Biosciences ، Orsay ، فرنسا) وتم تحليله بالكمية برنامج واحد (Bio-Rad). تم تحليل محتوى الأكتين كعنصر تحكم باستخدام جسم مضاد متعدد الأضلاع (من Sigma) مخفف 1: 2500 في TTBS مع 10 بالمائة من الحليب المجفف الخالي من الدسم).
تحليل احصائي.
تم تكرار كل تجربة ثلاث مرات على الأقل مع وجود علاقة ارتباط مرضية بين نتائج التجارب الفردية. البيانات المعروضة هي تلك الخاصة بتجربة تمثيلية ؛ كانت كل مجموعة في المتوسط من ثلاثة إلى أربعة أطباق ثقافية. يتم التعبير عن جميع البيانات على أنها متوسط ± SEM. تم تحليل النتائج بواسطة ANOVA. تم اعتبار القيم p الأقل من 0. 05 مهمة.

مكافحة مرض باركنسون:استخراج سيستانش
النتائج
التأثيرات السامة للخلايا للباراكوات في خلايا E18
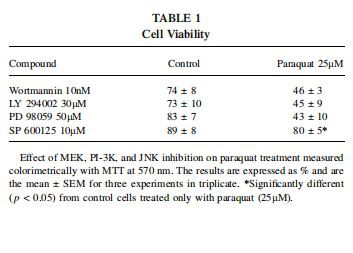
كما ورد سابقًا (Cappelletti et al. ، 1998 ؛ Chun et al. ، 2001 ؛ Gonzalez-Polo et al. ، 2004) ، فإن العديد من سلالات الخلايا حساسة للخصائص السامة للباراكوات. تسبب التعرض للباراكوات في انخفاض مرتبط بالجرعة في حيوية الخلية. (الشكل 1) في هذه الدراسة ، أظهرت الخلايا E18 المعالجة بباراكوات 25 لترًا لمدة 24 ساعة فقدًا بنسبة 50 في المائة في صلاحية الخلية. تم تقييم صلاحية الخلية عن طريق قياس التحول إلى MTT إلى صبغة فورمازان تمتص الضوء عند 570 نانومتر. يستخدم هذا الاختبار على نطاق واسع لرصد موت الخلايا في العديد من سلالات الخلايا ، بما في ذلك خلايا E18 (Donaire et al. ، 2005 ؛ Garcia-Roman et al. ، 2001) ، وإهانات مختلفة ، بما في ذلك الباراكوات (Chun et al. ، 2001 ؛ Gonzalez). -بولو وآخرون ، 2004).

التنشيط المستحث بالباراكوات لـ ERK1 / 2 في خلايا E18
تمت مراقبة الزيادات في تنشيط ERK1 / 2 في خلايا E18 المعالجة بالباراكوات بواسطة النشاف الغربي باستخدام الجسم المضاد ERK1 / 2 (Thr202 / Tyr204) الفسفوري. أدى تعريض خلايا الخلايا الأروماتية العصبية E18 مع باراكوات 25lM إلى زيادة ملحوظة في حالة الفسفرة (Thr202 / Tyr204) لـ ERK1 / 2 (44/42 كيلو دالتون) (الشكل 2 أ). حدثت الزيادات القصوى في الفسفرة بعد 5 دقائق ، وبعد ذلك تنخفض مستويات الفسفرة ببطء إلى ما يقرب من المستويات القاعدية. علاوة على ذلك ، لم تكن الزيادات في الفسفرة ERK1 / 2 التي يسببها الباراكوات تعتمد على التركيز (الشكل 2 ب). المعالجة المسبقة بمثبط MEK1 ، PD(مرض الشلل الرعاش)98059 (50lM ؛ Dudley et al. ، 1995) منع تمامًا الزيادات التي يسببها الباراكوات في ERK1 / 2 فسفرة (الشكل 3).


التنشيط المستحث بالباراكوات لـ PKB في خلايا E18
تم اكتشاف تنشيط PKB في خلايا E18 عن طريق النشاف الغربي باستخدام جسم مضاد خاص بالفوسفو (Ser473). أدى تحفيز خلايا E18 باستخدام 25lM باراكوات إلى زيادة ملحوظة في فسفرة PKB (الشكل 4 أ). تحدث هذه الزيادة بعد 20 دقيقة ، وهي مماثلة لتلك الخاصة بـ ERK1 / 2 الفسفرة بعد انخفاض مستويات الفسفرة ببطء إلى ما يقرب من المستويات القاعدية (الشكل 4 أ). علاوة على ذلك ، كانت الزيادات التي تتم بوساطة الباراكوات في فسفرة PKB تعتمد على التركيز بحد أقصى عند 25 لترًا من الباراكوات (الشكل 4 أ). نظرًا لأن PI -3 K مطلوب لتنشيط PKB ، فقد تم استكشاف دور PI -3 K في تنشيط PKB الناجم عن الباراكوات في خلايا E18 باستخدام مثبطات PI -3 K wortmannin و LY 294002.

تم حظر الزيادات بوساطة الباراكوات في فسفرة PKB تمامًا بعد المعالجة المسبقة (30 دقيقة) لخلايا E18 مع 100 نانومتر من الورتمانين و 30 ملي LY 294002 (الشكل 5). توضح هذه الملاحظات أن المسار المعتمد على PI -3 K يتوسط الزيادات التي يسببها الباراكوات في فسفرة PKB في خلايا E18.

تنشيط مستحث بالباراكوات لـ JNK1 / 2 في خلايا E18
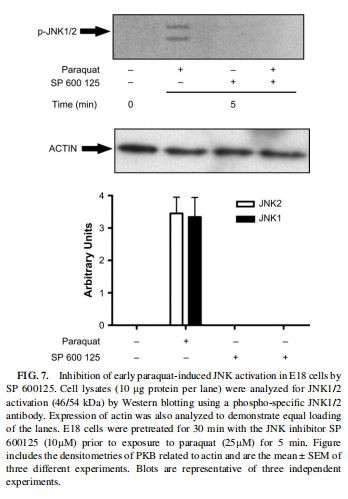
أظهرت الدراسات السابقة أن الباراكوات ينشط JNK1 / 2 في الخلايا العصبية (Chun et al.، 2001؛ Peng et al.، 2004) والخلايا غير العصبية (Bennett et al.، 2001؛ Cheng et al.، 2003). ومع ذلك ، فإن التركيزات المستخدمة أعلى إلى حد كبير من تلك المستخدمة في هذا العمل. بالإضافة إلى ذلك ، فإن الأوقات المحددة لتصور تنشيط JNK1 / 2 أطول أيضًا. تم اكتشاف تنشيط JNK1 / 2 في خلايا E18 عن طريق النشاف الغربي باستخدام جسم مضاد JNK (Thr183 / Tyr185) الفوسفوري. أدى تحفيز خلايا E18 باستخدام 25lM باراكوات إلى زيادة ملحوظة ومبكرة في فسفرة JNK (46/54 كيلو دالتون) (الشكل 6 أ). كانت هذه الزيادات قصوى بعد 5 دقائق وبعد ذلك انخفضت مستويات الفسفرة نحو المستويات القاعدية (الشكل 6 أ). ومع ذلك ، لم تكن الزيادات الوسيطة في الفسفرة JNK1 / 2 تعتمد على التركيز (الشكل 6 ب). كانت الزيادات بوساطة الباراكوات في الفسفرة JNK1 / 2 حساسة لمثبط JNK1 / 2 SP 600125 (10lM ؛ الشكل 7 ؛ بينيت وآخرون ، 2001). أخيرًا ، لم يحفز الباراكوات (25lM) زيادات قابلة للقياس في فسفرة p38 MAPK في خلايا E18 في نفس تجارب الدورة الزمنية (البيانات غير معروضة). تم إجراء هذه التجارب باستخدام الجسم المضاد p38 MAPK (Thr180 / Tyr182) الفوسفوري.

قياس قابلية بقاء الخلية بعد معالجة خلايا E18 بمثبطات الباراكوات والكيناز
بعد أن أظهرنا أن الباراكوات ينتج في جميع الحالات تنشيطًا مبكرًا ERK1 / 2 و PKB و JNK1 / 2 في خلايا E18 ، حددنا لاحقًا دور التنشيط السريع لمسارات كيناز هذه في موت الخلايا الناجم عن انخفاض تركيزات الباراكوات باستخدام محدد دوائي. مثبطات. كما هو مبين في الشكل 1 ، فإن تعرض خلايا E18 إلى 25 ميكرون من الباراكوات يسبب انخفاضًا كبيرًا في قابلية الخلية للحياة (حوالي 50 بالمائة). للتحقيق في دور ERK1 / 2 و PKB و JNK1 / 2 في موت الخلايا الناجم عن الباراكوات ، تم تحضين خلايا E18 مسبقًا لمدة 30 دقيقة باستخدام مثبطات الكيناز التالية: PD(مرض الشلل الرعاش)98059 (50lM ؛ MEK1 / 2inhibitor) ، LY 294002 (30lM ؛ مثبط PI -3 K) ، وورتمانين (100 نانومتر ؛ مثبط PI -3 K) ، و SP 600125 (10lM ؛ مثبط JNK1 / 2). كما هو مبين في الشكل 8 (وتم تلخيصه في الجدول 1) ، لم يكن لـ Wortmannin و LY 294002 و PD 98059 أي تأثير كبير على فقدان قابلية الخلية للبقاء الناجم عن 25lM باراكوات.

نقاش
في الآونة الأخيرة ، زادت الدراسات المختلفة من الاهتمام بإمكانية أن تكون السموم العصبية البيئية مثل مبيدات الآفات مرتبطة بتطور اضطراب الشخصية الحركية غير الجيني.(مرض الشلل الرعاش)(Cory Slechta et al.، 2005؛ Landrigan et al.، 2005؛ Norris et al.، 2004؛ Ritz and Yu، 2000؛ Sherer et al.، 2001). PQ هو أحد مبيدات الأعشاب المحتملة التي تدخل في PD ، بسبب التركيب الكيميائي المشابه لـ MPPþ والعلاقة القوية بين حدوث المرض وكمية PQused (Lanska ، 1997 ؛ Liou et al. ، 1997 ؛ Ritz و يو ، 2000). ومع ذلك ، لم يتم تحديد آلية السمية العصبية التي تحدث بسبب نقص التعرض لمستويات منخفضة من الباراكوات. على أي حال ، فإن الأعمال السابقة ليست مهتمة بالعملية المبكرة التي تم إثباتها بعد التعرض للباراكوات. الاكتشاف الرئيسي للدراسة الحالية هو أننا أظهرنا أن خلايا الأرومة العصبية E18 التي تعرضت لتركيزات منخفضة من الباراكواترامية زادت بشكل كبير من الفسفرة النشطة لمسارات الإشارات المضادة للخلايا بشكل عام PI -3 K / PKB و MEK ERK وأيضًا proapoptotic JNK1 / 2 خريطة. في المقابل ، لم يحفز الباراكوات الزيادات القابلة للقياس المعتمدة على الوقت أو التركيز في الفسفرة p38 MAPK. كما هو مبين أعلاه ، استخدمنا تركيزًا منخفضًا من الباراكوات. تمت مناقشة أهمية حقيقة ما إذا كان الباراكوات يمكن أن يدخل الدماغ أم لا لأنه جزيء مشحون. ومع ذلك ، كشفت النتائج الحديثة (Shimizu et al. ، 2001) أن الباراكوات يمكن أن يستخدم مضخة الأحماض الأمينية المحايدة للوصول إلى الدماغ. تشير النتائج المقدمة في هذا العمل إلى أن هناك حاجة إلى تركيز منخفض فقط من الباراكوات في الخلية لتحفيز العديد من مسارات الإشارات بسرعة ، بما في ذلك NK ، المتورط في عمليات موت الخلايا. تم اقتراح عمليات التنشيط المبكرة هذه بسبب التركيز المنخفض للباراكوات ، لأول مرة ، في العمل الحالي.
تم تخصيص القليل من الاهتمام لدراسة التغيرات في مستويات الفسفرة لـ PKB أو ERK1 / 2 التي يسببها الباراكوات (Cheng et al. ، 2003 ؛ Peng et al. ، 2004). على أي حال ، تستخدم التقارير السابقة (Peng et al. ، 2004) تركيزات عالية نسبيًا من الباراكوات (400 مل) ، تقيس درجة الفسفرة من ERK بعد 12-18 ساعة من التعرض. في هذه الأوقات ، لم يلاحظوا التغييرات في مستويات p-ERK. في عملنا ، اكتشفنا تنشيطًا مبكرًا (5-10 دقائق) ومهمًا لـ ERK1 / 2 (الشكل 2 أ). هذا التنشيط ينخفض ببطء إلى المستويات القاعدية. في ظروفنا ، تكون مستويات ERK1 / 2 الفسفرة (بعد 12-18 ساعة) هي نفسها الموجودة في عنصر التحكم ، مما يشير إلى أن هذا المسار غير نشط في هذه الأوقات (البيانات غير معروضة) كما وصفها Peng et al. (2004). لا يعتمد هذا التنشيط على التركيز ، مما يشير إلى النتيجة المتمثلة في الحصول على التحفيز القوي لـ ERK والحفاظ عليه بتركيزات منخفضة جدًا من الباراكوات. لم يتم بعد وصف التغييرات في مستويات PKB المفسفرة بعد التعرض للباراكوات. نوضح في الشكل 4 أن النتائج تعتمد على الوقت والتركيز ، وتظهر أقصى تأثير بعد 20- دقيقة من التعريض مع 25 لومن باراكوات. أي أن الزيادات المبكرة بوساطة الباراكوات في فسفرة PKB يمكن مقارنتها مع تلك الملاحظة forERK1 / 2. تكشف هذه البيانات عن زيادة مبكرة في تنشيط الفسفرة لكل من مسارات البقاء على قيد الحياة PKB و ERK. لا توجد بيانات عن التنشيط المبكر لـ PKB أو ERK في موت الخلايا الناجم عن الباراكوات. ومع ذلك ، تصف الدراسات السابقة (Halvorsen et al. ، 2002) زيادة مبكرة مماثلة في كلا المسارين في خلايا الورم الأرومي العصبي SH-SY5Y المعرضة لـ MPPþ ، وفي هذه الحالة ، لا تتحلل مستويات الفسفرة نحو المستوى الأساسي. هذه البيانات مثيرة للاهتمام بشكل خاص بسبب البنية المماثلة المرتبطة سابقًا بين الباراكوات و MPPþ ، مما يشير إلى بداية مختلفة للآلية الخلوية المتورطة في تأثير كلا الجزيئين.
تم تكريس مزيد من الاهتمام لدور مسار JNK1 / 2 في التوسط في الإشارات التي تساهم في موت الخلايا الناجم عن الباراكوات. في هذه الدراسة ، أظهرنا أن التركيزات المنخفضة (25 لترًا) من الباراكوات أدت إلى زيادات كبيرة في الفسفرة JNK1 / 2 (الشكل 6). كما يحدث في PKBor ERK1 / 2 ، يعتمد هذا التنشيط على الوقت مع بداية مبكرة جدًا (5 دقائق) وعودة بطيئة إلى المستويات الأساسية. تظهر الأعمال السابقة (Cheng et al.، 2003؛ Chun et al.، 2001؛ Peng et al.، 2004) عمليات التنشيط المتأخرة (12-18 ساعة) لمسار JNK1 / 2 التي تنتج في أي حال عن طريق تركيزات عالية نسبيًا من الباراكوات (من 400 ملي مولار). [Peng et al.، 2004] to 800lM [Chunet al.، 2001]). في ظروفنا ، تكون درجة الفسفرة لـ JNK1 / 2 في الأوقات المشار إليها قابلة للمقارنة مع عنصر التحكم. بشكل عام ، تشير هذه النتائج لأول مرة إلى أن تعرض الخلايا لتركيز منخفض جدًا من الباراكوات ينتج عنه تنشيط مبكر لمسارات PKB و ERK1 / 2 و JNK1 / 2.
بعد أن أثبتنا أن الباراكوات يتسبب في تنشيط PKB و ERK1 / 2 و JNK1 / 2 مبكرًا في خلايا E18 ، قمنا بعد ذلك بالتحقيق في دور مسارات البروتين كيناز هذه في موت الخلايا الناجم عن الباراكوات باستخدام عدة مثبطات دوائية. تمت مراقبة حيوية الخلية عن طريق قياس التحول إلى MTT إلى صبغة فورمازان تمتص الضوء عند 570 نانومتر. تم استخدام اختبار MTT لقياس إصابة الخلايا العصبية بدقة بعد مجموعة متنوعة من الإهانات بما في ذلك MPPþ أو الباراكوات (Gonzalez Polo et al. ، 2003 ، 2004 ؛ Schmuck et al. ، 2002 ؛ Sheng et al. ، 2002 ؛ Storch et al. ، 2004 ) ، وهي الطريقة الأكثر استخدامًا لتحديد موت الخلايا. كما هو مبين في الشكل 8 ، أدت المعالجة المسبقة باستخدام مثبط JNK1 / 2 الانتقائي SP 600125 إلى خفض موت الخلايا الناجم عن الباراكوات بشكل كبير. أدى تركيز SP 600125 هذا إلى منع التنشيط الناجم عن الباراكوات لـ JNK1 / 2 (الشكل 7). تشير هذه البيانات إلى أن تثبيط التنشيط المبكر لمسار JNK1 / 2 يحمي الخلايا من موت الخلايا الناجم عن الباراكوات. تتوافق هذه البيانات مع الدراسات السابقة (Chun et al. ، 2001 ؛ Peng et al. ، 2004) ، التي أظهرت أن JNK1 / 2 متورط في موت الخلايا العصبية الناتج عن الباراكوات. ومع ذلك ، تستخدم هذه الدراسات ما بين 15 و 30 مرة من تركيز الباراكوات أكثر من تلك المستخدمة في هذه الدراسة. كما أوضحنا أيضًا أن التركيزات المنخفضة من الباراكوات يمكن أن تنتج ليس فقط تنشيطًا ولكن أيضًا تنشيطًا مبكرًا لهذا المسار. تشير الحماية التي لوحظت في SP600125 أيضًا إلى أن مسار JNK1 / 2 متورط في موت الخلايا الناجم عن الباراكوات. بالإضافة إلى ذلك ، تم تصميم تثبيط JNK1 / 2 كإستراتيجية محتملة في علاج شلل الرعاش(مرض الشلل الرعاش)في العديد من النماذج في كل من الجسم الحي وفي المختبر (Wang et al. ، 2004).

تأثير اعصاب cistanche
أظهرت الدراسات السابقة أن كلا من PKB و ERKpathways متورطان في بقاء الخلايا العصبية (Guyton et al. ، 1996 ؛ Shin et al. ، 2001). في هذه الدراسة ، أظهرنا أن التركيزات المنخفضة من إنتاج الباراكوات تحفز مبكرًا كل من مسارات PKB و ERK. تشير هذه الملاحظات إلى أن تنشيط PKB و ERK الناجم عن الباراكوات قد يكون متورطًا في حماية الخلايا من موت الخلايا الناجم عن الباراكوات. للتحقيق في هذا الاحتمال ، استخدمنا مثبطات PI -3 K wortmannin و LY 294002 ومثبط ERK1 / 2 PD(مرض الشلل الرعاش)98059. ومن المثير للاهتمام أن كلا من تثبيط PKB و ERK لم يغير من قابلية الخلية للحياة في وجود الباراكوات ، مما يشير إلى أنه في ظروفنا ، فإن زيادة تنشيط PKB و ERK ليس ضروريًا للبقاء على قيد الحياة في موت الخلايا الناجم عن الباراكوات في خلايا E18.
من المعروف أن آلية السمية العصبية للباراكوات تتم ، من بين عوامل أخرى ، بوساطة الإجهاد التأكسدي (Gonzalez-Polo et al.، 2004؛ Mollace et al.، 2003). بهذا المعنى ، تم مؤخرًا وصف إجهاد مؤكسد خلوي سريع جدًا في أحداث موت الخلايا المبرمج المبكرة المتورطة في موت الخلايا الناجم عن الباراكوات (Gonzalez-Polo et al. ، 2004). نظرًا لأن الإجهاد التأكسدي ينشط أفراد عائلة MAPK (مثل ERK1 / 2 و JNK1 / 2) و PKB (كاماتا وهيراتا ، 1999) ، فإن هذا التنشيط المبكر لـ ERK1 / 2 و JNK1 / 2 و PKB يمكن أن يعزى إلى الأكسدة السريعة الناجم عن الإجهاد بعد تعرض الباراكوات.
باختصار ، تُظهر نتائجنا لأول مرة أن التركيزات المنخفضة من الباراكوات تحفز زيادات مبكرة جدًا وقوية في فسفرة PKB و ERK1 / 2 و JNK1 / 2 في خلايا E18. بالإضافة إلى ذلك ، أظهرنا أن تثبيط التنشيط المبكر لمسار JNK1 / 2 يحمي خلايا E18 من موت الخلايا الناجم عن الباراكوات. تشير هذه النتيجة إلى وجود بعض الأحداث المبكرة (مثل تنشيط JNK1 / 2 السريع) التي تلعب دورًا أساسيًا في موت الخلايا الناجم عن انخفاض تركيزات الباراكوات. تفتح هذه النتيجة أيضًا خطًا جديدًا ومثيرًا في دراسة سمية الباراكوات وآثارها المحتملة في تطور PD(مرض الشلل الرعاش).
ملاحظة: سيستانشهو عشب صيني تقليدي له تأثيرات على الخلايا العصبية وخلايا الدماغ. يُعرف أيضًا باسم الجينسنغ الصحراوي ، وهو علاج محتمل لأمراض الأعصاب مثلمرض الشلل الرعاشبناءً على الدراسة الدوائية الحديثة
