الميكروبيوم: المستقلب يكشف عن مساهمة محور الأمعاء والكلى في أمراض الكلى
Feb 22, 2022
يوان ‑ يوان تشن1†دان تشيان تشن1†وآخرون
الملخص
يمثل دسباقتريوز التغييرات في تكوين وهيكل مجتمع ميكروبيوم الأمعاء (الميكروبيوم) ، والتي قد تملي النمط الظاهري الفسيولوجي (الصحة أو المرض). أدت التطورات التكنولوجية الحديثة والجهود المبذولة في التحليلات الميتاجينومية والأيضية إلى نمو كبير في فهمنا للميكروبيوم ، ولكن لا تزال الآليات الكامنة وراء تفاعلات ميكروبيوم الأمعاء في الحالة الصحية أو المرضية بعيدة المنال وتوضيحها في مرحلة الطفولة. قد يؤدي اختلال الجراثيم المعوية الطبيعية إلى خلل نشاط الأمعاء ، واختلال وظيفي في الحاجز المعوي ، والانتقال البكتيري. يتم إنتاج السموم المفرطة اليوريمية نتيجة لتغير ميكروبيوتا الأمعاء ، بما في ذلك كبريتات الإندوكسيل ، كبريتات p ‑ cresyl ، وتراي ميثيل أمين N oxide ، وكلها متورطة في العمليات المتغيرة لـالكلىالأمراضتطوير. تركز هذه المراجعة على العلاقة المسببة للأمراض بين ميكروبيوتا الأمعاء وأمراض الكلى (محور الأمعاء والكلى) ، وتغطيكد، إعتلال الكلية بالجلوبيولين المناعي، تحص الكلية، ارتفاع ضغط الدم الحادالكلىإصابةوغسيل الكلى وغسيل الكلى البريتوني في العيادة. تتم مناقشة التدخلات المستهدفة بما في ذلك التدابير الحيوية ، والبريبايوتيك ، والتكافل من حيث قدرتها على إعادة إنشاء التعايش ، والاستراتيجيات الأكثر فعالية لعلاجالكلى الأمراضيقترح المرضى. تساعد الرؤى الجديدة في دسباقتريوز في ميكروبيوتا الأمعاء في أمراض الكلى في تطوير استراتيجيات علاجية جديدة للوقاية من أمراض الكلى ومضاعفاتها أو تخفيفها.
الكلمات الدالة:الميكروبيوم ، ميكروبيوتا الأمعاء ، الأيض ،الكلىالأمراض، البروبيوتيك
اتصال:joanna.jia@wecistanche.com/ واتساب: 008618081934791

خلفية
إن الكائنات الحية الدقيقة الموجودة في الأمعاء البشرية السليمة عبارة عن مجتمع معقد يضم أكثر من 100 تريليون خلية ميكروبية من بينها أكثر من 1000 نوع مختلف [1]. في حالة صحية ، تعيش هذه الميكروبات في علاقة تكافلية مع مضيفها ، وتعديل جهاز المناعة ، والحماية من مسببات الأمراض ، وتنظيم التمثيل الغذائي الداخلي للكربوهيدرات والدهون ، وبالتالي المساهمة في التوازن الغذائي [2]. ترتبط التغيرات في الميكروبيوم بشكل متزايد بتطور أمراض مختلفة مثل السمنة والسرطان والسكري ومرض التهاب الأمعاء وأمراض القلب والأوعية الدموية والكلىمرض[3]. يوضح الشكل 1 دسباقتريوز الميكروبيوم المعوي على تأثير الأمراض المختلفة. دسباقتريوز في ميكروبيوتا الأمعاء قد تورط في تطور مختلفالكلىالأمراض[4-10]. في الواقع ، غالبًا ما يُلاحظ dysbiosis في حالات اليوريمي المميزة للاحتفاظ بالسموم البوليسية ، والتي ينشأ معظمها من التخمير غير المتوازن لمستقلبات النيتروجين. تساهم هذه السموم البوليسية في تطور ومضاعفات مرض الكلى المزمن [11-15].

تركز هذه المراجعة على العلاقة المسببة للأمراض بين ميكروبيوتا الأمعاء والكلىأمراض (القناة الهضمية-الكلىالمحور) ، ولمس مرض الكلى المزمن ، وغسيل الكلى ، وغسيل الكلى البريتوني ، واعتلال الكلية المناعي أ (IgAN) ، وتحصي الكلية ، وارتفاع ضغط الدم ، والحادةالكلىإصابةمرضى (AKI). نظرًا لأننا نفكر في الدراسات ذات الصلة ونلخص النتائج المتراكمة ، توصلنا إلى ملاحظة مفادها أن البريبايوتكس والبروبيوتيك بالإضافة إلى مزيجهما من العلاجات المساعدة الهامة لعلاج مرض الكلى المزمن. توفر جراثيم الأمعاء ديسبيوتيك هدفًا علاجيًا محتملاً للوقاية من المضاعفات أو الاستفادة منها.
تطبيق مناهج ميكروبيوم الأمعاء لدراسة الميكروبات المعوية
لقد سهّل إنشاء تقنيات التسلسل المتقدمة من الجيل التالي ، بما في ذلك التحليل الجيني وتحليل تسلسل الحمض الريبي النووي الريبوزي 16S (rRNA) ، تحليل عدد أكبر بكثير من الكائنات الحية الدقيقة في الأمعاء. كلا النهجين لهما مزايا فريدة خاصة بهما. يهدف التسلسل الميتاجينومي إلى تحديد "ما يمكنهم فعله" عن طريق التسلسل العشوائي لجميع الحمض النووي المستخرج في العينة [16] ، بينما كان تحليل الرنا الريباسي 16S أكثر فائدة في العثور على "من هناك؟" من خلال تسلسل جين الرنا الريباسي 16S المحفوظ والموجود في جميع البكتيريا [17]. يعتمد التحليل الوظيفي بواسطة ميتاجينوميات البندقية بشكل كبير على معرفتنا الأساسية بكيفية ترميز تسلسل الجينات للوظائف الأنزيمية أو وظائف أخرى ، وتعد قواعد البيانات الأيضية مثل KEGG و MetaCyc موارد رائعة في هذا الصدد. يلخص الشكل 2 بعض المنهجيات المستخدمة في دراسة الميكروبيوم. على الرغم من بعض التقدم في سير عمل تسلسل الميكروبيوم ، تواجه أبحاث ميكروبيوم الأمعاء العديد من التحديات. إن الفهم المحدود للوظيفة الميكروبية في السببية المرضية يعيق بشدة توليد الفرضيات المتعلقة بالروابط الميكانيكية المعقدة بين ميكروبيوم الأمعاء والأمراض. يمكن لعلم الأيض أن يوفر بعض المعلومات المهمة في ميكروبيوم الأمعاء.

تم تعريف علم الأيض على أنه "القياس الكمي للاستجابة الأيضية الديناميكية متعددة المعلمات للكائنات الحية للتحفيز الفيزيولوجي المرضي أو التعديلات الجينية" [18-21]. كأداة مهمة لفهم وظيفة ميكروبيوتا الأمعاء ، ظهرت الأيضات كنهج منهجي للمستقلبات الذاتية منخفضة الوزن الجزيئي ويمكن فحص تغيراتها بعد المرض ، والتعرض السام ، أو الاختلاف الجيني [22-24]. يعتبر التحليل الطيفي بالرنين المغناطيسي النووي البروتوني والنهج القائم على قياس الطيف الكتلي من الأدوات التحليلية الرئيسية لبحوث الأيض [24 ، 25]. كمنصة تحليلية قوية ، تم مؤخرًا تطبيق المستقلبات على نطاق واسع لتسهيل تشخيص الأمراض المختلفة والتنبؤ بها ، واكتشاف العلامات الحيوية ، والتطوير الصيدلاني ، وتقييم فعالية / سمية الأدوية [26-31]. تم استخدام الأيض على نطاق واسع في دراسات أمراض الكلى المختلفة [18-20]. ومع ذلك ، فإن تطبيق المستقلبات على العينات المتأثرة بالميكروبيوم المعوي من أمراض الكلى أمر نادر الحدوث. هذه الدراسة ضرورية لفهم الروابط بين ميكروبيوتا الأمعاء وأمراض الكلى.
بشكل عام ، فإن مرحلة الطفولة في بيانات كل من ميكروبيوم الأمعاء وبيانات الأيض تستدعي الحاجة إلى تعزيز آلياتنا وأنماطنا الظاهرية في الروابط بين ميكروبيوتا الأمعاء وأمراض الكلى من خلال بحث متعدد النوى.

الحديث المتبادل الكامن وراء محور الأمعاء والكلى
ميكروبيوم الأمعاء كمصدر محتمل للسموم البوليسية
يتم تصنيف السموم اليوريمية تقليديا على أساس الخصائص الفيزيائية والكيميائية التي تؤثر على إزالتها أثناء غسيل الكلى. يحتوي Tese على جزيئات منخفضة الذوبان في الماء (الوزن الجزيئي <500 da)="" ،="" والجزيئات="" المتوسطة="" الأكبر="" (الوزن="" الجزيئي=""> 500 Da) ، والجزيئات المرتبطة بالبروتين. يمكن أيضًا تصنيف السموم اليوريمية بناءً على موقعها الأصلي: داخلية (استقلاب الثدييات) ، خارجية (نظام غذائي) ، أو جرثومية. حاليًا ، تشتمل السموم البوليسية المعروفة المشتقة من الأمعاء على كبريتات الإندوكسيل ، وكبريتات p-cresyl ، وحمض الأسيتيك الإندول -3 ، و TMAO ، و phenylacetylglutamine ؛ تم العثور على هذه مرتبطة بأمراض القلب والأوعية الدموية ، والوفيات في CKD ، وغيرها من سمية الأعضاء الطرفية.
يتم إنتاج كبريتات الإندوكسيل وحمض الأسيتيك {0}} عن طريق استقلاب التربتوفان الغذائي [32 ، 33]. يتم استقلاب التربتوفان في الإندول بواسطة التربتوفاناز من البكتيريا المعوية مثل الإشريكية القولونية. بعد الامتصاص المعوي ، يتم كبريت الإندول إلى كبريتات الإندوكسيل في الكبد. عادة ما تفرز كبريتات الإندوكسيل في البول. لا يمكن تنظيفه بكفاءة عن طريق غسيل الكلى التقليدي نظرًا لارتباطه الشديد بالألبومين [34].
يتم إنتاج p-Cresol / p-cresyl sulfate من تقويض فينيل ألانين وتيروزين بواسطة بكتيريا الأمعاء اللاهوائية. يتم تصريف p-Cresol بواسطة الميكروبات المعوية إلى p-cresyl sulfate و p-cresyl glucuronide. كبريتات p-Cresyl هي مادة سامة بسبب تركيزها المنتشر العالي وتأثيرها الكيميائي الحيوي على الجسم [35]. يترافق p-Cresol أيضًا في الكبد ويمكنه التنافس مع المواد الغريبة الحيوية التي لها بنية أو جزء متشابه في هيكلها العظمي ، والتي بدورها يمكن أن تؤثر على خصائصها الحركية الدوائية / الدوائية (بما في ذلك السمية / الآثار الضارة) [25] .
TMAO هو مستقلب سام مشتق من الأمعاء من الأيض البكتيري للأمينات الرباعية التي تشمل البيتين ، إل كارنيتين ، أو فوسفاتيديل كولين الذي يطلق ثلاثي ميثيل أمين [36]. يتم امتصاص ثلاثي ميثيل أمين وتحويله إلى TMAO عن طريق إنزيمات الفلافين مونو أوكسيجيناز في الكبد. على عكس المستقلبات السامة المرتبطة بالبروتين مثل كبريتات الإندوكسيل وكبريتات p-cresyl ، يمكن إزالة TMAO بكفاءة عن طريق غسيل الكلى.
Phenylacetylglutamine هو منتج ميكروبي آخر في القولون ، ينتج من تخمر فينيل ألانين. تقوم الميكروبات باستقلاب فينيل ألانين إلى حمض فينيل أسيتيك ، والذي يخضع لاقتران الجلوتامين لتكوين فينيل أسيتيل جلوتامين. مثل TMAO ، فهو قابل للتبديل. تم إثبات أن حالة اليوريمي تحفز التغييرات في ميكروبيوتا الأمعاء. على الرغم من عدم وجود فروق ذات دلالة إحصائية في الكمية الإجمالية للكائنات الحية الدقيقة ، فقد تم وصف تآكل البكتيريا الهوائية بواسطة البكتيريا اللاهوائية (خاصة Lactobacillus و Bifidobacterium) [37 ، 38]. عززت الزيادة في البكتيريا اللاهوائية تحلل مركبات النيتروجين في حالة اليوريمي المتدهورة [39].
دسباقتريوز من ميكروبيوتا الأمعاء والخلل الوظيفيالحاجز الظهاري المعوي
ظهارة الأمعاء هي طبقة واحدة من الخلايا الظهارية العمودية التي تفصل تجويف الأمعاء عن الصفيحة المخصوصة الكامنة [40]. يلعب دورًا مهمًا في امتصاص العناصر الغذائية وهو حاجز طبيعي يمنع أو يثبط الانتقال الجهازي لمسببات الأمراض والمستضدات [40]. ترتبط هذه الخلايا ببعضها البعض عن طريق تقاطعات ضيقة ، وتشكل معقدًا متعدد الوظائف كختم بين الخلايا الظهارية المجاورة [40]. تعمل بكتيريا البروبيوتيك على تحسين وظيفة الحاجز الظهاري المعوي في كل من الحيوانات والبشر [41]. نتج عن معالجة الطبقات الأحادية للخلايا الظهارية البشرية بالمستقلبات من الرضع Bifidobacterium زيادة في بروتينات الوصلة الضيقة ZO -1 والإكلودين مع انخفاض في الكلودين -2 ، ومن ثم تمت الإشارة إلى انتقائية الوصلة الضيقة [42]. علاوة على ذلك ، تساعد البكتيريا المتعايشة في الحفاظ على الحاجز الظهاري المعوي عن طريق قمع التهاب الأمعاء [43].
أولاً ، يتم تحلل اليوريا بواسطة اليوريا لإنتاج الأمونيا والكاربامات التي تتحلل تلقائيًا لإنتاج جزيء ثانٍ من الأمونيا والبيكربونات. ثم تخضع الأمونيا لتفاعل حمضي مع الماء لإنتاج هيدروكسيد الأمونيوم. ينتشر اليوريا في الدم في تجويف الأمعاء ويتم استقلابه بواسطة اليورياز المشتق من البكتيريا ، مما ينتج NH3 المتحلل بالماء إلى NH4OH ، مما يؤدي إلى تآكل الحاجز الظهاري [38 ، 44]. أدى هذا إلى تحفيز تدفق الكريات البيض ، مما أثار الآلية الثانية حيث تسبب الالتهاب المحلي وإنتاج السيتوكين في التراجع والالتقام الخلوي لبروتينات الوصلة الضيقة عبر الخلايا (كلودين وإوككلودين) [45]. كما ذكرنا سابقًا ، كان SCFA من بكتيريا الأمعاء مصدرًا مهمًا للمغذيات للخلايا المعوية ، ومن الناحية النظرية ، أدى التحول في السكان البكتيريين إلى تعريض صحة الحاجز الظهاري للخطر.
ميكروبيوم الأمعاء في مرضى الكلى
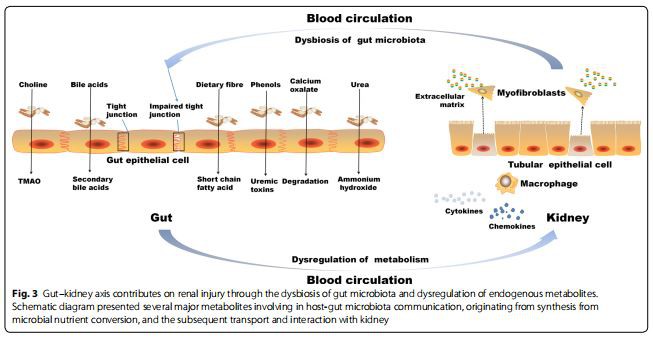
ارتبطت أمراض الكلى باحتقان جدار الأمعاء ، وذمة جدار الأمعاء ، وبطء عبور القولون ، والحماض الأيضي ، والاستخدام المتكرر للمضادات الحيوية ، وانخفاض استهلاك الألياف الغذائية ، وتناول الحديد عن طريق الفم ، مما يؤثر على الوصلات الضيقة المعوية ، مما يؤدي إلى زيادة نفاذية الأمعاء وجعلها. انتقال المنتجات الأيضية البكتيرية عبر الحاجز المعوي [46-49]. نتيجة لذلك ، يتم إثارة استجابة مناعية [46]. الاستجابة المناعية تفسر الالتهاب الجهازي الذي يساهم في تدهور أمراض الكلى [3 ، 50]. علاوة على ذلك ، أدى زيادة إفراز اليوريا المعدي المعوي إلى خلل في الجراثيم في الأمعاء وزيادة تكوين الأمونيا السامة. بالإضافة إلى ذلك ، ساهمت مكملات اليوريا في مياه الشرب في تغيير ميكروبيوتا الأمعاء البكتيرية [51]. قدم الشكل 3 مساهمة محور الأمعاء والكلى في التليف الكلوي من خلال dysbiosis من ميكروبيوتا الأمعاء و dysregulation من المستقلبات الذاتية.
ميكروبيوتا الأمعاء في كد
تشير الدلائل المتزايدة إلى أن ميكروبيوم الأمعاء قد تغير في المرضى الذين يعانون من مرض الكلى المزمن. تقريبًا ، كانت 190 وحدة تصنيفية تشغيلية ميكروبية (OTU) مختلفة بشكل كبير في الوفرة عندما تمت مقارنة ميكروبيوم الأمعاء للمرضى الذين يعانون من مرض الكلى في نهاية المرحلة (الداء الكلوي بمراحله الأخيرة) مع الضوابط الصحية [52]. تم تحديد أعداد أقل من عائلات Lactobacillaceae و Prevotellaceae (كلاهما يعتبران مجهريات البقعة الطبيعية) وأنواع البكتيريا المعوية والمكورات المعوية أعلى 100 مرة (والتي توجد عادة بنسب أقل) في مرضى CKD [52]. كان عدد البكتيريا الهوائية ، بما في ذلك أنواع المكورات المعوية والبكتيريا المعوية ، أعلى في المرضى الذين يعانون من الداء الكلوي بمراحله الأخيرة منه في الضوابط الصحية [53]. ساهم دسباقتريوزيس من ميكروبيوتا الأمعاء في المرضى الذين يعانون من مرض الكلى المزمن في ارتفاع تركيز السموم البوليسية والتي بدورها عززت تطور مرض الكلى المزمن [54 ، 55]. حدث خلل في ميكروبيوتا الأمعاء في مرض الكلى المزمن من الناحيتين الكمية والنوعية ، ويصاحب ذلك في كثير من الأحيان زيادة في أنواع Lachnospiraceae و Enterobacteriaceae و Ruminococcaceae ، وانخفاض في بعض أنواع Prevotellaceae و Bacteroidaceae وخاصة Lactobacillus و Bifidobacterium [56]. تم تقليل الكمية المطلقة من مجموع البكتيريا بشكل كبير في مرضى الداء الكلوي بمراحله الأخيرة. كان بريفوتيلا سائدًا في الضوابط الصحية بينما تم إثراء بكتيرويد في مرضى الداء الكلوي بمراحله الأخيرة. تم تقليل البكتيريا المنتجة للزبدة ، بما في ذلك بيلة الورد ، والبراز ، والمطثية ، والكوبروكوكس ، وبريفوتيلا ، في مرضى الداء الكلوي بمراحله الأخيرة [57].
أشارت دراساتنا أيضًا إلى أن خلل تنظيم الإجهاد التأكسدي والالتهاب كان مرتبطًا باضطرابات استقلاب الأحماض الأمينية في الدم ، والدهون ، والبيورين ، والدهون في CKD [58 ، 59] ، والتي ترتبط بعملية التمثيل الغذائي لميكروبات الأمعاء. بالإضافة إلى ذلك ، أظهرت الدراسات السريرية الحديثة أن الدهون الثلاثية في الدم ومستوى الكوليسترول HDL والاستجابة الأيضية المتوقعة للنظام الغذائي والدواء ارتبطت بتكوين ميكروبيوتا الأمعاء [60]. ضعف السمع
ساهمت وظائف الكلى و dysbiosis من ميكروبيوتا الأمعاء في زيادة TMAO في مرضى CKD [61]. تم إعطاء عينات براز من مرضى CKD وعناصر تحكم صحية إلى الفئران C57BL / 6 المعالجة بالمضادات الحيوية ، وكان لدى الفئران التي تلقت ميكروبيوتا الأمعاء من مرضى CKD أعلى بكثير من TMAO في البلازما وتكوين مجهريات الأمعاء المختلفة من الفئران المقارنة [61]. إلى جانب ذلك ، تم استقلاب الأمونيا من اليوريا بواسطة اليورياز الجرثومي. يمكن أن تسبب الأمونيا اضطرابًا هائلاً في بنية الحاجز الظهاري المعوي ووظيفته ، مما يؤدي إلى انتقال السموم اليوريمية المشتقة من الأمعاء ، والمستضدات ، والذيفان الداخلي ، والكائنات / المنتجات الميكروبية المعوية إلى الدورة الدموية [44 ، 62 ، 63]. ارتبطت كبريتات الإندوكسيل وكبريتات p-cresyl بزيادة المؤشرات الحيوية الالتهابية في المرحلة 3-4 من مرضى CKD ، مثل الجلوتاثيون بيروكسيديز والإنترلوكين -6 [64]. كشفت دراسة أخرى أن 19 عائلة ميكروبية كانت سائدة في مرضى الداء الكلوي بمراحله الأخيرة ، و 12 عائلة تمتلك اليورياز (مرض Alteromona ، Clostridiaceae ، Cellulomonadaceae ، Dermabacteraceae ، Halomonadaceae ، Enterobacteriaceae ، Methylococcaceae ، Moraxellaceae ، المكورات الدقيقة ، والحيوية ، والحيوية. uricase (Cellulomonadaceae و Mic- rococcaceae و Dermabacteraceae و Xanthomonadaceae و Polyangiaceae) ، و 3 إنزيمات مكونة للإندول والـ p-cresyl (على سبيل المثال ، عائلة التربتوفاناز التي تمتلك: المطثيات والبكتريا المعوية 65). Prevotellaceae و Lactobacillaceae ، العائلتان اللتان تمتلكان SCFA(الزبدات) الإنزيمات المكونة ، كانت من بين العائلات الميكروبية الأربعة التي استنفدت في مرضى الداء الكلوي بمراحله الأخيرة [65].
استنادًا إلى علم الأيض ، أوضحت دراساتنا السابقة أن اضطرابات استقلاب الأحماض الأمينية والدهون والبيورين في مصل الدم [66-70] وكذلك استقلاب حمض الصفراء والفوسفوليبيد في البراز مرتبطة بفئران CKD [71 ، 72]. أدى اضطراب الحاجز المعوي في مرض الكلى المزمن إلى انتقال السموم اليوريمية المشتقة من البكتيريا إلى الدورة الدموية الجهازية ، وبالتالي التسبب في الالتهاب وتحفيز الكريات البيض. باستخدام طرق الأيض ، أوضحت دراساتنا السابقة أن خلل تنظيم الإجهاد التأكسدي والالتهاب كان مرتبطًا باضطرابات الأحماض الأمينية في الدم ، والميثيلامين ، والبيورين ، والأيض الدهني في المرضى الذين يعانون من مرض الكلى المزمن [31 ، 73-75].
ميكروبيوتا الأمعاء في المرضى الذين يخضعون لغسيل الكلى وغسيل الكلى البريتوني
من خلال استبدال وظيفة إفراز الكلى ، يهدف غسيل الكلى إلى التخلص من مجمع الأعراض المعروف باسم متلازمة اليوريمي. جعل غسيل الكلى البقاء على قيد الحياة ممكنًا لأكثر من مليون شخص في جميع أنحاء العالم ممن يعانون من الداء الكلوي بمراحله الأخيرة (الداء الكلوي بمراحله الأخيرة) مع وظائف كلية محدودة أو معدومة [76 ، 77]. من خلال طرق التمثيل الغذائي ، أشارت دراساتنا السابقة إلى أن السموم البوليسية ومنتجات النفايات في غسيل الكلى تزيل عددًا كبيرًا من المستقلبات التي تم تحديدها والتي لم يتم تحديدها بعد [78]. أظهر تحليل المصفوفات الدقيقة الجينية الميكروبيوم المعوي لمرضى الداء الكلوي بمراحله الأخيرة مع غسيل الكلى ومقارنتها مع الأفراد الأصحاء ، مما يدل على زيادة في البكتيريا (في المقام الأول Gammaproteobacteria) ، Actinobacteria ، و Firmicutes (وخاصة sub- phylum Clostridia) [52]. ومع ذلك ، أظهر مرضى غسيل الكلى المؤشرات الحيوية الالتهابية والسموم البوليسية أعلى من المرضى الذين لا يخضعون لغسيل الكلى [79]. تم ربط إنترلوكين -6 و MCP -1 ، وهما من المؤشرات الحيوية الالتهابية ، بشكل إيجابي مع كبريتات الإندوكسيل وكبريتات p-cresyl [79]. أدى انخفاض مستويات السموم اليوريمية إلى انخفاض التعبير عن المؤشرات الحيوية الالتهابية [80]. تمت مقارنة ميكروبيوم القناة الهضمية في مرضى الأطفال الذين يخضعون لغسيل الكلى بمثيلاتها لدى الأفراد الأصحاء [81]. تمت زيادة داء البكتيريا بشكل ملحوظ بينما انخفضت البكتيريا المتقلبة بشكل ملحوظ في مرضى غسيل الكلى مقارنة بالأفراد الأصحاء [81]. بالإضافة إلى ذلك ، أظهر تحليل البراز أن مرضى غسيل الكلى أظهروا انخفاضًا في عدد البكتيريا التي يمكننا إنتاجها زبدات SCFA [65].
وصفت إحدى الدراسات انخفاضًا في ثبات الأمعاء والبكتيريا الشعاعية ، وخاصة Bifidobacterium catenulatum و Bifidobacterium bifdum و Bifidobacterium long و Lactobacillus Plantarum و Lactobacillus paracasei في مرضى غسيل الكلى البريتوني [82]. بشكل عام ، أظهر مرضى CKD استعمارًا أقل للأمعاء لأنواع Bifidobacterium و Lactobacillus [56]. لذلك ، ارتبط انخفاض السكان وتنوع بكتيريا Lactobacillus و Bifdo- في مرضى غسيل الكلى البريتوني بالعديد من الآثار الضارة. أظهر مرضى غسيل الكلى البريتوني لدى الأطفال وفرة أقل نسبيًا من بكتيريا الأمعاء داخل الثوابت والبكتيريا الشعاعية ، في حين زادت البكتيريا المتقلبة بشكل ملحوظ [81]. ارتبطت زيادة البكتيريا المتقلبة (البكتيريا المؤكسدة للحديد) بمكملات الحديد عن طريق الفم في مرضى غسيل الكلى البريتوني. بالإضافة إلى ذلك ، عزز مرضى غسيل الكلى البريتوني امتصاص الأمعاء للجلوكوز من غسيل الكلى البريتوني الذي روج للبكتيريا المعوية المخمرة للجلوكوز [81]. بالنظر إلى انتقال الجراثيم المعوية إلى التجويف البريتوني ، فقد افترض أن زيادة بكتيريا الأمعاء كانت مسؤولة عن تطور التهاب الصفاق في مرضى غسيل الكلى البريتوني لأن عائلة البكتيريا المعوية شكلت ما يصل إلى 12 في المائة من جميع نوبات التهاب الصفاق لدى هؤلاء المرضى [83].
ميكروبيوتا الأمعاء في IgAN
نظرًا لوجود الغلوبولين المناعي A (IgA) على نطاق واسع في الجهاز المناعي للأمعاء المخاطية ، فإن dysbiosis من ميكروبيوتا الأمعاء يلعب دورًا في التسبب في IgAN [55]. عززت الالتهابات البكتيرية المزمنة و dysbiosis لميكروبات الأمعاء الخلايا الظهارية لإفراز عوامل تنشيط الخلايا البائية ورابطًا محفزًا للتكاثر أدى إلى تسريع الإنتاج المفرط لـ IgA. بالإضافة إلى ذلك ، تم العثور على dysbiosis من ميكروبيوتا الأمعاء في IgAN [55]. تم فحص الفروق الحصرية في الجراثيم المعوية وتكوين الأيض في المرضى الذين يعانون من IgAN والضوابط الصحية [84 ، 85] ، وتم تغيير ميكروبيوتا الأمعاء ومستقلبات المسالك البولية (بما في ذلك الأحماض الأمينية الحرة والأيضات العضوية المتطايرة) بشكل كبير بين المرضى الذين يعانون من مرضى التطور وغير المصابين. التقدم IgAN [86]. تم التكهن بأن الأحماض الأمينية الخالية من المصل المرتفعة ساهمت في أمراض IgAN ربما كانت مرتبطة بامتصاص منخفض للبروتينات المعدية المعوية ، والتي من المفترض أنها عززت تحلل البروتين الميكروبي ، وتغيرت الجراثيم ، وساهمت في ارتفاع مستوى p-cresol في البراز. توجد صلة محتملة بين عديدات السكاريد الدهنية البكتيرية ونقص الجالاكتوزيل من IgA. يمكن أن تحفز عديدات السكاريد الدهنية البكتيرية الاستجابة الالتهابية الجهازية وشاركت عديدات السكاريد الدهنية في فرط الإنتاج ونقص الجلاكتوزيل لـ IgA1 ، وهو العامل المرضي المهم المتضمن في IgAN [87].
ميكروبيوتا الأمعاء في تحصي الكلية
تحص الكلية هو مرض معقد يمكن أن يكون سببه عوامل وراثية وبيئية مختلفة. حصوات الكلى عبارة عن رواسب صغيرة تتراكم في الكلى ، وتتكون من الكالسيوم والفوسفات ومكونات أخرى من الأطعمة. فرط أوكسالات البول هو عامل خطر مهم لظهور حصوات الكلى لأن 75 بالمائة من حصوات الكلى تحتوي على أكسالات الكالسيوم [88]. نظرًا لأن جسم الإنسان يعتمد بشكل أساسي على ميكروبيوتا الأمعاء لتوازن الأوكسالات ، فقد جذبت بكتيريا Oxalo- البكتيريا الغريبة الانتباه في الطب [89]. أظهرت Te Oxalobacterformigenes ، باعتبارها بكتيريا تحلل الأكسالات في الأمعاء ، فوائد صحية من خلال استتباب حمض الأكساليك [90]. تم إثبات وجود علاقة عكسية بين حصوات الكلى المتكررة والاستعمار المعوي مع Oxalobacterformigenes ، مما أدى إلى تقليل تركيز الأكسالات الذي كان متاحًا للامتصاص بمعدلات ثابتة في الأمعاء. يمكن أن تقلل أكسالات الجراثيم من إفراز الأوكسالات في البول وتحمي من تكوين حصوات أكسالات الكالسيوم في الكلى [91 ، 92]. إلى جانب ذلك ، شارك ميكروبيوم الأمعاء في الفيزيولوجيا المرضية لتشكيل حصوات الكلى [92]. المرضى الذين يعانون من تحص الكلى يمتلكون ميكروبيوتا فريدة من نوعها في الأمعاء مقارنة مع الضوابط الصحية [93]. Bacteroides spp. كان أكثر وفرة في صانعي حصوات الكلى بينما كان Prevotella spp. كان أكثر وفرة في الضوابط الصحية [93].
بالإضافة إلى ذلك ، تم إنتاج حمض السيانوريك من الميلامين في القناة الهضمية عن طريق التحول الجرثومي وكان بمثابة مكون مكمل لحصى الكلى المسؤولة عن التسمم الكلوي الناجم عن الميلامين في الجرذان [94]. تم التعرف على الكلبسيلا لاحقًا في البراز ويمكن أن تحول الميلامين إلى حمض السيانوريك مباشرة. أظهرت الفئران التي استعمرها كلبسيلا من السكان الأصليين تسمم كلوي متفاقم يسببه الميلامين [94]. تدعم البيانات المتاحة حاليًا أن معالجة بكتيريا الأمعاء قد توفر علاجًا جديدًا لمرضى حصوات الكلى في المستقبل.
ميكروبيوم الأمعاء في ارتفاع ضغط الدم
أظهر المرضى الذين يعانون من ارتفاع ضغط الدم الانقباضي و CKD تغيرًا في التركيب البكتيري وانخفاض الثراء البكتيري [95]. ترتبط وفرة ميكروبات الأمعاء ، والعضلات الصلبة والبكتيرية ، بزيادة ضغط الدم في العديد من نماذج ارتفاع ضغط الدم [96]. تم الإبلاغ عن أن أحد المكونات الرئيسية للمسار الشمي في الكلى ، Olfr78 ، كان عبارة عن مستقبل شمي يتم التعبير عنه في الجهاز المجاور للكبيبات الكلوية ، حيث يتوسط إفراز الرينين استجابةً لـ SCFAs. كانت SCFAs عبارة عن منتجات نهائية تخمر بواسطة ميكروبيوتا الأمعاء وتم امتصاصها في الدورة الدموية [97]. هناك رابط آخر محتمل بين ميكروبيوتا الأمعاء وارتفاع ضغط الدم وهو التمثيل الغذائي للميكروبات المعوية للكولين والفوسفاتيديل كولين ، والذي يقوم باستقلاب ثلاثي ميثيل أمين إلى TMAO. تريميثيلامين وفير في اللحوم الحمراء ويمكن استقلابه عن طريق الميكروبات المعوية من الكارنيتين الغذائي ، ويمكن أيضًا استقلابه في TMAO وتصلب الشرايين المعجل في الفئران [98].
ميكروبيوم الأمعاء في إصابة الكلى الحادة
في الآونة الأخيرة ، أشارت العديد من الدراسات إلى أن الكائنات الحية الدقيقة المعوية يمكن أن تنظم القصور الكلوي الحاد. كانت إحدى الآليات الممكنة هي الإجراء الكلوي لـ SCFAs ضد إصابة نقص التروية - ضخه في النماذج. تم إنتاج SCFAs ذات الخصائص المضادة للإنفلونزا بواسطة ميكروبيوتا الأمعاء [99]. أدى العلاج بثلاثة من SCFAs (الأسيتات ، والبروبيونات ، والزبدات) إلى تحسين الخلل الكلوي وتقليل الالتهاب. علاوة على ذلك ، أظهرت بكتيريا الأمعاء تأثيرًا ودورًا أوسع في أمراض الكلى المناعية الذاتية من خلال آثارها المعدلة للمناعة ، والمعروفة بتأثيرها على استقطاب مجموعات فرعية من الخلايا التائية والخلايا القاتلة الطبيعية [32].
تدخلات البروبيوتيك والبريبايوتيك والتزامن لتخفيف اضطرابات ميكروبيوم الأمعاء في أمراض الكلى
استخدام البروبيوتيك والبريبايوتكس من العلاجات الشائعة. البروبيوتيك هي كائنات حية يتم تناولها من خلال الطعام أو المكملات الغذائية التي يمكن أن تعزز صحة المضيف. تتكون البروبيوتيك من بكتيريا حية ، مثل العصيات اللبنية ، والمكورات العقدية ، وأنواع البيفيدوباكتيريا ، والتي يمكن أن تغير ميكروبيوتا الأمعاء وتؤثر على الحالة الالتهابية لإنتاج ميكروبات أقل مسببة للأمراض وبالتالي تقلل من إنتاج السموم البوليسية. أظهرت تجربة تجريبية متعددة الجنسيات أجريت على مرضى مصابين بمرض الكلى المزمن من 3 إلى 4 انخفاضًا ملحوظًا في اليوريا في الدم وتحسين نوعية الحياة بعد العلاج باستخدام تركيبة Renadyl من Lactobacillus acidophilus و Streptococcus thermophileslus و Bifidobacterium لمدة تزيد عن 6 أشهر [100]. ومع ذلك ، فشلت المتابعة العشوائية للمحاكمة في 22 مريضًا في خفض سموم اليوريم في البلازما ولم تحسن نوعية الحياة [101]. يمكن تفسير الفوائد القليلة للبروبيوتيك من خلال التغيرات المستمرة التي يسببها اليوريا في البيئة البيوكيميائية في القناة الهضمية والنظم الغذائية والطبية التي أدت إلى بيئة غير مواتية للميكروبات التكافلية [102]. لمعالجة هذا النقص ، قامت إحدى التجارب بالتحقيق في توليفة من علاجات البروبيوتيك والبريبايوتك على مدار 6 أسابيع في مرضى الكلى المزمن CKD قبل غسيل الكلى وأظهرت انخفاض مصل كبريتات p-cresyl وتغيرات ميكروبيوم الأمعاء [103]. لذلك فإن اختيار ميكروب بروبيوتيك مهم. تسبب إدراج البكتيريا التي أعربت عن اليورياز بقصد استقلاب اليوريا المعوية في زيادة منتجات المصب NH3 و NH4OH وعزز التهاب جدار الأمعاء [102 ، 104].
البريبايوتكس عبارة عن كربوهيدرات غير قابلة للهضم تحفز بشكل انتقائي نمو ونشاط بكتيريا الأمعاء المفيدة في القولون ، مثل بكتيريا Bifidobacteria [105]. تعمل البريبايوتكس على تعزيز نمو أنواع Bifidobacteria و Lactobacilli على حساب مجموعات أخرى من البكتيريا في الأمعاء [105]. كما نظم p-inulin المخصب ببريبايوتيك قليل الفركتوز فقدان الوزن ، ومنع الالتهاب ، وتحسين وظيفة التمثيل الغذائي [105]. يتم خفض مصل p-cresol و indoxyl sulfate عن طريق تناول p-inulin عن طريق الفم في مرضى غسيل الكلى [106]. ومع ذلك ، فإن إطعام الفئران اليوريمية المعالجة بنشا مقاوم للذرة الأميلوز يمكن أن يحسن تصفية الكرياتينين ويقلل الالتهاب والتليف الكلوي [107]. نظام غذائي منخفض الألياف شبه منقى أو نظام غذائي غني بالألياف أدى إلى تحسن كبير في الأيض في مصل الدم والبول والسوائل المعوية مصحوبًا بتقليل dysbiosis من ميكروبيوتا الأمعاء [108]. تنتقل النشويات المقاومة إلى القولون غير المهضومة ويتم التمثيل الغذائي بواسطة البكتيريا إلى SCFA والتي كانت مغذيات مهمة للخلايا المعوية. أدت إضافة أوليجوفركتوز-إينولين أو النشا المقاوم إلى خفض كبير في تعميم كبريتات الإندوكسيل وكبريتات p-cresyl في مرضى غسيل الكلى [106 ، 109].
Synbiotics هي مزيج من العلاجات البريبايوتيك والبروبيوتيك. أظهر العلاج باستخدام Probinul neutro ، العلاج المتزامن ، انخفاض في البلازما الكلية p-cresol دون تحسن الأعراض المعدية المعوية في 30 مرحلة 3-4 مرضى CKD لمدة 4 أسابيع [110]. أظهرت تجربة Te SINERGY انخفاضًا في كبريتات p-cresyl في المصل ولكن ليس في كبريتات الإندوكسيل وتغيرًا إيجابيًا في ميكروبيوم البراز في 37 مرحلة من 4 إلى 5 مرضى CKD [103]. أظهر العلاج بمزيج من سلالة Lactobacillus casei Shirota و Bifidobacterium breve سلالة Yakult بالإضافة إلى galactooligosaccharides انخفاضًا كبيرًا في مصل p-cresol وتحسين كمية ونوعية البراز في تسعة مرضى غسيل الكلى لمدة أسبوعين [39]. في الآونة الأخيرة ، أظهرت دراسة متعددة المراكز أجريت على 42 مريضًا بالديلزة الدموية تحسنًا في أعراض الجهاز الهضمي وانخفاض بروتين سي التفاعلي بعد العلاج لمدة شهرين [111].
ملاحظات ختامية
أثبتت الأدلة المتزايدة وجود علاقة ثنائية الاتجاه بين ميكروبيوم المضيف والأمعاء في المرضى الذين يعانون من أمراض الكلى المختلفة. هناك حاجة ماسة لمزيد من الدراسات لتوصيف ميكروبيوم الأمعاء في أمراض الكلى واستكشاف العلاقة بين أمراض الكلى المختلفة وميكروبيوم الأمعاء. يؤدي الالتهاب المعوي وانهيار الحاجز الظهاري إلى تسريع الانتقال الجهازي للسموم البوليسية المشتقة من البكتيريا بما في ذلك كبريتات الإندوكسيل ، كبريتات p-cresyl ، و TMAO ، ويسبب إصابة الإجهاد التأكسدي للكلى والقلب والأوعية الدموية وأنظمة الغدد الصماء. في الآونة الأخيرة ، فتحت دراسة محور الأمعاء والكلى طرقًا علاجية جديدة لإدارة الالتهاب وإصابة الكلى والبوليون في الدم لمنع النتائج السلبية في مرضى الكلى المزمن. تم إجراء العديد من التدخلات الواعدة لعكس اختلال التوازن الميكروبي في الأمعاء وإبطاء تقدم أمراض الكلى. تم استخدام البروبيوتيك أو منتجاتها الثانوية لتطوير تدخلات مبتكرة تستهدف الإشارات تتفوق على الأدوية التقليدية ذات الآثار الجانبية الواضحة. يمكن أن يؤدي اختيار أنواع معينة من الكائنات الحية المجهرية ذات وظائف التمثيل الغذائي المعروفة إلى التخفيف من حالات المرض المختلفة. على سبيل المثال ، يمكن استخدام Streptococcus thermophiles لتقليل اليوريا من البولينا. مطلوب الاهتمام والفحص المستقبلي لهذه التدخلات لجلب معرفة الجراثيم إلى فوائد عملية لمرضى CKD. ومع ذلك ، تحتاج التدخلات إلى مزيد من الفحص في تجارب كبيرة قبل أن تصبح علاجًا أوليًا للمرضى المصابين بأمراض الكلى.
تم استخدام الميتاجينوميات والأيضات لاستقصاء وظيفة المستقلبات الداخلية المنشأ ذات الوزن الجزيئي المنخفض والمشتقة من ميكروبيوم الأمعاء في أمراض الكلى. إن فهم القدرات الأيضية لميكروبات الأمعاء مهم جدًا في توضيح وظائفها على الصحة والمرض. على الرغم من استخدام تحليل تسلسل 16S rRNA لمسح تكوين وبنية ميكروبيوم الأمعاء بشكل ملائم ، إلا أن المعلومات المتعلقة بآثارها الأيضية كانت محدودة بسبب المعرفة غير الكاملة في قواعد البيانات الجينومية البكتيرية. تسلسل الميتاجينوم يعقب المزيد من المعرفة بالجينات الموجودة ، لكن وظائف معظم هذه الجينات لا تزال غير معروفة. KEGG و MetaCyc هما أكثر قواعد البيانات شمولاً لربط مجموعات الجينات المتعامدة بالتفاعلات والمستقلبات. لتحقيق مزيج أكثر فعالية من الميكروبيوم والأيض لفهم الأيض الميكروبي في الأمعاء في سياق أمراض الكلى ، يجب تطوير طرق تكامل متعددة. لتعزيز فهمنا للإمكانيات الوظيفية لميكروبات الأمعاء المرتبطة بالمضيف ، يمكننا ملء الفجوات في قواعد البيانات المذكورة أعلاه من خلال تسلسل الجينوم والكيمياء الحيوية غير المستهدفة والدراسات الوظيفية. وهكذا ، حتى مع هذه التحديات الهائلة ، وجدت الدراسات المتزايدة أن الميكروبات الرئيسية وإنزيماتها / مستقلباتها هي أهداف محتملة للتدخلات الطبية في سياق أمراض الكلى. من خلال تحسين فهم التفاعل الأيضي بين الميكروبيوم والمضيف ، يمكن استكشاف البريبايوتكس والبروبيوتيك الجديدة ، وسيصبح العلاج المخصص لمرض الكلى المزمن الذي يستخدم معرفة ميكروبيوم الأمعاء وتفاعلاتها مع المضيف أمرًا ممكنًا.

يمنع Cistanche deserticola أمراض الكلى ، انقر هنا للحصول على العينة
مراجع
1. De Sordi L، Khanna V، Debarbieux L. تسهل جراثيم الأمعاء الانجراف في التنوع الجيني وإصابة الفيروسات البكتيرية. ميكروب مضيف الخلية. 2017 ؛ 22 (801-808): e803.
2. روكس إم جي ، غاريت دبليو إس. ميكروبيوتا الأمعاء ، والمستقلبات ، ومناعة المضيف. نات ريف إمونول. 2016 ؛ 16: 341-52.
3. لي دي ، تانغ WHW. الدور المساهم لميكروبات الأمعاء ومستقلباتها تجاه مضاعفات القلب والأوعية الدموية في أمراض الكلى المزمنة. سيمين نفرول. 2018 ؛ 38: 193-205.
4. Afsar B، Vaziri ND، Aslan G، Tarim K، Kanbay M. هرمونات الأمعاء وميكروبات الأمعاء: الآثار المترتبة على وظائف الكلى وارتفاع ضغط الدم. J آم سوك هيبرتنس. 2016 ؛ 10: 954–61.
5. Liu R و Hong J و Xu X و Feng Q و Zhang D و Gu Y و Shi J و Zhao S و Liu W و Wang X وآخرون. ميكروبيوم الأمعاء وتغيرات أيض المصل في السمنة وبعد تدخل فقدان الوزن. نات ميد. 2017 ؛ 23: 859–68.
6. Wu H و Esteve E و Tremaroli V و Khan MT و Caesar R و Manners ‑ Holm L و Stahlman M و Olsson LM و Serino M و Planas ‑ Felix M et al. يغير الميتفورمين الميكروبيوم المعوي للأفراد الذين يعانون من مرض السكري من النوع 2 الساذج ، مما يساهم في التأثيرات العلاجية للدواء. نات ميد. 2017 ؛ 23: 850-8.
7. Imhann F ، Vich Vila A ، Bonder MJ ، Fu J ، Gevers D ، Visschedijk MC ، Spekhorst LM ، Alberts R ، Franke L ، van Dullemen HM ، et al. التفاعل بين الجينات المضيفة وميكروبات الأمعاء الكامنة وراء ظهور مرض التهاب الأمعاء والعرض السريري. القناة الهضمية. 2018 ؛ 67: 108-19.
8. Böhm M ، Schumacher H ، Teo KK ، Lonn EM ، Mahfoud F ، Mann JFE ، Mancia G ، Redon J ، Schmieder RE ، Sliwa K ، et al. حقق ضغط الدم ونتائج القلب والأوعية الدموية في المرضى المعرضين لمخاطر عالية: نتائج ONTARGET وتجاوز التجارب. لانسيت. 2017 ؛ 389: 2226–37.
9. Levin A و Tonelli M و Bonventre J و Coresh J و Donner J ‑ A و Fogo AB و Fox CS و Gansevoort RT و Heerspink HJL و Jardine M et al. صحة الكلى العالمية
2017 وما بعده: خارطة طريق لسد الفجوات في الرعاية والبحث والسياسة. لانسيت. 2017 ؛ 390: 1888-917.
10. Al Khodor S، Shatat IF. ميكروبيوم الأمعاء وأمراض الكلى: علاقة ثنائية الاتجاه. بيدياتر نيفرول. 2017 ؛ 32: 921–31.
11. Nallu A ، Sharma S ، Ramezani A ، Muralidharan J ، Raj D. Gut microbiome في مرض الكلى المزمن: التحديات والفرص. ترجمة الدقة. 2017 ؛ 179: 24-37.
12. رمزاني أ ، ماسي زا ، ميجر ب ، إيفينبول ف ، فانولدر آر ، راج دي إس. دور ميكروبيوم الأمعاء في التبول في الدم: هدف علاجي محتمل. أنا J الكلى ديس. 2016 ؛ 67: 483-98.
13. Di Iorio BR ، Marzocco S ، Nardone L ، Sirico M ، De Simone E ، Di Natale G ، Di Micco L. Urea واختلال محور الأمعاء والكلى في أمراض الكلى المزمنة. جي إيتا نفرول. 2017 ؛ 34: 1-11.
14. Ma SX ، Shang YQ ، Zhang HQ ، Su W. آليات العمل والأهداف العلاجية للتليف الكلوي. J نفرول أدف. 2018 ؛ 1: 4-14.
15. Chen DQ ، Hu HH ، Wang YN ، Feng YL ، Cao G ، Zhao YY. منتجات طبيعية للوقاية من أمراض الكلى وعلاجها. طب النبات. 2018 ؛ 50: 50-60.
16. Lepage P ، Leclerc MC ، Joossens M ، Mondot S ، Blottiere HM ، Raes J ، Ehr‑ lich D ، Dore J. نظرة ميتاجينومية في ميكروبيوم أمعائنا. القناة الهضمية. 2013 ؛ 62: 146-58.
17. كول جيه آر ، تشاي ب ، فارس آر جيه ، وانج كيو ، كولام ، سيد ، محيدين أس ، ماكغاريل دي إم ، بانديلا آم ، كارديناس إي ، غاريتي جي إم ، تيدجي جي إم. مشروع قاعدة البيانات الريبوزومية (RDP-II): إدخال مساحة myRDP والبيانات العامة الخاضعة للرقابة النوعية. الدقة الأحماض النووية. 2007 ؛ 35: D169-72.
18. Zhao YY، Lin RC. الأيض في السمية الكلوية. أدف كلين تشيم. 2014 ؛ 65: 69-89.
19. Zhao YY، Vaziri ND، Lin RC. الدهون الدهنية: نظرة جديدة لأمراض الكلى. أدف كلين تشيم. 2015 ؛ 68: 153-75.
20. Zhao YY. الأيض في أمراض الكلى المزمنة. كلين شيم اكتا. 2013 ؛ 422: 59-69.
