مناعة الخلايا التائية الموجودة مسبقًا ضد SARS-CoV -2 في عناصر التحكم الصحية غير المعرضة في الإكوادور ، كما تم اكتشافها باستخدام COVID -19 اختبار إطلاق إنترفيرون غاما
Mar 13, 2023
خلاصة
الخلفية: دراسات الاستجابات المناعية للخلايا التائية ضد السارس {2}} مهمة في فهم الحالة المناعية للأفراد أو السكان. هنا ، نستخدم مقايسة بسيطة ورخيصة وسريعة لتحفيز الدم الكامل - مقايسة إطلاق إنترفيرون غاما (IGRA) - لدراسة مناعة الخلايا التائية ضد السارس -2 في مرضى COVID -19 في فترة النقاهة واتصالات صحية غير مكشوفة من كيتو ، الإكوادور. الطريقة: تم قياس إنتاج الإنترفيرون-جاما (INF-g) في الدم المعالج بالهيبارين للأشخاص الناقدين وغير المعرضين للخطر بعد التحفيز لمدة 24 ساعة باستخدام SARS-CoV -2 بروتين Spike S1 ، بروتين مجال ربط المستقبلات (RBD) أو بروتين Nucleocapsid (NP) ، على التوالي. تم تحديد وجود الأجسام المضادة لبروتين IgG-RBD في مجموعتي الدراسة باستخدام ELISA "الداخلي". النتائج: وفقًا لقياس إنتاج INF-g ، كان لدى 80 بالمائة من مرضى COVID في فترة النقاهة -19 ، وجميعهم مصابين بمرض IgG-RBD ، استجابة قوية للخلايا التائية.
ومع ذلك ، وبشكل غير متوقع ، فإن 44 في المائة من عناصر التحكم الصحية غير المكشوفة ، وكلها مصل IgG-RBD ، لديها استجابة قوية للخلايا التائية الخاصة بالفيروس مع COVID -19 IGRA ، ربما بسبب التعرض المسبق لفيروسات كورونا المسببة لنزلات البرد أو غيرها المستضدات الفيروسية أو الميكروبية. الخلاصة والمناقشة: تشير النسبة المئوية المرتفعة من الأشخاص الأصحاء غير المعرضين الذين يتمتعون بمناعة موجودة مسبقًا إلى أن جزءًا من السكان الإكوادوريين من المحتمل أن يكون لديهم سارس- CoV -2 الخلايا التائية التفاعلية. نظرًا لأن تقنية IGRA بسيطة ويمكن توسيع نطاقها بسهولة لإجراء التحقيقات عند الحاجة إلى أعداد كبيرة من المرضى ، فقد يعمل هذا COVID -19 IGRA على تحديد ما إذا كانت استجابة الخلايا التائية فقط تمثل مناعة وقائية ضد السارس. عدوى -2 في دراسة سكانية. © 2021 المؤلفون. تم النشر بواسطة Elsevier Ltd نيابة عن الجمعية الدولية للأمراض المعدية.
في الوقت نفسه ، عندما تكون مناعتنا منخفضة ، هناك العديد من الطرق لتحسين المناعة ، وتناول الأطعمة التي يمكن أن تعزز المناعة ، مثل cistanche ، والسكريات ، والبروتينات ، والأحماض الأمينية ، وغيرها من المواد الموجودة في cistanche يمكن أن تنظم في كثير من الأحيان الجسمiنظام mmune.

انقر فوق cistanche tubulosa استخراج مسحوق المنتج
مقدمة
لا تتضمن الاستجابة المناعية لعدوى السارس -2 إنتاج الأجسام المضادة فحسب ، بل تؤدي العدوى أيضًا إلى استجابة الخلايا التائية لدى المرضى (ليبسيتش وآخرون ، 2020 ، ني وآخرون ، 2020). بشكل عام ، يتم تحديد وجود وحجم استجابة خلايا الذاكرة التائية المحددة لعدوى الفيروس التاجي هذا باستخدام اختبار ELISPOT عن طريق تحديد عدد الخلايا الليمفاوية التي تنتج IFN-g بعد التحفيز بمضادات أو ببتيدات خاصة بالمرض (Ni وآخرون ، 2020 ، باي وآخرون ، 2014 ، أباتي وآخرون ، 2013 ، براون وآخرون ، 2020 ، جريفونو وآخرون ، 2020 ، ليبرت وآخرون ، 2020 ، سيكين وآخرون ، 2020).
بالنسبة لهذه التقنية ، يتم عزل الخلايا أحادية النواة في الدم المحيطي (PBMCs) من الدم الطازج المعالج بالهيبارين عن طريق الطرد المركزي المتدرج الكثافة ؛ يتم قياس إفراز السيتوكينات بواسطة الخلايا التائية الفردية بواسطة المجهر أو بجهاز خاص - قارئ لوحة ELISPOT. اختبار ELISPOT هو أسلوب "لمختبرات البحث فقط" وهو أسلوب شاق للغاية ومتطلب تقنيًا ومكلفًا نسبيًا ولا يمكن استخدامه بسهولة في المختبر السريري أو تطبيقه في الدراسات السكانية. نظرًا للتكلفة والبنية التحتية ومتطلبات المختبر اللازمة لإجراء الفحص ، فقد يكون استخدامه في الأماكن محدودة الموارد مثل الإكوادور في حده الأدنى.
يمكن أيضًا تحديد الاستجابات المناعية الخلوية بمقايسة أكثر وضوحًا: مقايسة إطلاق الإنترفيرون-جاما (IGRA). هذا الفحص ، وهو اختبار دم في المختبر ، يحدد كمية السيتوكينات التي تفرزها الخلايا التائية (على سبيل المثال ، جاما إنترفيرون (IFN-g) ؛ ومع ذلك ، يمكن أيضًا قياس السيتوكينات الأخرى مثل TNF أو IL -2) عند تحفيز الدم الكامل (ليس فقط الخلايا الليمفاوية المعزولة) مع مستضدات محددة (باي وآخرون ، 2014 ، أباتي وآخرون ، 2013). يتم قياس السيتوكين المفرز IFN-g بمقايسة ELISA ، وهي تقنية متاحة بسهولة في معظم المختبرات ، وتتم قراءة النتائج باستخدام قارئ لوحة ELISA. وجدت IGRAs تطبيقًا في المختبر السريري وتستخدم لتحديد العدوى الكامنة مع Mycobacterium tuberculosis (MTB) وكذلك لقياس مناعة خلوية محددة من الفيروس المضخم للخلايا (CMV) والتنبؤ بعدوى CMV في متلقي الزرع (Pai et al. ، 2014 ، Abate et al. ، 2013). تم تقييم اختبارات IGRA هذه على نطاق واسع ، ومقارنتها بمقايسة ELISPOT ، فقد ثبت أنها تعرض قدرات مماثلة للتنبؤ بعدوى MTB أو CMV. علاوة على ذلك ، تتوفر العديد من المقايسات التجارية و FDA أو CE للكشف عن المناعة ضد السل أو CMV ويتم إجراؤها على نطاق واسع.
في هذه الدراسة ، نستكشف استخدام COVID -19 IGRA ونقيّم حجم إطلاق IFN-g في مرضى COVID المتعافين -19 وعناصر تحكم COVID الصحية -19 الساذجة استجابةً لبعض مستضدات فيروس SARS-CoV -2: بروتين RBD ؛ الجزء S1 من بروتين سبايك ؛ أو بروتين Nucleocapsid (N). بالإضافة إلى ذلك ، نحدد وجود أجسام مضادة IgG محددة لـ SARS-CoV -2 في هؤلاء المشاركين مع ELISA "داخليًا" (Amanat et al.، 2020، Guevara et al.، 2021). لقد أظهرنا أن نسبة كبيرة من المتبرعين غير المعرضين للمرض يمتلكون الخلايا التائية التفاعلية SARS-CoV -2 ، ونحن نناقش هذه النتائج.
المواد والطرق
مرضى COVID في فترة النقاهة -19 وعناصر تحكم صحية والإعدادات
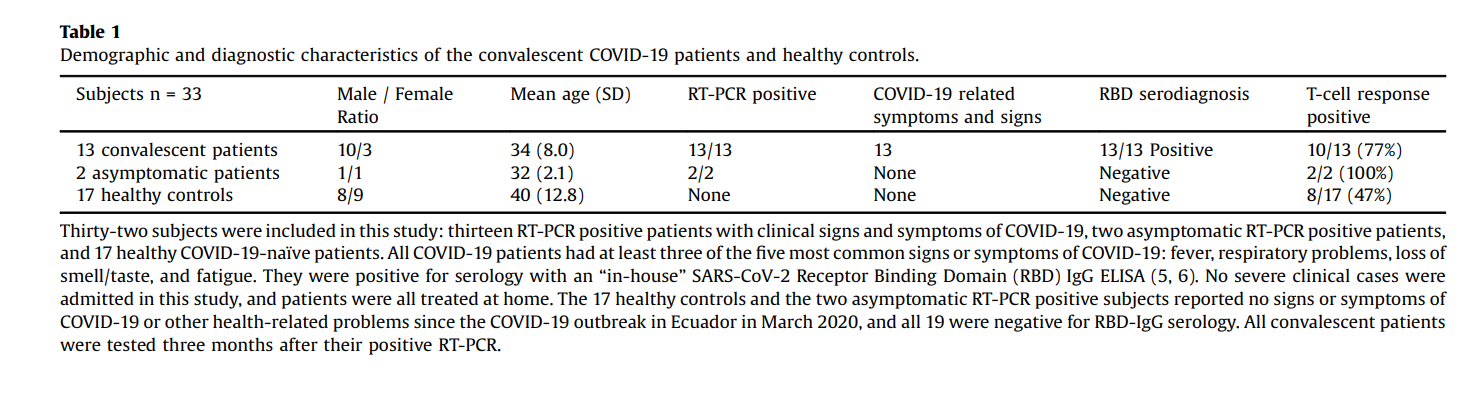
أجريت هذه الدراسة في كيتو ، الإكوادور ، في سبتمبر 2020. لم يتم استخدام أي طرق إحصائية لتحديد حجم العينة مسبقًا. يوضح الجدول 1 خصائص 32 مريضًا في هذه الدراسة: ثلاثة عشر مريضًا مصابًا بفيروس COVID -19 في فترة النقاهة ، وجميعهم يعانون من أعراض / علامات COVID غير شديدة -19 وتشخيص إيجابي لـ RT-PCR في حزيران (يونيو) 2020 ؛ و 17 ضوابط صحية غير مكشوفة. كانت عناصر التحكم الصحية حذرة للغاية أثناء الجائحة ، وتجنب الاتصال بأشخاص آخرين ، ولم تبلغ ذاتيًا عن أي من العلامات والأعراض النموذجية لـ COVID -19 طوال مدة الوباء ، مثل الحمى والسعال المستمر ، أو فقدان حاسة الشم أو التذوق. أيضًا ، تم تضمين اثنين من حاملي SARS-CoV -2 بدون أعراض في هذه الدراسة. لم يظهر هذان الموضوعان أبدًا أي أعراض أو علامات لمرض -19 COVID ؛ ومع ذلك ، تم تنفيذ تقنية RT-PCR عليهم كشرط للحصول على تصريح عمل في يونيو 2020 وأسفرت عن تشخيصات إيجابية.
الأمصال
تم إجراء دراسة الأمصال و IGRAs لجميع المرضى والضوابط خلال الأسبوعين الأخيرين من شهر سبتمبر 2020 ، بعد ثلاثة أشهر من تشخيص RT-PCR للمرضى النقاهة. لتحديد وجود الأجسام المضادة IgG الخاصة بفيروس كورونا في مجموعة الدراسة الخاصة بنا ، تم استخدام "داخلي" SARS-CoV -2 مجال ربط مستقبلات (RBD) IgG ELISA (9 ، 10).

فحص إطلاق إنترفيرون غاما (IGRA)
بالنسبة لـ IGRA ، تم أخذ عينة دم مملوءة بالهيبارين (4 مل) وقسمت إلى قسامات من 250 مل وتحفيزها باستخدام 2 مجم / مل على التوالي من بروتين RBD (إجراء العزل من المرجع 9) أو 2 مجم / مل من Nucleocapsid المتاح تجارياً (N) بروتين أو بروتين سبايك (S1) (ViroGen ، أرقام الكتالوج: 00 ، 221- V و 00 ، 226- على التوالي). تم استخدام منحنى تركيز الاستجابة للجرعة مع الدم من مرضى IGRA الإيجابي والسلبي IGRA لتحديد تركيز المستضدات الأمثل للتحفيز في IGRA. عند 2 ميكروغرام / مل ، تم العثور على أقصى استجابة IFN-g في الدم من الأشخاص المصابين بفيروس COVID -19 دون تحفيز في عناصر التحكم غير المصابة. لكل مشارك ، تم تضمين عنصر تحكم غير محفز (NIL) ، وقمنا بفحص عينة دم بحجم 250 مل باستخدام ميتوجين فيتوهيماجلوتينين (PHA) ، وهو عنصر تحكم إيجابي لتقييم معدل استجابة السيتوكين لعينة الدم. تم التحفيز في 96- صفيحة ELISA ذات قاع مسطح جيدًا عند 37 درجة مئوية لمدة 24 ساعة. تم حصاد البلازما ، وتم تحديد إنتاج IFN-g باستخدام الإنسان IFN-g ELISA (MaxTM Standard Set Biolegend cat. رقم 430 ، 101).
نتائج
أظهر RBD IgG ELISA أن جميع المرضى المصابين بأعراض COVID {0} (إيجابي RT-PCR) كانوا إيجابيين للأجسام المضادة IgG مقابل بروتين RBD بعد ثلاثة أشهر من تشخيص RT-PCR. كان كل من المرضى الموجودين بدون أعراض RT-PCR وجميع مرضى التحكم الأصحاء غير المعرضين سلبيين مع ELISA (انظر الجدول 1). تظهر نتائج تحفيز الدم الكامل في اختبار COVID -19 IGRA في الشكل 1. تم العثور على تحريض قوي لإنتاج IFN-g في 8 0 بالمائة من مرضى COVID -19 الذين يعانون من أعراض كانت جميع المستضدات الثلاثة ، ولكن بروتين N وبروتين S هما المحفزات الأكثر فعالية لاستجابة IFN-g (الشكل 1 A ، B ، C). أظهر المريضان اللذان لا تظهر عليهما الأعراض ولكن إيجابيًا لـ RT-PCR (المرضى 14 و 15) ، وكلاهما بدون أجسام مضادة محددة لـ SAR-CoV -2 ، استجابة مناعية قوية محفزة لخلايا T. من بين -19 مرضى COVID الساذجين ، أظهر 45 بالمائة مناعة محفزة للخلايا التائية. لم تكن الاستجابة في هذه الضوابط الصحية غير المعرضة للضوء مع استجابة الخلايا التائية مختلفة إحصائيًا في الحجم عن مرضى COVID في فترة النقاهة -19 لأي من المستضدات المحفزة (القيمة p=0. 271، 0.437، و 0.719 لبروتينات RBD و N و S1 على التوالي).

الشكل 1. إنتاج IFN-g بعد تحفيز الدم الكامل لمرضى COVID في فترة النقاهة -19 وعناصر تحكم صحية غير معرّضة لبروتين RBD أو N أو S1.
نتائج تحفيز مرضى النقاهة والضوابط باستخدام بروتين RBD أو N أو S1 ، على التوالي ، موضحة في الشكل 1 أ ، ب ، ج. في الشكل 1 د ، استجابات INF-g لكل مريض وللثلاثة يتم تجميع المستضدات. المرضى الذين يعانون من عدوى COVID المؤكدة -19 يتراوح عددهم بين 1 و 15 ، منهم 14 و 15 كانوا بدون أعراض. الأشخاص من 16 إلى 33 هم مرضى COVID {11}} الساذجين.
بعد 24 ساعة من التحفيز ، تم تحديد تركيزات IFN-g في البلازما باستخدام مجموعة مقايسة الممتز المناعي البشري المرتبطة بالإنزيم IFN-g (Biolegend cat. رقم 43 0 ، 101). تم التعبير عن حجم التحفيز من خلال الكثافة الضوئية عند 450 نانومتر (OD450) للدم المحفز باستخدام مستضد ناقص OD450 للدم دون تحفيز المستضد. OD 1.0 يتوافق مع حوالي 400 بيكوغرام / مل IFN-g. تم استخدام Phytohemagglutinin (PHA) كميتوجين بتركيز نهائي قدره 5 مجم / مل في IGRA لتقييم جودة وقدرة الدم على الاستجابة. أظهر جميع المرضى والضوابط الحد الأقصى من إنتاج السيتوكين مع هذا الميتوجين بمتوسط كثافة بصرية (OD450) 2.54 (SD=0 .13) ، وهو ما يمثل حوالي 1000 بيكوغرام / مل من IFN-g. لم يكن هناك اختلاف في متوسط مستوى IFN-g في الدم غير المحفز لمرضى النقاهة والضوابط الصحية (OD 450=0. 38 ، SD=0. 14 مقابل OD 450=0. 32. SD=0 16). لم يتم عرض هذه النتائج. تم رسم خط أفقي في كل رسم بياني لتمثيل القيمة الفاصلة للتحفيز. تم تحديد هذه القيمة من خلال حساب المتوسط زائد اثنين من الانحرافات المعيارية لاستجابة تسعة أفراد (المرضى 16 ، 18 ، 19 ، 22 ، 27-31) من المجموعة الضابطة مع أدنى إنتاج من INF-g بعد التحفيز.

المناقشة والاستنتاجات
باستخدام اختبار دم كامل سهل الأداء يقيم استجابات الخلايا التائية ، وجدنا أن معظم المرضى الذين نقاهوا ونسبة كبيرة من الأفراد الأصحاء غير المعرضين للخطر لديهم استجابة محددة وقوية للخلايا التائية محددة بإنتاج INF-g بعد التحفيز. مع مستضدات SARS-CoV -2 المحددة (الشكل 1). أبلغت العديد من الدراسات ، التي تستخدم جميعها اختبار ELISPOT ، عن وجود استجابة للخلايا التائية في معظم أو جميع مرضى COVID في فترة النقاهة -19 (Braun et al.، 2020، Grifono et al.، 2020، LeBert et al. ، 2020، Sekine et al.، 2020، Moderbacher et al.، 2020، Mateus et al.، 2020، Peng et al.، 2020).
ومع ذلك ، فيما يتعلق باستجابة الخلايا التائية في الضوابط الصحية غير المكشوفة ، تم الإبلاغ عن معدلات استجابة تتراوح بين 28 و 50 بالمائة (Doshi، 2020، de Vries، 2020، Lipsitch et al.، 2020، Sagar et al.، 2020) والعديد من تشير الدراسات إلى عدم استجابة الخلايا التائية في COVID -19 مرضى التحكم الساذجين (de Vries، 2020، Moderbacher et al.، 2020، Schwarzkopf et al.، 2021). تم إجراء معظم هذه الدراسات باستخدام اختبار ELISPOT ، ولكن في إيطاليا والولايات المتحدة الأمريكية ، تم استخدام IGRA أيضًا لاكتشاف استجابة الخلايا التائية السارس -2 (بتروني وآخرون ، 2020 ، موروجيسان وآخرون ، 2020). في كلتا الدراستين ، تم الكشف عن استجابة محددة للخلايا التائية في مرضى النقاهة. ومع ذلك ، لم تكتشف IGRA استجابة INF-g في موضوعات صحية غير معرّضة.
تمت مراجعة مناعة الخلايا التائية الموجودة مسبقًا ضد SARS-CoV -2 في COVID -19 مواضيع ساذجة في العديد من المنشورات (Altmann and Boyton، 2020، Dosho et al.، 2020، de Vries، 2020، سيت وكروتي ، 2020). لا يزال سبب اكتشاف استجابة COVID معينة -19 للخلايا التائية في موضوع سليم غير معرَّض غير واضح وهو موضوع تكهنات. استخدمت معظم دراسات ELISPOT التي أجريت على COVID -19 أشخاصًا ساذجين عينات دم بشرية مأخوذة قبل اكتشاف فيروس SARS-CoV -2 في عام 2019 ، وبالتالي قبل أي فرصة للتعرض. لهذا السبب ، خلصت دراسات ELISPOT هذه إلى أن استجابة الخلايا التائية في الأشخاص الأصحاء غير المعرضين للتعرض ربما تأتي من الاتصال المسبق بفيروسات كورونا المنتشرة "نزلات البرد" (Grifoni et al. ، 2020 ، Matheus et al. ، 2020) أو التعرض السابق للإنفلونزا و / أو فيروسات CMV (Mahajan et al. ، 2020) أو مستضدات فيروسية أو جرثومية أخرى (Tan et al. ، 2020). استخدمت دراستنا الدم المأخوذ أثناء الوباء من المتطوعين الذين أبلغوا بأنفسهم عن عدم وجود أي اتصال ، وكانوا سلبيين بالنسبة لمستضد COVID -19 RBD ، ولم يظهروا أبدًا أي علامات أو أعراض لـ COVID -19.
لذلك لا يمكننا استبعاد أن استجابة الخلايا التائية في بعض عناصر التحكم الصحية لـ COVID -19 "الساذجة" تأتي من عدوى فيروس SARS-CoV -2 بدون أعراض. المرضى 14 و 15 من دراستنا مثال على ذلك. تم تصنيف هؤلاء الأفراد على أنهم مرضى COVID -19 بسبب تفاعل البوليميراز المتسلسل RT-PCR الإيجابي ؛ ومع ذلك ، لم تظهر عليهم أعراض ولم يطوروا استجابة من الجسم المضاد لبروتين RBD ، لكن كلاهما أظهر استجابة قوية للخلايا التائية.
من المحتمل أنه بعد استعمار SARS-CoV -2 للبلعوم الأنفي ، ترك الجهاز المناعي لهذين المريضين عديمي الأعراض استجابة لخلايا الذاكرة فقط ، ولم تكن هناك أجسام مضادة محددة لـ SARS-CoV -2 الناجم عن. تفسير آخر هو أن استجابة الخلايا التائية تأتي من عدوى سابقة شبيهة بالكورونا ، والاستجابة المناعية للخلايا التائية الموجودة مسبقًا تحمي هذين المريضين من تطور نمط مرض أكثر تغلغلًا. يمكن أن تكون الخلايا التائية التفاعلية المتصالبة الموجودة مسبقًا مهمة في شرح بعض الاختلافات في معدلات الإصابة أو علم الأمراض (Le Bert et al. ، 2020 ، Sagar et al. ، 2020). فيما يتعلق بمجموعة الضوابط الساذجة ، استبعدنا أن هذه المجموعة تحتوي على عدد كبير من الأفراد المصابين بـ SARSCoV -2 المصابين بعدوى غير مصحوبة بأعراض ، وذلك أساسًا لأن جميع مجموعات التحكم في المجموعة الضابطة هي IgG سلبيًا لمولد الضد RBD.
سبب آخر هو أن انتشار العدوى في الإكوادور منخفض نسبيًا. في وقت هذه الدراسة ، في سبتمبر 2020 ، أبلغت الإكوادور عن حوالي 200 حالة 000 مؤكدة من COVID -19 (حوالي 1.1 بالمائة من السكان). بالطبع ، كان من الممكن أن يكون معدل انتشار العدوى الفعلي أعلى عدة مرات ، ولكن مع ذلك ، فمن غير المحتمل أن يكون 45 بالمائة من هذه المجموعة الضابطة قد أصيبوا بالعدوى ، وبالتالي فإننا نبحث في استجابة الخلايا التائية الخاصة بفيروس SARS-CoV { {9}} عدوى.
في الختام ، فإن اكتشاف نسبة عالية من الأشخاص الأصحاء غير المعرضين للخطر والذين يتمتعون بمناعة موجودة مسبقًا في كيتو ، الإكوادور ، يثير التوقعات بأن جزءًا كبيرًا من سكاننا من المحتمل أن يكون لديهم سارس- CoV -2 الخلايا التائية التفاعلية بسبب التعرض المسبق للإنفلونزا أو فيروسات الفيروس المضخم للخلايا أو فيروسات كورونا المسببة لنزلات البرد. يجب أن تهدف التحقيقات المستقبلية إلى تحديد ما إذا كانت الاستجابة المناعية الموجودة مسبقًا واقية و / أو يمكنها التغلب على مرض COVID -19 الأكثر خطورة أو المساهمة في التعافي بشكل أسرع.
أهمية هذه الدراسة وحدودها
أظهرت دراستنا أن COVID -19 IGRA هو أداة جديدة مفيدة وحساسة يمكنها تقييم التعرض لفيروسات كورونا أو التفاعل المتبادل مع فيروسات مماثلة من خلال تحديد إطلاق IFN-g بعد التحفيز باستخدام مستضدات خاصة بالفيروسات. هذه التقنية بسيطة ورخيصة نسبيًا ويمكن استخدامها في المختبر السريري. هذا بالتأكيد ليس هو الحال مع مقايسة ELISPOT. علاوة على ذلك ، يمكن توسيع نطاق مقايسة IGRA بسهولة للدراسات والتحقيقات المستندة إلى السكان حيث يلزم وجود أعداد كبيرة من المرضى. جنبًا إلى جنب مع علم الأمصال ، يمكن استخدام IGRA لفحص استجابات كل من الأجسام المضادة والخلايا التائية للمرضى الأفراد لفهم المناعة على مستوى السكان بشكل أفضل وتحديد المناعة الموجودة مسبقًا في الأفراد السلبيين.
أحد القيود المهمة لدراستنا هو أن عينة الدراسة لا تمثل السكان. لم يتم استخدام طرق إحصائية لتحديد حجم العينة مسبقًا. علاوة على ذلك ، لم يفرق اختبارنا بين إنتاج IFN-g لخلايا CD4 plus أو CD8 plus ، ولكن يمكن اعتبار التحفيز باستخدام ببتيدات CD8 (زائد) و CD4 (زائد) (Grifoni et al. ، 2020 ، Peng et al. ، 2020) وتم استخدامه في IGRAs الموصوفة في Petrone et al. ، 2020 و Murugesan et al. ، 2020). أيضًا ، يمكن قياس تحريض السيتوكينات الأخرى باستخدام IGRA (Petrone et al. ، 2020). وبالمثل ، يمكن استخدام IGRA لمتابعة التطعيم لتحديد تطور استجابة الخلايا التائية لدى الأفراد الملقحين أو يمكن استخدامها لتحديد ما إذا كان وجود خلايا الذاكرة التفاعلية المتصالبة مرتبطًا بالمناعة الوقائية ويمكن يقلل من مظاهر المرض من عدوى فيروس SARS-CoV -2 (Sagar et al. ، 2020).

موافقة الأخلاق والمشاركة
تم جمع الدم بعد الموافقة الخطية المستنيرة. وافقت لجنة الأخلاقيات في وزارة الصحة في الإكوادور على بروتوكول الدراسة 004-2020.
تضارب المصالح
الكتاب تعلن أنه ليس لديهم المصالح المتنافسة.
الكاتب الاشتراكات
تصميم الدراسة؛ JHW و GE ؛ جمع البيانات والتجارب المعملية: GE و AG و JC و AMR و MMV ؛ تحليل البيانات؛ JHW و GE و ET ؛ الكتابة: JHW و GE و ET.
شكر وتقدير
نعرب عن امتناننا لجميع المتبرعين وموظفي الرعاية الصحية المشاركين في هذا العمل ، وخاصة ساندرا فيفيرو وساندرا فونسيكا ، للمساعدة في جمع العينات. تم دعم هذه الدراسة من قبل صندوق بحثي من جامعة لاس أمريكا. قدم معهد العلوم المستدامة ، سان فرانسيسكو ، كاليفورنيا ، الولايات المتحدة الأمريكية ، ومؤسسة "بور تودوس" في الإكوادور بروتين RBD و ELISA "الداخلي". بفضل Howard E. Takiff و Flor Pujol (IVIC ، فنزويلا) ، Paulina E. Andrade (USFQ ، الإكوادور) ، وليلي فيرهاغن (UMC ، هولندا) لمناقشاتهم المثمرة.

مراجع
Abate D ، Saldan A ، Mengoli C ، Fiscon M ، Silvestre C ، Fallico L ، et al. مقارنة بين بقعة الامتصاص المناعي المرتبطة بالإنزيم المرتبط بالفيروس المضخم للخلايا (CMV) ومقايسات غاما لإطلاق الإنترفيرون الكمي للفيروس المضخم للخلايا في تقييم خطر الإصابة بعدوى الفيروس المضخم للخلايا في متلقي زرع الكلى. J كلين ميكروبيول 2013 ؛ 51 (8): 2501-7.
ألتمان دم ، بويتون ريج. SARS-CoV -2 مناعة الخلايا التائية: الخصوصية والوظيفة والمتانة والدور في الحماية. Sci Immunol 2020 ؛ 5 (49) eabd6160.
أمانات ف ، ستادباور د ، ستروهمير إس ، نغوين ثو ، كروميكوفا الخامس ، مكماهون إم ، وآخرون. اختبار مصلي لاكتشاف الانقلاب المصلي لـ SARS-CoV -2 في البشر. نات ميد 2020 ؛ 26: 1033-6.
براون J ، Loyal L ، Frentsch M ، Wendisch D ، Georg P ، Kurth F ، et al. SARS-CoV -2- الخلايا التائية التفاعلية في المتبرعين الأصحاء والمرضى المصابين بـ COVID -19. طبيعة 2020 ؛ 587: 270-4.
دي فريس آر دي. SARS-CoV -2- الخلايا التائية المحددة في البشر غير المعرضين: وجود خلايا ذاكرة تفاعلية لا يساوي المناعة الوقائية. سيج ترانسدكت تارجت ثير 2020 ؛ 5: 224.
كوفيد دوشي -19: هل يمتلك العديد من الأشخاص مناعة موجودة مسبقًا؟ BMJ 2020 ؛ 370: m3563.
Grifoni A و Weiskopf D و Ramirez SI و Mateus J و Dan JM و Moderbacher CR وآخرون. أهداف استجابات Tcell لفيروس كورونا SARS-CoV -2 في البشر المصابين بمرض COVID -19 والأفراد غير المعرضين. الخلية 2020 ؛ 181 (7) 1489-501.
Guevara A و Vivero S و Nipaz V و Guaraca V و Coloma J. وهو SARS-CoV منخفض التكلفة -2 rRBD ELISA لاكتشاف حالة المصل في السكان الإكوادوريين المصابين بفيروس COVID -19. Am J Trop Med Hyg [39_ TD $ DIFF] 2021.
Le Bert N و Tan AT و Kunasegaran K و Tham CYL و Hafezi M و Chia A et al. SARS-CoV -2- حصانة Tcell الخاصة في حالات COVID {2}} والسارس ، وعناصر التحكم غير المصابة. طبيعة 2020 ؛ 584 (7821): 457-62.
Lipsitch M و Grad YH و Sette A و Crotty S. خلايا الذاكرة المتفاعلة ومناعة القطيع ضد SARS-CoV -2. نات ريف إمونول 2020.
Mahajan S و Kode V و Bhojak K و Magdalene CM و Lee K و Manoharan M وآخرون. تكشف حواتم الخلايا التائية المناعية من فيروس SARS-CoV -2 عن مناعة قوية للخلايا التائية موجودة مسبقًا في الأفراد غير المعرضين. bioRxiv 2020.
ماتيوس جيه ، جريفوني أ ، تاركي أ ، سيدني جيه ، راميريز سي ، دان جم ، إت آل. حواتم الخلايا التائية الانتقائية والمتصالبة لـ SARS-CoV -2 في البشر غير المعرضين. العلوم 2020 ؛ 370 (6512): 89-94.
Moderbacher RC و Ramirez SI و Dan JM و Grifoni A و Hastie KM و Weiskopf D وآخرون. المناعة التكيفية الخاصة بمستضد ضد السارس {2}} في COVID الحاد -19 والارتباطات بالعمر وشدة المرض. خلية 2020 ؛ ص 0092-8674 (20): 31235–6.
Murugesan K و Jagannathan P و Pham TD و Pandey S و Bonilla HF و Jacobson K وآخرون. مقايسة إطلاق إنترفيرون-جاما للكشف الدقيق عن استجابة الخلايا التائية السارس-CoV -2. كلين إنفيكت ديس 2020 ؛ ciaa1537.
Ni L و Ye F و Cheng ML و Feng Y و Deng YQ و Zhao H وآخرون. الكشف عن -2- مناعة خلطية وخلوية محددة لـ SARS-CoV في -19 المصابين بفيروس كورونا المستجد. المناعة 2020 ؛ 52 (6) 971-7.
Pai M و Denkinger CM و Kik SV و Rangaka MX و Zwerling A و Oxlade O وآخرون. فحوصات إطلاق جاما إنترفيرون للكشف عن عدوى المتفطرة السلية. كلين ميكروبيول ريف 2014 ؛ 27 (1): 3-20.
Peng Y و Mentzer AJ و Liu G و Yao X و Yin Z و Dong D وآخرون. ذاكرة واسعة وقوية CD4 بالإضافة إلى خلايا CD8 بالإضافة إلى الخلايا التائية التي يسببها فيروس SARS-CoV -2 في الأشخاص الذين نقاهة في المملكة المتحدة بعد COVID -19. NatImmunol 2020.
Petrone L ، Petruccioli E ، Vanini V ، Cuzzi G ، Fard SN ، Alonzi T ، et al. فحص دم كامل لقياس الاستجابة المحددة لـ SARS-CoV -2- في مرضى COVID -19. كلين ميكروبيول إنفيكت 2020.
ساجار إم ، رايفلر ك ، روسي إم ، ميلر إن إس ، سينها بي ، وايت إل ، إت آل. ترتبط الإصابة الحديثة بفيروس كورونا المستوطن بمرض COVID أقل خطورة -19. J كلين إنفست 2020.
Schwarzkopf S و Krawczyk A و Knop D و Klump H و Heinold A و Heinemann FM وآخرون. المناعة الخلوية في حالات الإصابة بفيروس COVID -19 النقاهة المصابة بعدوى مؤكدة بواسطة تفاعل البوليميراز المتسلسل لكن مع فيروس SARS-CoV غير قابل للكشف -2- IgG محدد. Emerg تصيب ديس. 2021 ؛ 27 (1).
Sekine T و Perez-Potti A و Rivera-Ballesteros O و Strålin K و Gorin JB و Olsson A وآخرون. مناعة قوية للخلايا التائية في الأشخاص الناقحين المصابين بفيروس كوفيد غير المصحوب بأعراض أو خفيف -19. الخلية 2020 ؛ 183 (1) 158–68.
Sette A ، Crotty S. المناعة الموجودة مسبقًا ضد SARS-CoV -2: الأشياء المعروفة وغير المعروفة. نات ريف إمونول. 2020 ؛ 20 (8) 457–8.
تان CCS ، أوين CJ ، Tham CYL ، Bertoletti A ، van Dorp L ، Balloux F. لا يمكن تفسير التفاعل التبادلي عبر الخلايا التائية الموجودة مسبقًا مع فيروس SARS-CoV -2 فقط من خلال التعرض المسبق لفيروسات كورونا البشرية المتوطنة. bioRxiv 2020 ؛ 2020.
For more information:1950477648nn@gmail.com
