بيروبتوسيس في أمراض الكلى
Feb 19, 2022
جهة الاتصال: emily.li@wecistanche.com
Yujia Wang و Yinshuang Li و Yanfang Xu1
الملخص
في العقود العديدة الماضية ، تم اعتبار تداخل موت الخلايا المبرمج غير ذي صلة سريريًا في سياق الإصابة الكلوية. أدى الاكتشاف الأخير لموت الخلايا النخرية المبرمج ، بما في ذلك التنخر ، والتطعيم الحديدي ، والتضخم الحركي إلى تحديث فهمنا لدور موت الخلايا فيالكلىمرض. يتميز Pyroptosis بنوع من الالتهابات المسببة للالتهاب من موت الخلايا الناتج عن نفاذية الغشاء الناجم عن غازديرمين عن طريق تنشيط الكاسبيسات الالتهابية والأورام الالتهابية. يتم إطلاق الأنماط الجزيئية المرتبطة بالخطر (DAMPs) ، و alarmins ، والسيتوكينات المؤيدة للالتهابات من الخلايا الحرارية بطريقة غير منضبطة ، مما يؤدي إلى حدوث التهاب ، مما يؤدي إلى إصابات ثانوية في الأعضاء أو الأنسجة. إن الكاسبيسات والبروتينات المرتبطة بالتنشيط الملتهب والبروتينات المؤثرة المكونة للمسام المعروفة باسم GSDMD و GSDME متورطة في مجموعة متنوعة من الميكروبات الحادة والمزمنة وغير الميكروبية.الكلىالأمراض. هنا ، نستعرض التطورات الحديثة في الآليات المرضية لداء الحموضة فيالكلىمرضوتسليط الضوء على الاستراتيجيات العلاجية المحتملة في المستقبل.

انقر هنا لمعرفة المزيد عن طرق علاج أمراض الكلى
مقدمة
يلعب موت الخلايا المبرمج (PCD) دورًا مهمًا في كل من تطوير الكائنات متعددة الخلايا والحفاظ على الأنسجة البالغة. في تناقض حاد مع موت الخلايا العرضي (على سبيل المثال ، النخر) الذي يكون فوريًا وكارثيًا وغير قابل للسيطرة عليه ، يتم تنظيم PCD بإحكام ، مما يسمح بالتعديلات الدوائية والوراثية. العمليات (على سبيل المثال ، موت الخلايا المبرمج) والعمليات الالتهابية الشديدة (على سبيل المثال ، التهاب الحلق والتخثر). بالإضافة إلى وجود أو عدم وجود التهاب ، يمكن تمييز موت الخلايا المبرمج والتشكيل عن طريق التشكل. تشمل التغيرات المورفولوجية المميزة لموت الخلايا المبرمج انكماش الخلايا ، وتضخم الغشاء ، وتكوين الجسم الأبوطوزيكي ، وتفتت الحمض النووي ، ولكن لاالتهاب2 على العكس من ذلك ، يتميز التهاب الحنجرة بتورم الخلايا ، وتمزق الغشاء ، والإفراج غير المنضبط للمحتويات الالتهابية. يشترك التنخر في الخصائص المشتركة مع التهاب الحنجرة ، بما في ذلك الالتهاب الواضح وفقدان سلامة الغشاء.
على الرغم من أن كل من بيروبتوسيس وموت الخلايا المبرمج يعتمدان على كاسباس ، إلا أن أفراد عائلة الكاسباس المعينين مختلفين تمامًا. تتضمن كاسبيسات Apoptotic caspases -8 / 9/10 كبادئ و caspases -3 / 6/7 كمنفذين ، 4 بينما يعتمد Pyroptosis على caspases -1 / 4/5/11 في gasdermin D ( GSDMD) تَشَوُّرُ الكَاسْبَس والتَشَّرُّق بوساطة GSDMD -3 في التعرق الناتج عن غازديرمين E (GSDME) بوساطة .5،3 يستمر التنخر عن طريق التنشيط التدريجي لبروتين كيناز المتفاعل مع المستقبلات -3 (RIPK3) والنسب المختلط الكيناز الكاذب الذي يشبه مجال كيناز (MLKL) ، والذي يمكن تثبيطه بواسطة كاسباس -8. هذا يختلف عن GSDMs في التحلل الحراري ، والذي يعتمد تنشيطه على كاسباس. أصبحت العلاقة بين دقائق الجنس و MLKL في ظل الظروف الفسيولوجية موضوعًا ذا أهمية للبحث. معروف عن التفاعل بين داء الفيروبتوسيس والتشحم الحليمي.
تدعم الأدلة التجريبية المتزايدة الفرضية القائلة بأن التهاب الحلق هو عامل مهم فيالكلىالأمراض. في هذه المراجعة ، نناقش الآليات الجزيئية للالتهاب الحركي ، والبيانات الموجودة حول التهاب الحلق فيالكلىالأمراضوالعلاجات المحتملة.
نظرة عامة على بيروبتوسيس
المنفذون
يُعرَّف الانحراف الحراري بأنه يعتمد على غازديرمين لخطوته الرئيسية في تكوين المسام في غشاء البلازما التي يتم تنفيذها بواسطة العقول المدبرة ، مما يجعلها متميزة تمامًا عن الأنواع الأخرى من PCDs. GSDMD هو أول عضو في عائلة gasdermin الذي وجد أنه متورط في التهاب الحموضة .7–9 يظل GSDMD كامل الطول في حالة منع ذاتي من خلال ربط المجال C-terminal بمجال N-terminal. عند الانقسام ، يمكن للجزء N- طرفي من GSDMD (GSDMD N) أن يتحول إلى قليل لتشكيل مسام (بقطر داخلي من 12-14 نانومتر) على غشاء البلازما ، 10 مما يضعف حاجز النفاذية ويسبب تحلل الخلية. يتم التوسط في انقسام GSDMD من خلال المسارات الكنسية أو غير الكنسية التي تتضمن caspase -1 أو caspases -4 / 5/11 على التوالي. / 5/11 يتم تنشيطها بواسطة أنواع مختلفة من الالتهاب. كشفت الدراسات الحديثة أن انقسام GSDMD يمكن أن يحدث أيضًا بواسطة الإيلاستاز العدلات في العدلات الشيخوخة ، 12 وعن طريق كاسباس -8 في البلاعم أثناء عدوى يرسينيا.
تم تحديد الطفرة الجينية لـ GSDME ، وهو عضو آخر في عائلة gasdermin ، أولاً كسبب لفقدان السمع غير المتلازم الصبغي الجسدي السائد لدى البشر. وقد كشفت الدراسات الحديثة عن دور GSDME في التهاب الحرق. الأنسجة الطبيعية ومع ذلك ، يتم إسكاته في معظم الخلايا السرطانية بسبب فرط الميثيل المحفز ، وتعديل تعبيره بواسطة مثبط ميثيل ترانسفيراز الحمض النووي من شأنه تحسين حساسية العلاج الكيميائي. }} وهي مستقلة عن تكوين الجسيمات الالتهابية. يحدث التحلل العضلي بوساطة GSDME في اتجاه مجرى مسار موت الخلايا المبرمج للميتوكوندريا ، والتعبير العالي عن GSDME ونفاذية الميتوكوندريا المستمرة من شأنه أن يغير طريقة موت الخلية من موت الخلايا المبرمج إلى التهاب البروتوز.
الأعضاء الآخرون في عائلة gasdermin ، بما في ذلك GSDMA و GSDMB و GSDMC ، يتشاركون نطاقات غازديرمين- N و gasdermin-C المحفوظة للغاية مع GSDMD و GSDME. الذي قام برمجية ليجند الموت 1 بتحويل عامل نخر الورم (TNF) الناجم عن موت الخلايا المبرمج إلى التهاب الخلايا السرطانية ، وذلك بوساطة تعزيز النسخ الجيني GSDMC. تم تنشيط GMC بواسطة caspase -8 بعد علاج TNF-a ، في ظل حالة نقص الأكسجة. ومع ذلك ، تظل الآلية التي يتم من خلالها تنشيط GSDMA غير مستكشفة.
مسارات الإشارات
التهاب الحنجرة بوساطة GSDMD. يتم بدء التحلل العضلي بوساطة GSDMD من خلال التعرف على الأنماط الجزيئية المرتبطة بالعوامل الممرضة (PAMPs) وجزيئات النمط الجزيئي المرتبطة بالتلف (DAMPs) مع التنشيط الالتهابي اللاحق. ، المعروف أيضًا باسم المسار التابع لـ caspase -1. لطالما تورط Caspase -1 في موت الخلايا ، والذي كان مخطئًا سابقًا بسبب موت الخلايا المبرمج 23،24 والتخمر .25 في عام 2001 ، تم تمييز شكل PCD الذي يحتوي على caspase -1 عن موت الخلايا المبرمج والنخر من خلال استجابته الالتهابية والتشكيل المميز بما في ذلك فقدان سلامة الغشاء المبكر
استجابة لغزو مسببات الأمراض أو التحدي المناعي للمضيف ، فإن مستقبلات التعرف على الأنماط (PRRs) تدرك كلا من PAMPs و / أو DAMPs. في المسار المتعرج الكنسي ، العديد من PRR مثل الغائب في الورم الميلانيني 2 (AIM2) - المستقبلات الشبيهة (ALRs) ، مستقبلات قليلة القلة المرتبطة بالنيوكليوتيدات (NOD) أو بروتينات البيرين ، ومحولات الجسر مثل المرتبطة بالاستماتة ستقوم البروتينات الشبيهة بالبقع (ASCs) بتجميع منصة متعددة البروتينات (أي inflammasome) التي تجند pro-caspase -1 ثم تولد caspase نشطة -1. 28 كاستثناء ، يمكن لـ NLRC4 الارتباط بالأعضاء من عائلة NLR للبروتينات المثبطة لموت الخلايا المبرمج (NAIPs) بدلاً من ASC لتشكيل الجسيم الملتهب ، ثم تنشيط procaspase -1. 29 caspase المنشط -1 له نشاط معالجة pro-IL -1 ب و pro-IL -18 في أشكال ناضجة ، 30 التي تمنح التهاب الحويصلة وظائف مسببة للالتهابات ، مما يميزه عن موت الخلايا المبرمج. بالتوازي مع عملية السيتوكينات الالتهابية ، ينقسم كاسباس -1 المنشط GSDMD لتشكيل مسام الغشاء 22،31،32 (الشكل 1). يؤدي تكوين مسام الغشاء إلى اضطراب سلامة غشاء الخلية ، وإطلاق محتويات التهابية داخل الخلايا ، وفي النهاية تحلل الخلية. NLRP3 هو أكثر الجسيمات الالتهابية انتشارًا. 33 يستجيب NLRP3 لمجموعة متنوعة من الإجهاد ، بما في ذلك مسببات الأمراض داخل الخلايا ومحفزات الالتهاب خارج السيتوبلازم. الحمض النووي للميتوكوندريا ، وتوليد أنواع الأكسجين التفاعلي للميتوكوندريا (ROS) ، وتدفق البوتاسيوم خارج الخلية ، وإطلاق الكاثيبسين بعد زعزعة الاستقرار الليزوزومي .35 على الرغم من سنوات من الجهود المكثفة ، لا تزال الآليات الدقيقة لتنشيط NLRP3 قيد المناقشة. من المثير للاهتمام أنه يمكن تشغيل NLRP3 عن طريق إشارات التنخر ، 36-38 مما يشير إلى تداخل محتمل بين التنخر والتشقق. يتصرف الجسيم الملتهب AIM2 بشكل مختلف عن الإنفلونزا NLR حيث يمكنه التعرف على dsDNA الخلوي وربطه ، والذي يمكن إطلاقه أثناء عدوى مسببات الأمراض 39،40 أو يتولد في الخلايا السرطانية.

في المسار الحراري غير المتعارف عليه ، يعتبر الكاسبيز -11 (في الفئران) وكاسبيز -4 / 5 (في البشر) مسئولين عن انقسام GSDMD (الشكل 1). في عام 2011 ، أفاد Kayagaki وزملاؤه 43 أن فقد الكاسبيز -11 ولكن ليس الكاسبيز -1 يمكن أن يمنع نضوج IL -1 b والإفراز الناجم عن البكتيريا سالبة الجرام ، وبالتالي حماية الفئران من السمية الداخلية. صدمة. اكتشفت دراسات أخرى أن عديد السكاريد الدهني (LPS) ، وهو السم الرئيسي للبكتيريا سالبة الجرام ، هو المحفز للجسيم الالتهابي غير الكنسي. 44،45. قام أحد مكونات LPS.46 Activated caspase -11 في نهاية المطاف بشق GSDMD للحث على التعرق ، على غرار المسار المتعارف عليه. في الآونة الأخيرة ، تم إثبات أن الكاسبات البشرية -4 / 5 لها نفس وظيفة قاعدة كاسبيز الماوس -11. ذكر Poelzl وآخرون. 47 أن التيروزين كيناز 2 ، كيناز مرتبط بمستقبلات السيتوكين ، يمكن أن يعمل كمنظم مهم في المنبع من الكاسبيز -11 ويسمح بتنشيط الجسيم الالتهابي غير الكنسي أثناء التسمم الداخلي.
بالإضافة إلى هذه المسارات الكنسي وغير المتعارف عليه ، ألقت الدراسات الحديثة ضوءًا جديدًا على التهاب الحموضة بوساطة GSDMD. كامبارا وآخرون وجد أن z-YVAD-fmk ، مثبط كاسباس ، فشل في منع انقسام GSDMD المستخرج من العدلات ، مما يشير إلى أن انقسام GSDMD بواسطة محللة العدلات قد يكون مستقلًا عن الكاسبيز. العدلات. توصل Orning et al.13 و Sarhan et al 14 إلى اكتشاف كبير حول شكل جديد من انقسام GSDMD الناجم عن caspase -8 في الضامة المصابة بـ Yersinia. أظهرت هاتان المجموعتان أن تثبيط الكيناز المرتبط بعامل النمو (TGF) (TAK1) أثناء عدوى يرسينيا من شأنه أن يعزز تكوين مركب موت الخلية المكون من RIPK1 و caspase -8 ، ويؤدي إلى انقسام GSDMD في الضامة. علاوة على ذلك ، كشف Demarco وآخرون. 48 عن تفاصيل تورط caspase -8 في انقسام GSDMD وقدموا دليلًا مقنعًا على أن تنشيط GSDMD المعتمد على caspase -8 من شأنه أن يعزز الفتك الناجم عن TNF-a-indiversation بغض النظر عن تنشيط الجسيم الالتهابي.
التهاب الحنجرة بوساطة GSDME. على عكس أفراد عائلة caspase الآخرين ، لطالما تم تعريف caspase -3 ، وهو ساطور GSDME ، على أنه المنفذ الرئيسي لموت الخلايا المبرمج لكل من المسارات الداخلية والخارجية. تشترك عملية التسمم العضلي بوساطة GSDME في نفس المؤثرات الأولية مع موت الخلايا المبرمج ، حيث يلعب تلف الميتوكوندريا دورًا حاسمًا (الشكل 1). يؤدي الإفراط في التعبير عن GSDME في الخلايا السرطانية إلى تبديل موت الخلايا المبرمج الناجم عن العلاج الكيميائي إلى التهاب الحموضة .17 في المقابل ، عندما يتم إلغاء التعبير عن جين GSDME ، تظل البلاعم في مرحلة موت الخلايا المبرمج التي تتميز بنفث الغشاء وتشكيل الجسم الأبوطوزيكي ، بدلاً من الدخول في المرحلة الحركية المميزة. عن طريق تضخم الغشاء والانتفاخ .16 إلى جانب تأثيرات تعبير GSDME ، وجد Xu وآخرون 18 أن الانتقال المستمر لنفاذية الميتوكوندريا يمكن أن يدفع تجميع Apaf -1- caspase -4 / 11 pyroptosome الذي يطلق GSDME- التحمل المعتمد ، في حين أن نفاذية الغشاء الخارجي للميتوكوندريا تحث على تكوين موت الخلايا المبرمج للحث على موت الخلايا المبرمج. المثير للجدل ، أفاد باحثون آخرون أن نفاذية الغشاء الخارجي للميتوكوندريا الناتجة عن تنشيط BAX / BAK أو تجميع Tom20 / BAX يؤدي أيضًا إلى تحفيز بيربتوسيس المعتمد على GSDME في الخلايا السرطانية. علاوة على ذلك ، يمكن لـ GSDME-N أن ينفخ الميتوكوندريا ، ويطلق السيتوكروم ج من الميتوكوندريا ، ويعزز تنشيط الكاسبيز -3 ، ويشكل حلقة تغذية موجبة ذاتية التضخيم.
بيروبتوسيس في أمراض الكلى
في السنوات الأخيرة ، أدى اكتشاف مسارات تأشير بيروبتوتيك إلى توسيع فهمنا لتسبب أمراض الكلى بعد موت الخلايا المبرمج. ظهرت كآلية فاعلة في الاستجابات المناعية الفطرية ، لوحظ التهاب الحموضة أولاً في البلاعم والخلايا البلعمية الأخرى. 52 وقد بُذل الكثير من الجهود لتحديد توزيع العقول المدبرة والتعبير عنها ، خاصة GSDMD و GSDME ، في مختلف الأنسجة وأنواع الخلايا ، والتي لديها أظهر أن التهاب الحنجرة لا يقتصر على البالعات .5 مجموعة متنوعة منالكلىالأمراضالمستحثة بالمحفزات الميكروبية وغير الميكروبية تتميز عادة بموت الخلايا الكلوية والاستجابات المناعية النشطة. أظهرت بعض التجارب أن التهاب الحلق يحدث في خلايا الكلى المقيمة ويساهم بشكل كبير في تطور أمراض الكلى المختلفة. وقد أوضحت دراسات أخرى أن التهاب الحنجرة في الخلايا المناعية المشتقة من نخاع العظم ، والذي تسبب في موت الخلايا الكلوية ، يمكن أن يؤدي إلى تفاقم الحالة والحفاظ عليها.إصابةالتابعالكلى. لقد حددت الأبحاث الحديثة دور التهاب الحنجرة وكذلك مسارات الإشارات الالتهابية ذات الصلة في عدة أنواع منالكلىالأمراضبما في ذلك الحادةالكلىإصابة، مرض الكلى السكري ، التي يسببها الكريستالالكلىمرض، وإصابة الطعم الخيفي في زراعة الكلى. (الجدول 1) (الشكل 2)

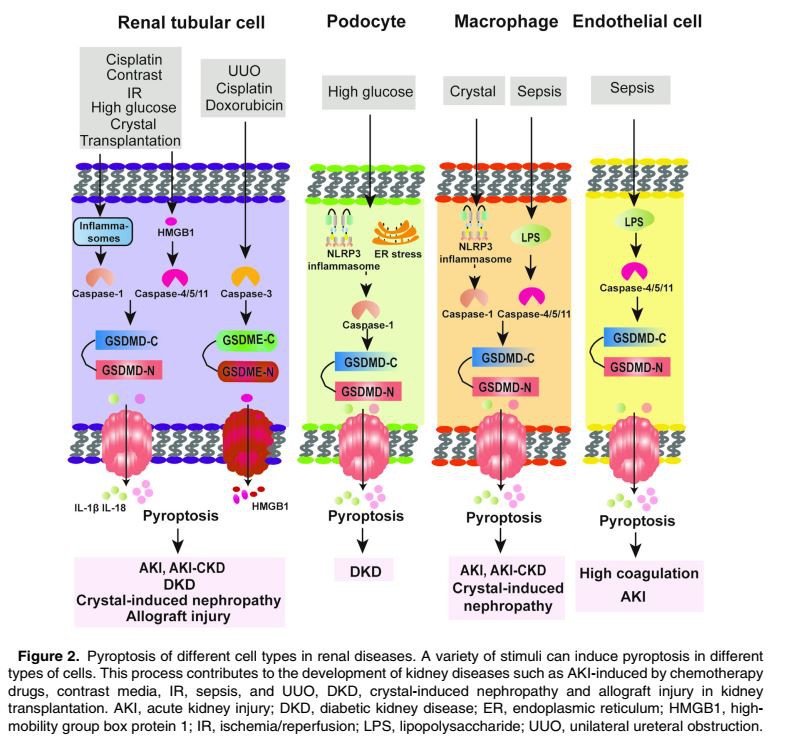
إصابة الكلى الحادة (AKI)
موت الخلية هو الحدث المرضي المحوري أثناء تطور القصور الكلوي الحاد. كان موت الخلايا المبرمج سابقًا مسؤولاً عن التسبب في أمراض القصور الكلوي الحاد .53 ومع ذلك ، فشل التثبيط الدوائي لمسارات إشارات موت الخلايا المبرمج في منع أو تخفيف AKI بشكل فعال. كشفت التطورات الحديثة دور التهاب الحلق في القصور الكلوي الحاد. في عام 2018 ، ذكر Zhang et al.54 أن الكاسبيسات -4 / 5/11 كانت مطلوبة لموت الخلايا الأنبوبية الظهارية الناجم عن التباين. لقد أظهروا كذلك أن هذه الكاسبيسات الالتهابية كانت مسؤولة عن انقسام GSDMD و IL -1 ب في الخلايا الظهارية الأنبوبية التالفة ، والتي كشفت عن الدور المطلوب للتضخم الظهاري في التهاب القصور الكلوي الحاد الناجم عن التباين. اكتشف مياو وزملاؤه 55 جزءًا مشقوقًا من GSDMD عن طريق تحليل لطخة غربية لمحلول الكلية الكاملة في كل من نماذج AKI التي يسببها السيسبلاتين ونقص التروية الناجم عن ضخه. كما أن الضربة القاضية لـ caspase -11 أو GSDMD حمت الفئران بشكل كبير من AKI الناجم عن السيسبلاتين ولكن هذا التحليل لم يتم إجراؤه في نموذج نقص التروية (I / R). لاحظ المؤلفون أيضًا انتقال GSDMD-N إلى غشاء البلازما الذي تم تعزيزه بواسطة caspase -11. اقترح تعليق بناء على هذا العمل من قبل Tonnus et al. 56 أن الهدف المحتمل لـ GSDMD-N على الأغشية داخل الخلايا والمزيد من العمل على التوزيع تحت الخلوي للجزء المشقوق من GSDMD كان مطلوبًا لفهم تشكيل محتمل مهم للمسام في داخل الخلايا. العضيات. دعمت الدراسات الإضافية مساهمة التهاب الحنجرة بوساطة GSDMD في AKI الناجم عن سيسبلاتين. وكشفت دراستنا السابقة أن التحلل العضلي بوساطة GSDMD متآزر مع تنخر بوساطة RIPK3 / MLKL لتضخيم الإشارات الالتهابية وتعزيز إصابة الأنسجة في عملية الإنتان. وجدت الحماية التراكمية ضد الإنتان الناجم عن ربط الأعور والثقب في الفئران بعد الحذف المشترك لـ Gsdmd و Ripk3 (أو Mlkl). تعاون هذان الشكلان من النخر للمساهمة في إصابة الأنسجة الحادة بما في ذلك الكلى والرئة والكبد والأمعاء والتخثر الجهازي في نموذج حيواني الإنتان. اقترحت دراساتنا حول زرع نخاع العظم أن التنخر والتشقق في الخلايا النخاعية وغير النخاعية ساهم بشكل كبير في تطور الإنتان. هناك اهتمام متزايد بالتأثيرات المجمعة لمسارات موت الخلايا المختلفة في حالة مرضية واحدة .59-61 أكدت دراسة أخرى حول شلالات التخثر في تعفن الدم أيضًا الدور المركزي لـ caspase -11 / GSDMD بوساطة البيروبتوس من أجل البدء للتخثر المنتشر داخل الأوعية (DIC) ، مما يوفر دليلًا داعمًا قويًا لخامسنا. 63- التأثيرات على القصور الكلوي الحاد وإصابات الكبد الحادة الناجمة عن تعفن الدم ، مما يحدد المسار الحركي من وجهة نظر تنظيمية.
أوضحت دراسة حديثة من مجموعتنا البحثية كيف عزز التهاب الحويصلات الهوائية بوساطة GSDME تطور إصابة النبيبات الكلوية التي يسببها انسداد الحالب والتليف الكلوي اللاحق. نموذج الانسداد (UUO) ، مما يشير إلى تورط التهاب الحموضة بوساطة GSDME في هذا النوع من إصابات الكلى. أكدنا بعد ذلك أن التهاب الحنجرة بوساطة GSDME كان مسؤولاً بالفعل عن AKI بعد UUO واعتلال الكلية اللاحق باستخدام الفئران Gsdme / و Casp 3- / -. أشارت الدراسات التي أجريت على زرع نخاع العظم إلى أن GSDME بوساطة التعرق العضلي في الخلايا المناعية المشتقة من نخاع العظم لم تكن مسؤولة عن التسبب في اعتلال الكلية الانسدادي. الخلايا الأنبوبية الكلوية (RTCs) - محددة وخلايا المكونة للدم تم إنشاء الكاسبيز المعيب للخلايا 3- من الفئران المعيبة للتحقق بشكل أكبر من حدوث التهاب الحويصلات البيروتية بوساطة GSDME في RTCs ، ولكن ليس في تسلل الخلايا المناعية ، ويساهم في الغالب في تطور إصابة الكلى والتليف الناجم عن انسداد الحالب. للتحقيق في الآليات الجزيئية الالتهابية في هذه العملية ، قمنا بمراقبة تسلل الخلايا الالتهابية وإنتاج السيتوكينات المسببة للالتهاب في الكلى. أظهرت النتائج أن التهاب الخلايا الأنبوبية يمكن أن يعزز إفراز HMGB1 والضامة وتجنيد العدلات بعد UUO. والجدير بالذكر أن دراسات أخرى أظهرت أن التهاب الحنجرة بوساطة GSDME قد يساهم في السمية الكلوية التي يسببها العلاج الكيميائي .65-66

من الجدير بالذكر أنه تم الإبلاغ أيضًا عن موت الخلايا التحللية الأخرى إلى جانب التهاب الحموضة في الإصابة بالفشل الكلوي الحاد. بالإضافة إلى التأثيرات التعاونية للتضخم الحركي والنخر في AKI الناجم عن الإنتان المذكورة أعلاه ، تدعم مجموعة متزايدة من الأدلة الدور المحوري للنخر في القصور الكلوي الحاد الناجم عن محفزات معينة. حدد Linkermann وزملاؤه (67) الدور الهام للنخر في نقص التروية الناجم عن نقص التروية الناجم عن ضخ الدم والناجم عن السيسبلاتين مثل RIPK 3- الفئران بالضربة القاضية وتطبيق مثبط RIPK1 كيناز نيكروستاتين (Nec) -1 يمكن أن يخفف كلاهما إصابة في الكلى. أثبتت مجموعتنا البحثية أن التنخر هو آلية رئيسية لموت الخلايا الأنبوبية القريبة في AKI الكلوي الناجم عن السيسبلاتين. الضربة القاضية أو مثبط كيميائي ، يمكن أن يقلل من تلف النبيب القريب الناجم عن سيسبلاتين في الفئران. في المقابل ، فإن الإفراط في التعبير عن RIPK1 أو RIPK3 عزز التنخر الناجم عن السيسبلاتين في المختبر. حددنا أيضًا التأثيرات الأساسية للنخر في الفيزيولوجيا المرضية لإصابة الأشعة تحت الحمراء والتقدم اللاحق لمرض الكلى المزمن (CKD) ، والذي تم خلاله تنشيط تنشيط NLRP3 الالتهابي. 69 غير واضح حتى الآن. بالإضافة إلى ذلك ، أظهرت العديد من الدراسات أن RIPK1 كمحرك مهم لتنشيط NF-jB ، وهو محفز فعال لـ NLRP3. في الضامة المصابة باليرسينيا ، مارس RIPK1 تحكمًا إيجابيًا في انقسام GSDMD الناجم عن كاسباس -8- ، والذي تم خلاله منع تنخر RIPK3 / MLKL. لم يتم اكتشافه في خلايا الكلى. تم الإبلاغ عن أن الداء الحديدي يسيطر على أشكال معينة من التهاب المفاصل الروماتويدي بما في ذلك الإصابة الكلوية التي يسببها سيسبلاتين وانحلال الربيدات. 71 - 72 Tonnus et al. 73 وجدوا أن الخلل الوظيفي في أنظمة مراقبة الإصابة بالتهاب الكبد الفيروسي الرئيسية من شأنه أن يزيد من حساسية الفئران للنخر الأنبوبي أثناء الإصابة بالتهاب المفاصل الروماتويدي. قام Martin-Sanchez، D. et al. 74 بدراسة توقيت مسارات موت الخلايا أثناء تطور القصور الكلوي الحاد ووجدوا أن الإصابة بالنخر الحديدي والنخر توسطت الموجتين الأولى والثانية ، على التوالي ، لموت الخلايا في AKI الناجم عن حمض الفوليك (FA). وقد تبين أن الإصابة بالفيروبتوسيس كانت مسؤولة عن بدء التهاب المفاصل الروماتويدي الناجم عن التهاب المفاصل الروماتويدي ، وقد سمح التنخر بالتهاب القصور الكلوي الحاد بالاستمرار. ينتج ROS في الميتوكوندريا أثناء الفسفرة المؤكسدة أو عند إجهاد الشبكة الإندوبلازمية (ER) ، ويؤدي إلى تحفيز بيروكسيد الدهون - العملية الأساسية لفرط الفيروس - ويتفاعل مع نظام الجلوتاثيون (GSH) -جلوتاثيون بيروكسيديز 4 (GPX4) ، والذي يمنع بشكل فعال الإصابة بالفيروسات. على الرغم من عدم وجود أدلة قوية على وجود علاقة تفصيلية بين داء الفيروبتوسيس و PCDs الأخرى ، فإن تلف الميتوكوندريا وتوليد ROS في الإصابة بالفيروبتوس يعطي أدلة محتملة على تداخله مع التنخر والتشقق (الشكل 3).

مرض الكلى السكري (DKD) DKD هو عملية مسببة للأمراض يحركها الجلوكوز وتحدث في الكلى لمرضى السكري. العوامل الرئيسية التي تنظم DKD ، بما في ذلك التدفق المفرط للجلوكوز ، والمنتجات النهائية للارتباط بالجليكوزيل المتقدم (AGEs) ، و ROS ، تعمل كأدوار حاسمة في عملية التسمم الحمضي إما كمحفزات للالتهاب أو كمنظم لمسار الإشارة. يمكن أن يؤدي إلى التهاب الحنجرة ، فقد كان NLRP3 قيد التحقيق الأكثر كثافة في DKD. يمكن تنظيم المستقبلات الشبيهة بالحصيلة (TLR) 2 و TLR4 ، PRRs المنبثقة من تنشيط NLRP3 ، من خلال ارتفاع نسبة الجلوكوز ، ويظهر مرضى السكري الذين يعانون من الفشل الكلوي زيادات كبيرة في تعبير TLR2 و TLR4 mRNA في الدم المحيطي. 76 تحفيز TLR2 و TLR4 هو ضروري لتفعيل NLRP3. 77-78 بروتين تفاعل Thioredoxin (TXNIP) ينتمي إلى نظام thioredoxin ويمكن أن يرتبط بـ thioredoxin (TRX) ، مما يقلل من التأثيرات المثبطة لـ TRX على الإجهاد التأكسدي. والاستجابات المدمرة للخلايا لـ DAMPs المتنوعة بما في ذلك التهاب الحنجرة. إشارة شائعة لتنشيط NLRP3 ويمكن أن تنشط NLRP3 من خلال مسارات مختلفة ، من بينها مسار NF-jB هو الأكثر دراسة على نطاق واسع. 85 NLRP3 يمكن أن يتحول الجسيم الملتهب إلى شكله النشط بشكل فعال من خلال ROS المشغل بمسار إشارات NF-jB. 86 - 88 في DKD ، يبدو أن قمع مسار ROS / NF-jB / NLRP3 يقلل من الاستجابات الالتهابية ويتحكم في تطور الكلى التقدمية تم تحديد إجهاد 89،90 ER باعتباره محفزًا آخر للجسيم الالتهابي NLRP3. 91،92 يمكن أن يؤدي ارتفاع السكر في الدم إلى إجهاد ER في الخلايا البادوسية ، والخلايا الظهارية الأنبوبية ، والخلايا المسراق. caspase -1 و IL -1 b و IL -18 ، والتي تساهم في تقدم DKD. قدمت الأبحاث الحديثة دليلًا على أن تثبيط NLRP3 / caspase -1- تخفف من حدة التغيرات المرضية في الكلى المصابة بداء السكري ، مما يشير إلى إمكاناتها العلاجية في DKD.96-98
يساهم التحلل الحراري في الخلايا المقيمة الكلوية المختلفة في تطوير DKD. يؤدي اضطراب البطانة الكبيبية إلى تغيير انتقائية الكبيبات ويحدث في المرحلة المبكرة من DKD. تمت ملاحظة تكتل جزئي لـ NLRP3 أو الكاسبيز المشقوق -1 مع الخلايا البطانية الكبيبية في الأقسام النسيجية للكلى البشرية أو الفئران المصابة بالسكري عن طريق الفحص المجهري متحد البؤر. تم اعتبار 99 خلية بودوسية "الحلقة الأضعف" في تطور DKD ، 100 ، ويرتبط عدد خلاياها ارتباطًا وثيقًا بالبيلة الزلالية في مرضى السكري .101 يعد فقدان الخلايا البودوسية ظاهرة مصاحبة في تطور DKD ، وتم الإبلاغ عن الإصابة بالتسمم الحبيبي. أن تكون واحدة من أهم آليات فقدان الخلايا البودوسية. الحذف الوراثي لـ TXNIP أو تثبيط NADPH أوكسيديز لتقليل ROS ، وكلاهما يتحكم سلبًا في تنشيط NLRP3 ، ويخفف بشكل كبير من إصابة خلايا الدم الناجم عن ارتفاع الجلوكوز ، مما يعطي دليلًا على دور الانحراف في فقدان خلايا البودوسية السكري .102 Liu et al. اكتشف نشاط caspase -1 المتزايد ومستويات IL -1 b و IL -18 المرتفعة في خلايا podocytes التي تعرضت لارتفاع الجلوكوز واكتشف Li et al. 104 أن GSDMD-N مشقوق في خلايا podocytes مصابة بارتفاع نسبة الجلوكوز ، تقديم المزيد من الأدلة الموثوقة على الإصابة بالتسمم العضلي في الخلية السكرية. ومن الجدير بالذكر أن المسار غير القانوني للاحتكاك العضلي يساهم أيضًا في إصابة خلية البودوسيت في DKD مع caspase -11 / 4 المتضمنة في العملية. نتيجة للإصابة الكبيبية ، يبدو أن المزيد والمزيد من الأبحاث تتحدى هذه الفرضية ، التي اكتشفت أن إصابة الأنابيب الصغيرة يمكن ملاحظتها في المرحلة المبكرة من DKD بل إنها تلعب دورًا قياديًا. 106107 في كليتي الفئران db / db وفي HK -2 من الخلايا التي تعرضت لظروف عالية من الجلوكوز ، لوحظ أن المحور ROS / TXNIP / NLRP3 / IL -1 b قد تم تنظيمه بشكل كبير ، وأن منع هذا المحور من شأنه أن يخفف من الإصابة الأنبوبية .108 اكتشف وانج وآخرون .109 أن تعبيرات TLR4 / NF-jB و GSDMD-N قد ازدادت في خلايا HK -2 تحت أجواء عالية من الجلوكوز وتثبيط TLR4 / NF-jB للإشارة يخفف كاسباس -1 / GSDMD بوساطة الخلايا الأنبوبية ، مشيرًا إلى أن التهاب الحلق الناجم عن TLR4 / NF-jB شارك في t إصابة الأنبوب السكري. من الجدير بالذكر أن التهاب الحنجرة قد لا يكون المسار الوحيد المهم لموت الخلايا في DKD. تم التحقيق في حالات الإصابة بمرض الفيروبتوسيس ، و التنخر 110 ، و موت الخلايا المبرمج 112 في العديد من الحالات. ومع ذلك ، لم يتم تحديد التمييز الواضح و / أو الارتباط بين مسارات موت الخلايا المختلفة في تطوير DKD بشكل كامل.
مرض الكلى الناجم عن الكريستال
يمكن أن تؤدي البلورات إلى إصابات في الكلى تتراوح من خفيفة / عابرة إلى شديدة / لا يمكن إصلاحها اعتمادًا على توطين وديناميكيات ترسب الكريستال. تظل الآليات الجزيئية لأمراض الكلى التي تحدثها البلورات غير معروفة إلى حد كبير على الرغم من الجهود البحثية الكبيرة. كشفت دراسة متقدمة أن البلورات يمكن أن تحفز تنشيط NLRP3 وأظهرت الدور المحوري للجسيم الملتهب في الخلل الوظيفي الناجم عن البلورات أو الأمراض. تم تحديده على أنه السبب الرئيسي لتطور اعتلال الكلية بالأكسالات 114 واعتلال الكلية بأكسالات الكالسيوم ، 115 مما يؤدي إلى تحويل النقطة الساخنة في البحث عن أمراض الكلى المستحثة بالبلورات من رواسب بلورية إلى استجابات التهابية. يمكن للبلورات المترسبة في الشرايين والنبيبات الكلوية تنشيط الجسيم الالتهابي NLRP3 والحث على الالتهاب المرتبط بـ IL - 1. بلورات الكوليسترول هي السبب الأكثر شيوعًا لتلف الأوعية الكلوية في اعتلالات البلورات الكلوية. اكتشف دويل وزملاؤه 116 أن بلورات الكوليسترول يمكنها تنشيط الجسم الالتهابي NLRP3 وتعزيز إنتاج IL -1 ب في البلاعم ، وهو أمر أساسي في التسبب في تصلب الشرايين الناجم عن البلورات. يمكن أن تؤدي الاعتلالات البلورية الأنبوبية ، التي تنتج عن ترسيب البلورات داخل التجويف الأنبوبي ، إلى تعزيز كل من الآفات الكلوية المزمنة والأمراض الكلوية المزمنة. اكتشف Liu وزملاؤه 118 تعبيرًا مرتفعًا عن تعبير GSDMD و IL -18 في الخلايا الأنبوبية المعرضة لبلورات أكسالات الكالسيوم من خلال علامة الكتلة الترادفية القائمة على كروماتوجرافيا السائل والقائمة على قياس الطيف الكتلي والتي تحدد التحليلات الكمية البروتينية والسلوكيات البيولوجية المرتبطة بالتضخم الالتهابي المُحدد من خلال علم الوجود الجيني وموسوعة كيوتو لتحليلات إثراء الجينات والجينوم. أكدت النتائج الإضافية تنشيط NLRP3 والتهاب الحمم المعتمد على GSDMD في الخلايا الظهارية الأنبوبية في النماذج المستحثة ببلورات أكسالات الكالسيوم. اكتشف دينج وزملاؤه 119 أيضًا مستويات بروتينية متزايدة من NLRP3 في متجانسات الكلى للفئران المصابة بتحصي الكلية الناجم عن الغليوكسيلات وفي خلايا HK {{30} المعرضة لبلورات أحادي الهيدرات أكسالات الكالسيوم. لوحظ في الوقت نفسه زيادة مستويات التعبير البروتيني لـ IL -1 b و GSDMD في الخلايا الظهارية الأنبوبية المعزولة من كليتي الفئران المعالجة بالجليوكسيلات ، مما يدعم فكرة أن الخلايا الأنبوبية المكشوفة للبلورات خضعت ل GSDMD. قدم عدد كبير من التجارب دليلاً على تنشيط NLRP3 بواسطة البلورات في الخلايا المناعية بما في ذلك الخلايا الضامة والخلايا التغصنية بطرق مختلفة ، 120-122 والتي تم تأكيدها في اعتلال الكلية الناجم عن البلورات. تطور مرض الكلى المزمن. أظهر كناوف وزملاؤه 114 أن محور NLRP 3- IL -1 ب تم تنظيمه في الفئران المصابة باعتلال الكلية بالأكسالات بينما كانت الفئران NLRP 3- / - محمية تمامًا من الفشل الكلوي التدريجي الناجم عن التغذية مع نظام غذائي غني بالأكسالات القابلة للذوبان. وصفت دراسة رائدة أخرى أجراها مولاي وزملاؤه 115 مشهدًا أكثر عمقًا حيث كان الفشل الكلوي الناتج عن اعتلال الكلية المؤكسد يعتمد بشدة على NLRP3 / ASC / caspase -1 / IL -1 المحور ب. ومع ذلك ، لم يكن هناك اكتشاف مباشر لانقسام GSDMD في عملية التليف الكلوي المرتبط بالبلورات. بشكل ملحوظ ، تم الإبلاغ عن أشكال أخرى من PCD بما في ذلك RIPK 3- مسار MLKL النخر 123،124 و ferroptosis125 للمساهمة في إصابة الكلى التي تسببها البلورات. ما إذا كانت هذه الوفيات المختلفة للخلايا تعاونية أو مستقلة لا يزال قيد التحقيق. إن تأثير النوع البلوري وديناميكياته على المصير الخلوي لخلايا الكلى له أيضًا أهمية كبيرة.
إصابة الطعم الخيفي في زراعة الكلى
لا يزال زرع الكلى هو الخيار الأمثل للمرضى الذين يعانون من مرض الكلى في نهاية المرحلة (الداء الكلوي بمراحله الأخيرة). نظرًا لتزايد عدد السكان الذين يحتاجون إلى زراعة الكلى خلال العقود الأخيرة ، فقد تم إيلاء اهتمام متزايد لإصابة الطعم الخيفي في كل من المتبرعين والمتلقين. يمكن إطلاق HMGB1 من الخلايا التي تعاني من التهاب الحنجرة. ووجد Kru¨ger وزملاؤه 126 أن الأنابيب من الكلى المتوفاة - ولكن ليس من متبرع حي - ملطخة بشكل إيجابي لـ HMGB1. أظهروا كذلك أن HMGB1 يمكن أن يحفز الاستجابات المسببة للالتهابات من خلال TLR4 ، مما ساهم في التهاب الكسب غير المشروع والإصابة المعقمة بعد الحفظ البارد والزرع. اكتشف تييري وزملاؤه 127 ارتفاعًا في نسبة HMGB1 البولي في أقرب وقت بعد 30 دقيقة من ضخه بعد زرع الكلى البشرية وتحدثوا عن دوره المحتمل كوسيط مناعي فطري في مثل هذه الإصابة. تم الإبلاغ عن زيادة السيتوكينات الالتهابية IL -1 ب في المتبرعين بالأعضاء المتوفين بالدماغ ، ومن المحتمل أن يشير 128129 إلى تورط التهاب الحموضة في عملية إصابة العضو. بذل الباحثون جهودًا مكثفة من أجل دراسة تنشيط الجسيم الملتهب في الخلل الوظيفي في الطعم الخيفي. وجد Design وآخرون 130 أن المتغيرات الجينية في جين NLRP3 تؤثر على خطر الرفض الحاد بعد زراعة الكلى. أظهر Wu et al.131 أن الفئران التي تعاني من نقص في بروتين محول TLR MyD88 كانت محمية من كل من رفض الطعم الخيفي الحاد والمزمن وزادت من بقائها بعد الزرع مقارنةً بعناصر التحكم من النوع البري. ذكرت دراسة أخرى أن نقص MyD88 المتبرع يثبط التعبير الخلوي الالتهابي وإجهاد ER ، وكان مرتبطًا بتحسين وظيفة الكسب غير المشروع وبقاء الطعم الخيفي لفترات طويلة. نموذج الزرع. لوحظ انخفاض في تنشيط الكاسبيز -1 ومستويات GSDMD-N بعد علاج Mcc950.
استهداف العلاجات المحتملة
تثبيط بيروبتوسيس: بالنظر إلى الدور الهام للتضخم في الأمراض الداخلية ، يعد تعديل هذه العملية مصدر قلق كبير. الأهداف المحتملة في بيروبتوتيك
Pathway تشمل inflflammasomes و caspases والعقول المدبرة و IL -1 b (الشكل 4). التهاب النكران الناجم عن الاستجابات المناعية للنخر بما في ذلك التنخر ، والتهاب الجلد ، والتهاب الأنسجة يؤدي إلى إصابة الأنسجة. سلط لينكرمان وزملاؤه 134،135 الضوء على الأهمية السريرية لاستهداف التهاب التنخر في إصابة الكلى. نظرًا لأن بعض المحفزات قد تؤدي إلى أكثر من مسار واحد لموت الخلية في الخلايا والأنسجة المصابة ، فقد جذبت إمكانات الاستراتيجيات المشتركة المستهدفة على مسارات موت الخلايا المختلفة اهتمامًا متزايدًا.

استهداف NLRP3 الالتهاب. يعمل NLRP3 inflflammasomes في اتجاه مجرى الانهيار الحراري بوساطة الكاسبيز -1 / GSDMD وقد تم تطوير العديد من الأدوية التي تستهدف NLRP3 بآليات تثبيط مختلفة. المتلازمات المصاحبة لـ NLRP 3- .137 في نموذج الفئران لاعتلال الكلية البلوري الناجم عن الأنظمة الغذائية الغنية بالأكسالات أو الأدينين ، قلل Mcc950 بشكل ملحوظ من التنشيط الالتهابي في الخلايا التغصنية الكلوية وما تلاه من IL -1 و IL {{13} } إنتاج. منع هذا المانع NLRP3 أيضًا بشكل فعال من الفيفيبروز الكلوي المستحث بالبلورات .138 BAY 11-7082 ، والذي تم الإبلاغ عنه في البداية لمنع الفسفرة IjBa وتنشيط NF jB ، وقد تم تحديد 139 كمثبط لـ NLRP3 ATPase. أوضحت جوليانا وزملاؤها 140 أن BAY 11-7082 يثبط تنشيط NLRP3 الالتهابي في الضامة التي تستعد لـ LPS بشكل مستقل عن تأثيره على NF-jB ويمنع NLRP 3- الناجم عن تكوين البيربتوزوم ASC عن طريق تثبيط نشاط NLRP3 ATPase. في الفئران التي تناولت نظامًا غذائيًا عالي الدهون وعالي الفركتوز ، خففت BAY 11-7082 من الزيادة التي يسببها النظام الغذائي في تعبير NLRP3 الملتهب ، مما أدى إلى تثبيط -1 تنشيط كاسباس والإنترلوكين (IL) {{33} } ب و IL -18 إنتاج في الكبد والكلى. حدت إدارة BAY 11-7082 المزمن بشكل كبير من التلف الكلوي الناجم عن النظام الغذائي عن طريق تحسين نسبة الألبومين إلى الكرياتينين. 141 في نموذج الفئران لاعتلال الكلية السكري ، تم العثور على علاج BAY 11-7082 لاستعادة البنية النسيجية للكلية بشكل ملحوظ ومستويات طبيعية من السيتوكينات الالتهابية بما في ذلك IL - 1 b ، مما يدعم التأثير الوقائي للكلية لـ BAY 11-7082 لـ DKD.142 b-Hydroxybutyrate (BHB) ، المنتج أثناء الحرمان من الطاقة أو اتباع نظام غذائي منخفض الكربوهيدرات ، مما أعاق تنشيط NLRP3 ومنع التليف الكلوي الكلوي الناجم عن التكلس الكلوي .143 ومع ذلك ، فإن التأثيرات الوقائية لم يتم التوسط فيها بالضرورة عن طريق إطلاق IL داخل الكلى -1 ، وما إذا كان BHB يؤثر على التهاب الحنجرة لا يزال بحاجة إلى توضيح. تم الإبلاغ عن مثبطات NLRP3 الأخرى بما في ذلك فلورو فينيدون 144 وترانيلاست 145 لتلعب أدوارًا واقية في نموذج انسداد الحالب أحادي الجانب (UUO) بينما الآلية الجزيئية الكامنة وراء التهاب الحالب لا تزال غير واضحة.
استهداف الكاسبيسات الحرارية. تم إجراء تحقيق مكثف في مثبطات الكاسبيسات الحرارية. Ac-YVAD-CMK ، مثبط -1 كاسباس ، يمكن أن يخفف من ضعف وظائف الكلى في نموذج الفئران AKI 146 ويقلل من التهاب الخلايا البطانية الكبيبية في نموذج فأر اعتلال الكلية السكري 99 VX -765 ، كاسباس آخر {{ 6}} ، كان كافيًا لتقليل عدد البلاعم المسببة للالتهابات في المرحلة اللاحقة من UUO.147 Chu et al. 148 أظهر أن الفسفوليبيد المؤكسد 1- بالميتويل -2- الأراكيدونيك نويل-سن-جليسيرول {{ 13}} يمكن أن يرتبط الفسفوريل كولين (oxPAPC) مباشرة بـ caspase -4 و caspase -11 ، ويتنافس مع LPS ، وبالتالي يمنع التهاب البروتونات الناجم عن LPS ، مما يوفر دليلًا جديدًا للدور الدقيق لـ oxPAPC في الاستجابة الالتهابية . يمكن أن يوفر oxPAPC ومشتقاته رؤية جديدة للعلاجات التي تستهدف التهاب الجلد غير الكنسي. أفاد Choi et al.149 أن عضو عائلة Serpin B 1 (SERPINB1) حد من نشاط caspase -1 / 4/5/11 عن طريق قمع oligomerization مجال التوظيف caspase (CARD) والتنشيط الأنزيمي ، مما يكشف عن آلية نقطة تفتيش جديدة لالتهاب الكاسبيسات. تعاون SERPINB1 مع بروتين Forkhead box O1 (FoxO1) لتحسين الإجهاد التأكسدي الناجم عن إنتاج ROS في DKD.150 ومع ذلك ، فإن الإمكانات العلاجية لاستهداف بروتين نقطة التفتيش هذه لا تزال قيد الاستكشاف.
استهداف العقل المدبر. إن تحديد العقول المدبرة كمنفذين للإصابة بالتهاب الحنجرة يثير أملاً جديدًا في العلاج الموجه للأمراض المرتبطة بالتهاب الحرق. أجرى Hu et al 151 فحصًا كيميائيًا حيويًا عالي الإنتاجية وحدد ديسفلفرام كمثبط فعال لتشكيل مسام GSDMD. أظهرت دراسة أخرى أن ديسفلفرام يمكن أن يحسن معدل الوفيات الناجم عن GSDMD في تعفن الفئران .152 بالإضافة إلى ذلك ، يتحكم الديسفلفيرام أيضًا بشكل سلبي في التنخر من خلال ربط MLKL.153. الأمراض واعدة. يمكن لمثبط مشتق من GSDMD ، Ac-FLTD-CMK ، أن يمنع انقسام GSDMD بواسطة الكاسبيسات -1 / 4/5/11 عن طريق الارتباط المباشر بالمنطقة المحفزة لهذه الكاسبيسات ، وبالتالي قمع فرط الحموضة في اتجاه مجرى النهر لكل من المسارات الكنسية وغير الكنسية .154 A 2020 أظهرت دراسة أن الكالسيوم (Ca) 2 بالإضافة إلى التدفق كان شرطًا أساسيًا لوظيفة GSDMD-N والمغنيسيوم (Mg) 2 بالإضافة إلى منع تدفق Ca2 plus عن طريق تثبيط قناة Ca2 plus P2X7 التي تحتوي على ATP ، مما يعيق الوظيفة. GSDMD-N وتثبيط الالتهاب غير الكنسي الناجم عن LPS. تشير هذه النتائج إلى تطبيقات العيادة المحتملة لمكملات المغنيسيوم لعلاج الإنتان
استهداف IL -1. أصبح IL -1 نقطة ساخنة للبحث لاستراتيجيات تعديل المناعة التي تستهدف الأمراض المرتبطة بالتهاب. على وجه الخصوص ، كان الجسم المضاد أحادي النسيلة IL -1 ب canakinumab البشري قيد التحقيق المكثف. قيمت دراسة CANTOS (دراسة نتائج تجلط التجلط المضاد للالتهاب من كاناكينوماب) فعالية كاناكينيوماب في 10061 مريضًا يعانون من احتشاء عضلة القلب سابقًا ومستوى بروتين سي التفاعلي عالي الحساسية يبلغ 2 مجم / لتر. وقد أظهر التحليل الفرعي لبيانات CANTOS. أن تثبيط IL -1 ب كاناكينيوماب قلل من معدلات الأحداث القلبية الوعائية العكسية الكبرى بين مرضى تصلب الشرايين المعرضين لمخاطر عالية مع CKD ، لا سيما بين أولئك الذين لديهم استجابة قوية مضادة للالتهاب للعلاج الأولي ، مما يشير إلى فائدة تطوير العامل المضاد للالتهاب في CKD.157
التنظيم المتزامن لـ PCDs المختلفة
في الآونة الأخيرة ، تم إيلاء المزيد من الاهتمام للحديث المتبادل والتنسيق بين PCDs المختلفة في بعض الأمراض. تم الكشف عن التأثيرات التعاونية للتضخم العضلي بوساطة GSDMD والنخر بوساطة MLKL في AKI58 وأمراض الأمعاء الالتهابية .59 علاوة على ذلك ، تم اقتراح مفهوم ناشئ حديثًا يسمى PANoptosis لوصف التنظيم المشترك بين التهاب الحموضة ، التنخر ، وموت الخلايا المبرمج. بروتين الربط 1 (ZBP1) ، وتحويل عامل النمو كيناز 1 المنشط بيتا (TAK1) ، FS 7- مستضد سطح الخلية المرتبط (Fas) - مجال الموت المرتبط (FADD) ، و Caspase -8 قد تتعاون مع العمل كمنظمين رئيسيين لداء الخلايا البانوبوتية في تنظيم مسارات موت الخلايا المتعددة. AKI. تضع هذه العناصر أساسًا لمقاربات علاجية فعالة لاستهداف مسارات موت الخلايا متعددة الأوجه في أمراض الكلى.

الاستنتاجات
اقترحت مجموعة من الأدلة الأدوار الحاسمة للتضخم الحركي في أمراض الكلى وكشفت عن عدد من العوامل المتضمنة في التهاب الحموضة مثل NLRP3 و caspase -1 و GSDMD و IL -1 ، والتي يمكن تعديلها وراثيًا و / أو دوائيا للاستخدام العلاجي. لقد ثبت أن التهاب الحويصلات المتعرجة بوساطة GSDMD يلعب دورًا مركزيًا ويمتلك الإمكانية كهدف علاجي في أمراض الكلى المختلفة ، بما في ذلك أمراض الكلى المزمنة ، وأمراض الكلى الناتجة عن البلورات ، وإصابة الطعم الخيفي في زراعة الكلى. لقد فتحت النتائج التي تم التوصل إليها حول الإصابة بالتسمم العضلي غير الكنسي بوساطة GSDMD ، والتي يتم تحفيزها بواسطة LPS ، طريقًا جديدًا لعلاج تلف الأعضاء الناجم عن الإنتان. كما أن الاكتشاف الأخير للتضخم العضلي بوساطة GSDME كمنظم رئيسي لـ AKI وما تلاه من تقدم AKI-CKD يوفر رؤى جديدة في إدارة AKI والوقاية من CKD. بالإضافة إلى ذلك ، قد يُظهر التنظيم المتزامن لمسارات موت الخلايا المتعددة تأثيرات أكثر فائدة على الكلى ، لأن بعض المحفزات عادةً ما تؤدي إلى أكثر من مسار موت واحد.
ومع ذلك ، لا يزال فهمنا للإصابة بالتهاب الكلى في سياق أمراض الكلى محدودًا. استندت الدراسات المنشورة حول التهاب الكلى في أمراض الكلى إلى عدد محدود من التجارب على الحيوانات والخلايا. لا يزال يلزم إعادة إنتاج البيانات الحالية بالإضافة إلى ترجمة البيانات التجريبية إلى الإعدادات السريرية. لا تزال آليات البصيرة لمسارات الانبعاث الحراري المختلفة في ظل ظروف إجهاد مختلفة و / أو في أنواع مميزة من الخلايا الكلوية ، بالإضافة إلى الحديث المتبادل والتفاعل بين التهاب الحنجرة وأشكال أخرى من موت الخلايا ، غير معروفة إلى حد كبير. من الأهمية بمكان إجراء مزيد من التحقيق في آليات الانقسام الحراري وكذلك تنسيق العديد من PCDs في الفيزيولوجيا المرضية الكلوية ، مما سيساعد على الاستفادة من إمكانات العلاجات المستهدفة لحل المعضلات السريرية وكسر عنق الزجاجة الإكلينيكي في أمراض الكلى.
من: "Pyroptosis في أمراض الكلى"Yujia Wang و Yinshuang Li و Yanfang Xu1
--- مجلة البيولوجيا الجزيئية
