R. Vesicarius L. يمارس تأثير كلوي ضد الإجهاد التأكسدي الناجم عن السيسبلاتين
Mar 26, 2022
جهة الاتصال: Audrey Hu Whatsapp / hp: 0086 13880143964 البريد الإلكتروني:audrey.hu@wecistanche.com
محمد الحسن محمود1، معظم. سايلا تاسمين2احمد محمد الشهاوي3منى محمد الصحي4ابو رضا1وأريفول حق2*
الملخص
خلفية:Cisplatin هو دواء بارز مضاد للسرطان ، لكن استخدامه قد انخفض بشكل ملحوظ بسبب السمية الكلوية الشديدة. R. بالنيابة L. هو نبات نباتي يتضح أنه مضاد لتولد الأوعية ، ومضاد للالتهابات ، ومضاد للتكاثر ، ومضاد لتكاثر الكبد ، ومضاد للكلى. لذلك ، تم تصميم هذه الدراسة لفحص مستخلص الميثانول (RVE) لمعرفة التأثير الكلوي المحتمل.
طُرق:في المقام الأول ، في المختبر ، تم تأكيد النشاط المضاد للأكسدة لـ RVE على أساس 2 ، 2- diphenyl -1- picrylhydrazyl (DPPH) كنس الجذور الحرة. بعد ذلك ، عولجت ذكور الفئران السويسرية البيضاء باستخدام سيسبلاتين (2.5 مجم / كجم) لمدة 5 أيام متتالية للحث على السمية الكلوية. تم فحص التعافي من السمية الكلوية عن طريق معالجة الحيوانات بـ RVE (25 و 50 و 100 ملغم / كغم) داخل الصفاق (IP) لمدة 5 أيام متتالية. بعد الانتهاء من العلاج ، تم التضحية بالفئران وجمع الكلى. تم تجانس جزء منه في محلول فوسفات الصوديوم لتقييم مستوى malondialdehyde (MDA) ، وتم استخدام جزء آخر لتقييم التعبير الجيني (NQO1 و p53 و Bcl -2). علاوة على ذلك ، تم تقييم قدرة تحييد بيروكسيد الهيدروجين (H2O2) لـ RVE في خلايا HK -2 في المختبر. أخيرًا ، تم تحديد المواد الكيميائية النباتية النشطة بيولوجيًا في RVE باستخدام مقياس الطيف الكتلي اللوني للغاز (GC-MS).
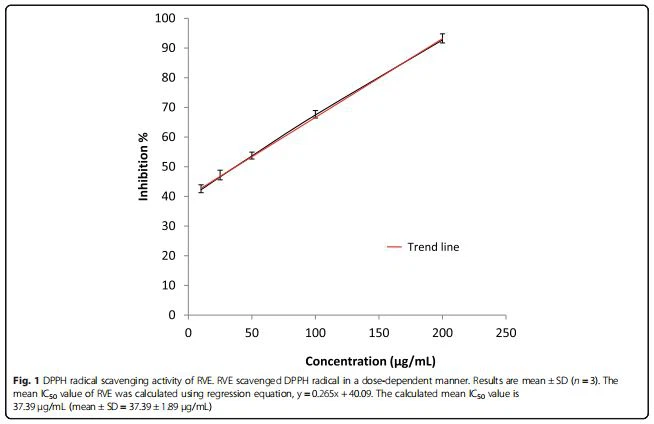
نتائج:أظهر RVE نشاطًا مضادًا للأكسدة في المختبر بطريقة تعتمد على الجرعة بقيمة 37.39 ± 1.89 ميكروغرام / مل IC50.
أدى العلاج باستخدام RVE بشكل ملحوظ (p <{0}}. 0="" 5)="" إلى="" انخفاض="" محتوى="" mda="" في="" أنسجة="" الكلى.="" إلى="" جانب="" ذلك="" ،="" تم="" تخفيف="" التعبير="" عن="" جينات="" nqo="" و="" p53="" و="" bcl="" -2="" بشكل="" كبير="" (p=""><0.05) بطريقة="" تعتمد="" على="" الجرعة="" بسبب="" إعطاء="" rve.="" عكس="" rve="" بشكل="" ملحوظ="" (p=""><0.05) مستوى="" h2o2="" في="" خلايا="" hk="" -2="" إلى="" المستوى="" الطبيعي="" تقريبًا.="" من="" gc-ms="" ،="" عشرة="" مركبات="" بما="" في="" ذلك="" ثلاثة="" مضادات="" أكسدة="" معروفة="" "4h-pyran="" -4-="" one،="" 2،="" 3-="" dihydro="" -3،="" 5-="" dihydroxy="" -6-="" methyl-"="" تم="" اكتشاف="" "حمض="" هيكساديكانويك"="" و="" "سكوالين".="" كان="" المستخلص="" غنيًا="" بمادة="" قلويد="" "13-="">
استنتاج:بشكل عام ، تمتلك RVE تأثيرًا وقائيًا ضد تلف الكلى الناجم عن السيسبلاتين.
الكلمات الدالة:سيسبلاتين ، R. بالنيابة ، الفئران ، الكلى ، خلايا HK {0} ، الإجهاد التأكسدي ، جين NQO1

يمنع Cistanche deserticola أمراض الكلى ، انقر هنا للحصول على العينة
مقدمة
ينتج الإجهاد التأكسدي عن عدم التناسب بين تكوين أنواع الأكسجين التفاعلية (ROS) وآليات الدفاع المضادة للأكسدة المنتظمة [1]. تؤدي التفاعلات الكيميائية الحيوية المنتظمة ، والتعرض المتكرر للبيئة غير المواتية ، وزيادة تناول المواد الغريبة الحيوية إلى إنتاج أنواع الأكسجين التفاعلية [1]. يتفاعل ROS مع بقايا السيستين لجزيئات التأشير الحساسة للأكسدة والاختزال بما في ذلك عوامل النسخ ، وبروتين فوسفاتيز التيروزين ، وكينازات البروتين ؛ وبالتالي ، فإن أكسدة مجموعات الثيول على هذه البقايا يرشد إلى تغييرات البروتينات المستهدفة ، والإجراءات البيولوجية ، وقدرات الإشارة ، والمناعة ، والنماذج الحية / الميتة للخلايا التكميلية [2]. تُعرف الأنواع الكيميائية المحتوية على الأكسجين والتي لها خصائص تفاعلية باسم ROS والتي تتضمن الجذور الحرة والجزيئات غير الجذرية مثل الأكسيد الفائق و H2O2 على التوالي [3]. يرتبط الإجهاد التأكسدي الناجم عن أنواع الأكسجين التفاعلية بمسببات العديد من الأمراض بما في ذلك السرطان. ابيضاض الدم النخاعي الحاد (AML) هو نمو سرطاني لخلايا الدم داخل نخاع العظام. تشمل الأحداث الخلوية والجزيئية الكامنة وراء ابيضاض الدم النقوي الحاد (AML) تلف الحمض النووي ، والتكاثر النسيلي ، وزيادة موت الخلايا ، وزيادة عدم الاستقرار الجيني ، والتي تنتج عن الإجهاد التأكسدي الناجم عن أنواع الأكسجين التفاعلية [4]. تم تزويد علم وظائف الأعضاء البشري بالعديد من الآليات التي يمكن أن تولد مضادات الأكسدة لممارسة الحماية ضد الإجهاد التأكسدي مما يؤدي إلى حماية الخلايا من التأثيرات السامة وخدمة الوقاية من الأمراض [5]. ومع ذلك ، تطور الخلايا آليات داخلية لمواجهة الإجهاد التأكسدي والحفاظ على ROS المطلوب [6].
NAD (P) H: quinone oxidoreductase 1 (NQO1) هو إنزيم فلافوينزيم [7] يمكنه تحفيز تخليص إلكترونين أو أربعة إلكترون ويستخدم هذه الخاصية لإزالة السموم من الكينينات [8]. يمكن أن تحمي الخلايا من الضرر التأكسدي عن طريق إبقاء دورة الأكسدة والاختزال جانبًا وتقليل إنتاج الجذور الحرة [8]. إلى جانب إزالة السموم من الكائنات الحية الغريبة ، يشارك NQO1 أيضًا في معادلة الأكسيد الفائق ، وتعديل تحلل البروتين البروتيني p53 [9] ، وتثبيط Bcl -2 [10] ، وتعزيز القابلية لإصابة الخلية [11].
سيسبلاتين هو أول دواء مضاد للسرطان معتمد من إدارة الغذاء والدواء (FDA) [12]. يمارس السيسبلاتين موت الخلايا المبرمج عن طريق إحداث الإجهاد التأكسدي والإفراط في التعبير عن الجين الكابت للورم p53 [12]. العديد من الآثار الضارة بما في ذلك السمية الكلوية ، والسمية الكبدية ، والسمية المعوية ، والسمية الأذنية ، وكبت النخاع ، والسمية العصبية هي نتيجة الإجهاد التأكسدي الناجم عن السيسبلاتين [12]. وقد أدت هذه الآثار الجانبية بشكل ملحوظ إلى انخفاض استخدام السيسبلاتين على الرغم من أن له نشاطًا بارزًا مضادًا للسرطان. ومن المعروف أن السيسبلاتين يسبب الإجهاد التأكسدي ويثبط الجين NQO1 في كلى الفئران [13]. لذلك ، أصبح البحث عن المصادر الطبيعية الفعالة لمضادات الأكسدة والتحقق منها مجالًا للوعي. قد يؤدي تناول مضادات الأكسدة الغذائية المشتقة من النباتات مثل الفلافونويد والكاروتينات والمركبات الفينولية إلى الحماية من أمراض القلب والأوعية الدموية وإعتام عدسة العين والسرطان [14].
يُعرف R. vicarious (Polygonaceae) باسم "Takpalong / Chukapalong / Amlabetom" في البنغالية [15]. ينمو في المناطق الصحراوية وشبه الصحراوية في آسيا وأستراليا وشمال إفريقيا [16]. إنه نبات مهدد بالانقراض تمت دراسته قليلاً في بنغلاديش. في بنغلاديش ، يستهلك الناس النبات بأكمله كخضروات بعد الطهي بالملح والتوابل المختلفة والزيت. في بعض الأحيان ، يستخدم الناس الأوراق الطازجة فقط في السلطة المختلطة كبديل للخس. الأوراق النيئة حامضة قليلاً ، لكنها تصبح شديدة الحموضة بعد الطهي. علاوة على ذلك ، عادة ما يتم خلط عدد قليل من الأوراق في أطباق السمك أثناء الطهي للحصول على طعم حمضي خفيف.
يتم استخدام هذا النبات كعشب نباتي وعشب طبي في جميع أنحاء العالم [17]. تستخدم الأوراق والبذور كمضاد لسم الأفعى والعقارب على التوالي [17]. في العلاج الشعبي ، يستخدم R. ملين ، معدي ، فاتح للشهية ، منشط ، مدر للبول ، ومسكن [18]. يحتوي هذا النبات على العديد من المركبات المهمة بيولوجيًا بما في ذلك مركبات الفلافونويد والأنثراكينون والكاروتينات والفيتامينات والدهون والأحماض العضوية ، والتي تُعرف جيدًا بمضادات الأكسدة ومضادات الميكروبات والعوامل المضادة للسرطان [19]. يحتوي كل جزء من هذا النبات على الكيرسيتين (الفلافونويد) بكمية مرتفعة [15]. يحتوي هذا النبات على 0. 25 مجم فيتامين أ ، 1.33 مجم فيتامين ج ، 2.37 مجم فيتامين هـ [15] ، 3.38 ملليجرام فلافونويد ، 5.66 ملليجرام بوليفينول [20] لكل 100 جرام وزن جاف.
أظهر الشحات وزملاؤه [21] تأثيرًا مضادًا لتولد الأوعية ومضادًا للتكاثر لمستخلص الميثانول (80 بالمائة) من الجزء الجوي للبكتيريا R. ضد سرطان الخلايا الكبدية في نموذج الفئران. وأظهرت دراسة أخرى في المختبر القدرة المضادة لتولد الأوعية من مستخلص ر. يوفر مستخلص الميثانول من نبات R. الكامل بالنيابة الحماية ضد السمية الكبدية التي يسببها رابع كلوريد الكربون في الجسم الحي [23]. كان التأثير المضاد للالتهابات في الأرانب واضحًا من خلال مستخلص أوراق الميثانول لـ R. أفادت دراسة حديثة [25] في التأثير الواقي للكلية في الجسم الحي لمستخلص R. الإيثانولي المجزأ ضد سمية الجنتاميسين وثاني كرومات البوتاسيوم.
مع مراعاة المعلومات المذكورة أعلاه ، كنا نهدف إلى فحص تأثير مستخلصات R.

الفوائد الصحية cistanche: علاج أمراض الكلى
المواد والأساليب
المواد الكيميائية والكواشف
تم شراء Cisplatin و 2 ، 2- diphenyl -1- picrylhydrazyl (DPPH) من SIGMA-ALDRICH (الولايات المتحدة الأمريكية).
تم شراء مجموعة فحص الكرياتينين اللوني (معرف المنتج - 700،460) من كايمان كيميكال (الولايات المتحدة الأمريكية). تم شراء Dulbecco's Modified Eagle's Medium (DMEM) ، ومصل الأبقار الجنيني (FBS) ، والمضادات الحيوية (10 ، 000 U / mL البنسلين و 10 ، 000 ميكروغرام / مل ستربتومايسين) من Gibco (مختبرات Gibco ، الولايات المتحدة الأمريكية). تم الحصول على مجموعة الفحص ROS-Glo ™ H2O2 و GoTaq® qPCR Master Mix من Promega (الولايات المتحدة الأمريكية). تم شراء مجموعة النسخ العكسي TIAN- Script M-MLV من TIANGEN (الصين) والبادئات من IDT (تقنيات DNA المتكاملة ، ماليزيا). كانت جميع المواد الكيميائية والكواشف الأخرى المستخدمة في هذه التجربة من الدرجة التحليلية.
جمع العينات النباتية وتحضير المستخلص
تم شراء نباتات طازجة من نبات R. تم التعرف على عينة النبات والمصادقة عليها من قبل الدكتور أحمد همايان كبير ، قسم النبات ، جامعة راجشاهي ، بنغلاديش. عينة تحت قسيمة رقم. 00095 تم تخزينها في المعشبة التابعة لقسم النبات بجامعة راجشاهي. تم تنظيف الأجزاء الهوائية من النبات وتجفيفها عند 37 درجة وطحنها إلى مسحوق خشن باستخدام مجفف إلكتروني وتخزينها في حاوية محكمة الغلق عند 4 درجات. تمت إذابة المسحوق الناعم (10 جم) في ميثانول (500 مل). تم صوت المحتوى (Soni- الإعدادية 150 ، الصين) عند 20 كيلو هرتز لمدة 10 دقائق. تم إجراء ترشيح المستخلص باستخدام ورق ترشيح الألياف الزجاجية (Macherey NAGEL ، GmBH ، ألماني) مع جهاز تصفية DURAN (ألماني). أخيرًا ، تم تركيز ناتج الترشيح باستخدام مجفف بالتجميد (VirTis Benchtop Pro ، SP SCIENTIFIC ، الولايات المتحدة الأمريكية). تم تسمية المقتطف أخيرًا RVE.
اختبار نشاط مضادات الأكسدة في المختبر
تم إجراء قدرة مضادات الأكسدة في المختبر لـ RVE على أساس تنظيف DPPH كما هو موضح سابقًا [26] مع القليل من التعديل. تم تقييم قدرة الكسح الجذري لـ DPPH لـ RVE على أساس تحويل اللون الأرجواني لـ DPPH إلى اللون الأصفر. يتكون خليط التفاعل في كل أنبوب طرد مركزي دقيق (2 مل) من 95 0 ميكرولتر من محلول ميثانولي من جذور DPPH (0.1 ملي مولار) و 50 ميكرولتر RVE من خمسة تركيز مختلف (200 ، 500 ، 1000 ، 2000 ، 4000 ميكروغرام) / مل ميثانول) لجعل التركيزات النهائية 10 و 25 و 50 و 100 و 200 ميكروغرام / مل. تم الاحتفاظ بأنبوب آخر يحتوي على 50 ميكرولتر من الميثانول و 950 ميكرولتر من محلول الميثانول من DPPH كعنصر تحكم. تُركت أنابيب الاختبار في مكان مظلم لمدة 30 دقيقة. تم أخذ امتصاص المخاليط عند 517 نانومتر باستخدام مقياس الطيف الضوئي GENESYS 10S UV-VIS (Thermo SCIENTIFIC ، الولايات المتحدة الأمريكية). أخيرًا ، تم حساب النسبة المئوية لنشاط الكسح الجذري (RSA) بناءً على تغير لون DPPH باستخدام الصيغة التالية RSA=[(ADPPH - ARVE) / ADPPH] × 100 حيث ADPPH هو امتصاص محلول DPPH (التحكم) و ARVE هو الامتصاص لمحلول RVE. تم تسمية التركيز الذي نتج عنه RVE بنسبة 50 بالمائة RSA على أنه قيمة IC50 وتم حسابه باستخدام رسم بياني يضع النسبة المئوية RSA مقابل تركيزات RVE المختلفة المستخدمة.
الحيوانات التجريبية والتصميم التجريبي
تم تأقلم ذكور الفئران البيضاء السويسرية البالغة من العمر 42 يومًا (30-32 جم من وزن الجسم) لمدة أسبوع واحد قبل بدء التجربة في غرفة (درجة حرارة حوالي 25 ± 2 درجة و ~ 50 بالمائة رطوبة ، 12 ساعة مظلمة / دورة ضوئية). تم توفير مياه الشرب والطعام بالشهرة الإعلانية.
تم فصل الفئران بشكل عشوائي إلى ثماني مجموعات (ن {{0}}). المجموعة الأولى (الضابطة) عولجت بـ 0. 2 مل من 0.9 بالمائة كلوريد الصوديوم. عولجت المجموعات الأربع التالية بسيسبلاتين عند 2.5 مجم / كجم لمدة 5 أيام بفاصل 24 ساعة. بعد إعطاء سيسبلاتين ، تركت مجموعة واحدة (المجموعة الثانية) دون أي علاج إضافي وتم تعيينها كمجموعة تحكم مضغوطة. عولجت المجموعات الثالثة والرابعة والخامسة أيضًا باستخدام RVE عند 25 و 50 و 100 ملغم / كغم على التوالي لمدة 5 أيام. تم علاج ثلاث مجموعات أخرى باستخدام RVE فقط عند 25 و 50 و 100 مجم / كجم على التوالي لمدة 5 أيام. تم إذابة سيسبلاتين و RVE في الماء المقطر. أعطيت جميع العلاجات داخل الصفاق. بعد 24 ساعة من العلاج الأخير ، تم قتل الحيوانات بطريقة القتل الرحيم بعد خلع عنق الرحم [25]. ثم تم فتح الصفاق بالمقص ، وتم جمع الدم بعد ثقب القلب ، وتم جمع الكلى باستخدام العضلة. تم إخضاع الدم للتحقق من مستوى الكرياتينين في مصل الدم. خضعت الكلى لتقييم مستوى malondialdehyde والتعبير الجيني.
قياس نسبة الكرياتينين في الدم
تم قياس كرياتينين المصل باستخدام مجموعة فحص الكرياتينين اللونية -700 ، 460 (كايمان كيميكال ، الولايات المتحدة الأمريكية) وفقًا لبروتوكول الشركة المصنعة المتوفر مع المجموعة.
قياس بيروكسيد الدهون الكلوية
Malondialdehyde (MDA) هو منتج نهائي لأكسدة الدهون في أنسجة الكلى وعادة ما يتم قياسه كمؤشر على إنتاج ROS. ومع ذلك ، تم قياس مستوى MDA في الأنسجة الكلوية وفقًا لدراسة سابقة [27]. في البداية ، تم تجانس النسيج الكلوي في محلول فوسفات الصوديوم (0. 1 م ، درجة الحموضة 7.4). محلول تفاعل يشتمل على 0. تمت إضافة 8 بالمائة حمض ثيوباربيتوريك (1.5 مل) ، 8.1 بالمائة SDS (200 ميكرولتر) ، 20 بالمائة (درجة حموضة 3.5) حمض أسيتيك (1.5 مل) ، و dH O (600 ميكرولتر) إلى 100 ميكرولتر من الأنسجة المتجانسة ، ثم تم تحضين الخليط عند 95 درجة لمدة ساعة واحدة. بعد التبريد ، تم طرد المخاليط عند 10 ، 000 جم لمدة 10 دقائق عند 4 درجات وتم قياس امتصاص المادة الطافية عند 532 نانومتر باستخدام معيار 1 ، 1 ، 3 ، 3- رباعي ميثوكسي بروبان. تم قياس كمية البروتين الكلي باستخدام مجموعة Bradford Protein Assay (BIO-RAD ، الولايات المتحدة الأمريكية) ، ومقارنتها بألبومين مصل البقر القياسي (BSA). تم التعبير عن شدة بيروكسيدات الدهون على شكل نانومولات (نانومتر) من MDA لكل مللي جرام (مجم) من البروتين.
تفاعل البلمرة المتسلسل في الوقت الحقيقي (تفاعل البوليميراز المتسلسل في الوقت الحقيقي)
تم إجراء PCR في الوقت الحقيقي كما هو موضح سابقًا [28 ، 29]. تم عزل إجمالي الحمض النووي الريبي من أنسجة الكلى باستخدام كاشف TRIzol® (Invitrogen) وفقًا للبروتوكول المقدم من قبل الشركة المصنعة. ثم تم تحويل الحمض النووي الريبي المعزول (1 ميكروغرام) إلى [كدنا]. أولاً ، تم أخذ 2 ميكرولتر عشوائي هيكسامير (10 ميكرومتر) ، 2 ميكرولتر dNTPs (10 مم) ، 1 ميكروغرام من الحمض النووي الريبي ، وخالي من نوكلياز H O حتى 15 ميكرولتر واحتضانها لمدة 5 دقائق عند 70 درجة. تم وضع الخليط على الفور على الجليد لمدة دقيقتين. ثم تمت إضافة 4 ميكرولتر من المخزن المؤقت الأول (5x) و 1 ميكرولتر من النسخ العكسي M-MLV في كل أنبوب وحضنت لمدة 10 دقائق و 50
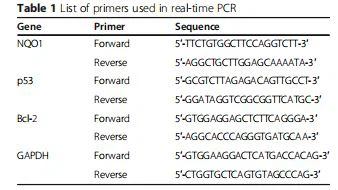
دقيقة عند 25 درجة و 42 درجة على التوالي. أخيرًا ، تم تعطيل إنزيم النسخ العكسي M- MLV عن طريق احتضان الخليط عند 95 درجة لمدة 5 دقائق. تعرضت منتجات (كدنا) المركبة إلى PCR في الوقت الحقيقي لتقدير التعبير الجيني NQO1 و p53 و Bcl -2 باستخدام بادئات محددة (الجدول 1). تم إجراء كل تفاعل (1 0 ميكرولتر) في ثلاث نسخ تتكون من 5 ميكرولتر GoTaq qPCR Master Mix (2x) (Promega ، الولايات المتحدة الأمريكية) ، 0.5 ميكرولتر (10 ملي مولار) من كل تمهيدي ، 3 ميكرولتر من الماء الخالي من نوكلياز ، و 1 ميكرولتر (كدنا) في 48- لوحات تفاعل جيدة. تم إجراء التدوير الحراري باستخدام آلة PCR في الوقت الفعلي (Eco ™ Real-Time PCR System ، Illumine® ، الولايات المتحدة الأمريكية) مع ظروف ركوب الدراجات التالية: 95 درجة لمدة 10 دقائق ، تليها 40 دورة 95 درجة لمدة 30 ثانية ، 50 درجة لمدة 30 ثانية ، و 72 درجة لمدة 25 ثانية. تم تأكيد خصوصية تفاعلات PCR من خلال تحليل منحنى الذوبان عند 95 درجة لمدة 15 ثانية ، و 45 درجة لمدة 15 ثانية ، و 95 درجة لمدة 15 ثانية. تم تأكيد خصوصية تفاعلات PCR من خلال تحليل منحنى الذوبان عند 95 درجة لمدة 15 ثانية ، و 45 درجة لمدة 15 ثانية ، و 95 درجة لمدة 15 ثانية. تم إجراء القياس الكمي النسبي للتعبير الجيني باستخدام جين GAPDH الداخلي كعنصر تحكم بناءً على طريقة ΔΔCq.
زراعة الخلايا وعلاجها
تم الحفاظ على خط الخلايا الظهارية للنبيبات الدانية الكلوية البشرية ، وخلايا HK {0} ، في DMEM مع 10 بالمائة من FBS والمضادات الحيوية (50 وحدة / مل من البنسلين و 50 ميكروغرام / مل من الستربتومايسين) في حاضنة مع 5 بالمائة من ثاني أكسيد الكربون و 95 نسبة الرطوبة عند 37 درجة.
مقايسة قياس H2O2
تم تقدير مستوى H2O2 في خلايا HK -2 باستخدام مجموعة اختبار ROS- Glo ™ H2O2 (Promega ، الولايات المتحدة الأمريكية) وفقًا للبروتوكول المقدم من قبل الشركة المصنعة للمجموعة. تم وضع خلايا HK -2 (1000 خلية) في 70 ميكرولتر DMEM في آبار لوحة ميكروترية البئر 96-. بعد السماح بربط الخلايا على سطح الجدار ، تم استبدال 10 ميكرولتر DMEM من آبار لوحة microtiter بـ 10 ميكرولتر سيسبلاتين (25 ميكرومتر في DMEM) واحتفظ بها في حاضنة لمدة 12 ساعة. بعد ذلك ، تمت إضافة 10 ميكرولتر من RVE لعمل تركيزات نهائية 125 و 250 و 500 ميكروغرام / مل في DMEM واحتضانها لمدة 12 ساعة أخرى. بعد ذلك ، تمت إضافة 20 ميكرولتر من محلول الركيزة H2O2 و 100 ميكرولتر من محلول الكشف ROS-Glo ™ لكل بئر. تم تحضين التفاعل عند درجة حرارة الغرفة لمدة 20 دقيقة. أخيرًا ، تم قياس اللمعان باستخدام GloMax Luminometer (Promega ، الولايات المتحدة الأمريكية).
تحليل GC-MS
تم إجراء تحليل GC-MS لـ RVE (المذاب في الميثانول) كما هو موضح سابقًا [3 0] باستخدام GCMS- QP2 0 2 0 (SHIMADZU) الذي يشتمل على جهاز أخذ عينات تلقائي (AOC { {5}} s) ، وحاقن تلقائي (AOC -20 i) ، وكروماتوجراف غاز (GC -2010 Plus) متصل بمطياف الكتلة المجهز بـ SH-Rxi {{1 {{ 37}}}} عمود شعري Sil MS (3 0 م × 0.25 ميكرومتر ID × 0.25 ميكرومتر DF). تم الاحتفاظ بغاز حامل الهليوم بمعدل تدفق ثابت قدره 1.72 مل / دقيقة ، وتعرض حجم حقن قدره 5 ميكرولتر بنسبة انقسام 10: 1. تم الحفاظ على درجة حرارة الحاقن عند 220 درجة ، وكانت درجة حرارة مصدر الأيونات 280 درجة ، وتمت برمجة درجة حرارة الفرن من 80 درجة (عقد لمدة دقيقتين) ، مع زيادة 5 درجات / دقيقة إلى 150 درجة (زمن الانتظار 5.0 min) ، ثم 5 درجات / دقيقة إلى 280 درجة ، وتنتهي بـ 8 دقائق متساوي الحرارة عند 280 درجة. تم أخذ أطياف الكتلة عند 1.5 كيلو فولت مع فاصل مسح قدره 0.5 ثانية وتم تشغيل العينة في نطاق 45-350 م / ض. كان تأخير المذيب من 0 إلى 3 دقائق ، وكان إجمالي وقت تشغيل GC-MS 55 دقيقة. تم قياس التركيز النسبي للمركبات المكتشفة من خلال مقارنة متوسط منطقة الذروة بالمساحة الكلية. تم إجراء تفسير الطيف الكتلي في GC-MS باستخدام قواعد بيانات المعهد الوطني القياسي والتكنولوجيا (NIST) بما في ذلك NIST08 و NIST08s و NIST.
تحليل احصائي
تم إجراء التحليلات الإحصائية بواسطة ANOVA متبوعة باختبار Dunnett's T3 باستخدام برنامج IBM SPPS (الإصدار 20). يتم توضيح البيانات كوسائل ± الانحراف المعياري (SD). تم النظر في المقارنة المهمة في p<0.05. all="" of="" the="" graphs="" were="" prepared="" using="" microsoft="" excel="" (version="">
نتائج
اختبار نشاط مضادات الأكسدة في المختبر
على الرغم من أنه تم الإبلاغ سابقًا عن RVE لوجود نشاط مضاد للأكسدة ، فقد أعدنا فحص نشاط مضادات الأكسدة في مستخلصنا باستخدام قدرة إزالة الجذور الحرة DPPH. RVE تحييد جرعة DPPH بالاعتماد على الجرعة (الشكل 1). كشفت RVE عن نشاط كبير في مضادات الأكسدة في المختبر وكانت قيمة IC المحسوبة لـ RVE 37.39 ± 1.89 ميكروغرام / مل.
قياس نسبة الكرياتينين في الدم
زاد مستوى كرياتينين المصل في الفئران بشكل ملحوظ (p <{0}. 05)="" بعد="" تناول="" سيسبلاتين="" (الجدول="" 2).="" أدى="" العلاج="" باستخدام="" rve="" بشكل="" ملحوظ="" (p=""><0.05) إلى="" تحسين="" مستوى="" الكرياتينين="" بطريقة="" تعتمد="" على="" الجرعة="" (الجدول="">
قياس بيروكسيد الدهون الكلوية
بالمقارنة مع السيطرة ، سيسبلاتين إلى حد كبير (p <{0}. 05)="" زيادة="" محتوى="" mda="" في="" الأنسجة="" الكلوية="" للفئران="" (الجدول="" 3).="" في="" المقابل="" ،="" أعاد="" علاج="" rve="" إلى="" حد="" كبير="" (p=""><0.05) mda="" إلى="" طبيعته="" تقريبًا="" بطريقة="" تعتمد="" على="" الجرعة="" (الجدول="">
الوقت الحقيقي PCR
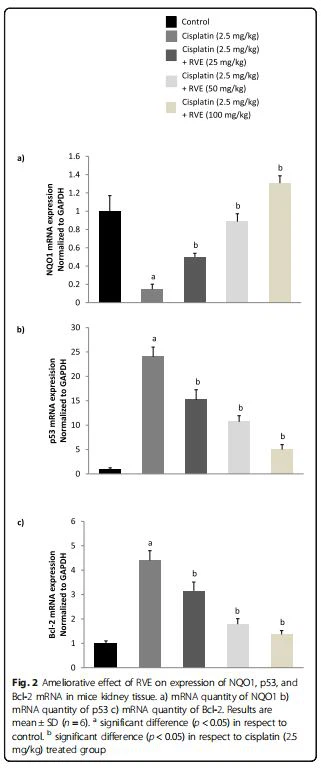
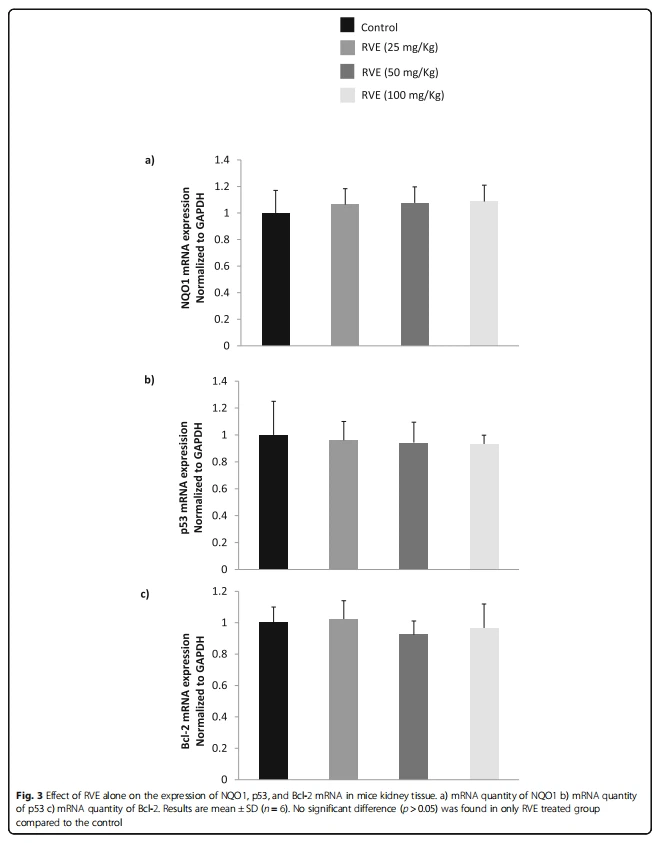
أدى Cisplatin بشكل ملحوظ (p <{0}}. 0="" 5)="" إلى="" خفض="" تعبير="" nqo1="" mrna="" بمقدار="" 0.="" 15-="" أضعاف="" وزيادة="" p53="" و="" bcl="" -2="" mrna="" التعبير="" بمقدار="" 24="" و="" 4.="" 2-="" أضعاف="" ،="" على="" التوالي="" (الشكل="" 2).="" rve="" إلى="" حد="" كبير="" (p=""><0. 0="" 5)="" تم="" تخفيف="" تعبير="" nqo1="" و="" p53="" و="" bcl="" -2="" mrna="" بطريقة="" تعتمد="" على="" الجرعة="" (الشكل="" 2).="" مقارنةً="" بالمجموعة="" الوحيدة="" المعالجة="" بالسيسبلاتين="" ،="" تمت="" زيادة="" تعبير="" nqo1="" mrna="" بمقدار="" 3.57="" و="" 6.36="" و="" 9.="" 28-="" ضعف="" عند="" 25="" و="" 5="" 0="" و="" 1="" 0="" 0="" ملغم="" كغم="" rve="" ،="" على="" التوالي="" (الشكل="" 2="" أ).="" مرة="" أخرى="" ،="" انخفض="" تعبير="" p53="" mrna="" بمقدار="" 0.="" 63="" و="" 0.46="" و="" 0.="" 21-="" ضعف="" عند="" 25="" و="" 50="" و="" 100="" مجم="" كجم="" من="" rve="" ،="" على="" التوالي="" (الشكل="" 2="" ب).="" تم="" أيضًا="" تقليل="" تعبير="" bcl="" -2="" mrna="" بمقدار="" 0.71="" و="" 0.40="" و="" 0.="" 32-="" ضعف="" عند="" 25="" و="" 50="" و="" 100="" مجم="" كجم="" من="" rve="" ،="" على="" التوالي="" (الشكل="" 2="" ج).="" ولكن="" ،="" لم="" يتم="" العثور="" على="" تغييرات="" كبيرة="" (p=""> 0.05) في مستوى التعبير لجينات NQO1 و p53 و Bcl -2 بسبب العلاج باستخدام RVE (الشكل 3).

H2O2فحص القياس
في مقايسة قياس H2O2 ، يكون H2O22O2تم اعتبار المستوى متناسبًا مع التلألؤ. أدت إدارة سيسبلاتين بشكل ملحوظ (p <{{0}}. 0="" 5)="" إلى="" زيادة="" مستوى="" h2o2="" بمقدار="" 2.="" 2-="" أضعاف="" (الشكل="" 4).="" انخفض="" العلاج="" باستخدام="" rve="" بشكل="" كبير="" (p=""><0. 0="" 5)="" مستوى="" h2o2="" بمقدار="" 0.25="" و="" 0.38="" و="" 0.="" 49-="" أضعاف="" عند="" 125="" و="" 250="" و="" 500="" ميكروغرام="" مل="" ،="" في="">

تحليل GC-MS
ما مجموعه 10 مركبات (الجدول 4 والشكل 5) بما في ذلك "Isoborneol، pentamethyldisilanyl ether (كحول سيسكيتيربين)" ، "ثايمين (نواة بيريميدين)" ، "4H-Py- ran -4- one، 2، {{ 8}} dihydro -3 ، 5- dihydroxy -6- methyl- (saponin) "،" Hexadecanoic acid ، methyl ester (fatty methyl ester) "،" 9 ، 12- حمض Octadecadienoic ، ميثيل استر (حمض دهني ميثيل استر) "،" 9- حمض Octadecenoic (Z) - ، ميثيل إستر (حمض ميثيل إستر دهني) "،" ميثيل ستيرات (حمض ميثيل إستر دهني) "،" دايسوكتيل فثالات (استر) "،" 13- Docosenamide ، (Z) - (قلويد) "، و" Squalene (tri-terpene) "تم اكتشافها في RVE.

فوائد cistanche tubolosa: خفض نسبة الدهون في الدم
مناقشة
تمت دراسة مضادات الأكسدة الطبيعية والاصطناعية بشكل شامل وتم الكشف عن فعاليتها سواء للوقاية أو التخفيف من السمية في فسيولوجيا الحيوان [31]. مكملات مضادات الأكسدة هي المكون الذي تم تطويره إما عن طريق التخليق الكيميائي أو عن طريق السحب من الأطعمة الطبيعية ولكن هذه ليست متطابقة في التركيب مثل مضادات الأكسدة المتوفرة في الغذاء [5]. وبالتالي ، يتم فصل الآراء بمرور الوقت حول ما إذا كانت مضادات الأكسدة الاصطناعية تعطي فوائد صحية مماثلة لمضادات الأكسدة الطبيعية أم لا [32]. هناك حاجة لتقليل استخدام المكملات المضادة للأكسدة الاصطناعية والبحث عن مصادر بديلة ورخيصة ومتجددة وطبيعية وربما أكثر أمانًا لمضادات الأكسدة الطبيعية الفعالة.
إحدى أهم الآليات هي مسار العامل النووي {{0} ذي الصلة -2 (Nrf2) الذي يحمي الخلايا بشكل عام من الإجهاد التأكسدي الناجم عن الضغوط الخارجية أو الداخلية [27]. تحفز مضادات الأكسدة الفعالة على التعبير عن Nrf2 ، والذي ينتقل أكثر إلى النواة ويرتبط بعنصر استجابة مضادات الأكسدة (ARE) الذي يثير التعبير عن المرحلة الثانية من إزالة السموم والجين المضاد للأكسدة NQO1 [33 ، 34]. يتم التعبير عن NQO1 على نطاق واسع وبشكل تفاضلي بطريقة خاصة بالأنسجة. NQO1 هو بروتين فلافوبروتين مضاد للأكسدة خلوي يحفز 2- اختزال الإلكترون للكينون إلى الهيدروكينون ، مما يؤدي إلى إزالة السموم من المركبات الكهربائية وتوقع دورة الأكسدة والاختزال [35]. وفقًا لدراسة سابقة [36] ، ينشط -lapachone NQO1 ، مما يزيد من مستوى NAD زائد داخل الخلايا ويحمي الكلى من الإصابة الحادة التي يسببها السيسبلاتين.
من المعروف أن السيسبلاتين يسبب تلفًا في غشاء الترشيح الكبيبي من خلال الإجهاد التأكسدي والالتهاب وموت الخلايا المبرمج مما يؤدي إلى انخفاض معدل الترشيح الكبيبي وفقدان نفاذية الغشاء الطبيعي [37]. لذلك ، تم زيادة مستوى الكرياتينين في الدم. الكرياتينين في الدم هو أحد مؤشرات وظائف الكلى المحتملة. أدى علاج السيسبلاتين إلى زيادة محتوى MDA في أنسجة الكلى وهو منتج ثانوي لبيروكسيد الدهون وهذا التقرير ثابت مع الدراسات السابقة [27 ، 35 ، 37 ، 38]. أدى العلاج باستخدام RVE إلى انخفاض كبير في محتوى MDA في أنسجة الكلى. في الوقت نفسه ، انخفض مستوى الكرياتينين أيضًا مما يشير إلى التأثير التحسني لـ RVE.
إلى جانب ذلك ، انخفض تعبير NQO1 بشكل ملحوظ ، وزاد تعبير p53 و Bcl -2 بشكل ملحوظ بعد التعرض لسيسبلاتين. فيما يتعلق بتعبير NQO1 و p53 في الجسم الحي ، تتوافق نتيجتنا مع دراسة سابقة [13]. أظهرت دراسة حديثة [39] أن السيسبلاتين قلل بشكل ملحوظ من تعبير Bcl -2 في كلية الفئران ، ولكن من المدهش أننا وجدنا تعبيرًا مرتفعًا. قد يكون هذا الاختلاف نتيجة اختلاف الجرعة [40] حيث استخدم محمد وزملاؤه [39] 8 مجم / كجم لمدة 12 يومًا ، بينما استخدمنا 2.5 مجم / كجم لمدة 5 أيام فقط. ذكرت دراسة أخرى [41] أن السيسبلاتين قد يزيد من تعبير Bcl -2 بجرعة عندما يكون غير سام للخلايا. مرة أخرى ، زيادة تعبير Bcl -2 يحسس الخلايا تجاه الإجهاد التأكسدي [40].
ومع ذلك ، فإن التعبير عن p53 منخفض في الظروف الفسيولوجية العادية ولكن من المتوقع أن يتم تنظيمه بمجرد معالجته باستخدام السيسبلاتين لأن عامل العلاج الكيميائي القائم على البلاتين ينشط مسار موت الخلايا المبرمج المعتمد على p53. بمجرد أن تعاملنا مع الفئران بالسيسبلاتين ، زاد البروتين p53 بشكل ملحوظ في كلى الفئران مقارنةً بالتحكم. يرتبط أيضًا جين بروتوني آخر Bcl -2 بمستوى تعبير NQO1. بمحاكاة تعبير p53 ، وجدنا أيضًا أن مستويات Bcl - 2 قد زادت مع علاج السيسبلاتين ، ولكن تمت إعادة تغطيتها بشكل كبير عند العلاج باستخدام RVE. هذا ممكن ، استجابة للإجهاد التأكسدي ، يتم تنشيط الجين p53 وينتج عنه إيقاف دورة الخلية ، أو الشيخوخة ، أو موت الخلايا المبرمج [6]. مع إزالة السموم ، غالبًا ما يُعتبر الإفراط في التعبير عن NQO1 مرتبطًا بالاستماتة في الخلايا السرطانية [10] ، على الرغم من أن الآلية الكامنة وراء موت الخلايا المبرمج والإفراط في التعبير عن NQO1 لا تزال مثيرة للجدل. علاوة على ذلك ، في سرطان الخلايا الكبدية ، يؤدي الإفراط في التعبير عن NQO1 إلى تقليل تعبير Bcl -2 [10]. يحتوي Proto-oncogene Bcl - 2 أيضًا على p53 مثل الارتباط بتعبير NQO1. p53 هو عامل نسخ خاص بالتسلسل يتم تنشيطه بواسطة أنواع عديدة من الإجهاد الخلوي [42] ، بينما يعمل التعبير الزائد Bcl -2 كمثبت مسام الميتوكوندريا لتسهيل إطلاق السيتوكروم ج عند الإجهاد التأكسدي [12]. في حالتنا ، قمنا بفحص كل من استجابات الجينات مع علاج سيسبلاتين في أنسجة الكلى الطبيعية ووجدنا زيادة في التعبير عنها. أعاد علاج RVE التعبير عن p53 و Bcl -2 إلى الطبيعي تقريبًا بطريقة تعتمد على الجرعة. تم عرض هذا النوع من إلغاء التعبير Bcl -2 أيضًا باستخدام ROS scavenger Trolox [43]. علاوة على ذلك ، ارتفع مستوى H2O2 بشكل ملحوظ في خلايا HK -2 بسبب العلاج بالسيسبلاتين في المختبر. بعد العلاج بـ RVE ، تم استعادة مستوى H2O2 بشكل ملحوظ إلى ما يقرب من الطبيعي. ربما يكون هذا بسبب تأثير علاج RVE الذي زاد من تعبير NQO1 [44] ، والذي يمارس الحماية ضد الإجهاد التأكسدي [6].
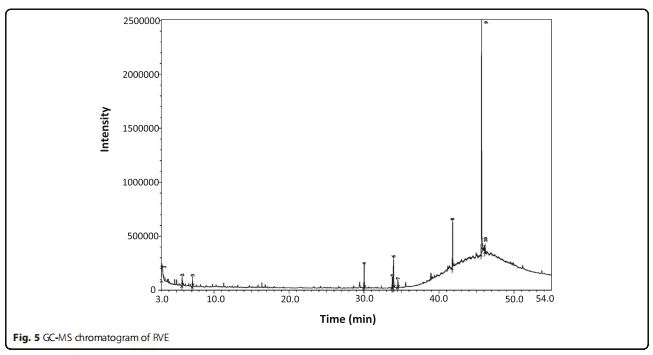
أكد مخطط كروماتوجرام GC-MS وجود عشرة مركبات في RVE. من بينها "4H-Pyran - 4- واحد و 2 و 3- ثنائي هيدرو -3 و 5- ثنائي هيدروكسي -6- ميثيل-" و "حمض هيكساديكانويك" و " السكوالين "من مضادات الأكسدة المعروفة [45-47]. من المحتمل أن تكون هذه المركبات الثلاثة قد مارست تأثيرًا تآزريًا على الكلى. أفادت الدراسات السابقة أيضًا عن تحريض تعبير NQO1 بواسطة فيتامين أ [48] وفيتامين ج [49] وفيتامين هـ [50] والفلافونويد [51] وبوليفينول [50]. لذلك ، يقترح هذا التقرير توضيح ما إذا كان هذا المستخلص بعينه يحتوي على أي شيء بين فيتامين أ وفيتامين ج وفيتامين هـ والفلافونويد والبوليفينول أم لا.
استنتاج
تشير النتائج الإجمالية إلى أن RVE فعال من الناحية الفسيولوجية في حماية الكلى من التلف الناجم عن السيسبلاتين. لذلك ، من الأهمية بمكان توضيح المركبات الدقيقة المسؤولة عن تخفيف السمية الكلوية التي يسببها السيسبلاتين والتي قد تصبح مفيدة للتطبيق البشري.
شكر وتقدير
الكتاب ممتنون لمجلس بنغلاديش للبحوث العلمية والصناعية (BCSIR) ، فرع راجشاهي لتوفير الدعم المختبري لتحديد كمية الحمض النووي الريبي.
مساهمات المؤلفين
نفذت MMH التصميم التجريبي والتجريب وتحليل البيانات وإعدادها وكتابة المخطوطات وتحريرها وتنقيح المخطوطات وصياغتها ؛ قامت MST و MME بالتجريب وتحليل البيانات ؛ ساهمت AME & MAR في الإشراف والموارد ؛ كان AH مسؤولاً عن وضع المفاهيم والإشراف والموارد وتحرير المخطوطات. كل المؤلفين
راجع المخطوطة. قرأ المؤلفون المخطوطة النهائية ووافقوا عليها.
التمويل
تم تمويل العمل الحالي من قبل مشروع دعم باحثي جامعة الطائف رقم (TURSP {0}} / 75) ، جامعة الطائف ، الطائف ، المملكة العربية السعودية.
توافر البيانات والمواد.
جميع البيانات ذات الصلة متاحة ويمكن تقديمها عند الطلب إلى المؤلف المقابل.
الإعلانات
موافقة الأخلاق والموافقة على المشاركة
تمت الموافقة على أخلاقيات إجراء هذه التجربة من قبل لجنة الحيوان المؤسسية ، والأخلاقيات الطبية ، والسلامة الحيوية ، والأمن الحيوي (IAMEBBC) ، ومعهد العلوم البيولوجية (IBSc) ، بجامعة راجشاهي ، وتم تقديمها بموجب المذكرة رقم 31 / {{1} } IAMEBBC / IBSc. تم تنفيذ جميع الأساليب وفقًا للإرشادات واللوائح المقدمة من قبل لجنة الأخلاقيات المذكورة أعلاه. أجريت هذه الدراسة وفقًا لإرشادات ARRIVE (أبحاث الحيوانات: الإبلاغ عن التجارب في الجسم الحي). "الموافقة على المشاركة" لا تنطبق على هذه الدراسة.
تفاصيل المؤلف
1 مختبر البيولوجيا الجزيئية وعلوم البروتين ، قسم الهندسة الوراثية والتكنولوجيا الحيوية ، كلية علوم الحياة والأرض ، جامعة راجشاهي ، راجشاهي 6205 ، بنغلاديش. 2 مختبر علم الأمراض الجزيئي ، معهد العلوم البيولوجية ، جامعة راجشاهي ، راجشاهي 6205 ، بنغلاديش. 3 قسم التقنية الحيوية ، كلية العلوم ، جامعة الطائف ، ص.ب 11099 ، الطائف 21944 ، المملكة العربية السعودية. 4 قسم الوراثة ، كلية الزراعة ، جامعة الإسكندرية ، الإسكندرية 21545 ، مصر.
مراجع
1. Bagchi K ، Puri S. الجذور الحرة ومضادات الأكسدة في الصحة والمرض: مراجعة. East Mediterr Health J. 1998 ؛ 4: 350-60.
2. Koh EM و Lee EK و Song CH و Song J و Chung HY و Chae CH وآخرون. Ferulate ، وهو مكون نشط من جرثومة القمح ، يخفف من اختلال PTK / PTP الناجم عن الإجهاد التأكسدي وتعطيل PP2A. ريس توكسيكول. 2018 ؛ 34 (4): 333–41.
3. حسن علي ، إبراهيم ر. بعض الملامح الجينية في كبد إيرليخ استسقاء الفئران الحاملة للورم تحت ضغط التشعيع. J Radiat Res Appl Sci. 2014 ؛ 7 (2): 188-97.
4. Zhou FL ، Zhang WG ، Wei YC ، Meng S ، Bai GG ، Wang BY ، et al. تدخل الإجهاد التأكسدي في انتكاس ابيضاض الدم النخاعي الحاد. J بيول كيم. 2010 ؛ 285 (20): 15010-5.
5. Pham-Huy LA، He H، Pham-Huy C. الجذور الحرة ومضادات الأكسدة في المرض والصحة. Int ياء علوم بيوميد. 2008 ؛ 4: 89-96.
6. Srijiwangsa P ، Na-Bangchang K. أدوار NAD (P) H-quinone oxidoreductase 1 (NQO1) في تطور السرطان والمقاومة الكيميائية. ياء نوتر أكسب أونكول. 2017 ؛ 6: 1-6.
7. Siegel D ، Yan C ، Ross D. NAD (P) H: quinone oxidoreductase 1 (NQO1) في حساسية ومقاومة الكينونات المضادة للورم. Biochem فارماكول. 2012 ؛ 83 (8): 1033-40.
8. Dinkova-Kostova AT، Talalay P. NAD (P) H: مستقبل الكينون oxidoreductase 1 (NQO1) ، وهو إنزيم مضاد للأكسدة متعدد الوظائف وحماية خلوية متعددة الاستعمالات بشكل استثنائي. قوس Biochem Biophys. 2010 ؛ 501 (1): 116-23.
9. Cullen JJ ، Hinkhouse MM ، Grady M ، Gaut AW ، Liu J ، Zhang YP ، et al. تثبيط ديكومارول لـ NADPH: يحفز أوكسيريدوكتاز الكينون تثبيط نمو سرطان البنكرياس عبر آلية تتوسط فيها الأكسيد الفائق. الدقة السرطان. 2003 ؛ 63 (17): 5513-20.
10. تشانغ إكس ، هان ك ، يوان د إتش ، منغ سي واي. الإفراط في التعبير عن NAD (P) H: quinone oxidoreductase 1 يمنع تكاثر خلايا سرطان الخلايا الكبدية ويحدث موت الخلايا المبرمج عن طريق تنشيط مسار AMPK / PGC -1. بيول خلية الحمض النووي. 2017 ؛ 36 (4): 256-63.
11. Zeekpudsa P، Kukongviriyapan V، Senggunprai L، Sripa B، Prawan A. قمع NAD (P) H-quinone oxidoreductase 1 عزز قابلية خلايا سرطان القنوات الصفراوية لعوامل العلاج الكيميائي. ياء أكسب نوتر ريس السرطان. 2014 ؛ 33 (1): 1-13.
12. Dasari S، Tchounwou PB. سيسبلاتين في علاج السرطان: آليات العمل الجزيئية. فارماكول Eur J. 2014 ؛ 740: 364–78.
13. Zhu X و Jiang X و Li A و Zhao Z و Li S. S-Allylmercaptocysteine يخفف من السمية الكلوية التي يسببها السيسبلاتين من خلال قمع موت الخلايا المبرمج والإجهاد التأكسدي والالتهاب. العناصر الغذائية. 2017 ؛ 9 (2): 166.
14. ماتكوفسكي أ. زرع في المختبر لإنتاج مضادات الأكسدة - مراجعة. Biotechnol Adv. 2008 ؛ 26 (6): 548-60.
15. البكري أ. ع ، مصطفى هام ، علم EA. النشاط المضاد للأكسدة من Rumex L. في المرحلة الخضرية من النمو. آسيا J فارم كلين ريس. 2012 ؛ 5: 111-7.
16. Rechinger KH. Rumex (Polygonaceae) في أستراليا: إعادة النظر. Nuytsia. 1984 ؛ 5:75 - 122.
17. شحات أ. أ ، السعيد إم إس ، أليحييا إم إيه ، هيجينز إم ، دينكوفا-كوستوفا إيه تي. NAD (P) H: نشاط محفز كينون أوكسيريدوكتاز 1 لبعض النباتات الطبية السعودية. بلانتا ميد. 2013 ؛ 79 (06): 459–64.
18. الهوارى ش ، سكر ن.م ، علي ذى ، يحيى م. لمحة عن المركبات النشطة بيولوجيًا لـ Rumex بالنيابة L.J Food Sci. 2011 ؛ 76 (8): C1195–202.
19. Barbosa-Filho JM، Alencar AA، Nunes XP، Tomaz AC، Sena-Filho JG، Athayde- Filho PF، et al. مصادر alpha- و beta- و gamma- و delta-و epsilon- carotenes: مراجعة القرن العشرين. القس براس. 2008 ؛ 18 (1): 135-54.
20. Laouini SE، Ouahrani MR. فحص كيميائي نباتي ، نشاط مضاد للأكسدة ومضاد للبكتيريا في مستخلص الرومكس L. دراسة العلوم: Chem Chem Engi Biotech Food Ind. 2017 ؛ 18: 367–76.

