مراجعة الاختبارات الجينية لدى مرضى أمراض الكلى: العائد التشخيصي لمتغيرات النوكليوتيدات المفردة وتغيرات أرقام النسخ التي تم تقييمها عبر مجموعات النمط الظاهري للكلى وداخلها
Aug 16, 2023
خلاصةمرض الكلى الوراثييشمل مجموعة متنوعة من الاضطرابات. يمكن تقسيمها تقريبًا إلى مجموعات النمط الظاهري (التشوهات الخلقية).الكلى والمسالك البولية، اعتلالات الهدبية، اعتلالات الكبيبات، اضطرابات الحصوات، مرض الكلى الأنبوبي الخلالي، واعتلالات الأنابيب. العديد من المسببات يمكن أن تؤدي إلى مرض الكلى المزمن الذي يمكن أن يتطور إلى مرض الكلى في المرحلة النهائية. على الرغم من أن كل مرض على حدة نادر، إلا أن هذه الاضطرابات الوراثية معًا تمثل نسبة كبيرة من حالات أمراض الكلى. ومع إدخال التسلسل المتوازي على نطاق واسع، أصبح الاختبار الجيني أكثر سهولة، ولكن لا يوجد تحليل شامل للعائد التشخيصي. تقدم هذه المراجعة لمحة عامة عن العائد التشخيصي للاختبارات الجينية عبر وضمن النطاق الكامل للأنماط الظاهرية لأمراض الكلى من خلال بحث منهجي في الأدبيات أدى إلى 115 مقالة متضمنة. يتم تسليط الضوء على خصائص المريض والاختبار والفوج التي يمكن أن تؤثر على العائد التشخيصي. تم وصف اكتشاف اختلافات أرقام النسخ ومساهمتها في العائد التشخيصي لجميع مجموعات النمط الظاهري. وأيضا تأثير التشخيص الوراثي على المريض وأفراد الأسرة، حيث يمكن تشخيصه،علاجي، والنذير، ويظهر من خلالالمقالات المدرجة. ستسمح هذه المراجعة للأطباء بتقدير الاحتمال المسبق لإيجاد سبب وراثي لأمراض الكلى لدى مرضاهم.
الكلمات الدالة:مرض الكلى المزمن، سي إن في،العائد التشخيصي، الاختبارات الجينية، MPS، تكوين الكلية، مراجعة

انقر هنا لمعرفة موعد علاج مرض الكلى المزمن
1|مقدمة
أمراض الكلى الوراثيةتشكل مجموعة غير متجانسة من الاضطرابات، والتي، على الرغم من أنها نادرة في الغالب، إلا أنها معًا متكررة ومن المهم تحديدها (Groopman et al., 2019). يعد تحديد السبب الوراثي لدى مرضى الكلى أمرًا ضروريًا للمرضى وأفراد أسرهم. بالنسبة للمريض، يمكن أن يؤدي التشخيص الجيني إلى معرفة المسببات والعلاج الشخصي وإمكانية الحصول على المشورة بشأن التشخيص وخيارات تنظيم الأسرة. يمكن تقديم المشورة لأفراد الأسرة بشأن خيارات الاختبار والفحص قبل ظهور الأعراض. يمكن أن يكون التشخيص الجيني مهمًا أيضًا للتبرع بالكلى من الأحياء. يمكن التمييز بين فئات مختلفة من أمراض الكلى الوراثية (هيلدبراندت، 2010). أحد العروض السريرية المهمة هو مرض الكلى المزمن (CKD) والذي يمكن أن يتطور إلى مرض الكلى في المرحلة النهائية (ESKD)، والذي ينطوي على عبء مرضي مرتفع (Coresh، 2017). يمكن أن تؤدي العديد من المسببات إلى نقطة النهاية المشتركة النهائية هذه (Groopman et al., 2019). بشكل عام، في مرض الكلى الوراثي، يمكن أن تسبب المتغيرات المسببة للأمراض في جينات متعددة نمطًا ظاهريًا واحدًا (عدم التجانس الوراثي)، ويمكن أن يكون للمتغيرات المسببة للأمراض في جين معين عروض سريرية متعددة (تعدد المظاهر) (Stokman et al.، 2016).
إن إدخال التسلسل المتوازي على نطاق واسع (MPS)، والذي يشار إليه سابقًا باسم تسلسل الجيل التالي، جعل اختبار أمراض الكلى أحادية المنشأ (MKD) أكثر سهولة وبالتالي تشخيص MKD أسهل. وقد أدى هذا إلى العديد من الأفكار الجديدة، ولكن لا يوجد تحليل شامل للعائد التشخيصي عبر الأنماط الظاهرية وداخلها. يعد تقدير العائد التشخيصي المحتمل للاختبارات الجينية، لدى مريض معين، أمرًا ضروريًا لتحديد فرصة تشخيص المرض أحادي الجين عند إجراء الاختبارات الجينية. هذا العائد المقدر، إلى جانب عوامل مثل التكلفة والتوافر، ولكن أيضًا الاحتياجات المحددة للمريض و/أو الوالدين فيما يتعلق على سبيل المثال بتنظيم الأسرة أو التبرع بالكلى المرتبطة بالحياة، يُعلم عملية صنع القرار المشتركة فيما يتعلق بالاختبارات الجينية. تشير دراسات متعددة إلى نتائج تشخيصية متفاوتة للاختبارات الجينية للأنماط الظاهرية لأمراض الكلى الوراثية. قد تكون نتائج التشخيص المختلفة المبلغ عنها نتيجة للاختلافات في (أ) خصائص المريض، (ب) خصائص الاختبار الجيني، و/أو (ج) خصائص الأتراب. عوامل المريض التي يمكن أن تؤثر على العائد التشخيصي هي التاريخ العائلي الإيجابي، والسمات خارج الكلوية، والعرض المتلازمي، والمرض الشديد، بما في ذلك البداية المبكرة للمرض ووجود ESKD (Knoers et al.، 2022). خصائص الاختبار التي يمكن أن تؤثر على العائد المبلغ عنه هي عدد الجينات التي تم تحليلها (تمتد إلى جميع الجينات [إكسوم] أو على مستوى الجينوم كحد أقصى)، وما إذا تم تقييم اختلافات عدد النسخ (CNVs)، وما إذا تم إجراء اختبارات إضافية للمناطق الجينومية الصعبة ( على سبيل المثال، MUC1 وexon 1 من PKD1)، ولكن أيضًا ما إذا كان يتم إجراء التحليلات الثلاثية (اختبار الطفل وكلا الوالدين) والفصل لتصنيف متغير إضافي. أيضًا، يمكن أن تكون تفاصيل المجموعة ذات أهمية. في المجموعة السريرية (من الحالات المتعاقبة)، غالبًا ما تكون الأنماط الظاهرية أقل تجانسًا، وقد يكون السكان أكثر تمثيلاً للمرضى الذين يتم فحصهم في العيادة الخاصة بالفرد. في مجموعة بحثية يتم تطبيق معايير مختلفة للإدراج والاستبعاد، وغالبًا ما يتم اختيار المرضى كحالات، الأكثر اشتباهًا في التشخيص الوراثي، من العديد من المراكز، ولا تكون نتائج العائد التشخيصي قابلة دائمًا للتعميم على بيئة التشخيص. قد يكون المتغير الآخر ذو الصلة هو حجم المجموعة.

في هذه المراجعة، نهدف إلى تحديد العائد التشخيصي للاختبارات الجينية ضمن وعبر مجموعة كاملة من الأنماط الظاهرية المحتملة لأمراض الكلى الوراثية. يتم تسليط الضوء على خصائص المريض والاختبار والأتراب التي تؤثر على العوائد المختلفة. نحن نقدم نظرة عامة مفصلة ودقيقة يمكن أن تساعد في تقييم معنى المنشورات المختلفة، مع معلومات مفيدة محتملة للممارسة السريرية. نسلط الضوء أيضًا على التأثير السريري للتشخيصات الجينية استنادًا إلى الدراسات المجمعة ونوضح كيف تطورت أساليب الاختبارات الجينية على مر السنين.
الجدول 1 مجموعات المصطلحات المستخدمة لإجراء بحث PubMed تم دمج المجموعتين (1) و(2) في بحث واحد باستخدام عامل التشغيل المنطقي "AND"، وقد تم نفس الشيء بالنسبة للمجموعتين (1) و(3) مصطلحات المجموعة في العنوان/الملخص
(1) الكلى أو الكلى أو Alport أو ADPKD أو ARPKD أو CAKUT أو اعتلال الهدب أو التهاب الكلية أو nephrol* أو nephron* أو الكلوية أو الكبيبات* أو المسالك البولية* أو المسالك البولية أو اعتلال الأنابيب* أو الكلوية
(2) المحصول التشخيصي أو المحصول أو الاختبار الجيني أو WES أو WGS أو تسلسل الإكسوم الكامل أو تسلسل الإكسوم الكامل أو الإكسوم الكامل أو الجينوم الكامل أو الإكسوم الكامل أو الجينوم الكامل أو لوحة الجينات أو لوحات الجينات أو لوحة الجينات المتعددة أو لوحات الجينات المتعددة أو تسلسل الجينوم الكامل أو MPS أو التسلسل المتوازي الهائل أو التسلسل المتوازي الكبير أو NGS أو تسلسل الجيل التالي أو تسلسل الجيل التالي أو التسلسل الخارجي أو التسلسل الجينومي أو تسلسل الجينات المستهدف* أو التسلسل المستهدف* أو اللوحة المستهدفة*
(3) CNV أو متغير رقم النسخ أو تباين رقم النسخ أو تباين رقم النسخ أو صفيف SNP أو صفيف SNP أو صفيف CGH أو صفيف CGH
2|طُرق
2.1|اختيار الدراسة
تم إجراء بحث منهجي في الأدبيات للإجابة على سؤال المراجعة: "ما هو العائد التشخيصي للاختبارات الجينية في أي نوع من أمراض الكلى وما هي خصائص المريض والفوج والاختبار التي تؤثر على العائد التشخيصي؟" لم يتم تسجيل هذه المراجعة في قاعدة بيانات المراجعة. تم البحث في قاعدة بيانات PubMed في 2 أبريل 2021، باستخدام المصطلحات المعروضة في الجدول 1. اختار اثنان من المراجعين بشكل مستقل المقالات بناءً على معايير الاشتمال المحددة مسبقًا باستخدام الريان (Ouzzani، Hammady، Fedorowicz، & Elmagarmid، 2016). تم حل الخلافات بالإجماع أو بمساعدة مراجع ثالث.
كانت جميع معايير الاشتمال هذه إلزامية: (أ) المقالة الأصلية المنشورة في السنوات العشر الماضية، (ب) المشاركون من البشر، (ج) العائد التشخيصي للاختبارات الجينية المبلغ عنها أو القابلة للاستدلال، (د) كان المرضى يعانون من نوع ما من أمراض الكلى، و (هـ) ) مجموعة لا تقل عن 30 مريضا لا علاقة لهم. تم استبعاد المقالات التي تركز على سرطان الكلى. تم تحديد المقالات الإضافية وإدراجها من خلال كرة الثلج.
2.2|استخراج البيانات
تم إجراء استخراج البيانات باستخدام حقول البيانات المحددة مسبقًا. تم تجميع الدراسات في مجموعات النمط الظاهري لأمراض الكلى التالية: مرض الكلى الأنبوبي الخلالي السائد (ADTKD)، التشوهات الخلقية في الكلى والمسالك البولية (CAKUT)، الاعتلالات الهدبية (مقسمة إلى مرض الكلى المتعدد الكيسات المهيمنة [ADPKD] وغيرها من الاعتلالات الهدبية/المختلطة) ، اعتلال الكبيبات (المتلازمة الكلوية [NS] وغيرها/مختلطة)، تحصي الكلية/تحصي البول، اعتلالات التاو، ESKD، والأنماط الظاهرية لأمراض الكلى المختلطة. لجميع الدراسات التفاصيل.

تم استخلاصها من خصائص المريض، وخصائص الأتراب، وعلى الاختبار الجيني الذي تم إجراؤه. وكانت تفاصيل الفوج التي تم استخراجها هي عدد المرضى المشمولين، والنمط الظاهري، ونوع الفوج (الفوج السريري أو الفوج البحثي). تم اعتبار المجموعة أترابية سريرية إذا كانت المجموعة مستمدة من بيئة سريرية محددة بوضوح (على سبيل المثال، جميع المرضى المتعاقبين الذين تلقوا عملية زرع كلية) و/أو الإبلاغ عن نتائج الاختبارات الجينية من بيئة تشخيصية (على سبيل المثال، جميع المرضى المحالين للحصول على الجينات اختبار اللوحة). وشملت خصائص المرضى التي تم استخلاصها: النسبة المئوية للحالات العائلية، والنسبة المئوية لأقارب الدم، والنسبة المئوية للحالات التي تظهر بمظاهر خارج الكلى، وعمر ظهور المرض، والنسبة المئوية للأشخاص الذين لديهم ESKD. بالنسبة للاختبار الجيني، تضمنت التفاصيل المستخرجة ما يلي: عدد الجينات التي تم فحصها وما إذا تم إجراء تحليل متغير النوكليوتيدات المفرد (SNV) و/أو CNV. تم اعتبار تحليل CNV ليتم إجراؤه، أيضًا إذا تم تقييم جين واحد فقط. تم تعريف CNVs هنا على أنها عمليات حذف أو تكرار كبيرة جدًا بحيث لا يمكن التقاطها بالتسلسل التقليدي. تم استخراج نوع الاختبار الجيني (على سبيل المثال، لوحة متعددة الجينات تعتمد على MPS، ومصفوفة تعدد أشكال النوكليوتيدات الفردية [SNP]، وتسلسل الإكسوم الكامل [WES]، وتسلسل الجينوم الكامل [WGS]، وما إلى ذلك)، بما في ذلك نوع تحليل CNV. تم اعتماد العائد التشخيصي من الورقة أو حسابه من البيانات. تم تضمين المتغيرات المسببة للأمراض والمتغيرات المسببة للأمراض في العائد التشخيصي ما لم يتم تحديد تفاصيل حول تصنيف المتغيرات من قبل المؤلفين. وفي هذه الحالة، تم استخراج العائد الذي أبلغ عنه المؤلفون. إذا استخدم المؤلفون مصطلحًا شاذًا لوصف المتغيرات (أي مصطلح آخر غير مسبب المرض [المحتمل]، على سبيل المثال، "ربما يسبب المرض" أو "يحتمل أن يكون مسببًا للأمراض")، فسيتم استخلاص هذا المصطلح والمحصول المرتبط به. ولوحظت أيضا المعايير المستخدمة لتقييم المتغيرات في كل مادة. لم يتم تضمين الجينات المرشحة في العائد التشخيصي، ولكن تم تسليط الضوء عليها تحت عنوان "جدير بالملاحظة". تم حساب العائد التشخيصي ولاحظه لكل النمط الظاهري في الأفواج ذات الأنماط الظاهرية المختلطة. عندما كانت التفاصيل متاحة فيما يتعلق بالفوج الذي تم اشتقاق المجموعة السكانية التي تم اختبارها منها، تم أيضًا حساب العائد التشخيصي المستقر على المجموعة الأكبر (على سبيل المثال، عندما تم اختبار مجموعة فرعية محددة من مرضى زرع الأعضاء وراثيًا، تم استقراء العائد التشخيصي للمجموعة بأكملها) مجموعة من المرضى المزروعين). إذا تم الإبلاغ عنها، فسيتم استخراج النسبة المئوية للحالات ذات المتغير غير المعروف الأهمية. قمنا أيضًا بحساب العائد بناءً على CNVs فقط وحددنا النسبة المئوية للعائد التشخيصي المُبلغ عنه الذي يمكن تفسيره بواسطة CNVs. عندما أبلغت الدراسة عن خصائص المريض التي أثرت بشكل إيجابي على العائد التشخيصي، لوحظ ذلك. تم أيضًا استخراج أي تفاصيل إضافية ذات صلة. وأخيرًا، حددنا عدد الجينات المسؤولة عن أفضل 50% من نتائج التشخيص. تمت ملاحظة الجينات المسؤولة ما لم تكن الجينات مسؤولة عن حالة إيجابية واحدة فقط و/أو جينات متعددة مكونة للنسب المئوية النهائية.
2.3|عرض مرئي للمعلومات
تم تلخيص البيانات من خلال الجمع بين خصائص الفوج والمريض والاختبار والنتائج على العائد التشخيصي لكل مجموعة النمط الظاهري في جدول ملخص. تم تلخيص لمحات عامة أكثر تفصيلاً لجميع الدراسات في جداول منفصلة لكل مجموعة مرضية. لقد نظرنا أولاً إلى خصائص المريض التي تؤثر بشكل إيجابي على العائد التشخيصي ضمن دراسة واحدة ووصفنا ذلك في جدول الملخص. بعد ذلك، قمنا بتقييم تأثير المريض، والأتراب، وخصائص الاختبار بين الدراسات المختلفة. لتصور تأثير هذه الخصائص، تم عمل مخططات مبعثرة، ومخططات مربعة، ومخططات دائرية باستخدام SPSS (الإصدار 26، IBM، New York، NY) للنظر في العلاقة بين متغيرين كميين ضمن دراسة واحدة، عبر جميع الدراسات. لتجنب الإفراط في تفسير البيانات المستمدة من الدراسات شديدة التباين، قررنا تصوير تمثيل مرئي فقط للبيانات وعدم إجراء اختبارات إحصائية.
3|نتائج
أسفر البحث في PubMed عن 5361 ورقة بحثية. بعد فحص العنوان والملخص والنص الكامل، بقي 98 ورقة استوفت معايير الاشتمال. بالإضافة إلى ذلك، تم تحديد سبعة عشر مقالاً وإدراجها من خلال كرة الثلج.
يقدم الجدول 2 لمحة عامة عن الغلة المبلغ عنها لكل مجموعة مرضية. لكل مجموعة مرضية، تم تضمين 4 إلى 25 مقالة مع اختلاف خصائص المريض والاختبار والأتراب لكل دراسة. اختلفت عائدات التشخيص بشكل كبير داخل كل مجموعة مرضية وبين مجموعات الأمراض المختلفة (الجدول 2؛ الشكل 1 أ). نجد أقل عائد تشخيصي في مجموعة مرض CAKUT وأعلى عائد تشخيصي في مجموعة الاعتلال الهدبي وداخل هذه المجموعة عائد أعلى لمجموعة ADPKD. ومع ذلك، في مجموعة مرض CAKUT، وجدنا أعلى عائد تشخيصي يعتمد فقط على CNVs (الشكل 1 ب). عندما ننظر إلى العائد المستقر على المجموعة الأكبر، نجد غالبًا عائدًا أقل مما تم الإبلاغ عنه في البداية، كما كنا نتوقع (الجدول 2). تمثل هذه القيم الحد الأدنى من العائد التشخيصي للسكان الأصليين.
في الجدول التكميلي 1، يتم عرض مجموعات المرض بمزيد من التفصيل. يتم وصف خصائص المريض والفوج والاختبار، بما في ذلك التفاصيل الجديرة بالملاحظة، لكل دراسة فردية. عندما يتم تضمين العائد التشخيصي المتاح لكل النمط الظاهري (خاصة في الجدول التكميلي 1 ح الذي يغطي الأنماط الظاهرية لأمراض الكلى المختلطة) والعائد التشخيصي المستقر على عدد أكبر من السكان الأصليين.
أبلغت خمس دراسات عن سكان ESKD الذين تم إدراجهم في قائمة الانتظار لإجراء جراحة زرع الأعضاء أو تلقوا عملية زرع كلية (الجدول التكميلي 1 ز). تراوح العائد التشخيصي في هذه الدراسات من 0.5% (فقط عمليات الحذف الجيني الكاملة في 20 جينًا تم تقييمها) إلى 50.9% في المرضى الذين تم اختبارهم وراثيًا في وقت الدراسة. عند استقراء ذلك على الأفواج الفردية من مرضى زرع الكلى (المدرجين في قائمة الانتظار)، تراوح العائد من 12.5 إلى 24.6٪.

أبلغت عشر دراسات من مجموعات مرضية مختلفة عن أمراض الكلى مجهولة المصدر (المرضى الذين لا يشير النمط الظاهري السريري لديهم إلى تشخيص محدد). تشتمل مجموعات النمط الظاهري على ADTKD (1)، ESKD (3)، وأنماط ظاهرية لأمراض الكلى المختلطة (6). كان العائد التشخيصي في مجموعة من المرضى الذين يعانون من التهاب الكلية العائلي لسبب غير معروف، الذين تم التحقيق في ADTKD، 29.5٪. في الدراسات التي تبحث في ESKD للمسببات غير المحلولة، تراوح العائد التشخيصي من 11.6 إلى 44.4٪. في الدراسات الست التي أجريت على الأنماط الظاهرية لأمراض الكلى المختلطة، تراوح العائد في المرضى الذين يعانون من اعتلال الكلية من أصل غير معروف من 17.1 إلى 56.3% عبر خمس دراسات وأفادت إحدى الدراسات عن عائد قدره 0% (خمسة مرضى فقط كانوا يعانون من اعتلال الكلية من أصل غير معروف في مجموعة من 204 مريضا). يقدم الجدول 3 نظرة عامة على التأثير السريري للتشخيصات الجينية التي أبرزتها الدراسات المختلفة، مقسمة إلى تأثير تشخيصي، وتأثير علاجي، وتأثير النذير.
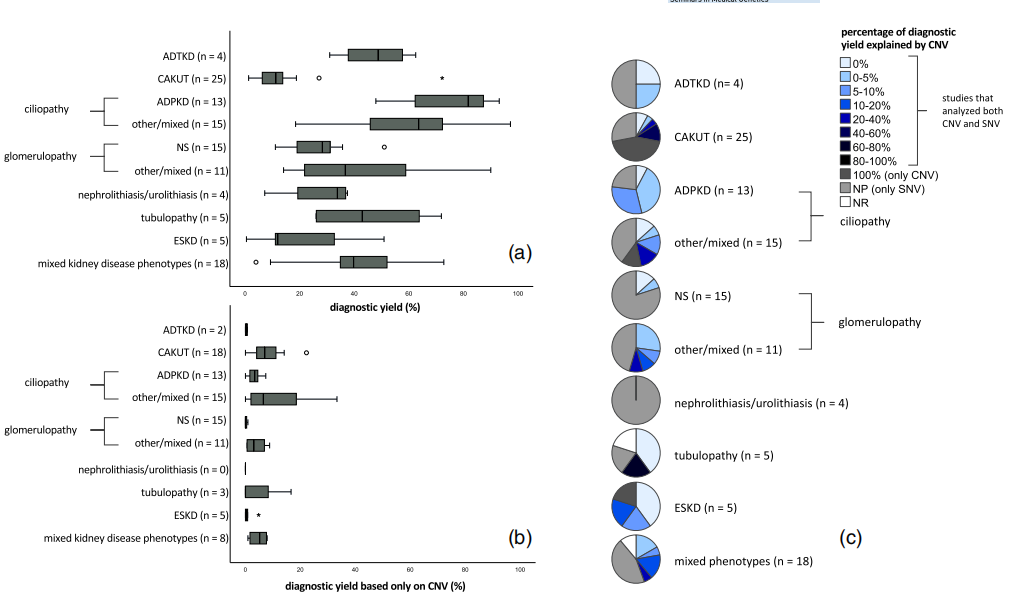
الشكل 1: العائد التشخيصي عبر فئات المرض. ( أ ) العائد التشخيصي لكل فئة مرض. لا يتم إضافة التقسيم الفرعي للأنماط الظاهرية المحددة داخل مجموعة "الأنماط الظاهرية لأمراض الكلى المختلطة" إلى مجموعات الأمراض المنفصلة المقابلة نظرًا لأن خصائص المريض/الاختبار/الفوج غير متوفرة لكل نمط ظاهري ضمن الدراسات في هذه المجموعة. بين قوسين عدد الدراسات المشمولة. ( ب ) يعتمد العائد التشخيصي فقط على اكتشاف تباين رقم النسخة (CNV). بين قوسين عدد الدراسات التي أجرت تحليل CNV. (ج) النسبة المئوية للعائد التشخيصي الإجمالي (أ) الموضح بواسطة CNVs (ب). بين قوسين العدد الإجمالي للدراسات. هذه هي النسبة بين اللوحتين الفرعيتين (ب) و(أ)، مما يوضح مقدار مساهمة اختبار CNV في العائد التشخيصي لكل دراسة
3.1|الخصائص التي تؤثر على العائد التشخيصي
3.1.1|خصائص المريض
بالنظر إلى خصائص المريض التي تؤثر على العائد التشخيصي ضمن دراسة معينة، نجد أن دراسات متعددة أبلغت عن تأثير إيجابي على العائد التشخيصي بناءً على تاريخ العائلة الإيجابي (عدد=18 من الدراسات)، وزواج الدم (ن=12)، خارج الكلى الميزات (ن=16)، والبداية المبكرة للمرض (ن=14)، و ESKD (ن=8) كما هو موضح في الجدول 2 والجدول التكميلي 1. تم ذكر بعض الميزات الإضافية أيضًا ، مثل الأنماط الظاهرية المحددة، وانخفاض تكرار ما بعد زرع الأعضاء، وعدم الاستجابة لمثبطات المناعة للنمط الظاهري NS (SRNS) المقاوم للستيرويد (الجدول 2).
عندما نقوم بتقييم هذه المتغيرات نفسها (تاريخ العائلة، والسمات خارج الكلوية، والبداية المبكرة للمرض، وESKD) بين الدراسات، نرى بوضوح أنه في الأفواج التي لديها نسبة عالية من الحالات العائلية وفي الأتراب مع نسبة عالية من الحالات خارج الكلوية، فإن التشخيص العائد أعلى (الشكل 2 أ، ب). ومع ذلك، فإننا لا نرى نفس النمط الواضح في الأفواج التي لديها نسبة عالية من قرابة الدم أو نسبة عالية من ESKD (الشكل 2ج، د). عندما ننظر إلى الأفواج ذات النسبة العالية من الحالات التي تظهر عند البالغين، نجد نسبًا منخفضة وعالية من العائد التشخيصي (الشكل 2 هـ). في الأفواج التي ليس لديها (0%) حالات إصابة بالبالغين، نرى نفس الشيء، مع شرح نسبة كبيرة من الدراسات ذات الإنتاجية المنخفضة بواسطة مجموعة CAKUT. يتم تسليط الضوء على أهمية تحليل CNV في الشكل 2f حيث لوحظ وجود عائد تشخيصي مرتفع في مرض بداية الطفولة مقارنة بمرض ظهور البالغين.
3.1.2|خصائص الفوج
في الشكل 3أ، نعرض عدد المرضى الذين تم اختبارهم في مجموعة فيما يتعلق بإنتاجية التشخيص. نجد أن العائد التشخيصي يتناقص في الأفواج الأكبر. عندما نقارن boxplots التي تمثل العائد التشخيصي في الأتراب السريري مقابل أفواج البحث، لا يبدو أن هناك فرقًا واضحًا (الشكل 3 ب). استخدمنا العائد التشخيصي في الأتراب السريري الذي تم اختباره وليس في الأتراب المستقراء، حيث لم تكن البيانات متاحة دائمًا للأتراب المستقرأ.
3.1.3|خصائص الاختبار يمثل الشكل 4 خصائص الاختبار بين الدراسات. يبدو أنه كلما زاد عدد الجينات التي تم تحليلها كلما انخفض العائد التشخيصي (الشكل 4 أ). عند ربط طرق التسلسل بالعائد التشخيصي، وجدنا أن اختبار الجين الواحد كان له عائد تشخيصي أقل مما كان عليه عند اختبار عدة جينات (2-10)، ووجدنا الشيء نفسه مع لوحات الجينات الصغيرة (<100) versus large gene panels (Supplementary Figure 1). However, the categories WES/WGS and SNP-array had a lower yield than the previously mentioned categories. 47/115 studies assessed SNVs, 12/115 assessed only CNVs and 55/115 assessed both (Figure 4b). As shown in Figure 4c, we found that the diagnostic yield was highest in cohorts where both SNVs and CNVs were assessed, and lowest in cohorts that only assessed CNVs. We saw that over the years there has been a shift from focusing either on SNVs or CNVs to including both in genetic testing (Supplementary Figure 2). There has also been a shift from enrichment-based panels to an exome-based approach. Noticeably in CNV testing, there is a shift toward the use of MPS-based CNV-calling.
3.1.4|تحليل CNV
تم تقييم CNVs في أغلب الأحيان في مجموعات المرض CAKUT، والاعتلال الهدبي، واعتلال التاووباثي، وESKD، والأنماط الظاهرية لأمراض الكلى المختلطة. في حالة تحصي الكلية/تحصي البول، لم يتم تقييم CNVs أبدًا. كان العائد التشخيصي المعتمد فقط على اختبار CNV هو الأعلى في مرضى CAKUT، تليها مجموعة المرض ذات الأنماط الظاهرية المختلطة والاعتلالات الهدبية. كانت مساهمة CNVs في العائد التشخيصي أيضًا أعلى في مجموعات CAKUT والاعتلال الهدبي. عندما قامت الدراسات بتقييم كل من CNVs وSNVs، وجدنا أعلى نسبة من CNVs في CAKUT ومرض التاووباثي (الشكل 1C). أوضحت عمليات حذف HNF1B التي تسبب اعتلال الأنابيب في Gitelman (مثل) النسبة العالية من CNVs في الحالة الأخيرة. تم استخدام طرق اختبار CNV المختلفة، مع أعلى عائد تم الحصول عليه عن طريق اختبار الجين الفردي واختبار CNV القائم على الصفيف (الشكل التكميلي 3).
3.2|الجينات الأساسية
في جميع الدراسات المشمولة، كان عدد محدود من الجينات مسؤولاً عن نسبة كبيرة من الحالات الموضحة كما هو موضح في الشكل 5. لقد وجدنا أن 10 جينات كحد أقصى كانت مسؤولة عن 50% على الأقل من الحالات التي تم حلها، وفي كثير من الأحيان واحد إلى أربعة فقط الجينات المسؤولة. في مجموعات النمط الظاهري ADTKD وAPDKD، كان جين واحد فقط (UMOD أو MUC1 وPKD1، على التوالي) مسؤولاً عن 50٪ من العائد المُبلغ عنه في دراسة واحدة. ولكن أيضًا في مجموعات النمط الظاهري ذات الأنماط الظاهرية المتنوعة لأمراض الكلى، وجدنا أن المتغيرات في 10 جينات كحد أقصى تعزى إلى 50% من العائد التشخيصي. يتم عرض الجينات المسؤولة عن العائد الأعلى بنسبة 50٪ في اللوحة (ب). يمكن الاطلاع على تفاصيل كل دراسة في الجدول التكميلي 3.

الشكل 2: مخططات التشتت توضح العلاقة بين العائد التشخيصي وخصائص المريض. يصف الأسطورة عددًا من الدراسات التي توفرت لها بيانات حول هذه الخاصية المحددة للمريض. تشير الألوان إلى مجموعة المرض التي اشتقت منها الدراسة. تمثل كل نقطة لدراسة واحدة النسبة المئوية لميزة معينة في تلك المجموعة وما هو العائد التشخيصي الذي تم الحصول عليه من تلك الدراسة نفسها. ( أ ) النسبة المئوية للحالات التي لها تاريخ عائلي إيجابي فيما يتعلق بإنتاجية التشخيص. ( ب ) النسبة المئوية للحالات ذات السمات الخارجية فيما يتعلق بالعائد التشخيصي. (ج) النسبة المئوية للحالات من عائلة الأقارب فيما يتعلق بإنتاجية التشخيص. ( د ) النسبة المئوية لحالات مرض الكلى في المرحلة النهائية (ESKD) فيما يتعلق بإنتاجية التشخيص. ( هـ ) النسبة المئوية لحالات ظهور المرض لدى البالغين فيما يتعلق بإنتاجية التشخيص. ( و ) النسبة المئوية لحالات ظهور المرض لدى البالغين فيما يتعلق بإنتاجية التشخيص فقط بناءً على اختلافات عدد النسخ (CNVs).
الخدمة الداعمة:
البريد الإلكتروني:wallence.suen@wecistanche.com
واتساب/هاتف:+86 15292862950
محل:
https٪3a٪2f٪2fwww.xjcistanche.com٪2fcistanche-shop






