سبب مرض الكلى المتعدد الكيسات
Mar 10, 2022
لمزيد من المعلومات: ali.ma@wecistanche.com
الإفراط في التعبير عن PKD1 يسبب مرض الكلى المتعدد الكيسات
كارولين ثيفيرج ، وألميرا كوربيغوفيتش ، ومارتن كويلارد ، وريتشارد غيوم ، وأوليفييه كوتي ، وماري ترود
الآليات الممرضة الكامنةالعامل الوراثي المسيطرمرض تكيس الكلى(ADPKD) لا يزال يتعين توضيحه. بينما توجد أدلة على أن Pkd1(مرض الكلى المتعدد الكيسات 1)يمكن أن يؤدي عدم كفاية الجينات الوراثية وفقدان الزيجوت غير المتجانسة إلى تكوين كيس في الفئران ، ومستويات عالية بشكل متناقض من Pkd1 (مرض الكلى المتعدد الكيسات 1) تم الكشف عن التعبير في كليتي ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى) المرضى. لتحديد ما إذا كان Pkd1(مرض الكلى المتعدد الكيسات 1)اكتساب الوظيفة يمكن أن يكون عملية مسببة للأمراض ، تم تعديل الكروموسوم الاصطناعي البكتيري البكتيري Pkd1 (Pkd 1- BAC) عن طريق إعادة التركيب المتماثل لاستهداف تعبير Pkd1 المستدام فقط بشكل تفضيلي للكلية البالغة ، تم إنشاء العديد من الخطوط المعدلة وراثيًا التي بالغت على وجه التحديد في التعبير عن التحوير Pkdl في الكلى 2- إلى 15- أضعاف على مستويات Pkd1 الذاتية. جميع الفئران المعدلة وراثيا طورت بشكل متكرر تكاليف أنبوبي وكبيبي وقصور كلوي وتوفيت بسبب الفشل الكلوي. يوضح هذا النموذج أن الإفراط في التعبير عن النوع البري Pkd1 وحده يكفي لتحفيز تكوين المثانة الذي يشبه ADPKD البشري (العامل الوراثي المسيطرمرض تكيس الكلى). كشفت نتائجنا أيضًا عن زيادة مذهلة في التعبير الكلوي c-myc في الفئران من جميع الخطوط المعدلة وراثيًا ، مما يشير إلى أن c-myc أمر بالغ الأهمية في المستجيب المصب في الجسم الحي لـ Pkd1(مرض الكلى المتعدد الكيسات 1)Dathwavs الجزيئية ، هذه الدراسة لم تنتج فقط PKD الأول الذي لا يقدر بثمن(مرض تكيس الكلى)نموذج لتقييم التسبب الجزيئي والعلاجات ولكنه يقدم أيضًا دليلًا على أن اكتساب الوظيفة يمكن أن يكون آلية مسببة للأمراض في ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى).

العامل الوراثي المسيطرمرض تكيس الكلى(ADPKD) هو أحد أكثر الأمراض الوراثية شيوعًا عند البشر. يتميز بالتطور التدريجي للكيسات الكلوية المتعددة التي تؤثر على جميع أجزاء النيفرون. تشمل المظاهر الأخرى تكوين أكياس في الكبد والبنكرياس وكذلك تمدد الأوعية الدموية داخل الجمجمة وعيوب القلب والأوعية الدموية. ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى)عادة ما يؤدي إلى قصور كلوي مع التقدم إلى المرحلة النهائية من مرض الكلى في أواخر منتصف العمر.
حوالي 85 بالمائة من ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى)ترتبط الحالات بطفرات في PKD1(مرض الكلى المتعدد الكيسات 1)الجين. هذا PKD1(مرض الكلى المتعدد الكيسات 1)الجين كبير ، يمتد 54 كيلو بايت ، ويتكون من 46 إكسون. يقوم بتوليد نسخة 14. 2- كيلوبايت وترميز 4. ، 302- بروتين من الأحماض الأمينية يسمى بوليسيستين -1 (4 ، 9-11). تم تحليل تعبير PKD1 البشري و polycystin -1 في الوضع العادي و ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى)الكلى. أثناء التطور الكلوي ، يتم اكتشاف البوليسيستين -1 بسهولة في الخلايا الظهارية الكبيبية والأنبوبية (تمت مراجعتها في المرجع 37 والمراجع الواردة فيه). في البالغين العاديين ، أظهرنا نحن وآخرون أن PKD1(مرض الكلى المتعدد الكيسات 1)يتم التعبير عن الحمض النووي الريبي والبروتين بمستويات معتدلة إلى منخفضة في الأنابيب التجميعية والبعيدة ، بينما زادت المستويات (~ 2- أضعاف) في ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى)الكلى (22 ، 39). ومن المثير للاهتمام ، أنه تم اكتشاف تعبير البوليسيستين المستمر أو المعزز -1 في غالبية الأكياس الظهارية الكلوية ، على الرغم من عدم وجود تلطيخ في أقلية كبيرة من الأكياس (29). بالإضافة إلى الكلى ، PKD1(مرض الكلى المتعدد الكيسات 1)ينتشر التعبير عادة في أنسجة البالغين الأخرى ، بما في ذلك أنواع الخلايا الظهارية وغير الظهارية (6 ، 14 ، 18 ، 29 ، 30 ، 39).
أكثر من 200 PKD1 مختلفة(مرض الكلى المتعدد الكيسات 1)تم وصف الطفرات ، ومعظمها عبارة عن طفرات حذف أو إدخال أو تغيير إطار أو طفرات غير منطقية. من المتوقع أن ينتج عن ذلك أشكال مبتورة من البروتين ، بما يتفق مع تعطيل أليل واحد.

ومع ذلك ، فإن نسبة كبيرة هي طفرات خاطئة أو داخل الإطار توجد في جميع أنحاء الجين وغالبًا ما تكون فريدة من نوعها لعائلة معينة (33 ، 34). كما يوحي الاسم ، ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى)هو المسيطر و PKD1 المتحور المنقول(مرض الكلى المتعدد الكيسات 1)الأليل كافٍ لإنتاج المرض. ومع ذلك ، فإن الطبيعة البؤرية للكيسات الكلوية في ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى)يقترح أن الآلية الطفرية لـ PKD1(مرض الكلى المتعدد الكيسات 1)يمكن أن تكون ضربتين أو فقدان الزيجوت غير المتجانسة. تم الحصول على دعم لهذه الآلية من خلال الكشف عن PKD1(مرض الكلى المتعدد الكيسات 1)الطفرات الجسدية النسيلية في الخلايا من نسبة كبيرة من الخراجات (3 ، 21 ، 32). يمكن لآلية فقدان الزيجوت غير المتجانسة أن تفسر النمط الظاهري المتنوع على نطاق واسع الذي يتم ملاحظته بشكل شائع في العائلات الفردية.
دراسات على الفأر Pkd1(مرض الكلى المتعدد الكيسات 1)قد يوفر الجين رؤى قيمة حول وظيفة (وظائف) PKD1 بسبب التشابه الوثيق بين الجين البشري والجين الفأري والمنتج الجيني. في التطور الطبيعي ، يتم التعبير عن الفئران Pkd1 بمستويات عالية من مرحلة التوتية ويتم اكتشافها في جميع مشتقات خلايا القمة العصبية. بما في ذلك الدماغ البالغ ، والقوس الأبهري ، والغضاريف ، والتكثف اللحمي (16 ، 17). تم الإبلاغ عن موت الفئران الطافرة متجانسة اللواقح المستهدفة لحذف Pkd1 في الرحم وتطور الكيسات الكلوية والبنكرياس (2،19 ، 24-26 ، 40). لسوء الحظ ، لم توفر هذه المحاولات السابقة لإنشاء نماذج الفئران حيوانات قابلة للحياة بعد الولادة. ومع ذلك ، فإن حدوث الخراجات الكلوية في هذه الفئران الطافرة متماثلة اللواقح Pkd1 سيكون متسقًا مع فرضية وجود آلية طفرة ثنائية الضربة في البشر تتضمن طفرة جرثومية وتعطيل جسدي للأليل الطبيعي. ومع ذلك ، فإن الفئران المتغايرة الزيجوت من أجل الحذف المستهدف Pkd1 أظهرت أيضًا PKD مع أكياس الكبد والبنكرياس العرضية على الرغم من ظهور البالغين المتأخر ، مما يدعم آلية قصور الفرد أو تقليل جرعة الجينات. علاوة على ذلك ، قد لا يكون فقدان تغاير الزيجوت أو عدم كفاية الفردانية هو الآلية الوحيدة لـ ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى)طريقة تطور المرض. في الواقع ، هذه الآليات تتعارض مع التعبير المستمر أو المحسن لـ PKD1(مرض الكلى المتعدد الكيسات 1)يُرى في غالبية الخراجات الكلوية البشرية ما لم يتم إنتاج بروتينات غير وظيفية. تثير هذه النتيجة لتعبير PKD1 المستمر أو المتزايد السؤال عما إذا كان اكتساب الوظيفة أو الإفراط في التعبير قد يكون فعالًا. للتحقيق في الآلية المسببة للأمراض لاكتساب الوظيفة Pkd1 ، قمنا بعزل وتمييز كروموسوم الفئران الاصطناعي البكتيري Pkd1 (Pkd 1- BAC) الذي تم تعديله لاحقًا عن طريق إعادة التركيب المتماثل في الإشريكية القولونية لاستهداف التعبير عن Pkd1(مرض الكلى المتعدد الكيسات 1)على وجه التحديد للكلى. أبلغنا عن إنتاج ثلاثة خطوط معدلة وراثيًا تعبر عن جين Pkd1 المحول على مستويات مختلفة. أظهرت جميع الفئران بشكل متكرر عددًا من أوجه التشابه مع ADPKD البشري وتطورت باستمرار في البداية المبكرة مع تقدم سريع في التغيرات المورفولوجية والوظيفية الكلوية وتوفيت بسبب الفشل الكلوي في منتصف العمر. بالإضافة إلى ذلك ، تصف الدراسة الحالية آلية في الجسم الحي يمكن من خلالها لـ Pkd1 التوسط في النمط الظاهري لـ PKD. تمثل هذه الفئران النموذج الأول من PKD الناتج عن الإفراط في التعبير الكلوي الوحيد عن PKD1 المتعامد(مرض الكلى المتعدد الكيسات 1)الجين.

المواد والأساليب
عزل استنساخ BAC المحتوية على Pkd1(مرض الكلى المتعدد الكيسات 1)المكان. تم عزل استنساخ Pkd 1- من سلالة البكتيريا المضيفة E. coli DH10B (RecA؛ RecBC) من مكتبة ماوس 129Sv pBelo11BAC (علم الوراثة البحثية). تم إجراء فحص تجمعات BAC الفائقة بواسطة PCR باستخدام الاشعال التالي: 5 مناطق ، 5- CTG ATGAGTTCTGGCCATGGATG -3 (الأمام Pkd1 exon 1) و 5- CTGCCA GCCAATGCCATAGTCAC -3 (عكس Pkd1 إكسون 1) ؛ و 3 مناطق ، 5- TCG GCCCTAGCGTCTGCAGCC -3 (إعادة توجيه Pkd1 exon 39) و 5- TCCAGTCC CACCTACAGCCAAC -3 (عكس Pkd1 exon 40). تم تحديد استنساخ واحد إيجابي لكل من التضخيم وتحليله على الرحلان الكهربائي للهلام والحقل النبضي (PFGE) متبوعًا بالنشاف الجنوبي. لتحليل اللطخة الجنوبية ، تم تصميم سبعة تحقيقات Pkd1 للماوس: exon الجيني 1 (516 نقطة أساس ؛ نيوكليوتيدات [nt] 1 إلى 516 ؛ رقم انضمام NCBI U70209) ، exon الجينومي 2-3 (220 نقطة أساس) ، exon الجينومي {{ 31}} (8479 نقطة أساس) ، cDNA exon 15-20 (1،724 bp ؛ nt 6455 إلى 8179) ، cDNA exon 25-34 (1،315 bp ؛ nt 9415 إلى 10730) ، cDNA exon 36-45 ( 1،655 نقطة أساس ؛ nt 10963 إلى 12618) ، والإكسون الجيني 45-46 (1،640 نقطة أساس) (16). تم أيضًا تسلسل العديد من المناطق بما في ذلك إدخال BAC لأطراف هذا الفئران Pkd 1- BAC وتأكد أنها متعامدة مع جين PKD1 البشري والمناطق المجاورة.
النتائج
إنتاج SBPkdl(مرض الكلى المتعدد الكيسات 1) rAc-BAC عن طريق إعادة التركيب المتماثل. لتحديد ما إذا كان كسب Pkd1 للوظيفة وحده كافياً لإنتاج ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى)النمط الظاهري ، قمنا أولاً بعزل استنساخ جينومي يحتوي على جين Pkdl بأكمله في مكتبة متجه 129 / Sv BAC. تم فحص هذه المكتبة بواسطة PCR بمجموعتين من البادئات للجين Pkd1 الذي امتد exon 1 في 5'end و exons 39 إلى 40 باتجاه 3'end (الشكل 1). تم تحديد استنساخ BAC موجب للجين Pkd1 والذي تضمن كامل الجسم الجيني Tsc2 المجاور. تم تمييز إدراج Pkd1 بالتفصيل للتأكد من أن التركيب الجيني يطابق بنية Pkd1 الذاتية(مرض الكلى المتعدد الكيسات 1)جين سلالة الماوس 129 / Sv التي تم اشتقاق الإدخال منها ومن السلالة الفطرية C57BL / 6J. بدت الخرائط الجينومية لموضع Pkd1 في BAC وفي هذه السلالات الفطرية بواسطة تحليل اللطخة الجنوبية ، مع أربعة عمليات هضم إنزيم مقيد وسبعة تحقيقات تغطي جين Pkdl بأكمله ، متطابقة مع عدم وجود دليل على إعادة الترتيب (الشكل 1). احتوى BAC هذا على ~ 121- kb insert بما في ذلك -37 kb of upstream و -39 kb of the downstream التسلسل من Pkd1(مرض الكلى المتعدد الكيسات 1)الجين على النحو الذي يحدده الرحلان الكهربائي والتسلسل.
تم تعديل استنساخ Pkd 1- BAC بواسطة حدثين متتاليين لإعادة التركيب المتماثل في الإشريكية القولونية. ال Pkd1(مرض الكلى المتعدد الكيسات 1)تم تمييز الجين في exon 10 عن طريق استبدال النيوكليوتيدات (G إلى A) لإنشاء موقع EcoRI جديد في الموضع 2355 على خريطة cDNA. تم إنتاج طفرة النقطة الصامتة هذه لتمييز Pkd1(مرض الكلى المتعدد الكيسات 1)الجين ونسخة BAC من الأصل الداخلي. بالإضافة إلى ذلك ، لقد استبدلنا العناصر التنظيمية 5 لـ Pkd 1- BACgene من خلال الاستفادة من العناصر الظهارية الكلوية المحددة مسبقًا "SB" من SBM (المرتبطة بـ c-Myc) أو SBF المرتبط بـ c- fos) بناء الجينات العابرة لتقييد التعبير عن الكلى (36 ، 38) (الشكل 2 أ).
تم هضم SBPkd1TAc-BAC الجديد مع Notl ، وهو موقع فريد يقع مباشرة في أعلى المنبع من عناصر SB ، و ClaI داخل جسم الجين Tsc2 ، مع اقتطاع العناصر التنظيمية لـ Tsc2 والنصف الخامس من جسم الجين لضمان نقص التعبير الخارجي لـ Tsc2 في جميع الأنسجة ولإزالة متواليات BACvector بدائية النواة (الشكل 1 و 2). تم عزل هذا الجزء الخطي 70- كيلو بايت من Notl-Clal وتنقيته وتحديد كمية الحقن المجهري للبويضات (36).
إنتاج وتحليل الفئران المعدلة وراثيا SBPkd1rAc. أربعة مؤسسين معدلين وراثيًا يحملون عدة نسخ من التحوير SBPkd1rAc طوروا باستمرار PKD(مرض تكيس الكلى). من الفئران الأربعة المؤسس لـ SBPkdlrAc التي تم تحديدها بواسطة التحليل الجنوبي ، تم إنشاء ثلاثة خطوط معدلة وراثيًا SBPkd1rAG مع نسختين إلى تسع نسخ من الجينات المحورة (الشكل 2 ب). تمت مراقبة توصيف تكامل الجينات المحورة في هذه السطور باستخدام 5 '، وداخلي ، و 3' بروب كما هو موضح في الأمثلة التمثيلية في الشكل 2 ب. تم الكشف عن الخطوط المعدلة وراثيًا باستخدام مسبار 5 "SB" نطاق بسرعة 10.9 كيلو بايت بما يتفق مع دمج الجين العابر SBPkd1rAc في اتجاه الرأس إلى الذيل وكشف عن النطاق 3'probe a 7. 1- kb band (الشكل 2 ب). بالإضافة إلى ذلك ، اكتشف المسبار الداخلي نطاق 9. 4- kb الداخلي Pkd1 بالإضافة إلى 6. 9- kb و 2. 5- نطاقي kb من الجينات المحورة بسبب موقع إدخال EcoRI في إكسون 10 (الشكل 2 ب). احتوت هذه الفئران على نسخ كاملة من الجينات المحورة بناءً على تحليل التركيب الجيني المتداخل.
Pkd1(مرض الكلى المتعدد الكيسات 1)اكتساب الوظيفة في الفئران المعدلة وراثيا SBPkdlrAc البالغة. تم فحص التعبير الجيني SBPkdlrAG و Pkd1 في أعضاء مختلفة. تم إجراء القياس الكمي لمستويات النسخ من الجين المحول و / أو الجين الداخلي عن طريق تحليل اللطخة الشمالية (الشكل 3 أ). كما هو متوقع ، كانت نسخ الجينات المعدلة وراثيًا ذات طول مماثل (14.2 كيلو بايت). بناءً على تعبير GAPDH للتحكم ، زادت الكلى من جميع خطوط الماوس SBPkd1TAG بشكل ثابت من تعبير النص مقارنة بمستويات Pkdl الطبيعية في الكلى البالغة (n=3) من نفس العمر. عرض الجينات المعدلة وراثيا والتعبير الداخلي للخطوط المعدلة وراثيا المختلفة نطاقًا من 2- إلى 15- أضعاف فوق مستويات Pkd1 الذاتية الكلوية الضابطة (الشكل 3 أ). }) أظهر Pkd1 أعلى(مرض الكلى المتعدد الكيسات 1)مستويات من الأسطر 3 (ن=3) و 41 (ن =4). علاوة على ذلك ، ترتبط مستويات التعبير Pkd1 المقاسة بواسطة تحليل اللطخة الشمالية بتلك التي تم الحصول عليها بواسطة PCR في الوقت الفعلي باستخدام البادئات في exons 1 و 2 (الشكل 3 ب).
تم إجراء القياس الكمي لمستويات التعبير الجيني على وجه التحديد بواسطة PCR في الوقت الفعلي و RT-PCR شبه الكمي في الخطوط الثلاثة المعدلة وراثيًا في سن البلوغ باستخدام البادئات في المنطقة 5 مترجمة (B ، -globin المروج) وفي exon 2 من Pkd1(مرض الكلى المتعدد الكيسات 1)(الشكل 3 ب). تمت مقارنة تعبير SBPkdlrAc في الفئران المعدلة وراثيًا بمنتج جين بروتين الريبوسوم S16 كمعيار داخلي. كانت الشروط المستخدمة لتضخيم RT-PCR شبه الكمي ضمن النطاق الخطي. أظهر التعبير الجيني بواسطة PCR في الوقت الحقيقي و RT-PCR الدلالي باستمرار وبشكل خاص أعلى تعبير في الكلى لجميع الخطوط المعدلة وراثيًا بالنسبة للأعضاء الأخرى (الشكل 3 ب و ج). كانت مستويات التعبير الكلوي لعينة فردية قابلة للتكرار بأي من تقنيات الكشف المستخدمة. أعلى مستويات Pkd1(مرض الكلى المتعدد الكيسات 1)تم قياس التعبير الكلوي المحول للخط 39 و 41. لرصد ما إذا كانت زيادة Pkd1(مرض الكلى المتعدد الكيسات 1)نتج التعبير عن الجين المحول أو الجين الداخلي ، تمت مقارنة نفس المجموعة من الفئران من الخطوط الثلاثة المعدلة وراثيًا للتعبير الكلوي المحول Pkd1 وللتعبير الكلوي Pkd1 الكلي (الجيني والداخلي) بواسطة PCR في الوقت الحقيقي. ومن المثير للاهتمام ، أن السطور 39 و 41 بالنسبة إلى السطر 3 أظهر أن زيادة التعبير الكلوي المحول Pkdl كان مشابهًا أو أعلى من التعبير الكلوي الكلي لـ Pkd1 ، مشيرًا إلى التحوير باعتباره المسؤول تحديدًا عن هذا التعبير المستحث. في أعضاء مختلفة (بما في ذلك القلب والرئة والدماغ والكبد والبنكرياس والطحال) ، أظهر التحوير SBPkd1rAg تعبيرًا ضعيفًا للغاية تم اكتشافه في الطحال والرئة ، مع القليل من التعبير غير القابل للاكتشاف في الأعضاء الأخرى (الشكل 3 ب). أظهر القياس الكمي بواسطة PCR في الوقت الفعلي مستوى 10- إلى مستوى 1 ، 000- أضعاف مستوى التعبير الجيني في الأنسجة خارج الكلية بالنسبة لتعبير الكلى (الشكل 3 ج). تمنح العناصر التنظيمية لـ SBPkdlrA في التحوير SBPkdlrA تعبيرًا كلويًا تفضيليًا ؛ تم تحديد توزيع الأعضاء هذا أيضًا عند استخدامه في الجينات المحورة المرتبطة بـ c-myc (SBM) و c-fos (SBF) (36 ، 38).
C-myc ، مستجيب مصب لـ Pkd1(مرض الكلى المتعدد الكيسات 1)مسارات الإشارات في الفئران SBPkdlrAc. لاكتساب نظرة ثاقبة على الآلية المسببة للأمراض داخل الخلايا لفئران SBPkdlrAg المعدلة وراثيًا ، سعينا بعد ذلك إلى مراقبة مستوى التعبير الكلوي c-myc استنادًا إلى ملاحظتنا السابقة لإلغاء تنظيم c-myc في ADPKD البشري (العامل الوراثي المسيطرمرض تكيس الكلى)الكلى (22). تم إجراء تحليل للكلى من جميع الخطوط الثلاثة المعدلة وراثيًا 3 (ن =4) و 39 (ن =7) و 41 (ن=4) بالإضافة إلى مجموعة التحكم (ن=4) كما هو مبين في الشكل ثلاثي الأبعاد ، هناك تعبير جوهري عن c-myc الداخلي المستحث في الفئران SBPkd1TAG بالنسبة لفئران التحكم ذات العمر المماثل. ومن المثير للاهتمام ، أن مستوى تعبير c-myc في بعض كلى SBPkd 1-. على وجه الخصوص السطر 39 ، وصلت إلى مستويات مماثلة لتلك التي لوحظت في نموذج الماوس المعدلة وراثيًا PKD SBM الناتج عن التعبير الكلوي c-myc.
التشوهات الكلوية في الفئران SBPkd1raG مشابهة لـ PKD(مرض تكيس الكلى). To characterize the phenotype caused by the transgene expression, gross and histologic examinations were undertaken on transgenic kidneys. Adult kidneys from all transgenic lines were affected bilaterally. Kidneys contained numerous cortical cysts that varied from microscopic to macroscopic in size(Fig.4a and b). SBPkdl-AG kidneys were pale, a typical finding in PKD. On histologic examination, all transgenic founder mice and progenies (n =25;n>6 لكل سطر) طور العديد من الأكياس الأنبوبية (T) والكبيبية (G) (الشكل 4 د ، و ، و ز). لوحظت الأكياس في الأنابيب من المناطق القشرية والنخية وكذلك تجميع الأنابيب من الحليمة (الشكل. 4 د و هـ). أظهرت الفئران المعدلة وراثيًا تضخمًا طلائيًا أنبوبيًا (رأس السهم) يشمل كل من الأنابيب الكيسية وغير الكيسية والتضخم المتكرر (الشكل 4 ز و ح) ، لكن تفاوتت شدته بين الفئران الفردية. لوحظ بشكل متكرر التليف الخلالي (F) ، التسلل اللمفاوي حول الأوعية الدموية ، والقوالب البروتينية (P) (الشكل 4 د و هـ).
لتحديد موقع الترجمة بدقة أكبر لـ Pkd1 المتزايد(مرض الكلى المتعدد الكيسات 1)في الكلى ، أجرينا تهجينًا في الموقع باستخدام مسبار exon 36-45 المستخدم سابقًا (16). تم تحديد إشارة التهجين على وجه التحديد للخلايا الظهارية المبطنة للكيس والأنابيب المفرطة التصنع بالإضافة إلى الأكياس الكبيبية. بالإضافة إلى ذلك ، شوهدت بعض الإشارات على ظهارة الأنابيب غير الكيسية أو المتوسعة قليلاً ، ومن المحتمل أن تحدد الأنابيب المعينة مسبقًا للخضوع لتغيرات كيسية مستقبلية (الشكل 4 ط و ي).
تم إجراء التحليل النسيجي الكلوي أيضًا على الفئران المعدلة وراثيًا عند الولادة (ن =8) ، يوم ما بعد الولادة 10 (P10) (ن =3) ، P20 (ن =5) ، P35 (ن { {7}}) ، و P45 (ن=3) بالمقارنة مع رفقاء القمامة السلبيين من نفس الفئة العمرية (ن 2 إلى 4). ومن المثير للاهتمام ، أن جميع الفئران المعدلة وراثيًا حديثي الولادة أظهرت توسعًا أنبوبيًا وكبيبيًا بالنسبة للتحكم في زملائه السلبيين (الشكل 4 كيلو ولتر) ، مما يشير إلى أن الشذوذ الكلوي بدأ في الرحم كما لوحظ في فئران SBM وفي ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى)المرضى. زاد التوسّع الأنبوبي والكبيبي من حيث الحجم والعدد مع تقدم العمر. بحلول P35 ، أظهرت الفئران المعدلة وراثيا تضخمًا شديدًا ودليلًا على تصلب الكبيبات. تغيير الوظائف الفسيولوجية الكلوية في الفئران SBPkd1TAG. عرض الوظائف الفسيولوجية الكلوية لجميع الفئران المعدلة وراثيا ميزات مماثلة ل PKD(مرض تكيس الكلى)، في حين أن الزملاء غير المعدلين وراثيًا لم يصابوا بالمرض أبدًا. في غضون بضعة أشهر بعد الولادة ، أصيبت الحيوانات المصابة بقصور كلوي مزمن. تم رصد هذه الحيوانات من أجل المعلمات الوظيفية الكلوية عن طريق قياس مستويات المصل والبول ، نيتروجين اليوريا في الدم (BUN) والكرياتينين ، الأسمولية في البول ، بروتين البول ، وإفراز الأيونات (الجدول 1). أظهرت جميع الفئران من الخطوط الثلاثة مقارنةً بالضوابط عيوبًا في التركيز ، وهي نتيجة شائعة في ADPKD ، وبالتالي أظهرت انخفاضًا في تركيز BUN والكرياتينين والبروتين والحديد في البول. تم رصد مؤسسي وذرية SBPkd1TAG المعدلة وراثيًا (ن 6) من كل سطر نوعيًا للبيلة البروتينية على عينات البول بواسطة SDS-PAGE (الشكل 5). أظهرت الفئران التي يزيد عمرها عن شهرين بيلة بروتينية غير انتقائية تتقدم مع تقدم العمر. بالإضافة إلى ذلك ، تمت زيادة مستويات BUN في المصل والكرياتينين في الدم ، مما يكشف عن القصور الكلوي (الجدول 2). نظرًا لأن القصور الكلوي المزمن يؤدي عادةً إلى تغييرات في المعلمات الدموية ، فقد تم فحصها في الفئران المعدلة وراثيًا SBPkd1TAG من عمر 3 إلى 14 شهرًا (الجدول 2). كانت هذه الفئران المعدلة وراثيا مصابة بفقر الدم كما يتضح من انخفاض عدد خلايا الدم الحمراء بشكل ملحوظ ، حيث وصل الهيموجلوبين والهيماتوكريت إلى نصف المستويات الطبيعية. لم تتأثر معلمات خلايا الدم الحمراء الأخرى ، مثل النسبة المئوية للخلايا الشبكية ، كما هو متوقع عندما تسببها عيب كلوي. ماتت هذه الحيوانات باستمرار بسبب الفشل الكلوي في 5. 9 2. 8 أشهر من العمر (ن 42) من السلالة الجينية المتحولة 39 وفي الأعمار اللاحقة ، 14. 6 3. شهر واحد (ن 20) و 11 . 7 6. 5 أشهر (رقم 7) ، للسطر 3 و 41 على التوالي.
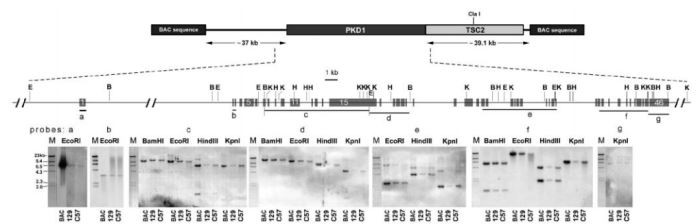
تين. 1. تمثيل تخطيطي وتحليل مفصل لخريطة التقييد للفأر Pkd 1- BAC.
أنماط هضم الحمض النووي الجيني لـ Pkd1(مرض الكلى المتعدد الكيسات 1)تم مقارنة BAC مع Pkd1(مرض الكلى المتعدد الكيسات 1)locus في سلالات الماوس الفطرية 129Sv و C57Bl / 6J. تم إنتاج سبعة مجسات تشمل معظم جين الفئران Pkd1:
(أ) إكسون 1 ، (ب) إكسون 2-3 ، (ج) إكسون 7-15 ، (د) إكسون 15-20 ، (هـ) إكسون 25-34 ، (و) إكسون 36-45 ، و (ز) exon 45-46 ، المسمىان من a إلى g على الجينوم Pkd1(مرض الكلى المتعدد الكيسات 1)التمثيل وفوق اللطخات الفردية.
تحليل اللطخة الجنوبية بعد هضم القيود (BamHI و EcoRI و HindIII و KpnI) للحمض النووي الجيني من Pkd 1- BAC و murine Pkd1(مرض الكلى المتعدد الكيسات 1)أظهر loci أنماطًا متطابقة مع جميع المجسات السبعة. M ، علامة HindIII ؛ 129 ، 129 / سيفرت ؛ C57 ، C57Bl / 6J.
نقاش
هنا ، نُبلغ عن عزل وتوصيف BAC الفئران Pkd 1-. هذا Pkd1(مرض الكلى المتعدد الكيسات 1)تم تمييز الجين واستبدال العناصر التنظيمية لاستهداف التعبير على وجه التحديد للكلى من خلال حدثين متتاليين لإعادة التركيب المتماثل. أظهرت الفئران المعدلة وراثيًا التي تم إنتاجها باستخدام هذا الجين SBPkd1TAG الجديد زيادة 2- إلى 15- أضعاف في تعبير Pkd1 وتغييرات مورفولوجية كلوية مبكرة بشكل متكاثر نموذجية لـ PKD. يظهر القصور الكلوي في منتصف العمر ، وتموت الفئران قبل الأوان بسبب الفشل الكلوي. تشير نتائجنا أيضًا إلى أن آلية التعبير الزائد Pkd1 المسؤولة عن هذا النمط الظاهري يتم توسطها عن طريق الإشارة إلى تنشيط c-myc في الجسم الحي. توضح هذه الدراسة أن اكتساب وظيفة الفئران Pkd1 في الكلى كافٍ لإنتاج النمط الظاهري الكلوي PKD. نظرًا لعدم تكرار جين الفئران Pkd1 كما هو الحال في البشر (27) ، فقد حددنا وعزلنا استنساخ BAC الذي يحتوي على جين Pkd1 بأكمله. أكد التوصيف الكامل لـ 129 / Sv murine Pkd 1- BAC ، مقارنة غير مباشرة مع سلالتين من الفئران الفطرية ، سلامة موضع Pkd1. احتوى إدراج Pkd 1- BAC على 37 إلى 39 كيلو بايت من التسلسلات الأولية والنهائية من جين Pkd1. أظهر تحليلنا أن جين Pkd1 في BAC هذا كان موضعاً من النوع البري الفأري حسن النية يمكن أن يخدم لمزيد من الدراسات. على الرغم من وجود دليل قوي على تكوين كيس في ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى)يمكن أن ينتج عن فقدان تغاير الزيجوت بعد تعطيل جسدي لـ PKD1 الطبيعي(مرض الكلى المتعدد الكيسات 1)allele (3 ، 21 ، 32) ، هناك أيضًا دليل موحٍ على استمرار أو زيادة تعبير polycystin -1 في الظهارة الأنبوبية الكيسية (22 ، 29). تثير الملاحظة الأخيرة مسألة ما إذا كان الإفراط في التعبير عن Pkd1 بحد ذاته سببًا قريبًا كافيًا لتكوين المثانة. في الفئران المعدلة وراثيا والتي تحمل PKD1 البشري(مرض الكلى المتعدد الكيسات 1)جينات TSC2 و RAB 26 و NTHL1 و SLC9A3R2 ، طورت أقلية فقط من الفئران الخراجات ولم يكن أي منها لديه تعبير جيني قابل للاكتشاف في مرحلة البلوغ على الرغم من 30 نسخة من الجين المحور (31). في تلك الفئران المعدلة وراثيًا ، كان من الصعب تحديد دور واضح لفرط التعبير Pkd1 في تكوين المثانة. يختلف نموذجنا ، حيث تم دمج نسختين إلى تسع نسخ من النوع البري من Pkd1 وحدها ، بدون جينات متجاورة ، في الفئران المعدلة وراثيًا. نظرًا لأن الجين Pkd1 له وظائف أساسية في أعضاء أو أنسجة مختلفة ، كما هو موصوف للعديد من الفئران مع استئصال الجين Pkd1 ، فإن الإفراط في التعبير الجهازي لـ Pkd1 يمكن أن يؤدي إلى تأثيرات مربكة إضافية. وبالتالي ، فقد تناولنا دور اكتساب وظيفة Pkd1 باستخدام نهج يستهدف Pkd1 على وجه التحديد للكلى. من خلال إعادة التركيب المتماثل ، قمنا أولاً باستبدال المنطقة التنظيمية الأولية لـ Pkd1 بعناصر تنظيمية مقيدة كلوية "SB" ، وبالتالي منع التعبير الجيني المنخفض الذي يُرى عادةً لـ Pkd1 في مرحلة البلوغ وكذلك تنظيم حلقة التغذية المرتدة الثانوية المحتملة (36 ، 38). ثانيًا ، قمنا بتمييز الجين المتحور Pkd1 للفأر (Pkd1TAG) بطفرة نقطة صامتة في exon 10 ولكننا لم نقم بإدخال علامة حلقية لضمان إنتاج بروتين "من النوع البري" يعمل بكامل طاقته مع بنية وسلامة محفوظين. من BAC المعدل ، تمت تنقية جزء SBPkd1TAG بعيدًا عن جين Tsc2 وناقل BAC لمنع التداخل بواسطة جين Tsc2 ، والذي يمكن أيضًا أن يحفز النمط الظاهري الكيسي (8 ، 20 ، 28) ، وكذلك لتجنب التأثير المثبط لـ متواليات بدائية النواة (5).
تم إنتاج أربعة فئران مختلفة معدلة وراثيا SBPkd1TAG وثلاثة خطوط مستقلة باستخدام Pkd كلوي محدد(مرض الكلى المتعدد الكيسات 1)-تعزيز التعبير. اللافت للنظر بشكل خاص هو الاختراق الكامل للنمط الظاهري في هذه الفئران المعدلة وراثيا. شارك مؤسس SBPkd1TAG وخطوط الماوس العديد من السمات الفيزيولوجية المرضية المشتركة مع ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى). وتشمل هذه تطور الخراجات في القشرة ، والنخاع ، والكبيبات مع تضخم الظهارة ، والتليف الخلالي ، والتهاب الخلالي البؤري.
لأن ملف PKD(مرض تكيس الكلى)لوحظ النمط الظاهري باستمرار في جميع الفئران المؤسس المعدلة وراثيا المختلفة وتكامل الجينات المعدلة وراثيا في جينوم الفأر هو ظاهرة عشوائية ، لا يمكن أن ينتج النمط الظاهري عن تأثير موضع الكروموسومات ولكن فقط من زيادة تعبير Pkd1. في الواقع ، تم إثبات أن التعبير عن الجينات المحورة Pkd1 في جميع السطور مقيد كلويًا ، كما لوحظ سابقًا بالنسبة للجينات المحورة الأخرى التي تنظمها عناصر "SB" (36 ، 38). علاوة على ذلك ، فإن هذا التعبير المتزايد عن Pkd1 كان ناتجًا عن الجينات المحورة وليس عن طريق تنشيط Pkd1 الداخلي غير المباشر. ومن ثم ، فإن نتائجنا تقدم دليلًا واضحًا على أن اكتساب وظيفة Pkd1 الوظيفية من النوع البري يمكن أن ينتج عدة أكياس كلوية. الأهم من ذلك ، أن هذه الفئران SBPkd1TAG تشكل أول نموذج للماوس تم إنشاؤه بواسطة التعبير المفرط الوحيد لتقويم الفأر لجين PKD1 البشري.
توضح الفئران SBPkd1TAG أن Pkd1(مرض الكلى المتعدد الكيسات 1)الإفراط في التعبير هو آلية ممرضة أولية لتكوين المثانة الكلوي. الأهم من ذلك ، يبدو أن أعلى مستويات التعبير الجيني في الكلى مرتبطة بتطور وشدة النمط الظاهري. وجدنا أيضًا أن تعبير Pkd1 الزائد في تطوير النمط الظاهري SBPkd1TAG من المرجح أن يشير إلى تنشيط c-myc في الجسم الحي. يمكن تصور أن يكون هذا التنشيط مباشرًا من خلال الذيل الطرفي C متعدد البوليسيستين -1 الذي يخضع لانقسام تحلل البروتين والانتقال النووي (7). نظرًا لأنه تم إظهار التعبير الكلوي المحسن لـ c-myc في الفئران البالغة لتحفيز PKD ، فسيكون دعم c-myc كمستجيب رئيسي في مجرى النهر لمسارات إشارات Pkd1 متسقة للغاية. ارتبطت هذه النتيجة أيضًا بالنتائج السابقة التي توصلنا إليها بشأن زيادة تعبير c-myc في الكلى لجميع ADPKD البشري (العامل الوراثي المسيطرمرض تكيس الكلى)تحليلها (22). إجمالاً ، تشير هذه النتائج إلى أن c-myc هو وسيط رئيسي لـ Pkd1(مرض الكلى المتعدد الكيسات 1)تكوّن المثانة. تشير نتائجنا من نموذج اكتساب الوظيفة Pkd1 ، جنبًا إلى جنب مع عدم كفاية الفردانية لدى الفئران Pkd1 وفقدان الوظيفة ، إلى أن أي خلل في تنظيم Pkd1 يمكن أن يؤدي إلى تكون المثانة (2 ، 19 ، 23-26 ، 31 ، 40).
شديد Pkd1(مرض الكلى المتعدد الكيسات 1)عدم التوازن في الفئران الناجم عن Pkd1(مرض الكلى المتعدد الكيسات 1)تسبب الاجتثاث أو الإفراط في التعبير الجيني في ظهور مبكر وتطور سريع للخراجات الكلوية وأثر على نسبة عالية من الأنابيب. على النقيض من ذلك ، أدى اختلال توازن Pkd1 المعتدل مثل عدم كفاية الفردانية إلى تقدم أبطأ في PKD مع مزيد من الأكياس البؤرية. يمكن تفسير التطور المتناقض الظاهر لنمط ظاهري مشابه عن طريق خلل تنظيم البوليسيستين المعاكس بالنتيجة الشائعة ، أي عدم توازن نسبي في تركيز البروتين الذي يمكن أن يغير تكوين أو وظيفة معقد متعدد البروتينات النشط. مجتمعة ، تجادل نتائجنا ونتائج المحققين الآخرين بأن آلية تكوين الكيس في ADPKD (العامل الوراثي المسيطرمرض تكيس الكلى)من المحتمل أن تنشأ من ثلاث آليات ممرضة: اكتساب الوظيفة ، وفقدان الوظيفة ، وتأثيرات جرعة الجينات. تشكل الفئران SBPkd1TAG الجديدة نموذجًا قويًا لتكوين المثانة الكلوي الذي يمكن أن يوفر رؤى رئيسية في الفيزيولوجيا المرضية لـ PKD(مرض تكيس الكلى)، Pkd1(مرض الكلى المتعدد الكيسات 1)مسارات تحويل الإشارات ، والشركاء المتفاعلون. قد تؤدي دراسة هذا النموذج أيضًا إلى تطوير استراتيجيات علاجية جديدة لاستعادة توازن البروتين الطبيعي داخل مجمع Pkd1 متعدد القوالب.

المراجع
1. بلوين ، إم جي ، إتش بيوتشمين ، إيه رايت ، ميدي بايبي ، إم سوريت ، إيه. بلوب. ناكاموتو. C.-N و Ou و G. Stamatovannopoulos و M. Trudel 2000. التصحيح الجيني لمرض الخلايا المنجلية: رؤى باستخدام نماذج الفئران المعدلة وراثيًا. نات. ميد. 6: 177-182.
2. بولتر ، سي ، إس مولروي ، إس ويب ، إس فليمينغ ، ك.برندل ، وآر ساندفورد. 2001 عيوب القلب والأوعية الدموية والهيكل العظمي والكلوي في الفئران مع الاضطراب المستهدف في Pkd1(مرض الكلى المتعدد الكيسات 1)الجين. ناتل. أكاد. علوم. USA 98: 12174-12179.
3. Brasier ، JL ، و EPHenske. 1997 ، فقدانمرض تكيس الكلىتدعم منطقة (PKD1) للكروموسوم 16p13 في خلايا الكيس الكلوي نموذج فقدان الوظيفة لإمراض الكيس. J. كلين. التحقيق 99: 194-199.
4. Burn و TC و TD Connors و WRDackowski و LRPetry و TJVan Raay و JM Millholland و M. Venet و G.Miller و RM Hakim و GMLandes و KW Klinger و F. Qian و LF Onuchic و T.Watnick و GG Germino و لا دوجيت 1995 تحليل التسلسل الجينومي لالعامل الوراثي المسيطر مرض تكيس الكلى(PKD1) الجين يتنبأ بوجود تكرار غني باللوسين. همم. مول. Genet.4: 575-582.
5- تشادا ، كيه ، جي ماغرام ، كيه رافاييل ، جي راديس ، إي لاسي ، إف كوستانتيني ، 1985. تعبير محدد عن جين أجنبي -جلوبين في خلايا كرات الدم الحمراء للفئران المعدلة وراثيا. Nature 314: 377-380.
6. شوفيه ، في ، إف كيان ، إن بوتي ، واي كاي ، بي فاكديكيتاتشاروين ، إل إف أونوتشيك ، تي أتى بيتاتش ، إل جويشارنو ، أو ديفويست ، جي جي جيرمينو ، إم سي. جوبلر 2002. التعبير عن PKD1(مرض الكلى المتعدد الكيسات 1)و PKD2(مرض الكلى المتعدد الكيسات 2)النسخ والبروتينات في الجنين البشري وأثناء نمو الكلى الطبيعي. أكون. J. باتول 160: 973-983.
7.Chauvet، V.، X. Tian، H.Husson، DHGrimm، T.Wang، T.Hiesberger، P. Igarashi، AM Bennett، O. Ibraghimov-Beskrovnava، S. Somlo، and MJ Caplan، 2004. تحفز المنبهات الميكانيكية الانقسام والانتقال النووي لمحطة بوليسيستين -1 سي. J. كلين. التحقيق. 114: 1433-1443.
8. تشيدل ، جي بي إم بي ريف ، جي آر سامبسون ، ودي جي كوياتكوفسكي. التقدم الوراثي الجزيئي في التصلب الحدبي. همم. جينيت 107: 97-114. 9. الاتحاد ، EPKD1993. تحديد وتوصيف جين التصلب الجلدي على الكروموسوم 16. الخلية 75: 1305-1315.
10. الاتحاد ، EPKD1994 ، الجين 1 لمرض الكلى المتعدد الكيسات يشفر نسخة 14 كيلو بايت ويقع داخل منطقة مكررة على الكروموسوم 16. الخلية 77: 881-894.
11. كونسورتيوم IPKD1995. مرض الكلى المتعدد الكيسات: البنية الكاملة لمرض الكلى المتعدد الكيسات 1(مرض الكلى المتعدد الكيسات 1)الجين وبروتينه. الخلية 81: 289-298.
12.Couillard، M.، R. Guillaume، N. تانجي ، في داجاتي ، وم. تروديل 2002. موت الخلايا المبرمج المستحث بـ c-myc في مرض الكلى المتعدد الكيسات مستقل عن تفاعل FasL Fas. الدقة السرطان. 62: 2210-2214.
13. De Paepe، ME، and M. Trudel، 1994. الماوس المعدلة وراثيا SAD: نموذج من اعتلال كبيبات الخلايا المنجلية البشرية. الكلى Int. 46: 1337-1345.
14. Geng، L.، Y. Segal، B.Pissel، N.Deng، Y. Pei، F. Carone و HGRennke و AM Glücksmann-Kuis و MC Schneider و M. Ericsson و STReeders و J.Zhou. 1996 تحديد وتوطين البوليسيستين ، PKD1(مرض الكلى المتعدد الكيسات 1)منتج الجينات. J. كلين. التحقيق. 98: 2674-2682.
15. Gong، S.، XWYang، C. Li، and N.Heintz.2002. تعديل عالي الكفاءة للكروموسومات الاصطناعية البكتيرية (BACs) باستخدام ناقلات مكوكية جديدة تحتوي على أصل R6Ky للتكرار. الدقة الجينوم. 12 ؛ 1992-1998.
