الإمكانات العلاجية لجليكوسيدات فينيلثانويد: مراجعة منهجية
Sep 29, 2022
الملخص:
جليكوسيدات فينيلثانويد(PhGs) هي مركبات فينولية قابلة للذوبان في الماء وتوجد في العديد من النباتات الطبية. حتى يونيو 2020 ، تم عزل وتحديد أكثر من 572 PhGs. PhGs تمتلكمضادات الأكسدة,اعصاب, مضاد التهاب, مضاد للجراثيم, مضاد فيروسات, مضاد لمرض السكر, مضاد للسرطان، وخصائص مضادة للسمنة. على الرغم من هذه الفوائد الواعدة ، فشلت PhGs في تلبية تطبيقاتها العلاجية بسبب ضعف التوافر البيولوجي. يتم التحقيق في محاولات فهم مسارات التمثيل الغذائي الخاصة بهم لتحسين التوافر البيولوجي. في مقالة المراجعة هذه ، سنلخص أولاً عدد مركبات PhGs غير الدقيقة في الأدبيات. سيتم مراجعة أحدث المعلومات حول الأنشطة البيولوجية ، والعلاقات بين الهيكل والنشاط ، والآليات وخاصة التطبيقات السريرية لـ PhGs. سيتم تلخيص التوافر البيولوجي للـ PhGs وسيتم تحليل العوامل التي تؤدي إلى التوافر البيولوجي المنخفض. كما تم تلخيص التطورات الحديثة في طرق مثل المحسنات الحيوية وتكنولوجيا النانو لتحسين التوافر البيولوجي للـ PhGs. تتم أيضًا مناقشة الفجوات العلمية الحالية في PhGs في المعرفة ، مما يسلط الضوء على اتجاهات البحث في المستقبل. الكلمات الرئيسية: جليكوسيدات فينيلثانويد ؛ التوافر البيولوجي؛ أكتيوسيد. ساليدروسيد.إشيناكوسايد
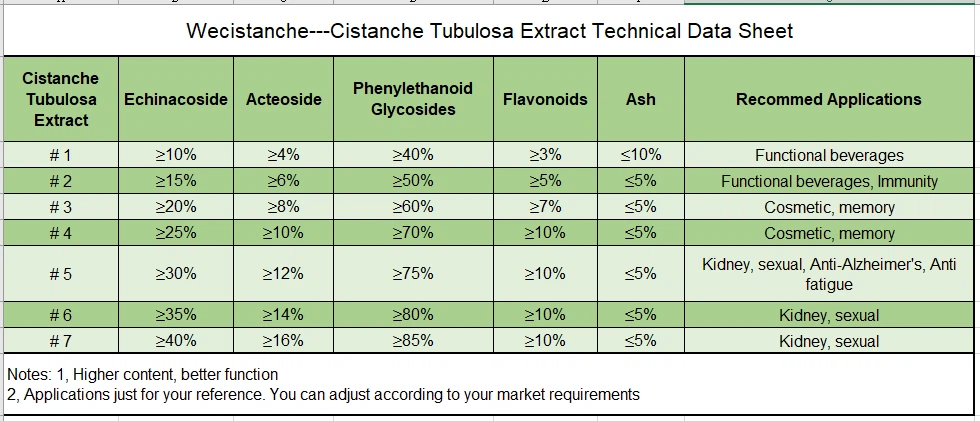
مواصفات جليكوسيدات فينيلثانويد في Cistanche Herba
مقدمة
جليكوسيدات فينيلثانويد (PhGs) هي بشكل عام مركبات فينولية قابلة للذوبان في الماء وتحدث في العديد من النباتات الطبية. تم عزل PhGs من الجذور والسيقان واللحاء والأوراق والزهور والفواكه وبذور النباتات الطبية ، وكذلك من مزارع الخلايا المعلقة وأنسجة الكالس ومزارع الجذور المشعرة. توجد أيضًا في العديد من الأطعمة النباتية مثل الزهور الصالحة للأكل والشاي. ومع ذلك ، فإن تراكماتها في كل عضو نباتي قد تختلف إلى حد كبير 1-3. تم الإبلاغ عن PhGs الرئيسية من عائلات Acanthaceae و Berberidaceae و Asteraceae و Gesneriaceae و Lamiaceae و Loganiaceae و Magnoliaceae و Oleaceae و Orobanchaceae و Plantaginaceae و Portulacaceae و Rosaceae و Scrophulariacenaceae. على سبيل المثال ، تم عزل ما مجموعه 69 و 51 و 21 و 16 درجة حموضة من Cistanche herba5 و Forsythiae fructus6 و Magnoliae officinalis7 و Houttuynia cordata8 على التوالي. يتم توزيع Acteoside (المعروف أيضًا باسم acteoside) ، وهو أحد مكونات PhGs التمثيلية ، على نطاق واسع في عائلة Lamiaceae و Plantaginaceae و Scrophulariaceae و Orobanchaceae. في عام 1994 ، لخص Jiménez و Riguera الهياكل والأنشطة البيولوجية لـ 155 PhGs المبلغ عنها قبل عام 19922. في عام 2008 ، فو وآخرون. قدم لمحة عامة عن التقدم المحرز في 190 PhGs الجديدة المعزولة من 1997 إلى 200710. تم تقديم المعلومات التفصيلية لـ 116 PhGs الجديدة التي تم تحديدها خلال 2009-2016 في 20163. في المراجعة الحالية ، قمنا بتلخيص 111 PhG 11-56 التي لم تتم مراجعتها سابقًا (1993-1997 ، 2007-2009 و 2016- موجودة) في الجدول 1 والجدول 2. آخر تم نشر PhGs الجديدة (Ginkgoside C و D) في 16 يونيو 2020. تم تحديد ما يصل إلى 572 PhGs من الطبيعة حتى يونيو 2020. يتم توزيع 572 PhGs في 21 طلبًا و 35 عائلة من المملكة النباتية (الشكل 1). وتجدر الإشارة إلى أن بعض PhGs التي تم تحديدها لم يتم نشرها باللغة الإنجليزية. وبالتالي ، يجب أن يكون العدد الفعلي المحدد أكثر من 572. بشكل عام ، يتكون الهيكل الأساسي لـ PhGs من وحدة hydroxyphenylethyl مثل aglycone والتي يتم ربطها بجزء من السكر في الغالب a -D-glucopyranose من خلال رابطة جليكوسيدية عند C {{41 }} موقع. في معظم الحالات ، يتم أسترة جزء الجلوكوز بمشتق حمض الهيدروكسيسيناميك مثل حمض الكافيك وحمض الكوماريك وحمض سيناميك وحمض الفيروليك. يمكن أيضًا ربط رامنوز ، وزيلوز ، وأرابينوز ، وألوز ، وجالاكتوز ، وأبيوز ، من بين أمور أخرى ، ببقايا الجلوكوز (الشكل 2 ، الجدول 1 و 2). تنوع شقوق السكر و hydroxyphenylethyl يجعل التباين الوافر لـ PhGs. بشكل عام ، يتراوح عدد السكريات من واحد إلى ثلاثة. ومع ذلك ، توجد أيضًا بقايا أربعة سكر وخمسة سكر في بعض الأحيان. وفقًا لعدد السكريات المرتبطة بشقوق هيدروكسي فينيل إيثيل ، يمكن تصنيف PhGs إلى PhGs أحادي السكريات ، PhGs غير السكاريد ، PhGs trisaccharidic ، PhGs tetrasaccharidic ، و pentasaccharidic PhGs4. حتى الآن ، تم الإبلاغ عن 10 دكاترة رباعي السكاريد ، وهي ماغنولوسيدات C57 ، و ballotetroside58 ، و trichosanthoside B59 ، و marruboside60 ، و velutinosides I61 ، و velutinosides II61 ، و lunariifolioside62 ، و raduloside63 ، و barlerinoside64 ، و poliumoside B65. تم الإبلاغ عن PhGs خماسي واحد فقط يسمى yulanoside A من M.salicifolia في 201566
معظم PhGs المنقى هي مساحيق غير متبلورة بيضاء أو برتقالية أو صفراء ذات قطبية عالية. إنها قابلة للذوبان في المذيبات القطبية ولكنها غير قابلة للذوبان في المذيبات العضوية غير القطبية. نظرًا لخصائص امتصاص الأشعة فوق البنفسجية القوية (UV) في PhGs ، فمن السهل مراقبة هذه المركبات بواسطة مقياس الطيف الضوئي بالأشعة فوق البنفسجية. يمكن أيضًا استخدام أطياف الأشعة فوق البنفسجية المحددة لكل PhGs كمؤشر لاستنتاج البنية. على سبيل المثال ، قمم امتصاص الأشعة فوق البنفسجية لأكتيوسيد وإيزو أكتيوسيد هي 232 ، 246 ، 289 ، 332 نانومتر ، و 232 ، 246 ، 286 ، 328 نانومتر ، على التوالي. وهذا منإشنكوسايدهي 236 ، 288 ، 330 نانومتر 69. أظهرت PhGs والمستخلصات الغنية بـ PhGs فوائد مختلفة ، مثل النشاط المضاد للأكسدة ، وتأثير الحماية العصبية ، والنشاط المضاد للالتهابات ، والنشاط المضاد للبكتيريا ، والنشاط المضاد للفيروسات ، والنشاط المضاد لمرض السكري ، والنشاط المضاد للسرطان ، والنشاط المضاد للسمنة 3 ، 9. الشكل 3 يوضح عدد الأوراق والأوقات التي تم الاستشهاد بها للأوراق المفهرسة في Web of Science المتعلقة بـ "PhGs" ، مما يوضح زيادة كبيرة في النشر في هذا المجال. على الرغم من أنه تم عزل وتحديد أكثر من 572 PhGs ، إلا أن القليل منها فقط تمت دراسته على نطاق واسع. على سبيل المثال ، عدد الأوراق على salidroside ، Acteoside ،إشنكوسايد، forsythoside و isoActeoside هي 1746 و 1258 و 538 و 370 و 230 على التوالي. وعدد الاقتباسات من الأوراق حول Acteoside ، salidroside ،إشنكوسايدو forsythoside و isoActeoside هي 19356 و 14352 و 6468 و 3234 و 4 0 98 على التوالي. PhGs الأخرى لديها أقل من 100 ورقة منشورة. عدد الأوراق المنشورة وعدد الاقتباسات من أوراق PhGs محددة موضحة أيضًا في الشكل 3. على الرغم من العديد من الأنشطة البيولوجية الواعدة ، فشلت PhGs في تلبية التطبيقات العلاجية بسبب ضعف التوافر الحيوي الفموي. تم العثور على التوافر البيولوجي لـ Acteoside بنسبة 0.12 في المائة في الفئران بعد إعطاء Acteoside بجرعات 100 مجم / كجم عن طريق الفم (po) و 3 مجم / كجم من الحقن في الوريد (iv) 70 ، ولكن التوافر البيولوجي للكلاب vActeosidein كان حوالي 4 في المائة بعد إعطاء vActeosidewas عند 40 مجم / كجم من الإعطاء داخل المعدة (ig) و 5 مجم / كجم من الوريد. التوافر البيولوجي لـإشنكوسايد, and angoroside C in rats at the dose of 100 mg/kg i.g. and 5 mg/kg i.v., was reported to be 0.83%72 and 2.1%73 , respectively. The bioavailability of forsythiaside (100 mg/kg p.o. and 5 mg/kg i.v.) and poliumoside (200 mg/kg p.o. and 10 mg/kg i.v.) in rats was 0.5%74 and 0.69%75 , respectively. Feng et al. compared the pharmacokinetic and bioavailability characteristics of savaside A, vActeoside and isovActeosidein rats after the compounds were given at the dosages of 1000 mg/kg p.o. and 5 mg/kg i.v.. The bioavailability order of the three PhGs appears to be vActeoside> isovActeoside>سافاسايد A76. قام Zhang et al بالتحقيق في الحرائك الدوائية لأربعة PhGs (vActeoside isovActeoside martynoside ، و crenatoside) بعد تناول 1 0. 0 جم عشب Acanthus ilicifolius الخام / كجم للفئران. على الرغم من أن الأربعة PhGs تشترك في هياكل جزيئية متشابهة ، إلا أنها أظهرت فترات نصف عمر مختلفة للتخلص (T1 / 2) ، ومناطق مختلفة تحت المنحنيات (AUC 0 - t) ، تتراوح من 3.4 إلى 9.0 ساعات ، و 1826.3 إلى 23.6 ug / L × h على التوالي 77. قد تؤثر الجرعات المختلفة والأنماط الإدارية على التوافر البيولوجي لـ PhGs. ومع ذلك، هناك استثناء واحد. تم الإبلاغ عن التوافر البيولوجي للساليدروسيد بنسبة 51.97 في المائة. أما بالنسبة للأسباب التي جعلت التوافر البيولوجي للساليدروسيد أعلى بكثير من غيره من مواد PhGs ، فقد يُعزى ذلك إلى هيكله البسيط نسبيًا (الشكل 2). ينتمي Salidroside إلى PhGs أحادي السكاريد المكون من فينيل إيثانول وسكروز ، وقد سمحت القطبية الكبيرة نسبيًا بإفرازه بسهولة من البول دون عمليات التمثيل الغذائي المعقدة. قد يؤدي الامتصاص العالي للساليدروسيد أيضًا إلى التوافر البيولوجي العالي الواضح له مقارنةً بغيره من مواد PhGs (القسم 5.1). تم تطبيق العديد من الأساليب مثل المُحسنات الحيوية ، وتغليف سيكلودكسترين ، ودرجة الحموضة الدهنية ، والجسيمات النانوية ، ومركب الفسفوليبيد لتحسين التوافر الحيوي للـ PhGs. كان هناك عدد من المراجعات على PhGs منذ التسعينيات. في وقت مبكر من عام 1994 ، قام Jiménez و Riguera بمراجعة العزل والتنقية والتركيب والنشاط البيولوجي لـ PhGs2. بان وآخرون. سلط الضوء على الأنشطة الدوائية من PhGs الطبيعية في 200379. فو وآخرون. لخص الكيمياء النباتية والنشاط الحيوي لمواد PhGs في عام 200810. Radev et al. نشرت مراجعة مصغرة عن التأثيرات الدوائية للتعليمات الدوائية في 201080. لخص Xue و Yang التطورات في كيمياء النبات وعلم العقاقير والحركية الدوائية في PhGs في عام 20163. Alipieva et al. استعرض التخليق الحيوي والأهمية الدوائية لـ vActeoside الأكثر شيوعًا في فينيل إيثانويد جليكوسيد في عام 2014. ليو وآخرون. تعمم التوزيع وطرق الاستخراج وسوء الحرائك الدوائية والاستخدامات العلاجيةإشنكوسايدفي 201881. تاو وآخرون. قدم ملخصًا تفصيليًا للدراسات الكيميائية والدوائية والسمية والسريرية لمختلف أنواع رهوديولا مع ساليدروسايد كمكونات كيميائية مميزة في عام 201982. ومع ذلك ، لا توجد مراجعات شاملة فيما يتعلق بالاستقرار ، والتحول البيولوجي ، والتطبيق السريري والتوافر البيولوجي لـ PhGs. ستلخص هذه المراجعة أحدث المعلومات حول الكيمياء ، وعلم العقاقير ، والاستقرار ، والتطبيق السريري ، والحرائك الدوائية ، والمستقلبات ، والتحول الأحيائي لـ PhGs. كما سيتم تلخيص التطورات الحديثة في طرق مثل المحسنات الحيوية وتقنية النانو لتحسين التوافر البيولوجي للـ PhGs. تتم أيضًا مناقشة الفجوات العلمية الحالية في PhGs في المعرفة ، مما يسلط الضوء على اتجاهات البحث في المستقبل
2. علم الأدوية من PhGs
تم الإبلاغ عن PhGs لديها العديد من الأنشطة الحيوية في نماذج الخلية والحيوانية. هنا ، يتم تلخيص الفوائد الصحية المحتملة من PhGs ، ويتم تسليط الضوء على العلاقة بين الهيكل والنشاط وآليات علم الصيدلة PhGs.
2.1 نشاط الكسح المضاد للأكسدة والجذور الحرةجليكوسيدات فينيلثانويد
أظهرت العديد من مكونات PhGs والمستخلصات الغنية بـ PhGs نشاطًا قويًا مضادًا للأكسدة. تم عزل اثنين من PhGs جديدة تسمى macrophylloside E و macrophylloside F ، مع ثمانية PhGs معروفة (jionoside C و forsythoside B و alyssonoside و Acteoside و isoActeoside و martinoside و isomartinoside و leucosceptoside) من Callicarpa macrophylla. أظهرت جميع مركبات PhG العشرة تأثيرًا مضادًا للأكسدة مرتفعًا إلى متوسطًا مع IC5 0 من 2.72 إلى 38.65 ميكرومتر في اختبار DPPH. يمكن للأكتيوسيد المعزول من لسان الحمل الكبير أن يزيل بشكل كبير كل من جذور DPPH (IC ، 11.27 ميكرومتر) وجذور الأكسيد الفائق (IC50 ، 1.51 ميكرومتر). يمكن أن يمنع Acteoside أيضًا إنتاج أكسيد النيتريك الناجم عن عديد السكاريد الدهني في RAW264.7 الضامة (IC50 ، 75.0 ميكرومتر) 83. أظهرت سبعة PhGs (plantalide A ، vActeoside plantamajoside ، martynoside ، healoside B ، desrhamnosyl isovActeosidica) المكتشف من P. نشاط الكسح مع قيم IC التي تتراوح من 22.9 إلى 88.5 ميكرومتر. بينما أظهر 22 مركبًا آخر من P. asiatica نشاطًا ضعيفًا لمضادات الأكسدة 85. بالإضافة إلى ذلك ، تم إثبات أن VActeosidevActeosidean و salidroside هما عنصران رئيسيان من PhG يساهمان في القدرات المضادة للأكسدة الكبيرة لزهور Osmanthus fragrans. تم العثور على جميع PhGs التسعة (ماغنولوسيدات Ia و Ib و Ic و IIa و IIb و IIIa و Iva و Va و crassifolioside) من M. officinalis إمكانات قوية لكسح الجذور الحرة مع IC50 تتراوح من 11.79 إلى 20.99 ميكرومتر ، وماغنولوسيد Ia (IC50 ، 11.79 ميكرومتر) كان الأقوى 86. كانت قدرة الكسح الجذري لـ DPPH لـ crassifolioside (IC50 ، 21.38 ميكرومتر) ، ماغنولوسيد IIa (22.94 ميكرومتر) ، وماغنولوسيد IIb (24.62 ميكرومتر) أضعف من ماجنولوسيد Ia (11.79 ميكرومتر) ، ماغنولوسيد Ic (12.99 ميكرومتر) (ماغنولوسيد Ic (12.99 ميكرومتر) (ماغنولوسيد Ic) 16.23 ميكرومتر) ، وماغنولوسيد فيرجينيا (20.99 ميكرومتر). كما يمكننا أن نرى من هياكل هذه المركبات ، احتوى كراسيفوليوسيد ، ماغنولوسيد IIa ، وماغنولوسيد IIb على ثلاثة سكريات بينما احتوى ماغنولوسيد Ia ، و magnoloside Ic ، و magnoloside Ib ، و magnoloside Va على اثنين من السكريات. يعني المزيد من السكريات عائقًا فائقًا أكبر في المركبات ويمنعها من الاقتراب بسهولة من الجذور الحرة ، مما يؤدي في النهاية إلى ضعف قدرة الكسح الجذري لـ DPPH. بالإضافة إلى ذلك ، مقارنة مع السبعة الأخرى PhGs ، أظهر Magnoloside IIIa (32.18 ميكرومتر) و Magnoloside IV (35.17 ميكرومتر) مع مجموعتين فينوليتين متجاورتين فقط في جانب واحد نشاطًا ضعيفًا 86. علاوة على ذلك ، يمكن زيادة اقتران مستوى حلقة البنزين في PhGs من خلال هياكل استر غير مشبعة مقترنة وتسمح بإلغاء تحديد موقع الإلكترون لتثبيط الجذور الحرة 86.
2.2 التأثير الوقائي العصبي لجليكوسيدات فينيليثانويد
أكتوسيدو salidroside وإشنكوسايدعرضت أنشطة مضادات الأكسدة والوقاية العصبية في بيروكسيد الهيدروجين الناجم عن موت الخلايا المبرمج في خلايا PC12 عبر المسار ذي الصلة بالعامل النووي الكريات الحمر 2- 87. CaleolariosideB و paraboside B و paraboside II المعزولة من Paraboea martinii عملت على حماية خلايا PC12 بشكل فعال من الضرر الناجم عن H2O 2- عن طريق تنظيم H O -1 88. يُعتقد أن ببتيد الأميلويد (أ) هو سبب رئيسي لمرض الزهايمر 89. إجمالي PhGs المستخلص من C. Herba بتركيزات 5 و 25 و 50 ميكروغرام / مل زاد من الصلاحية وقلل من إطلاق LDH و MDA بواسطة خلايا PC12 المصابة بـ A 1‑4290. تم إثبات Torenoside B و Savatiside savatiside A لتحسين نشاط إنزيم GSH Px و SOD ، وتقليل محتوى MDA و ROS ، وتقليل تركيز Ca2 زائد داخل الخلايا وتعبير Calnexin في خلايا SH SY5Y المستحثة 25-35. يمتلك VActeoside salidroside و PhGs من C. Herba إمكانات وقائية كبيرة ضد الإجهاد التأكسدي الناجم عن A 92 ، 93. علم الأمراض المميز في مرض باركنسون هو تنكس الخلايا العصبية الدوبامين في المادة السوداء بارس كومباكتا 94. يمكن للكامبنيويد وتوبولوسيد ب حماية الخلايا العصبية من موت الخلايا المبرمج الناجم عن 1- الميثيل -4- فينيل بيريدينيوم في الجسم الحي 95 ، 96. يمتلك VActeoside قيمة علاجية محتملة ضد PD من خلال تخفيف الإجهاد التأكسدي وتفعيل مسار إشارات Nrf2 / ARE. تم إعطاء SAMP8 الفئران ، نموذج لمرض الزهايمر ، بواسطة PhGs المستخرجة من C. Herba يوميًا داخل الصفاق عند 25 أو 50 أو 100 مجم / كجم / يوم لمدة 30 يومًا. تم العثور على PhGs لتحسين العجز المعرفي في الفئران SAMP8 عن طريق تحسين التشابك العصبي واللدونة التشابكية. تم الإبلاغ عن أن متوسط عمر التهاب caenorhabditis elegans قد تم تمديده بنسبة 13.64 في المائة و 15.82 في المائة بعد العلاج بـ 200 ميكرومتر و 300 ميكرومتر ECH ، على التوالي. كان التأثير الوقائي لـ ECH على السمية المستحثة من A في C. elegans مساويًا تقريبًا لتأثير ginkgolide A ، وهو عامل معروف له تأثيرات إيجابية لـ AD99. ليو وآخرون. قام بتجميع ثمانية مشتقات PhGs على أساس الكالسيولاريوزيد A ، ودرس تأثيرها العصبي في خلايا PC12. أظهرت النتائج أن سبعة مركبات يمكن أن تحمي من تلف الخلايا أو الموت من ضرر الجذور الحرة باستثناء التناظرية المستبدلة بالكلورو. أشارت العلاقة بين البنية والنشاط إلى أن جزء الكاتيكول قد لا يحتكر النشاط الحيوي ولكن ربما يمكن أن يلعب دورًا مهمًا في الحماية العصبية ويبدو أن جزء الجلوكوز غير مهم للحماية العصبية. كانت النتائج متسقة مع النشاط البنيوي الأخير لنظير حمض الفينيثيل إستر 101 ، 102

انقر هنا لمعرفة المزيد من المعلومات حول
كيف تأخذ القسطرة تأثيرًا على صحة الإنسان
2.3 التأثير الوقائي للكبد من جليكوسيدات فينيليثانويد
أكتوسيد, إشنكوسايدو tubuloside B و cistanoside A و 2- acetylacteosid تقدم تأثيرات كبدية عبر آليات متعددة بما في ذلك تعزيز نظام الدفاع المضاد للأكسدة ، وإزالة الجذور الحرة ، ومنع التحول الحيوي للسيتوكروم P450. Leucoseceptoside A و crenatoside و martynoside و 3- O-methylcrenatoside المستخرج من Incarvillea Compacta التخفيف من CCl 4- تسبب في السمية الكبدية عن طريق تعزيز نشاط ديسموتاز الفائق ، وتقليل ROS داخل الخلايا ومحتوى malondialdeatingdeF وكذلك مسار κ104. 14 تم تقييم أربعة عشر PhGs معزولة من Forsythia suspensa لتأثيراتها الواقية للكبد على تلف خلايا HepG2 الناجم عن APAP. لقد وجد أن فورسيثوسيد N ، فورسيثوسيد O ، فورسيثينسايد أ وفورسيثينسايد ب تمارس أنشطة كبدية كبيرة مع معدلات بقاء الخلية من 52.48 في المائة إلى 67.15 في المائة ، 67.61 في المائة ، و 64.88 في المائة بتركيز 10 ميكرومتر ، على التوالي. يمكن للسيستانوسيد أ (125 و 250 و 500 ملغم / كغم / يوم) أن يخفف من السمية الكبدية التي يسببها الإيثانول في الفئران عن طريق تحسين أنشطة إنزيمات استقلاب الطاقة (Ca2 plus -Mg2 plus -ATPase و ATPase و Na plus -K plus -ATPase) ، والإنزيمات المضادة للأكسدة في الميتوكوندريا (SOD ، GST و CAT) ، ونظام الدفاع المضاد للأكسدة 105. إلى جانب ذلك ، قام cistanoside A (100 ، 75 ، 50 ، 25 ميكروغرام / مل) بقمع موت الخلايا المبرمج للخلايا الكبدية عن طريق زيادة تعبير Bcl -2 وقمع cfos105.إشيناكوسايد(6 0 مجم / كجم ، IP) يمكن أن تحمي بشكل كبير من إصابة الكبد الحادة التي يسببها LPS و D-galactosamine في الفئران بسبب أنشطتها المضادة للاستماتة والمضادة للالتهابات 106. تم تقييم PhGs من C. يمكن لتركيزات 0.33 ، 1. 00 ، 3. 00 ملغم / مل من PhGs أن تحسن قابلية خلايا HepG2 للحياة إلى ما يقرب من 10 بالمائة و 22 بالمائة و 35 بالمائة على التوالي. بعد تناوله عن طريق الفم مع PhGs عند 200 أو 600 أو 1800 ملغم / كغم لمدة 31 يومًا متتاليًا ، أظهرت الفئران ICR المصابة بإصابة الكبد الناجمة عن الكحول مؤشرات كبدية محسّنة (ديسموتاز الفائق ، الجلوتاثيون Stransferase ، الجلوتاثيون ، الجلوتاثيون بيروكسيديز ، مالونديالديهايد وثلاثي الجليسريد). أشارت العلاقة بين التركيب والنشاط إلى أن جزء الكاتيكول الموجود على درجة حرارة الجسم كان مهمًا للنشاط الوقائي للكبد 108. Acteoside (IC50 ، 4.6 ميكرومتر) ، 2ʹ-acetylActeoside (4.8 ميكرومتر) ، isoActeoside (5.3 ميكرومتر) ، توبولوسيد A (8.6 ميكرومتر) وإشنكوسايد (10.2 μM) inhibited D-GalN-induced death of hepatocytes109 . Acteoside (IC50, 4.6 μM) showed significantly stronger activity than kankanose (>100 μM), and echinacoside (10.2 μM) showed significantly stronger activity than cistanoside F (>100 ميكرومتر) ، مما يشير إلى أن aglycone كانت مجموعة مهمة للنشاط 109. نظرًا لأن نشاط isovActeoside (5.3 ميكرومتر) كان أعلى من kankanoside G (14.8 ميكرومتر) ، يمكن استنتاج أن aglycone مع مجموعة هيدروكسي 4- أظهر نشاطًا أضعف من ذلك الذي يحتوي على 3 ، 4- مجموعة ثنائي هيدروكسي 109. أظهر الجزء 8- O - - D-glucopyranosyl مع مجموعة 6ʹ-O-caffeol (Tubuloside B ، 14.6 ميكرومتر) نشاطًا أضعف من ذلك مع مجموعة 4ʹ-O-caffeoyl (2ʹ-acetylvActeoside 4.8 ميكرومتر) 109 . إن إدخال 6- O - - D-glucopyranosyl (echinacoside < vActeoside وشق 2ʹ-O-acetyl (2ʹ-acetylvActeosidevActeoside يمكن أن يقلل من الحماية

2.4 نشاط مضاد للسرطان من جليكوسيدات فينيلثانويد
في دراسة حديثة ،إشنكوسايدتم الإبلاغ عن امتلاك أنشطة مضادة للتكاثر (20 ميكروغرام / مل ، 9.57 في المائة ؛ 50 ميكروغرام / مل ، 26.67 في المائة ؛ 100 ميكروغرام / مل ، 37.20 في المائة) على خلايا HepG2 عن طريق تعطيل مسار AKT وتقليل تعبير TREM2. أكتوسيد ،إشنكوسايد، cistantubuloside A ، cistanoside A ، و 2´- acetylActeoside منع انتشار خط خلايا سرطان الجلد الميلانيني KML مع معدل تثبيط يتراوح من 33 بالمائة إلى 93 بالمائة 111. المعالجة المسبقة باستخدام 5 و 1 0 و 20 و 40 و 50 ميكرومتر من ساليدروسايد لمدة 48 ساعة يمكن أن تمنع انتشار خلايا MCF لسرطان الثدي البشري -7 إلى ما يقرب من 70 بالمائة و 60 بالمائة و 55 بالمائة و 45 بالمائة و 30 في المائة على التوالي. قد تكون الآلية مرتبطة بزيادة نشاط caspase ، والتنظيم المنخفض لتعبير Bcl -2 ، والتنظيم الأعلى لتعبير Bax. علاوة على ذلك ، أدى علاج الساليدروسايد إلى تثبيط نمو الورم في نموذج ورم طعم أجنبي. مقارنة بمجموعة التحكم ، بعد العلاج بالساليدروزيد (50 مجم / كجم من وزن الجسم) في أيام بديلة لمدة 3 أسابيع ، انخفض وزن وحجم الورم بمقدار 0.7 جم و 300 مم 3 على التوالي. تم الإبلاغ عن أن الساليدروسيد يمتلك نشاطًا مضادًا للورم ضد ورم ويلمز 113 ، وسرطان الثدي 114 ، وسرطان المبيض 115 ، وسرطان المعدة 116 ، وسرطان الجلد 117 ، وسرطان الخلايا الكلوية 118 وسرطان القولون والمستقيم. لي وآخرون. التحقيق في تأثير مستخلصات PhGs من C. tubulosa (CTPG) على تثبيط نمو خلايا الورم الميلانيني (B 16- F10). في المختبر ، أدى 100 ميكروغرام / مل من CTPG لمدة 48 ساعة أو 200 ميكروغرام / مل من CTPG لمدة 72 ساعة إلى تثبيط معدلات نمو خلية B 16- F10 إلى أعلى من 60 بالمائة و 90 بالمائة على التوالي. يمكن لـ CTPG زيادة تنظيم تعبيرات BAX ، وخفض تنظيم تعبيرات BCL -2 ، وزيادة توليد ROS ، وتقليل إمكانات غشاء الميتوكوندريا في المختبر. علاوة على ذلك ، فإن إعطاء 400 مجم / كجم من CTPG تحت الجلد في الفئران كل يومين لمدة تصل إلى 15 يومًا استمر في بقاء الفئران على قيد الحياة من 8.3 بالمائة إلى 41.7 بالمائة 120. يمكن أن يمنع Acteoside من Pedicularis striata نمو الخلايا السرطانية ودورة الخلية في طور G2 / M ، ويحفز موت الخلايا المبرمج ويثبط نشاط التيلوميراز ويقلل من طول التيلومير. وتجدر الإشارة إلى أن ليس كل PhGs تحمل خصائص مضادة للسرطان. على سبيل المثال ، Kirmizibekmez et al. اختبرت النشاط السام للخلايا لأربعة من حامض الفطر (لسان الحمل D ، كالسيولاريوزيد D ، نيوكالسيولاريوزيد D و lugrandoside) ضد سلسلة سلالات الخلايا السرطانية ، وهي SH-SY5Y ، T98G ، A375 ، HT29 ، MCF -7 ، PC3. لم تظهر جميع المركبات الأربعة أي سمية ضد خطوط الخلايا السرطانية الستة بتركيز 1-50 ميكرومتر 122. أثبت عدد من العلاقات بين البنية والنشاط أن مجموعة حمض الكافيك ومجموعة الكاتيكول ضرورية للتسمم الخلوي للـ PhGs. يلعب عدد شقوق الأسيتيل وموقعها في الحلقات الأليفاتية أيضًا دورًا مهمًا في الأنشطة المضادة للتكاثر لـ PhGs 123-125. كان النشاط المضاد للتكاثر من Acteoside ضعف نشاط Acteosideإشنكوسايدوكاليسولاريوزيد. يشير النشاط السام للخلايا المماثل لـ calceorioside A و vActeosides إلى أن استبدال rhamnose لا يؤثر على النشاط السام للخلايا لـ PhGs126. مثبط VActeoside حوالي 23 في المائة - 30 في المائة من نشاط تكاثر الخلايا السرطانية ، وهو ضعف ما يقرب منإشنكوسايد(10 في المائة - 18 في المائة) ، كالسيولاريوزيد أ (13 في المائة - 18 في المائة) ، وكالسيولاريوزيد ب (5 في المائة - 15 في المائة). قد يكون النشاط المضاد للتكاثر الأعلى مرتبطًا بوحدة -Rha- (1 → 3) - Glc disaccharide ووظيفة caffeoyl 4- في vActeoside. أشارت العلاقات بين التركيب والسمية الخلوية بين 14 مركبًا من مركبات PhGs إلى أنه كلما قل عدد وحدات السكر لديهم ، زادت الأنشطة الأقوى لديهم. علاوة على ذلك ، لا يؤثر موضع حمض الفينول على النشاط. إلى جانب ذلك ، فإن مثيلة مجموعات الهيدروكسيل الفينولية لها تأثير سلبي على النشاط 128.
2.5 النشاط المضاد للالتهابات من جليكوسيدات فينيلثانويد
غالبًا ما يرتبط النشاط المضاد للالتهابات لـ PhGs بقمع مسارات MAPK و NF-B و JAKSTATs وتفعيل مسار Nrf2. وو وآخرون. أكد أن PhGs (Acteoside و parvifloroside A و syringalide A و 3 ′ - - L-rhanmnopyranoside و forsythoside B و poliumoside و alyssonoside) من C. kwangtungensis وفرت الحماية ضد الاستجابة الالتهابية التي يسببها LPS في RAW 264.7 الضامة / الضامة التنشيطية Nrf2 / HO -1 مسار الإشارات 130.إشيناكوسايد attenuated LPS-induced inflammation in rat intestine epithelial cells by suppressing the mTOR/STAT3 pathway131 . Acteoside can inhibit the release of β-hexosaminidase, arachidonic acid and histamine in RBL-2H3 cells through inhibiting MAPK and JNK pathways and Ca2+ independent phospholipase132-134 . Acteoside (30, or 60 mg/kg) was shown to decrease inflammatory response against LPS-induced acute lung injury in mice by inhibiting NF-κB signaling pathway135. Gao et al. investigated the anti-inflammatory effects of vActeoside isovActeoside torenoside B and savaside A and found that isovActeoside(80 μM), possessed the strongest activity on inhibiting the expression of iNOS and COX-2 136. IsovActeosideexerts anti-inflammatory via modifying NF-κB and MAPK pathways136 . Forsythiaside A was reported to have protective potential on LPS-induced inflammation in BV2 microglia cells and primary microglia cells via increasing Nrf2 and HO-1 levels and suppressing NF-κB pathway137 . Forsythiaside A could attenuate inflammation in acute liver injury animals by activating Nrf2 and inhibiting NF-κB pathway138 . PhGs from Phlomis younghusbandii exerted anti-inflammatory properties on acute hypobaric hypoxia-stimulated HACE in rats by rehabilitating the oxidative stress levels and inhibiting the expression of pro-inflammatory cytokines regulated by the NF-κB signaling pathways139 . The anti-inflammatory activity of seven PhGs on inhibiting NO production showed that leucosceptoside A (IC50, 9.0 μM ), lipedoside A-I (11.6 μM ), vActeoside(12.8 μM ), isovActeoside(13.7 μM ), and campneoside II (22.1 μM ) possessed stronger activity than martynoside (>100.0 μM) and angoroside C (>1 0 0.0 ميكرومتر). يشير هذا إلى أن مجموعتي هيدروكسيد المتجاورتين في PhGs قد تكون مرتبطة بنشاطهما المضاد للالتهاب 140. يانغ وآخرون. أظهر أن PhGs مع مجموعتين من السكر تمتلك أنشطة أضعف من غيرها 141.

2.6 مضاد للفيروسات ، نشاط مضاد للجراثيم ومضاد للأوالي من PhGs
اثنين من PhGs جديدة ، Llippiarubelloside A و lippiarubelloside B ، مع أربعة PhGs معروفة ، Acteoside forsythoside A ، والجانب المنصة ، معزولين عن Lippia rubella ، يمكن أن يثبط بشدة نمو المستخفيات المستخفية بتركيزات {0}} ميكروغرام / مل 32. أظهر إجمالي مستخلص PhGs من Monochasma savatieri تأثيرات كبيرة مضادة للبكتيريا بتركيز يتراوح من 0. 0 625 إلى 16 مجم / مل 142. أظهر VeActeosidend forsythoside B أنشطة مضادة للجراثيم عالية ضد خمس سلالات من المكورات العنقودية الذهبية من 64 جم / لتر إلى 256 جم / لتر ، والتي كانت مماثلة لتلك الموجودة في النورفلوكساسين. عند استخدامه بمفرده بجرعة 2 0 0 ميكروغرام / مل ، فإن نشاط veActeosidead المثبط ضد العزلة الإكلينيكية للإشريكية. القولونية والمكورات العنقودية. المذهبة. ومع ذلك ، أظهرت الإدارة المشتركة لـ veActeosidend gentamicin تأثيرًا تآزريًا ضد E. coli و S. aureus .. وهذا يشير إلى أنه يجب استخدام veActeoside للتغلب على المقاومة البكتيرية التي تسببها الأدوية التقليدية. Isoforsythiaside و forsythiaside هي المكونات الرئيسية المضادة للبكتيريا في فورسيثيا المعلق ، والتي غالبا ما تستخدم لعلاج العدوى في الجهاز التنفسي العلوي. يمنع Isoforsythiaside و forsythiaside نمو E. coli و P. aeruginosa و S. aureus 145، 146. بالإضافة إلى ذلك ، أظهر forsythoside H تأثيرات مثبطة قوية ضد B. vulgare و B. dysenteriae و M. pneumoniae و A. bacillus. نشاط VeActeosideas المضاد للفيروسات في النشاط المختبر ومضاد الأنفلونزا في الجسم الحي. والآلية المضادة للفيروسات الخاصة بـ veActeosideas المتعلقة بتنشيط ERK وتعزيز IFN- إنتاج 148. أظهر فورسيثياسايد وكاليسولاريوزيد ب إمكانات كبيرة مضادة للفيروسات على الفيروس المخلوي التنفسي في المختبر 149. يثبط فورسيثياسيد عدوى فيروس التهاب القصبات الهوائية المعدية 15 0. Taraffinisoside A ، وهو مركب PhGs جديد معزول من Tarphochlamys affinis ، أظهر نشاطًا مضادًا لالتهاب الكبد B بقيم IC5 0 0.50 و 0.93 ملي مولار ضد مستضد التهاب الكبد B السطحي والتهاب الكبد B ، على التوالي. أدى Forsythoside A من F.uspensa إلى خفض التتر الفيروسي لأنواع فرعية من فيروس الأنفلونزا في مزارع الخلايا بجرعة 160 ميكرومتر. زاد Forsythoside A أيضًا من معدل بقاء الفئران في نموذج عدوى فيروس الأنفلونزا عند 5 أو 10 ميكروغرام / غرام من وزن الجسم 151. Hu et al. قام بتقييم تأثيرات الفيروس المضاد للإنفلونزا من PhGs في المختبر وفي الجسم الحي. يمكن أن تمنع PhGs عند 0.5 مجم / مل من عدوى نوع فيروس الأنفلونزا A H1N1 لخلايا الكلى مادين داربي في المختبر. خفضت PhGs عند 300 و 900 مغ / كغ بشكل كبير مؤشر رئة الفأر (p 0.05) ، وخففت من الفتك والأعراض السريرية التي تسببها الإنفلونزا ، ووقت بقاء الفأر لفترات طويلة (p 0.05). قد تكون الآلية متعلقة بأعلى تنظيم IFN - 152. تم الإبلاغ عن وجود نشاط مضاد للبكتيريا يحتوي على فاكتوزيد ضد المثقبيات البروسية الروديسية ، الليشمانية الطفولية ، L. donovani ، و L. amazonensis 153 ، 154. أظهر VeActeoside وجود EC50 قدره 19 ميكرومتر ضد L. promastigotes وهو مثبط للأرجيناز التنافسي مع Ki من 0.7 ميكرومتر 155. من بين سبعة PhGs المستخرجة من Tecoma mollis ، أظهر luteoside B و luteoside A أقوى نشاط مضاد للسماني مع قيم IC50 البالغة 6.7 و 15.1 ميكروغرام / مل على التوالي. يتوفر القليل من المعلومات حول العلاقة بين التركيب والنشاط لـ PhGs في أنشطتها المضادة للفيروسات والبكتيريا. كيرياكبولو وآخرون. اكتشف أن الساميوسيد أكثر نشاطًا من veActeosid ضد أربع سلالات من البكتيريا ، مما يشير إلى أن جزءًا إضافيًا من السكر (apiose) عند C -4 من rhamnose يمكن أن يساهم في النشاط المضاد للبكتيريا 157. على الرغم من أن فلوسيد C و forsythoside B لهما هيكل مماثل ، فإن الفلوسيد C بالكاد يثبط السلالات المقاومة للأدوية المتعددة من S. aureus. يشير هذا إلى أن إدخال الجليكوسيد الثالث (رامنوز) إلى فورسيثوسيد ب قد يتسبب في عدم نشاطه.
2.7 النشاط المضاد لمرض السكر من PhGs
أظهرت مادة PhGs جديدة تسمى flavaioside من Scrophularia flava أنشطة مثبطة للجلوكوزيداز بقيمة IC50 تبلغ 6.50 ميكروغرام / مل. بالإضافة إلى ذلك ، يمتلك الفلافايوسيد نشاطًا مثبطًا كبيرًا على إنزيم الجلوكوزيداز ، وكان النشاط التثبيطي (91.85 بالمائة) مشابهًا للعقار المعروف لمرضى السكري من النوع 2 ، أكاربوز (92.87 بالمائة) 158. أظهرت التجارب في المختبر أن veActeosideإشنكوسايدو isoveActeoside2'-acetylveActeosidetubulosides A و tubulosides B و syringalide A '3- O- rhamnose و campneoside I و kankanoside J1 من C. و 1.2 و 4.6 و 0. 0 71 و 8.8 و 4.0 و 11.1 و 0.53 و 9.3 ميكرومتر على التوالي. على وجه الخصوص ، أظهر 2-acetylveActeoside نشاطًا مشابهًا مع epalrestat ، وهو مثبط اختزال الألدوز الإكلينيكي. VeActeosidendإشنكوسايدتم إثبات قدرته على تحسين تحمل الجلوكوز وتقليل مستوى الجلوكوز في الفئران بجرعات تبلغ 250-500 مجم / كجم 159. VeActeosidendإشنكوسايديمكن أن يحد من زيادة مستوى الجلوكوز في الدم بعد الأكل عن طريق تثبيط امتصاص الجلوكوز الناقل للجلوكوز 1- بوساطة 160. يمكن أن يثبط Isocampneoside II المعزول من P. coreana بشكل كبير اختزال الألدوز البشري المؤتلف مع IC50 البالغ 9.72 ميكرومتر. علاوة على ذلك ، قام veActeosideisoveActeosideisocampneoside II و cistanoside F بشكل فعال بتثبيط تراكم السوربيتول في عدسة الفئران المحتضنة مع تركيز عالٍ من الجلوكوز بنسبة 70.6 و 47.9 و 71.3 و 31.7 بالمائة تقريبًا عند 50 ميكرومتر على التوالي. مقارنة مع المجموعة الضابطة ، تسبب الإعطاء الفموي لمدة ثلاثة أسابيع لـ veActeoside10 و 20 و 40 مجم / كجم) في انخفاض كبير في نسبة الجلوكوز في الدم إلى 111.30 و 74.88 و 75.15 مجم / ديسيلتر على التوالي في الجرذان المصابة بداء السكري. فيما يتعلق بمستويات الأنسولين في الدم ، فإن العلاج عن طريق الفم باستخدام veActeoside10 و 20 و 40 مجم / كجم) رفع مستوى الأنسولين في الدم إلى 3.23 و 5.38 و 6.80 ميكرو وحدة دولية / مل ، على التوالي ، في الفئران المصابة بداء السكري.

2.8 أنشطة أخرى من PhGs
وو وآخرون. التحقيق في الخصائص المضادة للسمنة من PhGs من Ligustrum purpurascens. أظهرت النتائج أن PhGs تثبط الكيموتريبسين ، التربسين والبيبسين بقيم IC5 0 0. 42 ، 0. 38 ، و 0.68 مجم / مل ، على التوالي. قام VeActeosid بممارسة التأثيرات المضادة للسمنة عن طريق تثبيط ليباز البنكرياس. VeActeosideounded إلى الليباز عند Ka=1. 88 × 104 / لتر مول 163. ارتبط التأثير المضاد للسمنة لـ PhGs من L. purpurascens ضد الفئران التي تتغذى على النظام الغذائي الدهني مع زيادة تنظيم الرنا المرسال ومستويات البروتين من الليبتين الدهني.إشيناكوسايد(0. 01-10 nmol / L) يعزز تجديد العظام في خلايا MC3T 3- E1 عن طريق تعزيز منشط مستقبلات NF-κB ligand (RANKL) 165. وبالمثل ، فإن تناول ig يوميًا لمدة 12 أسبوعًا منإشنكوسايد(30 و 90 و 270 مجم / كجم / يوم) إلى الفئران التي تم استئصالها المبايض (OVX) أدت إلى زيادة كبيرة في مستوى osteoprotegerin (OPG) وانخفاض مستوى RANKL. مقارنة بمجموعة OVX ، 270 مجم / كجم / يومإشنكوسايدتسبب العلاج في أعلى مستويات نسب OPG و OPG / RANKL (150.14 بالمائة و 197.64 بالمائة) 166. بعد 12 أسبوعًا من تناول إشنكوسايد يوميًا عن طريق الفم (30 ، 90 ، 270 ملغم / كغم / يوم) في الفئران OVX ، زاد تركيز الكالسيوم والفوسفور غير العضوي والهيدروكسي برولين في البول بنسبة 92.23 في المائة و 66.67 في المائة و 36.41 في المائة على التوالي ، في مجموعة 270 مجم / كجم / يوم 167. تم العثور على Cistanoside A (ص ، 20 ، 40 و 80 ملغم / كغم / يوم لمدة 12 أسبوعًا) لتعزيز تكوين العظام ومنع ارتشاف العظام في فئران OVX عن طريق تقليل تنظيم TRAF6 ، وتنسيق تثبيط مسار NF-kB وتحفيز مسار PI3K / Akt168 .

If you have any question, please send us Email: wallencesuen@wecistanche.com
