الانتقال النشط لمرحلة ذاكرة الخوف من إعادة التوحيد إلى الانقراض من خلال منع إعادة التوحيد بوساطة ERK
Mar 20, 2022
جهة الاتصال: Audrey Hu Whatsapp / hp: 0086 13880143964 البريد الإلكتروني:audrey.hu@wecistanche.com
الاسترجاع ذاكرة الخوفيستحث عمليتين متعارضتين للذاكرة ، أي إعادة التوحيد والانقراض. يؤدي الاسترجاع الموجز إلى إعادة التوحيد للحفاظ على أوتعزيز ذاكرة الخوف ،بينما الاسترجاع المطول يطفئ هذه الذاكرة. على الرغم من التحقيق في آليات إعادة الاندماج والانقراض ، إلا أنه لا يزال من غير المعروف كيف يتم تحويل مراحل ذاكرة الخوف من إعادة التوحيد إلى الانقراض أثناء استرجاع الذاكرة. هنا ، نوضح أن عملية انتقال الذاكرة المعتمدة على كيناز خارج الخلية (ERK) بعد الاسترجاع تنظم تبديل مراحل الذاكرة من إعادة التوحيد إلى الانقراض عن طريق منع تحريض إعادة التوحيد في مهمة تجنب المثبطة (IA) في ذكور الفئران. أولاً ، تم تحديد مرحلة الذاكرة الانتقالية ، التي تلغي تحريض إعادة الاندماج ، ولكنها غير كافية لاكتساب الانقراض ، بعد إعادة التوحيد ، ولكن قبل مراحل الانقراض. ثانيًا ، أظهرت مراحل إعادة الدمج والانتقال والانقراض بعد استرجاع الذاكرة توقيعات جزيئية وخلوية متميزة من خلال بروتين ربط العناصر المستجيب لـ cAMP (CREB) وفسفرة ERK في اللوزة ، والحصين ، وقشرة الفص الجبهي الإنسي (mPFC). أظهرت مرحلة إعادة التجميع زيادة في فسفرة CREB ، بينما أظهرت مرحلة الانقراض العديد من المجموعات العصبية مع مجموعات مختلفة من الفسفرة CREB و / أو ERK ، في مناطق الدماغ هذه. ومن المثير للاهتمام ، أن مراحل الذاكرة الثلاث ، بما في ذلك المرحلة الانتقالية ، أظهرت تنشيطًا عابرًا لـ ERK بعد الاسترجاع مباشرة. الأهم من ذلك ، أن الحصار المفروض على ERK في اللوزة أو الحصين أو mPFC في مرحلة الذاكرة الانتقالية أدى إلى تعطيل تعزيز ذاكرة IA الناجم عن إعادة التوحيد. تشير هذه الملاحظات إلى أن مسار إشارات ERK ينظم بفعالية انتقال مرحلة الذاكرة من إعادة التوحيد إلى الانقراض ، وتعمل هذه العملية كمفتاح يلغي إعادة توحيد الخوفذاكرة.
الكلمات الرئيسية: ERK ؛ انقراض؛ذاكرة الخوف؛ إعادة توحيد انتقال
1 قسم العلوم البيولوجية ، كلية علوم الحياة ، جامعة طوكيو للزراعة ، طوكيو 156-8502 ، اليابان ، و
2 Graduate School of Agriculture and Life Sciences ، جامعة طوكيو ، طوكيو 113-8657 ، اليابان
بيان الأهمية
استعادة ذاكرة الخوفيستحث عمليتين متعاكستين للذاكرة ؛ إعادة توحيد والانقراض. إعادة توحيد تحافظ /يقوي ذاكرة الخوفبينما الانقراض يضعف ذاكرة الخوف. يبقى غير معروف كيف يتم تبديل مراحل الذاكرة من إعادة التوحيد إلى الانقراض أثناء الاسترجاع. هنا ، حددنا عملية انتقال ذاكرة نشطة تعمل كمفتاح يمنع إعادة الاندماج. أظهرت مرحلة انتقال الذاكرة هذه زيادة عابرة في فسفرة كيناز المنظمة بإشارة خارج الخلية (ERK) في اللوزة ، والحصين ، وقشرة الفص الجبهي الإنسي (mPFC). ومن المثير للاهتمام ، أن تثبيط ERK في هذه المناطق في المرحلة الانتقالية أعاق تعزيز ذاكرة التجنب المثبط (IA) بوساطة إعادة التوحيد. تشير هذه النتائج إلى أن عملية الذاكرة الانتقالية تنظم بشكل فعال تبديل مراحل ذاكرة الخوف لذاكرة الخوف عن طريق منع تحريض إعادة الاندماج من خلال تنشيط مسار إشارات ERK.
مقدمة
استرجاع الذاكرةليست عملية سلبية ولكنها عملية ديناميكية تسمح بالحفاظ على الذاكرة الأصلية أو تقويتها أو إضعافها أو تغييرها / تحديثها (ميسانين وآخرون ، 1968 ؛ شنايدر وشيرمان ، 1968 ؛ لويس ، 1979 ؛ ماكتوتوس وآخرون. ، 1979 ؛ جوردون ، 1981 ؛ نادر وآخرون ، 2000 ؛ نادر وهاردت ، 2009 ؛ دوداي ، 2012 ؛ فوكوشيما وآخرون ، 2014). الأهم من ذلك ، أن ذاكرة الخوف المكيفة المستردة عن طريق إعادة التعرض لفترة وجيزة للمحفز المشروط (CS) تصبح قابلة للتحلل وتتطلب إعادة توحيد تعتمد على التعبير الجيني لصيانتها أو تعزيزها (Nader et al. ، 2000 ؛ Dudai ، 2002 ؛ Kida et al. ، 2002 ؛ سوزوكي وآخرون ، 2004 ؛ ترونيل وآخرون ، 2005 ؛ فوكوشيما وآخرون ، 2014). على العكس من ذلك ، يؤدي التعرض المستمر أو المتكرر لـ CS إلى انقراض الذاكرة ، مما يضعف ذاكرة الخوف (Pavlov ، 1927 ؛ Rescorla ، 2001 ؛ Myers and Davis ، 2002). وهكذا ، فإناسترجاع ذاكرة الخوفيستحث عمليتين متعاكستين للذاكرة ، أي إعادة التوحيد والانقراض ، على الرغم من أن كلا العمليتين يتم تحفيزهما عن طريق إعادة التعرض لـ CS متطابق ، لكنهما يختلفان وفقًا لمدة إعادة التعرض لـ CS.
السمة الكيميائية الحيوية المشتركة والحاسمة لإعادة التوحيد والانقراض هي مطلب التعبير الجيني بوساطة بروتين رابط للعناصر المستجيب لـ cAMP (CREB) (Mamiya et al. ، 2009). ومن المثير للاهتمام ، أننا أظهرنا تواقيع جزيئية وتشريحية وسلوكية متناقضة بين مرحلتي إعادة توحيد وانقراض ذاكرة الخوف السياقية (سوزوكي وآخرون ، 2004 ؛ ماميا وآخرون ، 2009). يؤدي حظر تخليق البروتين أثناء مرحلة إعادة التوحيد إلى تعطيل ذاكرة الخوف الأصلية ، بينما يفشل منع تخليق البروتين أثناء مرحلة الانقراض في القيام بذلك ، على الرغم من إعادة تنشيط ذاكرة الخوف السياقية. تختلف متطلبات مناطق الدماغ التي تظهر تنشيط التعبير الجيني بوساطة CREB بين إعادة التوحيد والانقراض ؛ يعتمد التوحيد على اللوزة المخية والحصين ، في حين يعتمد الانقراض على اللوزة المخية وقشرة الفص الجبهي الإنسي (mPFC). ومع ذلك ، فإن المسار الزمني لتنشيط اللوزة الدماغية يختلف بين مرحلتي إعادة توحيد الذاكرة وانقراضها. تشير هذه الملاحظات إلى أن مراحل إعادة الدمج والانقراض ليست مستقلة ، بل تتفاعل مع بعضها البعض. ومن المثير للاهتمام ، أن الدراسات الحديثة قد حددت نافذة زمنية (مرحلة انتقالية) لا تُظهر تنشيط كيناز منظم بإشارات خارج الخلية (ERK) في اللوزة بعد إعادة التوحيد ، ولكن قبل مراحل الانقراض التالية لاسترجاع ذاكرة الخوف السمعي (Merlo et al. ، 2018 ). مجتمعة ، تشير هذه النتائج إلى الآليات المحتملة التي يتم من خلالها تبديل مراحل الذاكرة من إعادة التوحيد إلى الانقراض أثناءاسترجاع ذاكرة الخوف. بمعنى آخر ، من الممكن أن تنظم عملية انتقال الذاكرة هذا المفتاح بشكل فعال.
في مهمة التجنب المثبط (IA) ، تتلقى الفئران صدمة كهربائية بعد دخولها مقصورة مظلمة من حجرة الضوء وتشكلهاذاكرةلتجنب المقصورة المظلمة. سابقًا ، باستخدام هذه المهمة ، أظهرنا أنه يمكن التمييز بين مرحلتي التوحيد والانقراض في الوقت الذي يدخل فيه الماوس إلى حجرة مظلمة من حجرة إضاءة أثناء جلسة إعادة التعريض (فوكوشيما وآخرون ، 2014). لذلك ، تسمح لنا هذه المهمة بتوصيف التواقيع الجزيئية المنظورة لمراحل إعادة التوحيد والانقراض ، على عكس نموذج تكييف الخوف السياقي الكلاسيكي الذي يؤدي فيه إعادة تنشيط ذاكرة الخوف المشروطة عن طريق إعادة التعرض إلى CS إلى إعادة التوحيد والانقراض ؛ يؤدي التعرض القصير (3 دقائق) للسياق المشروط إلى إعادة التوحيد ، بينما يؤدي التعرض الطويل (30 دقيقة) أو إعادة التعرض المتكرر لهذا السياق إلى الانقراض (Eisenberg et al. ، 2003 ؛ Pedreira and Maldonado ، 2003 ؛ Suzuki et al. ، 2004 ؛ لي وآخرون ، 2008 ؛ ماميا وآخرون ، 2009). علاوة على ذلك ، وجدنا أن ذاكرة IA المستردة يتم تحسينها من خلال إعادة توحيد الذاكرة في هذه المهمة (Fukushima et al. ، 2014).
لفهم آلية الانتقال من إعادة التوحيد إلى الانقراض خلالاسترجاع ذاكرة الخوف، كنا نهدف إلى تحديد وتوصيف التوقيعات الجزيئية والخلوية والسلوكية لمراحل إعادة التوحيد والانتقال والانقراض لذاكرة IA. قمنا بتحليل تنشيط CREB و ERK في اللوزة والحصين و mPFC في مراحل إعادة التوحيد والانتقال والانقراض وفحصنا أدوار تنشيط ERK في عمليات الذاكرة هذه.

المواد والأساليب
تم إجراء جميع التجارب على الفئران وفقًا لدليل رعاية واستخدام حيوانات المختبر (جمعية علم الأعصاب اليابانية وجامعة طوكيو للزراعة). تمت الموافقة على جميع التجارب التي أجريت على الحيوانات في هذه الدراسة من قبل لجنة رعاية واستخدام الحيوان التابعة لجامعة طوكيو للزراعة (التفويض رقم 280037). تم إجراء جميع العمليات الجراحية تحت التخدير Nembutal وبذل كل جهد ممكن لتقليل المعاناة. تم الحصول على ذكور الفئران C57BL / 6N من نهر تشارلز. تم إيواء الفئران في أقفاص من خمسة أو ستة ، وتم الحفاظ عليها في دورة مظلمة / فاتحة 12/12 ساعة ، وتم السماح لها بالوصول إلى الطعام والماء. كان عمر الفئران ثمانية أسابيع على الأقل عند الاختبار. تم إجراء الاختبار أثناء مرحلة الضوء من الدورة. أجريت جميع التجارب عمياء عن حالة علاج الفئران.
اختبار IA يتألف جهاز IA التدريجي (OHARA Pharmaceutical) من صندوق به مقصورات منفصلة فاتحة ومظلمة (كلاهما 15.5 12.5 11.5 سم). تمت إضاءة حجرة الضوء بضوء فلورسنت (25 0 0 لوكس ؛ فوكوشيما وآخرون ، 2008 ، 2014 ؛ تشانغ وآخرون ، 2011 ؛ إيشيكاوا وآخرون ، 2016). قبل بدء تدريب IA ، تم التعامل مع الفئران بشكل فردي لمدة دقيقتين كل يوم لمدة أسبوع واحد. خلال جلسات التدريب ، سُمح لكل فأر بالتعود على حجرة الضوء لمدة 30 ثانية ، وتم رفع باب المقصلة للسماح بالوصول إلى المقصورة المظلمة. يعتبر الكمون لدخول الحجرة المظلمة بمثابة مقياس للاكتساب. بمجرد دخول الفأر إلى المقصورة المظلمة ، تم إغلاق باب المقصلة. بعد 5 ثوانٍ ، تم تسليم صدمة قدم (0.2 مللي أمبير) لمدة إجمالية قدرها 2 ثانية (تدريب). في 24 ساعة بعد جلسة التدريب ، تم وضع الماوس مرة أخرى في حجرة الضوء حتى دخل الحجرة المظلمة (متوسط 459 6 15. 49 ثانية). مباشرة بعد دخول الفأرة المقصورة المظلمة ، تم إغلاق باب المقصلة وظل الفأر في المقصورة المظلمة لفترة زمنية متفاوتة (0 ، 1 ، أو 10 دقائق) بدون صدمة قدم (إعادة تنشيط). تم تقييم الذاكرة بعد 48 ساعة [اختبار الذاكرة طويلة المدى لما بعد التنشيط (PR-LTM)] مثل زمن انتقال الماوس لدخول الحجرة المظلمة عند استبداله في حجرة الضوء ، كما هو الحال في إعادة التنشيط.
في التجربة الأولى ، درسنا تأثير تثبيط تخليق البروتين بعد إعادة التنشيط (إعادة التعرض للحيز المظلم لمدة 0 أو 1 أو 1 0 دقيقة ؛ الشكل 1). تم إذابة مثبط تخليق البروتين anisomycin (ANI؛ Wako) في محلول ملحي (تم تعديل الرقم الهيدروجيني إلى 7. 0 - 7.4 مع هيدروكسيد الصوديوم). تم تدريب الفئران على النحو الموصوف أعلاه ، وبعد 24 ساعة ، تلقوا مركبة (VEH) أو ANI (150 مجم / كجم ، IP) مباشرة بعد إعادة التعرض للمقصورة المظلمة لمدة 0 أو 1 أو 10 دقائق بدون صدمة قدم (إعادة التنشيط). عند هذه الجرعة ، يثبط ANI بنسبة 90٪ من تخليق البروتين في الدماغ خلال أول ساعتين (Flood et al. ، 1973). في 48 ساعة بعد جلسة إعادة التنشيط ، تم وضع الفئران الفردية مرة أخرى في حجرة الضوء وتم تقييم زمن الانتقال المتقاطع.
بالنسبة للتجربة الثانية [مادة CREB فسفرة (pCREB) وكيمياء مناعية فسفرة ERK (pERK) ؛ تين. 2-5] ، فحصنا مناطق الدماغ التي تم تنشيطها بعد إعادة التعرض للضوء (حتى دخلت الفئران الحجرة المظلمة ، وأعيد التعرض للحيز المظلم لمدة 0 دقيقة) أو المقصورة المظلمة (إعادة التعرض للمقصورة المظلمة لمدة 1 أو 1 0 دقيقة). تم تقسيم الفئران إلى أربعة فوكوشيما وآخرون. · انتقال مراحل ذاكرة الخوف بعد الاسترداد J. Neurosci. ، 10 فبراير 2021 ، • 41 (6): 1288-1300 • 1289 مجموعة. في 24 ساعة بعد التدريب ، تم إعادة تعريض الفئران الفردية إلى حجرة الضوء ثم بقيت في المقصورة المظلمة بعد دخولها من المقصورة المظلمة [إعادة التنشيط: 0 دقيقة في المقصورة المظلمة ، مجموعة إعادة التوحيد (Recon) ؛ 1 دقيقة ، مجموعة انتقالية (Tran) ؛ 10 دقائق ، مجموعة الانقراض (Ext)]. لم يتم إرجاع مجموعة أخرى من الفئران إلى حجرة الضوء / الظلام [مجموعة غير معاد تنشيطها (NR)]. ثم تم تخدير الفئران باستخدام Nembutal (750 مجم / كجم ، IP) عند 5 أو 15 أو 30 دقيقة بعد إعادة التنشيط.
بالنسبة للتجربة الثالثة (التسريب الدقيق لـ U {{2 {22}}} 126 ؛ الأشكال 6،7) ، قمنا بفحص تأثيرات تثبيط ERK في اللوزة أو الحصين أو mPFC على إعادة توحيد / تحسين الذاكرة ، والانتقال ، والانقراض. تم إذابة مثبط MEK U 0 126 (Sigma-Aldrich) في السائل الدماغي الشوكي الاصطناعي الذي يحتوي على ثلاث قطرات من Tween 8 0 (Sigma) في 2.5 مل من 7.5 بالمائة ثنائي ميثيل سلفوكسيد (Wako) وتعديله إلى الرقم الهيدروجيني 7.4 مع هيدروكسيد الصوديوم. تم تدريب الفئران كما هو موضح أعلاه ، وبعد 24 ساعة ، تم وضعها مرة أخرى في حجرة الضوء (إعادة التنشيط). تم حقن الفئران بشكل دقيق مع U0126 (1 مجم) أو VEH في مناطق الدماغ المختلفة مباشرة بعد (الأشكال 6A ، C ، E-H ، 7A-C) أو بعد 30 دقيقة بعد إعادة التنشيط (الشكل 6 ب ، د). في 48 ساعة بعد إعادة التنشيط ، تم وضع الفئران الفردية مرة أخرى في حجرة الضوء وتم تقييم زمن الانتقال المتقاطع (PR LTM). تم إجراء الحقن المجهري في الحصين و mPFC (0.5 مل) بمعدل 0.25 مل / دقيقة. تم إجراء تسريب دقيق في اللوزة (0.2 مل) بمعدل 0.1 مل / دقيقة. تُركت قنية الحقن في مكانها لمدة دقيقتين بعد التسريب المجهري ثم أعيدت الفئران إلى أقفاصها المنزلية. تم إذابة مثبط MEK SL327 (Santa Cruz Biotechnology) في ثنائي ميثيل سلفوكسيد وتم تخفيفه بمحلول ملحي. تم تدريب الفئران كما هو موضح أعلاه ، وبعد 24 ساعة ، تم إعادة الفئران الفردية إلى حجرة الضوء (إعادة التنشيط). تم حقن الفئران بشكل منهجي بـ SL327 (10 أو 20 مجم / كجم) أو VEH مباشرة بعد إعادة التنشيط (الشكل 7D-F). في 48 ساعة بعد إعادة التنشيط ، تم وضع الفئران الفردية مرة أخرى في حجرة الضوء وتم تقييم زمن الانتقال المتقاطع (PR-LTM).
تم إجراء الكيمياء الهيستولوجية المناعية كما هو موضح سابقًا (Mamiya et al. ، 2009 ؛ Suzuki et al. ، 2011 ؛ Zhang et al. ، 2011 ؛ Fukushima et al. ، 2014 ؛ Ishikawa et al. ، 2016 ؛ Hasegawa et al. ، 2019). بعد التخدير ، تم ترطيب جميع الفئران بنسبة 4 في المائة من بارافورمالدهيد. تمت إزالة الأدمغة ، وتثبيتها بين عشية وضحاها ، ونقلها إلى 30 في المائة من السكروز ، وتخزينها في 4 درجات. تم قطع المقاطع الاكليلية (30 ملم) في ناظم البرد.
بالنسبة لتلطيخ pCREB و pERK ، تمت معالجة الأقسام العائمة الحرة بنسبة 1 في المائة من H2O2 وحضنت طوال الليل باستخدام جسم مضاد متعدد الأضلاع مضاد للفوسفو CREB (سيرين 133 ؛ S133) (1: 1 0 00 ؛ # {{10 }} ، Millipore) و / أو جسم مضاد أحادي النسيلة مضاد للفوسفو ERK1 / 2 (T202 / Y204) (1: 300 ؛ # 4370 ؛ تقنية تشوير الخلية) في محلول منع (محلول ملحي مخزّن بالفوسفات بالإضافة إلى 1 بالمائة من ألبومين الماعز ، 1 مجم / مل من ألبومين مصل البقر ، و 0.05 بالمائة Triton X -100). تم غسل المقاطع بمحلول ملحي مخزّن من الفوسفات وحضنت باستخدام الفجل الفجل المترافق مع بيروكسيداز الحمير IgG (1: 500 ؛ Jackson ImmunoResearch) من أجل pCREB أو الفجل المترافق مع بيروكسيداز الماعز المضاد للأرنب IgG لـ pERK لمدة ساعة واحدة في درجة حرارة الغرفة. تم تضخيم إشارات pCREB بواسطة biotin tyramide وتم تصورها باستخدام streptavidin المترافق من Alexa Fluor (Invitrogen). تم تضخيم إشارات بيرك باستخدام TSA-FCM (Invitrogen). تم تركيب المقاطع على شرائح ومغطاة باستخدام وسط تصاعد (ميليبور).
تم إجراء القياس الكمي كما هو موضح سابقًا (Frankland et al. ، 2006 ؛ Fukushima et al. ، 2014 ؛ Mamiya et al. ، 2009 ؛ Zhang et al. ، 2011 ؛ Suzuki et al. ، 2008). تم تحديد الهياكل تشريحيًا وفقًا لأطلس فرانكلين وباكسينوس (1997). تم إحصاء جميع الخلايا العصبية المناعية من قبل مجرب أعمى عن حالة العلاج

نتائج
توصيف مراحل الذاكرة بعد الاسترجاع في مهمة IA
تسمح لنا مهمة IA بالتمييز بين مرحلتي إعادة التوحيد والانقراض عند النقطة الزمنية عندما يدخل الماوس إلى حجرة مظلمة من حجرة إضاءة (فوكوشيما وآخرون ، 2014). لفهم الآلية الكامنة وراء تبديل مراحل الذاكرة من إعادة التوحيد إلى الانقراض ، قمنا بتمييز مراحل ذاكرة IA بعد استرجاع الذاكرة من خلال فحص تأثيرات تثبيط تخليق البروتين المطلوب لإعادة توحيد وانقراض ذاكرة IA (فوكوشيما وآخرون ، 2014). تم وضع الفئران لأول مرة في حجرة الضوء. في 5 ثوانٍ بعد دخولهم المقصورة المظلمة ، تم تسليم صدمة كهربائية قصيرة (تدريب). تم إعادة تعريض الفئران إلى حجرة الضوء بعد 24 ساعة من التدريب (جلسة إعادة التنشيط ، الشكل 1 أ) وتم تقييم زمن انتقالهم للدخول إلى الحجرة المظلمة (الشكل 1 ب). أعيدت الفئران إلى أقفاصها المنزلية فور دخولها في الحجرة المظلمة من حجرة الضوء (0- دقيقة من إعادة التعرض للحجرة المظلمة ؛ مرحلة إعادة التجميع) أو بقيت في المقصورة المظلمة لمدة 1 ، 3 ، أو 10 دقائق دون تلقي صدمة قدم (مرحلة الانقراض ، الشكل 1C-E). مباشرة بعد جلسة إعادة التنشيط ، تلقت الفئران حقنة جهازية من VEH أو مثبط تخليق البروتين ANI. في 48 ساعة لاحقًا ، تم تقييم زمن الانتقال المتقاطع PR-LTM.
تمشيا مع دراستنا السابقة (فوكوشيما وآخرون ، 2 0 14) ، تسبب إعادة التعرض لمقصورة الضوء (0 مجموعة دقيقة) في إعادة توحيد وتعزيز ذاكرة IA. كشفت ANOVA ثنائية الاتجاه عن تأثيرات كبيرة للوقت (F (1،24)=10. 433، p=0. {{2 0}} 036) ، عقار (F (1 ، 24)=23. 197، p، 0.0001) والتفاعل الدوائي الزمني (F (1،24)=25. 022، p، 0.0001؛ Fig. 1B). أظهر اختبار Bonferroni اللاحق واختبار t المقترن أن مجموعتي VEH و ANI ، تعرضان زيادة أو نقصانًا ملحوظًا ، على التوالي ، في زمن الانتقال المتقاطع في PR-LTM مقارنة بجلسة إعادة التنشيط (ps ، 0.05 ؛ VEH ، t (6) {{28) }} 5.134، p=0. 0021، ANI، t (6)=4. 804، p=0. 003؛ Fig. 1B). تشير هذه الملاحظات إلى أن استرجاع ذاكرة IA في حجرة الضوء عزز الذاكرة ، بينما أدى تثبيط تخليق البروتين إلى تعطيل الذاكرة المستردة ، مما يؤكد الملاحظة السابقة بأن استرجاع ذاكرة IA يعزز الذاكرة من خلال إعادة التوحيد بطريقة تعتمد على تخليق البروتين.
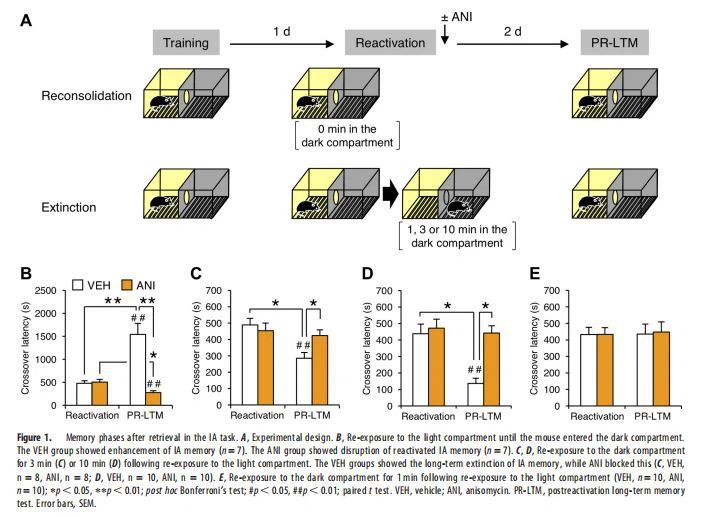
في المقابل ، تسبب إعادة التعرض للحيز المظلم في انقراض طويل الأمد [ثنائي الاتجاه ANOVA ، الوقت (الشكل 1C ، F (1،28)=9. 575 ، ص=0. { {5 0}} 0 4 ؛ الشكل 1D، F (1،36)=11. 699، p=0. 0 016) ، عقار (الشكل 1C، F (1،28)=4. 674، p=0. 039؛ Fig. 1D، F (1،36)=12. 285، p {{29 }}. 0012) ، التفاعل الدوائي الزمني (الشكل 1C، F (1،28)=7. 916، p=0. 009؛ Fig. 1D، F (1،36) {{41 }}. 915 ، ص=0. 0079)] ، كما لوحظ سابقًا (فوكوشيما وآخرون ، 2014). أظهرت مجموعات VEH التي بقيت في المقصورة المظلمة لمدة 3 أو 10 دقائق انخفاضًا ملحوظًا في زمن الانتقال في PR-LTM مقارنة بجلسة إعادة التنشيط ، في حين عرضت مجموعات ANI زمن انتقال قابل للمقارنة في PR-LTM مقارنة بجلسة إعادة التنشيط وإلى مجموعات VEH (بعد اختبار Bonferroni بعد ذلك ، ps ، 0.05 ؛ اختبار t الزوجي ، الشكل 1C ، VEH ، t (7)=4. 976، p=0. 0016، ANI، t (7) { {59}}. 796، p. 0.05؛ Fig. 1D، VEH، t (9)=10. 211، p، 0.0001، ANI، t (9)=1. 02، p. 0.05 ). تشير هذه الفتحات الملحوظة إلى أن إعادة التعرض للحجرة المظلمة لمدة 3 أو 10 دقائق تنطفئ ذاكرة IA وأن تثبيط تخليق البروتين منع الانقراض على المدى الطويل. وبالتالي ، فإن استرجاع ذاكرة IA في المقصورة المظلمة يطفئ ذاكرة IA بطريقة التعبير الجيني المعلقة.
الأهم من ذلك ، أظهرت مجموعة VEH تقاطعًا مشابهًا للكمون في PR-LTM مقارنة بجلسة إعادة التنشيط ومجموعة ANI عندما بقوا في الحجرة المظلمة لمدة دقيقة واحدة [ثنائي الاتجاه ANOVA ، الوقت (F (1،36) {{ 5}}. 0 3 ، ص 0. 0 5) ، عقار (إناث (1،36)=0. 0 19 ، ص. 0. 0 5) ، التفاعل الدوائي للوقت (F (1،36)=0. 011، p. 0.05) ؛ بعد اختبار Bonferroni المخصص ، ملاحظة. 0.05 ؛ اختبار t المقترن ، VEH ، t (9)=0. 091 ، ص. 0.05 ، ANI ، t (9)=0. 328 ، ص. 0.05 ؛ الشكل 1E]. تشير هذه الملاحظات إلى أن مجموعة VEH لم تظهر أي تعزيز أو انقراض لذاكرة IA وأن مجموعة ANI لم تظهر أي اضطراب في ذاكرة IA. لذلك ، أدى إعادة التعريض إلى المقصورة المظلمة لمدة دقيقة واحدة إلى منع كل من التعطيل الناجم عن ANI لذاكرة IA المعاد تنشيطها ، ولكن لم يتم إطفاء ذاكرة IA ، مما يشير إلى أن هذا 1- دقيقة من إعادة التعريض تلغي تحريض إعادة التوحيد ، لكنها غير كافية لإطفاء ذاكرة IA.

باختصار ، أشارت هذه النتائج إلى أن إعادة التعرض لحجرة الضوء يؤدي إلى مرحلة إعادة التجميع ، في حين أن التعرض لفترة أطول للحيز المظلم (3 أو 10 دقائق) يؤدي إلى مرحلة الانقراض. الأهم من ذلك ، أن البقاء لمدة دقيقة واحدة في المقصورة المظلمة يؤدي إلى المرحلة الانتقالية من إعادة التجميع إلى الانقراض ، مما يمنع الخوف من إعادة توحيد الذاكرة دون التسبب في الانقراض.
التوقيعات الجزيئية لمراحل إعادة التوحيد والانتقال والانقراض في اللوزة والحصين و mPFC بعد استرجاع ذاكرة IA
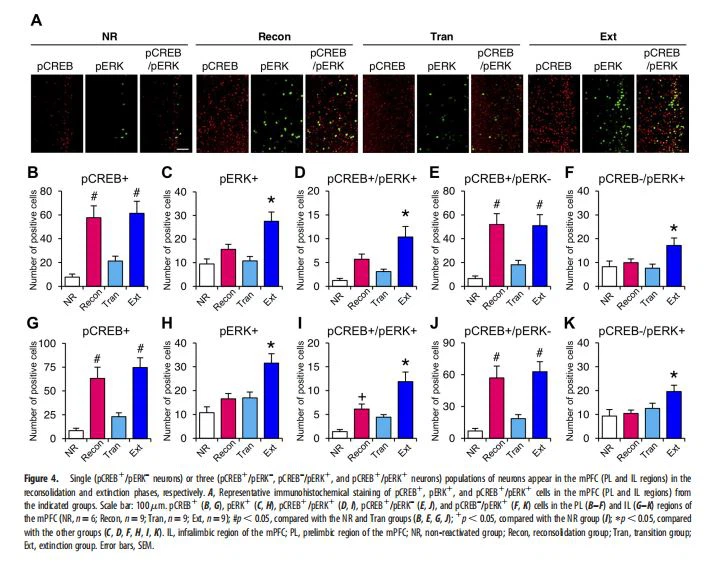
تظهر إعادة توحيد وانقراض ذاكرة الخوف السياقية زيادات في فسفرة CREB في S133 ، وهي علامة لتنشيط التعبير الجيني المطلوب لإعادة التوحيد والانقراض على المدى الطويل ، ولكنها تظهر ديناميكيات مميزة لتفسف CREB (Mamiya et al. ، 2 0 09 ). ومن المثير للاهتمام ، أن الدراسات الحديثة أظهرت أنه لا توجد زيادة في فسفرة ERK ، وهو منظم رئيسي لـ CREB (Impey et al. ، 1998 ؛ Wu et al. ، 2001) ، في المنطقة القاعدية من اللوزة عند الانتقال من إعادة التوحيد لانقراض ذاكرة الخوف ، على الرغم من أن هذه الفسفرة تزداد في المنطقة القاعدية عندما يتم إعادة توحيد ذاكرة الخوف الملحوظة وإخمادها (ميرلو وآخرون ، 2014 ، 2018). أشارت دراسة أخرى إلى أن Hippocampal ERK يتم تنشيطه فقط عندما يتم إخماد ذاكرة الخوف السياقية ، ولكن لا يتم إعادة توحيدها (Tronson et al. ، 2009). تشير هذه النتائج إلى أن مراحل إعادة الدمج والانتقال والانقراض تظهر توقيعات جزيئية وخلوية متميزة. لذلك ، قمنا بقياس ومقارنة مستويات pCREB و pERK في مراحل إعادة التوحيد والانتقال والانقراض باستخدام الكيمياء الهيستولوجية المناعية. أجرينا جداول تجريبية مماثلة كما في الشكل 1B ، D ، E باستخدام أربع مجموعات تجريبية. تم إعادة تعريض الفئران إلى حجرة الضوء في 24 ساعة بعد التدريب ثم بقيت في المقصورة المظلمة [إعادة التنشيط: 0 دقيقة في المقصورة المظلمة ، مجموعة إعادة التوحيد (Recon) ؛ 1 دقيقة ، مجموعة انتقالية (Tran) ؛ 10 دقائق ، مجموعة الانقراض (Ext)]. لم يتم إرجاع مجموعة أخرى من الفئران إلى حجرة الضوء / الظلام (مجموعة NR غير المعاد تنشيطها). قمنا بحساب الخلايا العصبية الإيجابية لـ pCREB (pCREB1) ، والخلايا العصبية الإيجابية (pERK1) ، والخلايا العصبية المزدوجة الإيجابية (pCREB1 / pERK1) في اللوزة ، والحصين ، و mPFC في 30 دقيقة بعد جلسة إعادة التنشيط.
تم تنشيط Amygdala (المنطقة الجانبية) CREB في مرحلتي الانقراض وإعادة التوحيد ، بينما تم تنشيط ERK فقط في مرحلة الانقراض (الشكل 2A-C). كشفت ANOVA أحادية الاتجاه عن تأثير كبير للمجموعة (الشكل 2 ب ، و (3،29)=14. 85 ، ص ، 0. 0 001). على غرار النتائج السابقة (Mamiya et al. ، 2009) ، أظهر اختبار Newman-Keuls اللاحق أن مجموعتي Recon و Ext أظهرتا عددًا أكبر بكثير من الخلايا العصبية pCREB1 مقارنة بالمجموعات الأخرى (ص ، 0.05). أشارت هذه الملاحظات إلى أنه على غرار الملاحظات على المستويات السلوكية (الشكل 1) ، فإن التعرض للحجرة المظلمة لمدة دقيقة واحدة (مرحلة انتقالية) يلغي "تشغيل" فسفرة CREB التي ستزداد في مرحلة إعادة التوحيد. في المقابل ، لوحظ عدد أكبر بكثير من الخلايا العصبية pERK1 في المجموعة Ext مقارنة بالمجموعات الأخرى ، على الرغم من وجود عدد أقل بكثير من الخلايا العصبية pERK1 مقارنة بالخلايا العصبية pCREB1 في المجموعة Ext (F (3،29)=3. 793، p { {23}}. 0207 ؛ الشكل 2 ج).
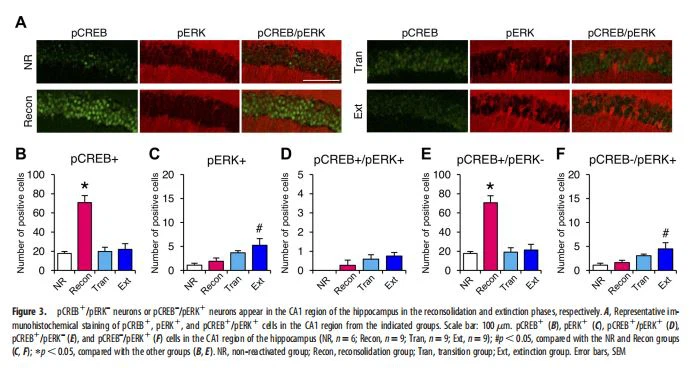
باستمرار ، لوحظ وجود عدد أكبر بشكل ملحوظ من الخلايا العصبية الموجبة المزدوجة (pCREB1 / pERK1) في المجموعة Ext (F (3،29)=6. 698، p=0. 0 0 14 ؛ الشكل 2D) ، بينما لوحظ عدد أكبر بكثير من الخلايا العصبية pCREB1 / pERK- (إيجابية مفردة pCREB) في مجموعتي Recon و Ext (F (3،29)=13. 689، p، 0 . 0 001 ؛ الشكل 2E). وهكذا ، أظهرت مرحلة إعادة الاندماج مجموعة واحدة فقط من الخلايا العصبية pCREB1 / pERK. في المقابل ، أظهرت مرحلة الانقراض مجموعتين من الخلايا العصبية pCREB1 / pERK- و pCREB1 / pERK1 ، مما يشير إلى أن ERK يتم تنشيطه فقط في مجموعة فرعية من الخلايا العصبية pCREB1. الأهم من ذلك ، لوحظت نتائج مماثلة في المنطقة القاعدية الوحشية من اللوزة (الشكل 2G، F (3،29)=13. 042، p، 0.0001؛ الشكل 2H، F (3،29) {{32} } .824، p=0. 0201؛ Fig. 2I، F (3،29)=12. 633، p، 0.0001؛ Fig. 2J، F (3،29)=12 .505 ، ص ، 0.0001).
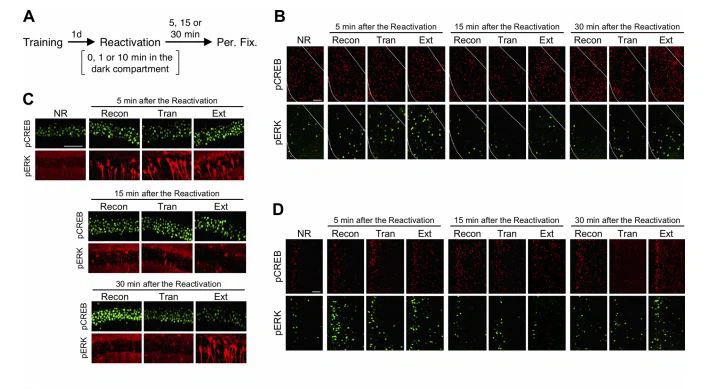
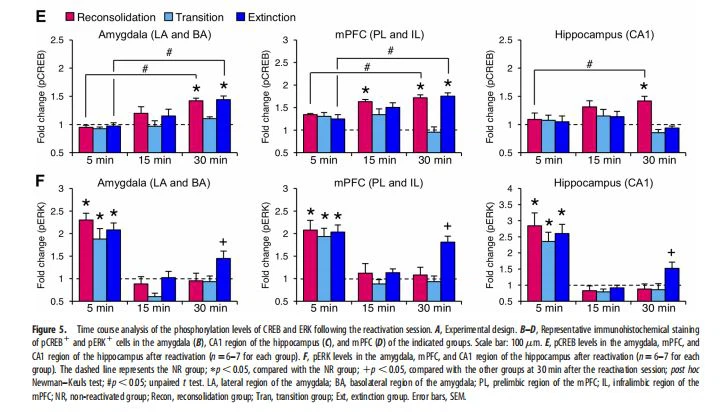
التنشيط ثنائي الطور لـ ERK في مرحلة الانقراض ERK هو المنشط الأولي لـ CREB ، وبالتالي ، فإن تنشيط ERK مطلوب لتوحيد وإعادة توحيد ذاكرة الخوف (Schafe et al. ، 2 0 0 {{31 }} ؛ Duvarci وآخرون ، 2 0 0 5). ومع ذلك ، بشكل غير متسق ، لم يلاحظ أي تنشيط ERK في اللوزة أو الحصين أو mPFC في مرحلة إعادة التجميع عندما تم قياس pERK في 3 0 دقيقة بعد جلسة إعادة التنشيط (الأشكال. 2-4). لذلك ، قمنا بفحص الدورات الزمنية للفسفرة ERK و CREB. لقد أجرينا تجربة مماثلة كما في الأشكال 2-4 ، فيما عدا أنه تم قياس مستويات pCREB و pERK في 5 و 15 و 3 {{59} دقيقة بعد جلسة إعادة التنشيط (إعادة التعرض للحيز المظلم لمدة {{ 66}} أو 1 أو 1 0 دقيقة ؛ الشكل 5 أ). تمشيا مع البيانات الموضحة في الأشكال 2-4 ، لوحظت زيادات كبيرة في الخلايا العصبية pCREB1 في 30 دقيقة ، ولكن ليس في 5 دقائق ، بعد جلسة إعادة التنشيط في Recon (اللوزة ، mPFC والحصين) و Ext (اللوزة و mPFC) ) ، ولكن ليس مجموعة Tran (الشكل 5E ، ANOVA أحادي الاتجاه ، اللوزة ، 5 دقائق ، F (3،23)=0. 346 ، الصفحة 0.05 ، 30 دقيقة ، F (3،23)=15. 272، p، 0.0001؛ mPFC، 5 min، F (3،23)=1. 169، p. 0.05، 30 min، F (3،23)=32. 346، p، 0.0001؛ hippocampus، 5 min، F (3،23)=0. 154، p. 0.05، 30 min، F (3،23)=16. 197، p، 0.0001؛ اختبار t غير مقترن ، اللوزة ، إعادة الدمج ، 5 مقابل 30 دقيقة ، t (12)=7. 807 ، p ، 0.0001 ، انقراض ، 5 مقابل 30 دقيقة ، t (12)=5. 405 ، ص { {73}}. 0002؛ mPFC ، إعادة الدمج ، 5 مقابل 30 دقيقة ، t (12)=5. 727، p، 0.0001، extinction، 5 vs 30 min، t (12)=4. 188 ، p=0. 0013؛ hippocampal CA1 area، reconsolidation، 5 vs 30 min، t (12)=2. 339، p=0. 0374).
ومن المثير للاهتمام ، لوحظت زيادات كبيرة في الخلايا العصبية pERK1 في اللوزة ، و mPFC ، والحصين من مجموعات Recon ، و Tran ، و Ext في 5 دقائق بعد جلسة إعادة التنشيط مقارنة بمجموعة NR (الشكل 5F ، اللوزة ، F (3،23)=10. 961 ، ص=0. 0 0 0 1 ؛ mPFC، F (3،23)=7. 525، p { {13}}. 0011؛ hippocampus، F (3،23)=6. 924، p=0. 0017). أشارت هذه الملاحظات إلى أن ERK يتم تنشيطه فورًا بعد جلسة إعادة التنشيط في جميع مراحل الذاكرة. ومع ذلك ، فإن هذه الزيادات في عدد الخلايا العصبية pERK1 عادت إلى المستويات القاعدية (يمكن مقارنتها مع مجموعة NR) في 15 دقيقة بعد جلسة إعادة التنشيط (الشكل 5F ، اللوزة ، F (3،20)=2. 676 ، ص 0.05 ؛ mPFC، F (3،23)=0. 683، p. 0.05؛ hippocampus، F (3،20)=0. 74، p. 0.05). علاوة على ذلك ، تمشيا مع النتائج الموضحة في الأشكال 2-4 ، لوحظ عدد أكبر بكثير من الخلايا العصبية pERK1 في اللوزة ، و mPFC ، والحصين في 30 دقيقة بعد جلسة إعادة التنشيط فقط في المجموعة الخارجية (الشكل 5F ، اللوزة ، F ( 3،23)=6. 616، p=0. 022؛ mPFC، F (3،23)=8. 012، p=0. 0008؛ hippocampus، F ( 3،23)=6. 206 ، ص=0. 003). وبالتالي ، تظهر مراحل إعادة الدمج والانتقال تنشيطًا عابرًا لـ ERK فقط في النقطة الزمنية المبكرة (5 دقائق) ، بينما تُظهر مرحلة الانقراض تنشيطًا ثنائي الطور لـ ERK في النقاط الزمنية المبكرة (5 دقائق) والمتأخرة (30 دقيقة) بعد إعادة التنشيط جلسة. أشارت هذه الملاحظات إلى أن آليات تنظيم تنشيط ERK تختلف في مراحل إعادة التوحيد / الانتقال والانقراض. بشكل جماعي ، أظهرت ملاحظاتنا أن مراحل إعادة الدمج والانتقال والانقراض تظهر توقيعات جزيئية مميزة.
أدوار تنشيط ERK في مراحل إعادة توحيد وانقراض ذاكرة IA
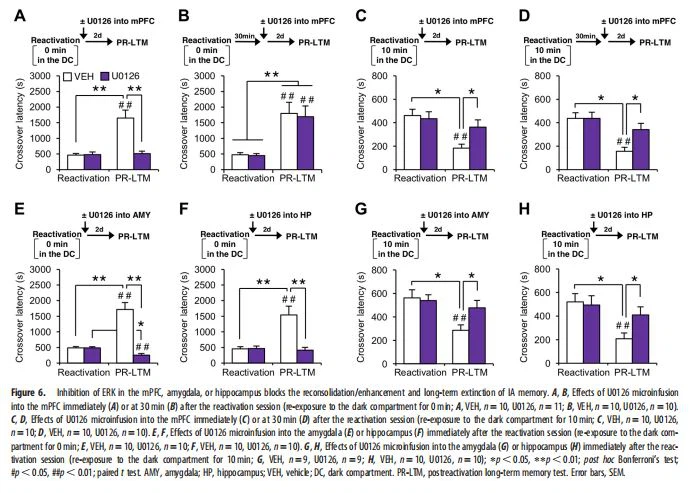
أظهرت مراحل إعادة التوحيد / الانتقال والانقراض تنشيط ERK أحادي الطور وثنائي الطور ، على التوالي. قمنا بعد ذلك بالتحقيق ومقارنة أدوار تنشيط ERK المبكر (5 دقائق) والمتأخر (30 دقيقة) في mPFC في مرحلتي إعادة التوحيد والانقراض من خلال فحص تأثيرات تثبيط ERK (الشكل 6).
مناقشة
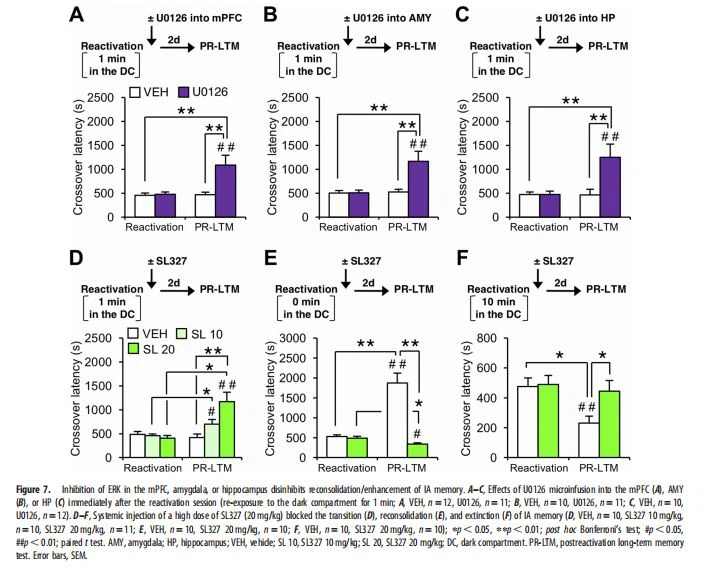
في هذه الدراسة ، قمنا بالتحقيق في آليات انتقال الذاكرة من مراحل إعادة الدمج إلى مراحل الانقراض بعد استرجاع ذاكرة IA. قمنا أولاً بتمييز التوقيعات السلوكية لمراحل ذاكرة IA بعد الاسترجاع. تمشيا مع دراستنا السابقة (فوكوشيما وآخرون ، 2 0 14) ، إعادة توحيد وانقراض الناجم عن استرداد ذاكرة IA عن طريق إعادة التعرض للضوء (0 دقيقة في المقصورة المظلمة) والظلام ( 3 أو 10 دقائق) ، على التوالي. ومن المثير للاهتمام ، أن ذاكرة IA لم يتم تحسينها أو إخمادها وأظهرت مقاومة لتثبيط تخليق البروتين عندما تم إعادة تعريض الفئران للحيز المظلم لمدة دقيقة واحدة فقط. لذلك ، تشير هذه الملاحظات إلى أن 1- دقيقة من التعرض مرة أخرى للحيز المظلم يلغي تحريض إعادة التجميع ، ولكنه غير كافٍ لإطفاء ذاكرة IA. علاوة على ذلك ، وجدنا أنه تم تنشيط ERK في اللوزة ، الحصين ، و mPFC في نقطة زمنية مبكرة (5 دقائق) بعد إعادة التعرض للحجرة المظلمة لمدة 0 أو 1 أو 10 دقائق. باستمرار ، أدى تثبيط ERK في مناطق الدماغ هذه إلى منع إعادة توحيد / تعزيز وانقراض ذاكرة IA. الأهم من ذلك ، أن تثبيط ERK في اللوزة ، والحصين ، و mPFC بعد 1- دقيقة من إعادة التعرض للمقصورة المظلمة ، أعاقت التحسين بوساطة إعادة التوحيد لذاكرة IA ، مما يشير إلى أن تنشيط ERK بعد إعادة التعرض لفترة وجيزة (دقيقة واحدة) إلى المقصورة المظلمة مطلوب لتثبيط إعادة توحيد ذاكرة IA. على العكس من ذلك ، فإن 1- دقيقة من إعادة التعرض للمقصورة المظلمة لم تكن كافية لإخماد ذاكرة IA ، على الرغم من أن إعادة التعرض الطويل للمقصورة المظلمة (3 أو 10 دقائق) أخمدت هذه الذاكرة. لذلك ، تشير نتائجنا إلى أن التعرض مرة أخرى لمدة 1- دقيقة للحيز المظلم يحفز عملية انتقال الذاكرة التي تلغي إعادة التوحيد / التحسين ولكنها لا تبدأ تعلم الانقراض. بشكل جماعي ، نقترح أن عملية انتقال الذاكرة تساهم في تبديل مراحل الذاكرة من إعادة التوحيد إلى الانقراض من خلال منع إعادة التوحيد بوساطة ERK.
على غرار ملاحظاتنا الحالية ، أظهرت دراسة حديثة باستخدام تكييف الخوف السمعي أن عروض CS الفردية (1) أو المطولة (10) تحفز إعادة توحيد الذاكرة والانقراض ، على التوالي ، من خلال زيادة مستويات pERK في المنطقة القاعدية من اللوزة. في المقابل ، لا تغير عروض CS المتوسطة (4-7) مستويات pERK في المنطقة القاعدية الوحشية من اللوزة. الأهم من ذلك ، أن تثبيط ERK في عروض CS الوسيطة لم يؤثر على ذاكرة الخوف. اقترحت هذه الدراسة أن هناك انتقالًا لمرحلة الذاكرة من إعادة التجميع إلى الانقراض بعد استرجاع ذاكرة الخوف (Merlo et al. ، 2018). في هذه الدراسة ، قمنا بتوسيع هذه النتيجة واقترحنا أن مرحلة الانتقال تقوم بتبديل مراحل الذاكرة بشكل فعال من إعادة التوحيد إلى الانقراض من خلال تنشيط مسار تحويل إشارة ERK. على عكس النتائج السابقة (Merlo et al. ، 2018) ، وجدنا أن المرحلة الانتقالية تتضمن فسفرة ERK في اللوزة ، الحصين ، و mPFC. قد تكون هذه التناقضات بسبب اختلاف النقاط الزمنية التي تفحص فسفرة ERK ؛ قامت الدراسة السابقة بقياس مستويات pERK عند ؛ 12 دقيقة بعد عرض CS (Merlo et al. ، 2018) ، بينما أظهرت دراستنا أن زيادة مستويات pERK عادت إلى المستوى الأساسي في هذه النقطة الزمنية تقريبًا (15 دقيقة بعد إعادة التعرض). بالإضافة إلى ذلك ، من المهم ملاحظة أن مهمة IA تمكن من مراقبة تعزيز ذاكرة IA من خلال إعادة التوحيد ، مما يؤدي إلى اكتشافنا أن تثبيط ERK في المرحلة الانتقالية يثبط تعزيز ذاكرة IA.
أظهرت الدراسات السابقة أن فسفرة ERK تزداد في المنطقة القاعدية الوحشية من اللوزة في 20-60 دقيقة بعد تعلم الانقراض لذاكرة الخوف (Herry et al. ، 2006 ؛ Merlo et al. ، 2014 ، 2018) ، بينما يظهر قرن آمون هذا التنشيط في ساعة واحدة بعد تعلم الانقراض لذاكرة الخوف السياقية (Fischer et al. ، 2007 ؛ Tronson et al. ، 2009). في هذه الدراسة ، حصلنا على ملاحظات مماثلة أن pERK يزداد في 30 دقيقة بعد جلسة إعادة التنشيط في مرحلة الانقراض. تشير هذه النتائج إلى أن فسفرة ERK هي علامة جزيئية شائعة لمرحلة الانقراض المتأخرة (20-60 دقيقة).
علاوة على ذلك ، لاحظنا أن تنشيط ERK يحدث ثنائي الطور في النقاط الزمنية المبكرة والمتأخرة (5 و 30 دقيقة) بعد جلسة إعادة التنشيط في مرحلة الانقراض ، بينما يحدث هذا التنشيط أحادي الطور في النقطة الزمنية المبكرة في مرحلة إعادة التوحيد (الشكل 5) . باستمرار ، منع ERK في مناطق الدماغ في هذه النقاط الزمنية من مراحل إعادة توحيد والانقراض منع إعادة توحيد / تعزيز والانقراض على المدى الطويل ، على التوالي (الشكل 6A ، C - H). تشير هذه الملاحظات إلى أن تنشيط ERK أحادي الطور وثنائي الطور مطلوب من أجل التعزيز بوساطة إعادة التوحيد وانقراض ذاكرة IA ، على التوالي. من المهم أن نلاحظ أن ERK يعمل كمنظم أولية للفسفرة CREB. لذلك ، قد يساهم التنشيط العابر لـ ERK في مرحلة الذاكرة المبكرة ، جزئيًا على الأقل ، في فسفرة CREB ، التي تنشط التعبير عن الجينات المطلوبة لإعادة التوحيد والانقراض طويل المدى.

على غرار النتائج السابقة التي توصلنا إليها باستخدام تكييف الخوف السياقي (Mamiya et al. ، 2009) ، تم تنشيط CREB في مراحل إعادة التوحيد (اللوزة / الحصين / mPFC) والانقراض (اللوزة / mPFC) ، بينما تم تنشيط ERK فقط في مرحلة الانقراض في 30 دقيقة بعد جلسة إعادة التنشيط. بشكل ثابت ، لوحظ فقط مجموعة واحدة من الخلايا العصبية pCREB1 / pERK في مرحلة إعادة التجميع ، بينما لوحظ وجود مجموعات عصبية مميزة في مرحلة الانقراض: pCREB1 / pERK- و pCREB1 / pERK1 الخلايا العصبية في اللوزة (الشكل 2) ؛ الخلايا العصبية pCREB– / pERK1 في قرن آمون (الشكل 3) ؛ و pCREB1 / pERK- و pCREB- / pERK1 و pCREB1 / pERK1 الخلايا العصبية في mPFC (الشكل 4). تشير هذه الملاحظات ، خاصة الملاحظة المتناقضة للخلايا العصبية pCREB- / pERK1 و pCREB1 / pERK ، إلى أن تنشيط CREB و ERK يتم تنظيمه بشكل مختلف في كل منطقة من مناطق الدماغ عند إطفاء الذاكرة وأن تنشيط المرحلة المتأخرة من ERK يلعب بشكل محدد ومتميز أدوار لانقراض ذاكرة الخوف مقارنة بعمليات الذاكرة الأخرى مثل التوحيد وإعادة التوحيد كما هو موضح أدناه. ومن المثير للاهتمام ، أننا لاحظنا أن الخلايا العصبية pERK1 كانت أكثر وفرة في mPFC مقارنة مع الحصين واللوزة ، حيث أظهر mPFC نسبة أعلى من الخلايا العصبية pERK1 (مرحلة الانقراض) والخلايا العصبية pCREB1 (مرحلة إعادة التوحيد) مقارنة مع الحصين واللوزة ، مما يشير إلى ذلك يلعب تنشيط ERK في mPFC دورًا أكثر تحديدًا في انقراض الذاكرة.
لا يزال من غير الواضح ما إذا كان يتم تنشيط مجموعات الخلايا العصبية نفسها أو مجموعات مختلفة في مراحل إعادة توحيد الذاكرة والانتقال والانقراض. حددت دراسة سابقة تنشيط "الخلايا العصبية للخوف" و "الخلايا العصبية للانقراض" في اللوزة عند إعادة تنشيط ذاكرة الخوف أو إخمادها ، على التوالي (هيري وآخرون ، 2008). لذلك ، من الممكن أن يتم تنشيط ERK و CREB في مجموعات مختلفة من الخلايا العصبية ذات الملامح الزمنية المختلفة (على سبيل المثال ، "الخلايا العصبية لإعادة التوحيد" والخلايا العصبية المنقرضة). كما نوقش أعلاه ، قد تنظم الخلايا العصبية pCREB1 ، بما في ذلك الخلايا العصبية pCREB1 / pERK1 ، إعادة توحيد وانقراض ذاكرة IA على المدى الطويل من خلال تنشيط التعبير الجيني كخلايا عصبية إعادة توحيد وانقراض ، على التوالي. على العكس من ذلك ، قد يساهم تنشيط ERK في الخلايا العصبية pCREB- / pERK1 في إلغاء تنشيط النسخ بوساطة CREB والذي سيكون مطلوبًا لإعادة التوحيد نظرًا لأن تنشيط ERK هذا لوحظ تحديدًا في مرحلة الانقراض المتأخرة ؛ تم تنشيط ERK في الخلايا العصبية لإعادة التوحيد لإلغاء تنشيط التعبير الجيني في مرحلة الانقراض. ومن المثير للاهتمام ، أظهرت دراسة سابقة أن تنشيط ERK الحُصيني يمنع تحريض c-fos عندما تنطفئ ذاكرة الخوف السياقية (Guedea et al. ، 2011) ، مما يزيد من احتمال أن يؤدي تنشيط ERK هذا إلى استعداء مسار إشارات CREB. من المهم تحديد مجموعات الخلايا العصبية التي تنظم إعادة التوحيد والانتقال والانقراض والتحقيق في التواقيع الجزيئية والأهمية الوظيفية لتلك الخلايا العصبية. بالإضافة إلى ذلك ، لا تزال التفاعلات بين المجموعات العصبية التي تم تحديدها في هذه الدراسة غير معروفة. من الممكن أن تعدل "عصبونات الانقراض (الانتقال)" وظيفة الخلايا العصبية المعاد توحيدها لإلغاء منع إعادة الاندماج من خلال التفاعلات بينها (Eisenberg et al. ، 2003 ؛ Merlo et al. ، 2014). لذلك ، من المهم أيضًا فحص هذه التفاعلات في وبين اللوزة الدماغية و mPFC والحصين.
سابقًا ، أظهرنا أن الحصين لا يظهر أي تغيير في فسفرة CREB وتعبير القوس بعد تعلم الانقراض للخوف السياقي ، وأن تثبيط تخليق البروتين في الحصين في مرحلة الانقراض يفشل باستمرار في منع الانقراض على المدى الطويل (Mamiya et al. ، 2009). أثارت هذه الملاحظات احتمال أن الحُصين غير مطلوب للانقراض على المدى الطويل. ومع ذلك ، فقد أظهرنا أن ERK يتم تنشيطه في الحُصين بعد تعلم الانقراض لذاكرة IA ، ويؤدي منع تنشيط ERK في الحصين باستمرار إلى إعاقة الانقراض على المدى الطويل. لذلك ، تشير ملاحظاتنا الحالية إلى الأدوار الأساسية للحصين في انقراض الذاكرة. بالاقتران مع النتائج السابقة التي توصلنا إليها ، نقترح أن الحُصين مطلوب لانقراض الذاكرة ولكن ليس لعملية شبيهة بعملية التوحيد لتثبيت "ذاكرة الانقراض" من خلال تنشيط التعبير الجيني.

