نشاط Antinociceptive من Herba Cistanche
Mar 21, 2022
جهة الاتصال: Audrey Hu Whatsapp / hp: 0086 13880143964 البريد الإلكتروني:audrey.hu@wecistanche.com
نشاط مضاد للألم من Cistanche salsa stolons ، ينمو في جمهورية كازاخستان
Elmira B. Kartbaevaa، et al
نبذة مختصرة
هيرباسيستانش(أنواع Cistanche) في الطب الصيني التقليدي يستخدم لعلاج العديد من الأمراض والأعراض ، بما في ذلك الألم. كان الهدف من هذه الدراسة هو تقييم تأثير مضاد مسبب للألم من الهيدرويثانولمقتطف منسيستانشالصلصا(كامي) بيك ، Orobanchaceae ، stolons في نماذج حيوانية من الألم. التركيب الكيميائي لـهيرباسيستانشتم تحليله بواسطة HPLC-UV. تمت معالجة الفئران السويسرية ويبستر (25-30 جم ، ن=6) مسبقًا بالفمهيرباسيستانش(10 ، 30 ، أو 100 مجم / كجم) وتم تقييمها في اختبار الفورمالين وفي استجابة اللعق التي يسببها الكابسيسين أو الغلوتامات. الكازاخستانيةهيربا سيستانشيتكون بشكل رئيسي من جليكوسيدات فينيل بروبانويد ، والتي منهاإشنكوسايد, أكتيوسيد، وتوبولوسيدب هي المكونات الرئيسية. متيهيرباسيستانشتم إعطاؤه للفئران كان له تأثير في كلا مرحلتي اختبار الفورمالين (نشاط 77 بالمائة عند 30 مجم / كجم للمرحلة الأولى و 62 بالمائة من النشاط عند 100 مجم / كجم للمرحلة الثانية) مما يشير إلى خصائص مسكنة ومضادة للالتهابات. الكازاخستانيةهيرباسيستانشكان قادرًا على تقليل وقت لعق الحيوانات بعد حقن الجلوتامات (انخفاض بنسبة 81 بالمائة عند 30 مجم / كجم) والكابسيسين (تقليل بنسبة 81 بالمائة عند 100 مجم / كجم). نستنتج أن الفينولات الموجودة في المستخلص المائي الإيثانولي من C. salsa يمكن أن تكون مسؤولة عن ملفها الدوائي. من أجل الحصول على مادة خام عالية الجودة للطب الصيني التقليدي ، أوصينا باستخدام هذه الأنواع الكازاخستانيةإشنكوسايد و أكتيوسيدكعلامات.
الكلمات الدالة:هيربا سيستانش ،HPLC-UV ،إشيناكوسايد ، أكتيوسيد, توبولوسيدالتوحيد
مقدمة
سيستانشالصلصا(CA Mey) Beck ، Orobanchaceae ، هو نبات طفيلي من جمهورية كازاخستان حيث يتم استخدامه كمادة أولية صناعية (Sarsenbayev et al. ، 2011 ؛ Grudzinskaya and Gemedzhieva ، 2012). تتعلق القيمة العلمية لهذه العشبة في الطب الصيني التقليدي بعلاج مشاكل الكلى (التي تتراوح من الألم إلى القصور) ، والعجز الجنسي ، والعقم عند النساء ، وسيلان الدم المرضي ، ونزيف المريء الغزير ، والإمساك الخرف (قاموس كلية جيانغسو الطبية الجديدة للأدوية الصينية التقليدية ، 1977 ؛ الأعشاب الطبية الصينية ، 1988). التركيب الكيميائي ل stolons من الأنواع الأخرى منسيستانشتم بالفعل دراسة تفصيلية من قبل العلماء الصينيين. تم تحديد المركبات الفينولية التالية:إشنكوسايد, توبولوسيد, أكتيوسيد، إلى جانب قشور ، إيريدويد ، وعديد السكاريد المعقد (Yong andTu ، 2009 ؛ Zhang et al. ، 2003 ؛ Xie et al. ، 2005 ؛ Jiang et al. ، 2009 ؛ Suiet al. ، 2011 ؛ Liu et al. ، 2013 ؛ Zhou et al. ، 2014).
شيمودا وآخرون (2009) أن هذه العشبة تمتلك تأثير نقص الكوليسترول في الدم بينما Yang et al. (2013) حدد نشاطه الكبدي. نان وآخرون. (2013) عن نشاط مضاد للالتهابات لمستخلصاته. أظهر عديد السكاريد المعقد المعزول سابقًا من هذا النبات تأثيرات مناعية (وانج وآخرون ، 2009).
على الرغم من وجود قدر كبير منسيستانشstolons في جمهورية كازاخستان ، لا يوجد استخدام شائع لهذا النبات من قبل سكان كازاخستان على الرغم من أن الجيران في الصين يستخدمونه على نطاق واسع. نظرًا لوجود مشكلة كبيرة في الوقت الحاضر فيما يتعلق باستبدال / غش النباتات الطبية والحاجة المتزايدة لتوحيد الأدوية المستخدمة في الطب الصيني التقليدي ، فقد تم تصميم هذه الدراسة للتأكد من التركيب الكيميائي الفينولي لهذه المادة النباتية الخام التي تنمو في كازاخستان المجاورة وكذلك لتقييم استخدامه كمضاد للألم لتخفيف الألم - وهو ما يميز أحد الاستخدامات الرئيسية له في الطب الصيني التقليدي.
المواد والأساليب
المواد النباتية
سيستانشالسالسا (CAMey.) بيك ، Orobanchaceae ، تم جمع stolons في صحراء Moinkum ، قرية Bakanas ، في يوليو 2014 في ألماتي. تم التعرف على المادة النباتية من قبل الدكتور ج. سيتباييف من معهد علم النبات والإنتاج النباتي ، وزارة التعليم والعلوم في جمهورية كازاخستان حيث تم إيداعها تحت الرقم 01-04 / 306.
تحليل كيميائي
تم إخضاع ستولونات من C. salsa (2 جم) لاستخلاص الميكروويف. في البداية ، تم طحن المادة إلى 0. 0 0 1-2. 000 ملم ثم تم وضعها في وعاء محكم ليتم استخلاصها لمدة 0 دقيقة عند 1 0 0-1100 درجة مئوية مع إيثانول 80 بالمائة (نسبة 1:10). تم تحليل الاستخراج المائي الإيثاني (CSHE) بواسطة HPLC-MS. تمت إذابة المستخلص الخام في ميثانول (9.6 مجم / مل) وترشيحه من خلال غشاء تفلون 0.45 مم قبل التحليل. كروماتوجراف سائل طراز HP 1100 Series (شركة Agilent Technologies ، Inc. ، CA ، الولايات المتحدة الأمريكية) ، مزود بمزيل غاز متدفق ، ومضخة متدرجة للضغط بأربعة قنوات ، وحاقن تلقائي. تم فصل المركبات الفينولية كروماتوجرافيًا بواسطة عمود Zorbax Eclipse XDB-C18 ، 2.1 × 50 مم ، مملوءة ببوليمر هلام السيليكا octadecylsilyl (1.8). تم إجراء التحليل الكروماتوغرافي باستخدام تدفق طور متحرك قدره 0.2 مل / دقيقة ، وضغط تشغيل شاذ يبلغ 175-200 كيلو باسكال ، ودرجة حرارة فرن العمود 30 درجة مئوية ، وحجم عينة 2 مل ، ووضع تغذية شطف متدرج: 0-36 دقيقة 10 بالمائة A - 90 بالمائة ب ؛ 36 دقيقة - 100 بالمائة ب (eluent A: ميثانول ، eluent B: 0.2 بالمائة محلول حمض الفورميك). تم إجراء الكشف بواسطة الأشعة فوق البنفسجية بأطوال موجية 254 و 334 و 350 و 410 و 450 و 550 نانومتر. تم استخدام مقارنة أوقات الاحتباس التي تم الحصول عليها والأشعة فوق البنفسجية وأطياف الكتلة مع تلك الخاصة بالمركبات المرجعية لتحديد المركبات الكيميائية في المستخلص. تم إجراء التحليل الكمي باستخدام المعيارفيرباسكوسايدوإشنكوسايدتحليلها تحت نفس الظروف الكروماتوغرافية. سمحت منحنيات المعايرة الخاصة بهم بحساب كمية كل من جليكوسيد فينيل بروبانويد الآخر في مستخلص الإيثانول لهذا النبات. لم يتم التحقق من صحة الطريقة.

الحيوانات
تم استخدام فئران ويبستر السويسرية (20-25 جم ، شهرين من العمر) في هذه الدراسة (تم التبرع بها من قبل Instituto Vital Brazil ، Niterói ، RJ ، البرازيل). تم الاحتفاظ بالحيوانات في ظروف قياسية (دورة مظلمة فاتحة تبلغ 12 ساعة ، 22 ± 2 درجة ، ورطوبة 70-80 في المائة. طعام وماء إعلان بالشهرة). حصلت الحيوانات على الماء فقط من أجل تجنب تدخل الغذاء في امتصاص المواد قبل 12 ساعة من بدء التجارب. حدث التأقلم مع ظروف المختبر لمدة ساعة واحدة على الأقل قبل كل اختبار. تم إجراء جميع البروتوكولات وفقًا للمبادئ التوجيهية الخاصة بالمعايير الأخلاقية للتحقيق في الألم التجريبي في الحيوانات واتبعت المبادئ والإرشادات التي اعتمدها المجلس الوطني للتحكم في التجارب على الحيوانات (CONCEA) ، والتي وافق عليها معهد العلوم الطبية الحيوية / UFRJ ، الأخلاقية لجنة أبحاث الحيوان ، وحصلت على رقم DFBCICB 015-04 / 16. تم تنفيذ جميع البروتوكولات التجريبية خلال مرحلة الضوء. تم الاحتفاظ بأرقام الحيوانات لكل مجموعة كحد أدنى ووفقًا لقواعد CONCEA. في نهاية كل تجربة ، قُتلت الفئران بجرعة زائدة من الكيتامين / زيلازين.
العلاجات
في هذه الدراسة ، تم تقييم CSHE عند 10 و 30 و 100 ملغم / كغم. تمت إذابة المستخلص في ثنائي ميثيل سلفوكسيد (DMSO ، FisherBiotech) من أجل تحضير محلول مخزون عند 100 مجم / مل. تم استخدام PBS كمخفف لتحضير الجرعات المختلفة. محاليل تحتوي على 10 و 30 و 100 ملغم / كغم من مستخلص الهيدرويثانولسيستانشالصلصاتم تحضيرها. كانت الأدوية القياسية المستخدمة هي المورفين 2.5 مجم / كجم (Merck ، المخفف في محلول ملحي للفوسفات (PBS)) ، وحمض أسيتيل الساليسيليك 2 0 0 مجم / كجم (Sigma Aldrich ، مذاب مع 5 M من هيدروكسيد الصوديوم (NaOH) في 0.9 في المائة من محلول ملحي) وكبسازيبين 10 نانومولبر باو. أعطيت Saline plus DMSO (بنفس التركيز كما في أعلى معاملة بالمستخلص) لمجموعة التحكم السلبية. تم إعطاء جميع العلاجات (المستخلص والمعايير المختبرة) عن طريق الفم. كان الاستثناء الوحيد هو الكبسازيبين الذي تم إعطاؤه عن طريق الحقن داخل العظم.
الآلام الحادة التي يسببها الفورمالين
تم حقن محلول من 2.5 بالمائة فورمالين (37 بالمائة فورمالدهيد) (20 مايكرولتر) في المنطقة الأخمصية من القدم الخلفية اليمنى للفئران بعد العلاج 60 دقيقة (مستخلص الهيدرويثانول منسيستانشالصلصاأو acetylsalicylicacid 2 0 0 مجم / كجم أو المورفين 2.5 مجم / كجم) (Matheus et al.، 2005). تم وضع الثيانيمالات بشكل فردي في حجرة زجاجية شفافة وتم تسجيل المدة الزمنية بالثواني التي أمضوها في لعق حقن الفورمالين الخاص بهم وتحليلها على فترتين منفصلتين ، المرحلة المبكرة من الألم العصبي (0-5 دقائق بعد الحقن) والمرحلة المتأخرة- الألم الالتهابي (15-30 دقيقة بعد الحقن).
الشعور بالألم الناجم عن الكابسيسين
اعتمد هذا الاختبار على الطريقة التي وصفها ساكورادا وآخرون مع بعض التعديلات (ساكورادا وآخرون ، 1992). تم حقن الكابسيسين (20 مايكرولتر) C18H27NO3 (جالينا ، كامبيناس ، SP) في المنطقة الأخمصية للقدم الخلفي الأيمن للفئران (1.6 ميكروغرام / مخلب) بعد علاج واحد (مستخلص الهيدرويثانول منسيستانشالسالسا أو capsazepine1 0 nMol / paw). تم وضع الحيوانات بشكل فردي في غرفة زجاجية وتم تسجيل مدة (فترات) لعق المخالب بين 0 و 5 دقائق بعد حقن الكابسيسين ثم تحليلها.
الشعور بالألم الناجم عن الغلوتامات
في الطريقة التي وصفها بيريث وآخرون. (2002) ، تم حقن محلول الغلوتامات في PBS (20 ميكرولتر) (حمض الجلوتاميك L ، Sigma-Aldrich ، 3.7 نانوغرام / مخلب) في المنطقة الأخمصية من القدم الخلفية اليمنى للفئران بعد ساعة واحدة من العلاج (مستخلص الهيدرويثانول منسيستانشالسالسا أو المورفين 2.5 مجم / كجم). تم وضع الحيوانات بشكل فردي في غرفة زجاجية وتم تسجيل مدة لعق المخالب (بالثواني) بين 0 و 15 دقيقة بعد حقن الغلوتامات ثم تحليلها.
تحليل احصائي
يتم تقديم البيانات الكيميائية على أنها متوسط ± SD لخمس تجارب. تتكون جميع المجموعات التجريبية الدوائية من ستة فئران كحد أدنى. سمح تحليل التباين أحادي الاتجاه (ANOVA) متبوعًا باختبار Dunnett بتصور الأهمية الإحصائية بين المجموعات باستخدام برنامج GraphPad Prism 5. 0. تم اعتبار القيم pvalues هامة عندما كانت أقل من 0. 0 5 (p <>
نتائج
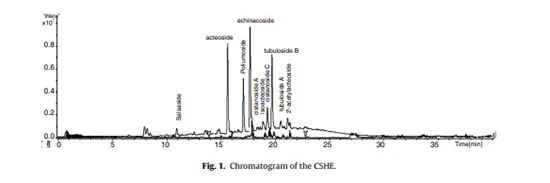
سيستانشيظهر في الشكل 1. مستخلص هيدرويثانول السالسا (تخفيفان مختلفان) كروماتوجرام. يوضح الجدول 1 تحديد المركبات الفينولية مع فترات الاحتفاظ الخاصة بها في مخطط الكروماتوجرام.

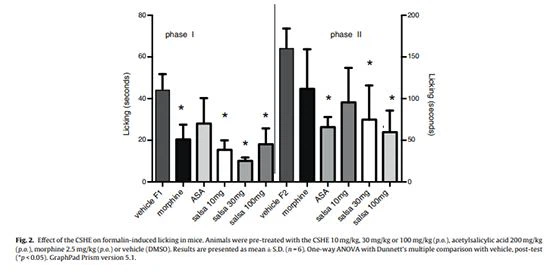
تأثير CSHE على الآلام الحادة التي يسببها الفورمالين
في اختبار الألم الحاد الناجم عن الفورمالين ، كان CSHE عند 10 و 30 و 100 ملغم / كغم قادرًا على تقليل لعق الكف في المرحلة الأولى من الاختبار المعروف باسم مرحلة الألم العصبي ، كانت هذه التخفيضات 60 و 77 و 58 بالمائة على التوالي . بالإضافة إلى ذلك ، كانت فعالة أيضًا في تقليل الألم الالتهابي الناتج خلال المرحلة الثانية من الاختبار ، وكانت النسبة المئوية لتثبيط الألم الالتهابي 42 و 46 و 62 بالمائة على التوالي (الشكل 2). قدم المورفين (2.5 مجم / كجم) وحمض أسيتيل الساليسيليك (200 مجم / كجم) النتائج التالية: 55 بالمائة / 33 بالمائة و 31 بالمائة / 54 بالمائة للمرحلتين الأولى والثانية على التوالي.
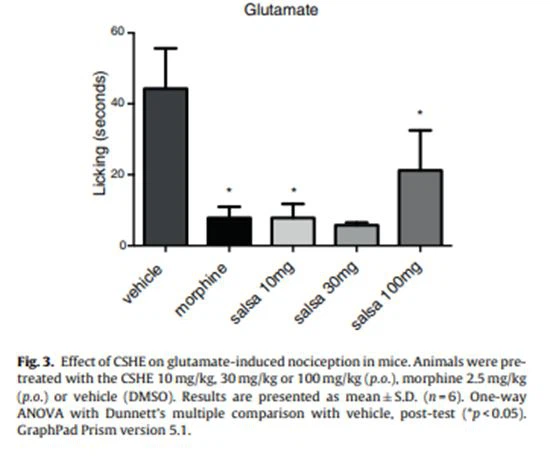
تأثير CSHE على الألم الناجم عن الغلوتامات
قلل CSHE اللعق الناجم عن الغلوتامات عند الجرعات الثلاثة التي تم اختبارها ، 10 و 30 و 100 ملغم / كغم بنسبة 76 و 81 و 53 بالمائة على التوالي (الشكل 3). المورفين بنسبة 2.5 في المائة أدى إلى انخفاض بنسبة 76 في المائة
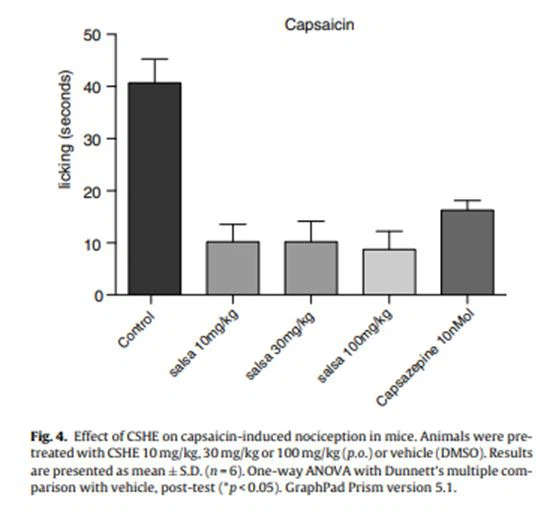
تأثير CSHE على الشعور بالألم الناجم عن الكابسيسين
من أجل التحقق مما إذا كان CSHE سيؤثر على الشعور بالألم من خلال مستقبلات TRPV1 ، تم اختباره في نموذج للألم الناجم عن الكابسيسين. لوحظ تأثير مضادات مستقبلات الذقن من خلال هذا النموذج للـ CSHE في الجرعات الثلاث المختبرة ، بنسبة 76 و 79 و 81 بالمائة على التوالي (الشكل 4). أدى Capsazepine 10 nMol / paw إلى انخفاض بنسبة 60 بالمائة.
مناقشة
تم تحديد ما مجموعه عشرة جلوكوزيدات فينيل بروبانويد في مستخلص هيدروإيثانول C. salsa (ينمو في كازاخستان).إشيناكوسايد(10.98 مجم / جم) ،أكتيوسيد(9.44 مجم / جم) و tubuloside B (7.94 مجم / جم) كانت المركبات الرئيسية المحددة. ارتبطت البيانات التي تم الحصول عليها مع الأدبيات المتاحة لأنواعسيستانشتنمو في مناطق مختلفة من آسيا (Zhou et al. ، 2014 ؛ Xieet al. ، 2005 ؛ Jiang et al. ، 2009).إشيناكوسايدوأكتيوسيدهي المكونات الرئيسية التي تشكل الأساس لتوحيد الأنواع المحليةسيستانشالصحراء وسيستانشtubulosa ، المدرجة في دستور الأدوية الصيني في 2005. نقترح أن هذه المركبات يمكن أن تستخدم أيضًا لتوحيدسيستانشالسالسا ستولونس من كازاخستان ، حيث أنها الرئيسية في استخراج الإيثانول المائي المدروس.
وفقًا للنتائج الدوائية لهذه الدراسة ، من الممكن أن نقترح أن CSHE عامل فعال ضد الألم العصبي والالتهاب كما لوحظ في اختبار الفورمالين. أفضل ما نعرفه،سيستانشلم يتم اختبار السالسا فيما يتعلق بأفعالها المضادة للألم. دراسة من عام 2002 معسيستانشأظهر Deserticola (Lin et al. ، 2002) أن هذا النبات يقدم أنشطة مضادة للألم ومضاد للالتهابات عند تقييمه في نماذج مثل التلوي الكلي ، وذمة مخالب الفورمالين. على الرغم من عدم وجود محاولة لفحص المكونات الرئيسية في المستخلص التي كانت نشطة ، فقد اعتبروا أن مستخلص البيوتانول وطبقة الماء هي المكونات النشطة. ليس من المستغرب أن تكون هذه المذيبات مقياس قطبية يتطابق مع جليكوسيدات فينيل بروبانويد الموجود فيسيستانشالصلصا. علاوة على ذلك ، أثبت لين وزملاؤه أن التأثير المضاد للألم لـسيستانشلم تكن مستخلصات الجرجير بسبب تأثير المركب في مستقبلات الأفيون أو مرتبطة بجهاز المناعة. في دراستنا ، أظهر المستخلص الغني بالفينيل بروبانويد نشاطًا في مرحلتي اختبار الفورمالين. كان النشاط الذي تمت ملاحظته يرجع في الواقع إلى الهدف الدوائي الذي تم فحصه وليس إلى أي تغيير محتمل في المحرك كما يتضح من اختبار ثيروتارود. تشير نتائج اختبار الفورمالين إلى احتمال حدوث ألم عصبي بالإضافة إلى الألم الناجم عن وسطاء التهابية. في البداية ، قررنا التحقيق في مسار الألم العصبي. نظرًا لأن المركبات المماثلة من الأنواع الأخرى التي تمت دراستها سابقًا لم تظهر أي نشاط لمستقبلات الأفيون ، فقد قررنا اختبار نماذج أخرى ، مثل نماذج الجلوتامات والكابسيسين.
الغلوتامات هو ناقل عصبي مثير له دور مهم في تعديل الألم في جميع أنحاء الجهاز العصبي المحيطي والمركزي. يتم التوسط في هذا الإجراء عن طريق مستقبلات الغلوتامات المتضاربة بالبوابات (iGluRs) ومستقبلات الغلوتامات الأيضية. يمكن تقسيم iGluRs إلى N-methyl-d-aspartate (NMDA) و -amino -3- hydroxy -5- methylisoxazole -4- propionicacid (AMPA) (Kolber ، 2015). أظهرت الأبحاث أنه عند استعداء مستقبلات NMDA و AMPA مع الكيتامين والكينات ، على التوالي ، لوحظت تأثيرات مضاد للألم. ومع ذلك ، فإن المضادات التي تستهدف هذه المستقبلات قد تسببت حتى الآن في حدوث تأثير ضار كبير ولهذا السبب ، يركز بحث جديد على mGluRshoping حيث أن الدواء الذي يتم توسطه من خلال هذا المستقبل قد يتسبب في حدوث آثار جانبية أقل (Palazzo et al. ، 2014). أظهرت نتائج اختبار CSHE أن هذا العلاج كان فعالًا في تقليل الألم الناجم عن الجلوتامات. ومع ذلك ، لا يزال من غير المعروف ما إذا كان هذا التأثير يتم توسطه من خلال مستقبلات التأين و / أو مستقبلات التمثيل الغذائي. المورفين هو أحد الأدوية المتاحة التي لها تأثير على انتقال الجلوتامات (Deyama et al. ، 2007). تم الإبلاغ في الأدبيات أن تنشيط مستقبلات الجلوتامات يزيد من استجابة TRPV1 (Szteyn et al. ، 2015). لهذا السبب ، من الممكن أن يكون التأثير الملحوظ لـ CSHE ناتجًا عن نشاط على TRPV1 وليس بالضرورة من خلال استجابة مباشرة على مستقبلات الغلوتامات.
كانت الخطوة التالية من هذا البحث هي إجراء اختبار لعق المخالب باستخدام الكابسيسين كعامل مؤثر ، وهو ناهض مستقبلات TRPV1. أظهرت النتائج أن CSHE بالفعل قلل من الألم من خلال مستقبل TRPV1.
في حالة CSHE ، في جميع المنهجيات المختبرة تقريبًا ، يمكن ملاحظة أن جرعة 30 مجم / كجم حققت نتيجة أفضل من 100 مجم / كجم. يمكن أن يكون هذا بسبب تشبع المحلول الذي يقود إلى المركبات المترسبة وكمية أقل من الأدوية المتاحة بيولوجيًا.
كان تأكيد التركيب الكيميائي المستقر لمستخلص كازاخ CSHE خطوة مهمة لأن المكونات الرئيسية الموجودة فيه قد تم بالفعل تأكيد تأثيرها المضاد للالتهاب / مضادات الالتهاب بطريقة ما.إشنكوسايدكواحد من المبادئ الفعالة المسؤولة عن التأثير المضاد للألم لإشنسا (هوستتمان ، 2003). كما أشارت دراسة سابقة قام بها شابوفال وزملاؤه (شابوفال وآخرون ، 1998) إلى ذلكأكتيوسيدكأحد المكونات النشطة الرئيسية في مستخلص الإيثانول المحضر مع Stachytarpheta cayennensis كما تم تقييمه بواسطة وذمة المخلب ونماذج الألواح الساخنة. Backhouse and co-work (Backhouse et al.، 2008) كذلكأكتيوسيدليكون المبدأ النشط لـ Buddleja globosausing العديد من نماذج تقييم الألم ، بما في ذلك اختبار الفورمالين. يتم الآن تطوير تركيبات جديدة باستخدام حالة معرفة القلب لزيادة الاستقرار وإطالة تأثير antinociceptiveaأكتيوسيد(Isacchi et al.، 2016).

استنتاج
تم التعرف على عشرة مواد ذات طبيعة فينولية في ستولونس الكازاخستانيةسيستانشالسالسا عن طريق تحليل HPLC / MS. يمكن أن تكون هذه المركبات مسؤولة عن نشاط مضادات التقرن التي لوحظت في النماذج التجريبية التي تم إجراؤها هنا. مع الأخذ بعين الاعتبار أن على أراضي كازاخستان الجنسسيستانشيتم تمثيلها بشكل رئيسي من قبل الأنواعسيستانشالسالسا ، يمكننا أن نوصي بحصادها وتوحيدها باستخدامإشنكوسايدوأكتيوسيدكمركبات قياسية ، لمصدر مادة خام ذات نوعية جيدة للطب التقليدي الصيني.
الإفصاحات الأخلاقية
حماية الإنسان والحيوان. يعلن المؤلفون أن الإجراءات المتبعة كانت متوافقة مع لوائح لجنة أخلاقيات البحث الإكلينيكي ذات الصلة ومع تلك الواردة في مدونة أخلاقيات الجمعية الطبية العالمية (إعلان هلسنكي).
سرية البيانات.
يعلن المؤلفون أنه لا توجد بيانات مريض تظهر في هذه المقالة.
الحق في الخصوصية والموافقة المستنيرة. يعلن المؤلفون أنه لا توجد بيانات مريض تظهر في هذه المقالة.
مساهمات المؤلفين
قام EBK بجمع المصنع وإعداد الاستخراج وتحليل النتائج الكيميائية بالإضافة إلى كتابة الورقة ؛ GRD ، نفذت جميع الاختبارات الدوائية ؛ ZBS ، صمم الدراسة بالاشتراك مع FB ؛ LNI و ENB ، شاركوا في تصميم الأدوية الخاصة بالدراسة لإدراج النتائج التي تم الحصول عليها في دستور الأدوية الكازاخستاني ؛ IIT ، نفذت تحليلات HPLC ؛ قام PDF ، بتصميم الدراسة الدوائية و FB ، بتنظيم الفريق معًا من أجل كتابة هذه الورقة.
تضارب المصالح
أعلن المؤلفون أنه لا يوجد اختلاف في الاهتمامات.
شكر وتقدير
يشكر المؤلفون من البرازيل السيد آلان مينهو على المساعدة التقنية ومعهد البرازيل الحيوي للتبرعات بالحيوانات المستخدمة. كما يريدون الاعتراف بالمنح المقدمة من CNPq و Fundac¸ ão Carlos Chagas Filho de Apoio à Pesquisa do Estadodo Rio de Janeiro. يرغب المؤلفون من أيرلندا في الاعتراف ببرنامج البحوث التابع لهيئة التعليم العالي في مؤسسات المستوى الثالث بالدعم التمويلي للدورة الخامسة لـ TBSI ولتعزيز أهمية برنامج SFI ISCA-Brazil (المنحة. SFI / 13 / ISCA / 2843) الذي ساهم في العمل التعاوني بين البرازيل وايرلندا. الكتاب من كازاخستان يريدون الاعتراف بـ KazNMU للدعم المالي المسموح به لتنفيذ هذا العمل.
من: "النشاط المضاد للألم من Cistanche salsa stolons ، المتنامي في جمهورية كازاخستان" بواسطة Elmira B. Kartbaevaa ، وآخرون
--- إي بي كارتبايفا وآخرون / Revista Brasileira de Farmacognosia 27 (2017) 587-591
مراجع
Backhouse، N.، Delporte، C.، Apablaza، C.، Farias، M.، Goïty، L.، Arrau، S.، Negrete، R.، Castro، C.، Miranda، H.، 2008. Antinociceptive activity of Buddleja globose (ماتيكو) في عدة نماذج للألم. ياء إثنوفارماكول. 119 ، 160–165.
Beirith، A.، Santos، ARS، Calixto، JB، 2002. الآليات الكامنة وراء الشعور بالألم ووذمة المخلب الناتجة عن حقن الغلوتامات في مخلب الفأر. Res الدماغ. 924 ، 219-228.
الأكاديمية الصينية للعلوم الطبية ، 1988. معهد النباتات الطبية ، الأعشاب الطبية الصينية ، المجلد. 4. ، الطبعة الثانية. دار النشر الطبية الشعبية ، بكين.
Deyama، S.، Yamamoto، J.، Machida، T.، Tanimoto، S.، Nakagawa، AT، Kaneko، S.، Satoh، M.، Minami، M.، 2007. تثبيط انتقال الجلوتاماتيرج عن طريق المورفين في الجانب السفلي تقلل نواة اللوزة من النفور الناجم عن الألم. نيوروسسي. الدقة. 59 ، 199-204.
Grudzinskaya، LM، Gemedzhieva، NG، 2012. قائمة النباتات الطبية في كازاخستان. دار النشر التابعة لمعهد علم النبات و Phytointroduction من RK ، ألماتي.
Hostettmann ، K. ، 2003. تاريخ النبات: مثال إشنسا. فورش كومب. كلاس. نات. ملحق. 1 ، 9-12.
Isacchi، B.، Bergonzi، MC، Iacopi، R.، Ghelardini، C.، Galeotti، N.، Bilia، AR، 2016.
تركيبة دهنية لزيادة الاستقرار وإطالة النشاط المضاد للاعتلال العصبي من فيرباسكوسايد. بلانتا ميد. 83 ، 412-419.
Jiang، Y.، Li، SP، Wang، YT، Chen، XJ، Tu، PF، 2009.هيرباسيستانشعن طريق بصمات الأصابع مع مطياف الكتلة اللوني السائل عالي الأداء. تشروماتوجر. 1216 ، 2156-2162.
قاموس كلية جيانغسو الطبية الجديدة للأدوية الصينية التقليدية ، 1977. الطبعة الأولى ، ناشر شنغهاي العلمي والتكنولوجي ، شنغهاي.
كولبر ، BJ ، 2015. mGluRs من الرأس حتى أخمص القدمين من الألم. بروغ. مول. بيول. ترجمة. 131 ، 281-324.
Lin، LW، Hsieh، MT، Tsai، FH، Wang، WH، Wu، CR، 2002. النشاط المضاد للألم والمضاد للالتهابات الناجم عن Cistanche deserticola في القوارض. ياء إثنوفارماكول. 83 ، 177-182.
Liu، XM، Li، J.، Jiang، Y.، Zhao، MB، Tu، PF، 2013. المكونات الكيميائية من Cistanche Sinensis (Orobanchaceae). بيوتشيم. النظام. ايكول. 47 ، 21-24.
Matheus، ME، Berrondo، LF، Vieitas، EC، Menezes، FS، Fernandes، PD، 2005. تقييم الخواص المضادة للمسببات من مستخلصات السيقان Brillantaisia palisotii Lindau. ياء إثنوفارماكول. 102 ، 377-381.
Nan، ZD، Zeng، KW، Shi، SP، Zhao، MB، Jiang، Y.، Tu، PF، 2013. جليكوسيدات فينيلثانويد مع أنشطة مضادة للالتهابات من سيقان Cistanche deserticola المستزرعة في صحراء تاريم. فيتوتيرابيا 89 ، 167–174.
Palazzo، E.، Marabese، I.، de Novellis، V.، Rossi، F.، Maione، S.، 2014. مستقبلات الغلوتامات فوق النخاع الشوكي: هدف لتخفيف الآلام وما بعدها. يورو. J. نيوروسسي. 39 ، 444-454.
Sakurada، T.، Katsumata، K.، Tanno، K.، Sakurada، S.، Kisara، K.، 1992. اختبار الكابسيسين في الفئران لتقييم مضادات التاكيكينين في الحبل الشوكي. علم الأدوية العصبية 31 ، 1279-1285.
Sarsenbayev، KN، Isabaev، SO، Kolosov، NG، 2011. وقائع المؤتمر العلمي الدولي "الحالة البيئية الحديثة لمنطقة بحر الآرال ، آفاق حل المشكلات" ، كيزيلوردا ، ص 195 - 200.
Schapoval، EES، Vargas، MRW، Chaves، CG، Bridi، R.، Zuanazzi، JA، Henriques، AT، 1998. الأنشطة المضادة للالتهابات ومضادات التعرق من المستخلصات والمركبات المعزولة من Stachytarpheta cayennensis. ياء إثنوفارماكول. 60 ، 53-59.
Shimoda، H.، Tanaka، J.، Takahara، Y.، Takemoto، K.، Shan، SJ، Su، MH، 2009. تأثيرات نقص الكولسترول لمستخلص Cistanche tubulosa ، وهو دواء خام صيني تقليدي ، في الفئران. أكون. J. تشين. ميد. 37 ، 1125-1138.
Sui، ZF، Gu، TM، Liu، B.، Peng، SW، Zhao، ZL، Le، L.، Shi، DF، Yang، RY، 2011. مركب كربوهيدرات قابل للذوبان في الماء من أجسامهيرباسيستانش: العزل وتأثيره الكاسح على الجذور الحرة في الجلد. الكربوهيدرات. بوليم. 85 ، 75-79.
Szteyn، K.، Rowen، MP، Gomez، R.، Du، J.، Carlton، SM، Jeske، NA، 2015. ينسق بروتين A-kinase المثبت 79/150 تحسس مستقبلات الغلوتامات الأيضية للخلايا العصبية الحسية المحيطية. الألم 156 ، 2364-2372.
Wang، XY، Qi، Y.، Cai، RL، Li، XH، Yang، MH، Shi، Y.، 2009. تأثير Cistanche deserticola polysaccharides (CDPS) على تنشيط البلاعم. ذقن. فارماكول. ثور. 25 ، 787-789.
Xie، JN، Zhao، MB، Wu، FW، Tu، PF، 2005. البصمة الكروماتوغرافية لـ Cistanche deserticola بواسطة HPLC. ذقن. طراد عشب. المخدرات 36 ، 268-271.
Yang، FR، Wen، DS، Fang، BW، Lou، JS، Meng، L.، 2013. الوقاية من مستخلص السالسا الكبدي على التليف الكبدي الناجم عن رابع كلوريد الكربون في الفئران. ذقن. عشب. ميد. 5 ، 199-204.
Yong، J.، Tu، PF، 2009. تحليل المكونات الكيميائية في أنواع Cistanche. تشروماتوجر. 1216 ، 1970-1979.
Zhang، X.، Li، X.، Rena، K.، Du، NS، 2003. RP-HPLCأكتيوسيدفيهيرباسيستانشالمزروعة على أنواع وموائل طفيلية مختلفة. ذقن. J. فارم. شرجي. 23 ، 254-256.
Zhou، J.، Zhang، Q.، Bing Sun، J.، Li Sun، X.، Zeng، P.، 2014.إشنكوسايد, توبولوسيد B, أكتيوسيدو isoacteoside في بلازما الفئران بعد تناول مستخلص Cistanche salsa عن طريق الفم بواسطة كروماتوجرافيا سائلة عالية الأداء. J. فارم. بيوميد. شرجي. 94 ، 30–35.



