مسار الالتهام الذاتي والليزوزومي كهدف علاجي محتمل في مرض باركنسون
Jun 28, 2022
الرجاء التواصلoscar.xiao@wecistanche.comللمزيد من المعلومات
الملخص:اكتسبت أنظمة مراقبة الجودة الخلوية الكثير من الاهتمام في العقود الأخيرة. من بين هذه ، الالتهام الذاتي هو آلية طبيعية للحفاظ على الذات تقضي باستمرار على المكونات الخلوية السامة وتعمل كعملية لمكافحة الشيخوخة. إنه أمر حيوي لبقاء الخلية والحفاظ على التوازن. تم الإبلاغ عن العديد من مسارات الالتهام الذاتي المعتمدة على نوع الخلية والتي تظهر درجات متفاوتة من الانتقائية فيما يتعلق بالركائز المستهدفة. نقدم هنا مراجعة محدثة لآلية الالتهام الذاتي ونناقش دور الأشكال المختلفة من الالتهام الذاتي في الأمراض التنكسية العصبية ، مع التركيز بشكل خاص على مرض باركنسون. نصف النتائج الأخيرة التي أدت إلى اقتراح استراتيجيات علاجية تستهدف الالتهام الذاتي لتغيير مسار تطور مرض باركنسون.
الكلمات الدالة:الالتهام الذاتي. الجسيمات المحللة؛ مرض التنكس العصبي. مرض الشلل الرعاش؛ المناعة الذاتية

الرجاء الضغط هنا لمعرفة المزيد
1 المقدمة
على الرغم من وصف بعض عناصر مرض باركنسون (PD) منذ وقت طويل جدًا ، فقد نشر جيمس باركنسون أول وصف طبي واضح لهذا المرض في عام 1817 [1]. منذ ذلك الحين ، بُذلت جهود كبيرة لفهم العوامل المرضية الكامنة وراء هذا المرض المعقد ، من حيث التغيرات العصبية المرضية والتشريحية المرضية [2-5]. PD هو مرض متعدد العوامل مع عوامل مسببة غير متجانسة ، بما في ذلك المكونات الجينية والبيئية والجزيئية والخلوية. يتميز شلل الرعاش بمجموعة واسعة من العلامات والأعراض الحركية وغير الحركية. وهي تشمل رعاش الراحة ، وبطء الحركة ، وعدم الاستقرار الوضعي / المشية غير المستقرة ، والصلابة ، إلى جانب الاضطرابات النفسية ، واضطرابات النوم ، واضطرابات خلل الحركة ، والألم ، وفقدان حاسة الشم ، والاضطرابات المعرفية. تنتج العلامات الحركية في المقام الأول عن فقدان الخلايا العصبية الدوبامينية (DA) في المادة السوداء بارس مضغوطة (SNpc) والشوائب داخل الخلايا من السينوكلين المجمعة وغير المطوية (c-syn) ، المغلفة أو غير المغلفة في أجسام ليوي (LB) وعصابات ليوي ( LN) في الخلايا العصبية [3،6] (الشكل 1 ؛ انظر الملحق لمعرفة التعريف).
تتطور أعراض شلل الرعاش تدريجيًا مع تقدم العمر.ما هو الكفالةيمكن أن تبدأ بهزة خفيفة في يد واحدة وشعور بالصلابة في الجسم ؛ بطء الحركة متكرر. تؤكد الدراسات الحديثة أن أكثر من 3 في المائة من عامة السكان من سن 65 عامًا يعانون من شلل الرعاش. ولكن في 5 بالمائة -10 بالمائة من الحالات ، تظهر أعراض شلل الرعاش مبكرًا ؛ يشار إلى هذا باسم PD (YOPD). الرجال أكثر عرضة بنسبة 50 في المائة للإصابة بمرض شلل الرعاش مقارنة بالنساء ، ولكن يبدو أن الخطر على النساء يزداد مع تقدم العمر.
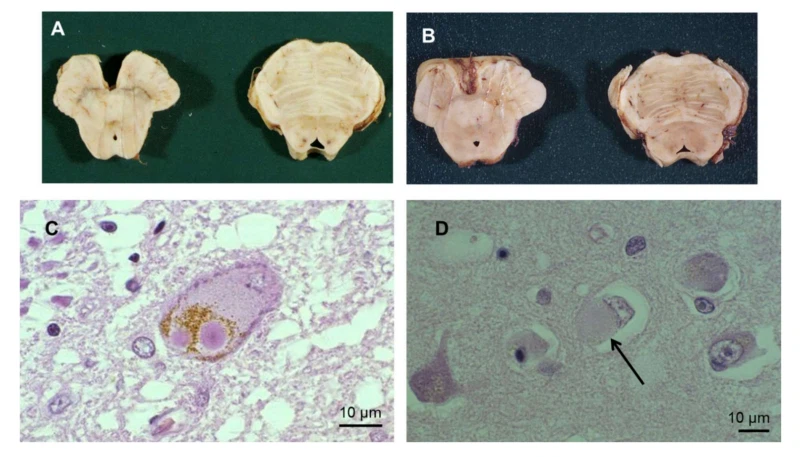
الشكل 1. النتائج العصبية المرضية في مرض باركنسون. (أ ، ب) الدماغ المتوسط بعد الوفاة والجسور من مريض تحكم (أ) ومن مريض مصاب بالتهاب المفاصل الروماتويدي (ب): ظهر SN شاحبًا في ب بسبب إزالة التعصيب الدوباميني. (C) ، تلطيخ SN ، H&E (× 250) (D): تلطيخ H&E (× 250) من LB في الخلايا العصبية القشرية. يظهر السهم الأسود LB. الاختصارات غير الموصوفة في النص: H&E و hematoxylin و eosin.
لا يزال السبب الجذري لمرض باركنسون غير معروف إلى حد كبير.بيوفلافونويدستم ربط بعض حالات شلل الرعاش بالطفرات الجينية ، ولكن يصعب تحديد الأسباب الوراثية الواضحة لهذا المرض. في الواقع ، 15 بالمائة فقط من مرضى شلل الرعاش لديهم تاريخ عائلي للمرض. ارتبطت بعض الجينات بأشكال مميزة ، أو نموذجية ، أو نادرة من المرض ، والتي تشمل الأحداث أو البالغين ، أو مبكرًا أو متأخرًا ، أو صبغيًا جسديًا متنحيًا ، أو سائدًا ، أو مرتبطًا بالكروموسوم X [4 ، 7-9]. كما تم تحديد عوامل الخطر المسببة المرتبطة بمجموعات عرقية معينة. الجينات الأكثر ارتباطًا بـ PD تشمل GBA و LRRK2 و PRKN و SNCA و ATP13A2 و ATP10B و DI -1 و DNAIC6 و FBXO7 و HTRA2 و MAPT و PINK1 و PLA2G6 و VPS35 و VPS13C [4 ، {{19} }]. تقوم غالبية هذه الجينات بتشفير البروتينات المرتبطة بشكل مباشر أو غير مباشر بآليات مراقبة الجودة التي تعتبر حيوية في الحفاظ على التوازن الخلوي ، ومسارات النقل الحويصلي ، وعمليات الالتهام الذاتي ، والنظام الداخلي الليزوزومي. ارتبطت التغيرات الجينية الأخرى أيضًا بـ PD ، بما في ذلك التغيرات اللاجينية ، مثل مثيلة الحمض النووي ، وإعادة تشكيل الكروماتين ، وتعديلات هيستون ، و microRNAs ، و RNAs طويلة غير مشفرة [4،14].
2. التسبب في الأمراض وعلم الأمراض
تكشف الدراسات الإكلينيكية المرضية عن التقدم البطيء لمرض باركنسون من المنطقة البطنية الوحشية للـ SNPC ، مع انتشاره لاحقًا إلى مناطق الدماغ الأخرى [15]. تصبح الأعراض السريرية للـ PD قابلة للاكتشاف عندما يتطور انحطاط الخلايا العصبية DA داخل SNPC. لوحظ LBs في مواقع تلف الخلايا العصبية (الشكل 1). في علم وظائف الأعضاء العادي ، يؤدي الـ -syn المترسب في هذه الهياكل وظائف مركزية في الالتقام الخلوي. تهريب الحويصلات؛ تخليق وتخزين وإطلاق الدوبامين ؛ Ca2 بالإضافة إلى التوازن. ديناميات الأنابيب الدقيقة. وعمليات أخرى [16]. وبالتالي ، فإن نشاط الخلايا العصبية يعتمد كليًا على -syn ، وكذلك على توازن الميتوكوندريا. على الرغم من وجود -syn في الغالب في LBs الخلوي الحمضي ، فقد تم اكتشافه أيضًا في الميتوكوندريا والليزوزومات والعضيات الأخرى في أدمغة PD بعد الوفاة. إن وجود LBs في الجهاز العصبي المحيطي والمعوي والمركزي (CNS) له دور في كل من الأعراض الحركية وغير الحركية لـ PD [17 ، 18].شراء cistancheتؤدي الطفرات النقطية في تسلسل -syn أو غيرها من الإهانات المرضية إلى تكوين أوليغومرات ، والتي قد تتجمع معًا في شكل تجمعات أكبر. يمكن لهذه المجاميع أن تغير العديد من المسارات الخلوية والجزيئية في الخلايا العصبية - على وجه الخصوص بما في ذلك البلعمة الذاتية وعمليات البروتوزوم ، مثل وظيفة الميتوكوندريا ، والاتجار بالحويصلات ، والعضيات ، وتدهور البروتين - وكلها تؤدي إلى التنكس العصبي. في وقت لاحق ، نتيجة للتنكس العصبي ، ترسبت مجاميع o-syn في SN ، حيث تنشط الخلايا الدبقية الصغيرة [19]. هذا التنشيط الذي لا يمكن السيطرة عليه يمكن أن يولد إشارات مؤيدة للالتهابات [20] والتي قد تؤدي إلى مزيد من التنكس العصبي عند الوصول إلى عتبة حرجة.

يمكن للسيستانش مكافحة الشيخوخة
2.1 المظاهر العصبية النفسية لمرض باركنسون
لا يوجد اختبار محدد لتشخيص شلل الرعاش. وبالتالي ، يعتمد التشخيص على التاريخ الطبي ، ومراجعة العلامات والأعراض ، والفحص العصبي والجسدي (الإطار 1). تبدأ العلامات الحركية لمرض باركنسون في حوالي 60 عامًا من العمر [21] ، لكن الإصابة بالعمر الشرياني الصغير ليست نادرة ، خاصة في بعض الأشكال الوراثية [22]. يعد بطء الحركة من جانب واحد أو غير المتماثل و / أو رعاش الراحة من الأعراض الأولى للمرض [23]. يظهر رعاش الراحة في استرخاء العضلات ويختفي أثناء الحركة والنوم. يمكن زيادتها عن طريق الحساب الذهني. إن بطء الحركة ، الذي يُعرَّف من خلال بطء الحركة وانخفاض السعة أو السرعة ، يؤدي إلى صعوبات في الحركات المتكررة ، والتصوير المجهري ، والمشي بخطوات صغيرة ، وصعوبات في الكلام (نقص النطق وخلل النطق) ، والتي ستظهر مع تطور المرض.سيستانشقد يسبب التصلب الألم ويساهم في تشوه الوضع (ثني العمود الفقري الصدري القطني). يكون التقدم بطيئًا مع الامتداد الثنائي للحركة ، والرعشة ، وفرط التوتر ، يليه عدم استقرار الوضع ، وتجميد المشية ، والسقوط ، وفي بعض المرضى ، كامبتوكورميا. قد تظهر بعض العلامات غير الحركية (premotor) قبل ظهور الأعراض الحركية الأولى بعدة سنوات ؛ وتشمل هذه الاكتئاب ، ونقص حاسة الشم ، والإمساك ، واضطرابات نوم حركة العين السريعة [24]. قد يكون القلق واللامبالاة موجودان منذ بداية شلل الرعاش ، في حين أن خلل النطق الشديد (انخفاض ضغط الدم الانتصابي ، ضعف في وظيفة البول بسبب فرط النشاط الناقص) ، تفتيت النوم ، الاضطرابات المعرفية (اضطرابات خلل الترقيم) ، والهلوسة تظهر لاحقًا ، وسوف تساهم في فقدان الاستقلالية [ 24،25].

2.2. العلاجات الحالية لشلل الرعاش والإدارة السريرية
علاج الأعراض هو الخيار السريري الوحيد المتاح حاليًا [26] ، مع علاجات تهدف إلى تعويض نقص الدوبامين. تعتبر أدوية الدوبامين (الليفودوبا المرتبطة بمثبطات الدوبا-ديكاربوكسيلاز ، أو منبهات الدوبامين ، أو مثبطات مونوامين أوكسيديز من النوع ب) ، المستخدمة بشكل فردي أو في أنظمة العلاج المتعدد ، فعالة للغاية خلال المراحل المبكرة من المرض. ومع ذلك ، تصبح الإدارة أكثر صعوبة مع تقدم العام. في الواقع ، يمكن أن تؤدي علاجات الدوبامين ، التي تعمل على تحسين العلامات الحركية ، إلى مضاعفات شديدة الإعاقات. تحدث ظاهرة التلاشي (نهاية فشل الجرعة) وخلل الحركة بعد عدة سنوات من علاج ليفودوبا [27]. اضطرابات السيطرة على النبض (القمار المرضي أو التسوق ، النشاط الجنسي المفرط ؛ [28] ، الهلوسة ، أو الذهان قد تؤدي أيضًا إلى تعقيد العلاجات الدوبامينية ، وتحدث بشكل متكرر مع ناهضات الدوبامين. [29] العلاجات الأخرى ، بما في ذلك مثبطات الكاتيكول- O- ميثيل ترانسفيراز لعلاج التقلبات الحركية أو الأمانتادين لخلل الحركة [26] يمكن استخدامها لاحقًا مع تقدم المرض. علاج الخط الثاني (التسريب المستمر تحت الجلد من الآبومورفين ، إعطاء الصائم المستمر لجل دروكسيدوبا ، التحفيز النووي تحت المحيط الثنائي) عندما تصبح التقلبات الحركية وخلل الحركة كبيرة [30]. تهدف هذه العلاجات إلى تحقيق تحفيز مستقر للدوبامين المخطط ولكن ليس لها تأثير على تطور المرض. علاوة على ذلك ، بعض الأعراض المحورية (عسر التلفظ ، عدم استقرار الوضعية) ليست حساسة للدوبا ، وإدارة سريرية لغير الحركية الأعراض لا تزال صعبة [31،32].
أدت عقود من التحقيقات إلى تطوير استراتيجيات علاجية أدت بلا شك إلى تحسين نوعية حياة المرضى. ومع ذلك ، لا يزال إبطاء تقدم المرض يمثل تحديًا ، وأولوية مستمرة [33] ، وننتظر بفارغ الصبر مناهج جديدة لتعديل المرض [3،34]. على الرغم من أن وظائف البروتوزوم والالتهام الذاتي ، بما في ذلك الالتهام الذاتي والالتهام الذاتي بوساطة المرافقة (CMA) ، معروفة منذ فترة طويلة بأنها تساهم في تصفية -syn [35 ، 36 لتر ، عدم تنظيم هذه العمليات لا يزال غير مفهوم جيدًا في PD.cistanche أسترالياترتبط العديد من الطفرات الجينية والتعديلات على البروتينات المتضمنة في شلل الرعاش ارتباطًا وثيقًا بالبلعمة الذاتية ، ولا سيما مسارات التلتهم والالتهام الليزوزومي. في هذه المراجعة ، نركز على مشاركة الالتهام الذاتي في PD ، ونعلق على الأسئلة الرئيسية التي لم تتم الإجابة عليها في هذا المجال ونقترح اتجاهات جديدة للتدخلات العلاجية المحتملة التي تستهدف مسارات الالتهام الذاتي.
3. الالتهام الذاتي
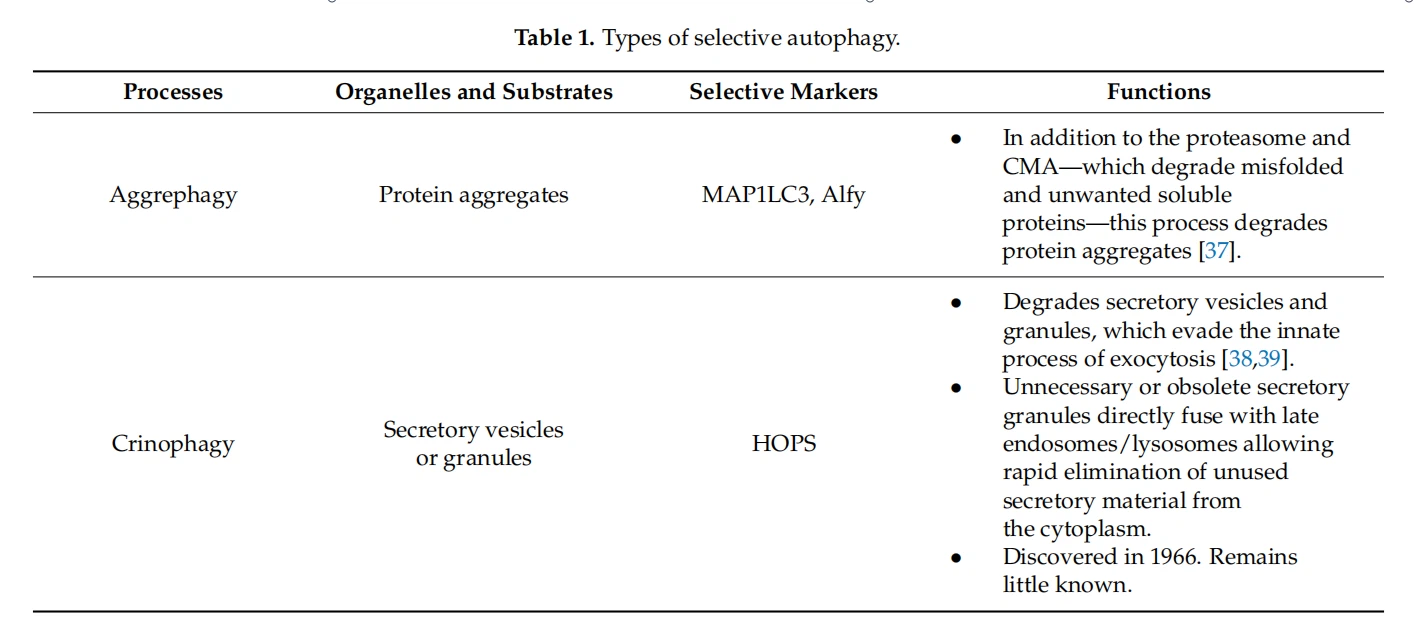
الالتهام الذاتي هو نظام تحلل خلوي رئيسي يتم من خلاله تسليم المواد السيتوبلازمية إلى الجسيمات الحالة للتحلل. بناءً على المسار الذي يتم من خلاله تسليم المحتوى إلى الجسيمات الحالة ، تم تحديد عدة أشكال من الالتهام الذاتي. تحتوي هذه الأشكال المختلفة أيضًا على درجات متفاوتة من الانتقائية للبضائع المستهدفة (الجدول 1 ؛ الشكل 2). الأنواع الرئيسية الثلاثة لعمليات الالتهام الذاتي هي الالتهام الكلي ، CMA ، والتلوث الجزئي / التداخل الكهرومغناطيسي. أيا كان مسار التسليم ، فإن الدور الرئيسي لهذه العمليات هو تحطيم ماتي الريال غير المرغوب فيه المعيب ، أو قد يكون سامًا ، أو المنتج بكميات زائدة ، وبالتالي الحفاظ على التوازن الخلوي.
3.1 آلات الالتهام الذاتي
تم فحص آليات الالتهام الذاتي بشكل شامل ومراجعتها بالتفصيل من قبل العديد من المؤلفين [61-63]. يتم عرض السمات العامة للمسارات الثلاثة في الشكل 2. التطورات الحديثة المتعلقة بعمليات البلعمة الذاتية الكنسية وغير الكنسية - خاصة في أنظمة الثدييات - قد أضافت إلى فهمنا للآليات التي قد تلعب أدوارًا مهمة في الأمراض التنكسية العصبية مثل PD. ومع ذلك ، فإن العديد من الاكتشافات الجزيئية التي يعتمد عليها فهمنا الحالي لتنظيم الالتهام الذاتي نشأت من التحليلات التي تنطوي على الخميرة. في الخلايا ، تتعايش الأشكال الثلاثة من الالتهام الذاتي وتلعب أدوارًا حيوية في الحفاظ على التوازن الخلوي. ومع ذلك ، فإن الغالبية العظمى من النتائج المتاحة في هذا المجال تتعلق بالتلوث الكلي. تم تقسيم هذه العملية إلى الخطوات التالية: التنوي ، والاستطالة ، وتشكيل البلعمة الذاتية ، واندماج الجسيم الذاتي ، والتدهور (الشكل 2). كل خطوة منظمة وراثيًا وتلعب دورها المحدد في الحفاظ على الطبيعة الديناميكية للعملية. على سبيل المثال ، يعمل عدد من البروتينات المرتبطة بالبلعمة الذاتية المحفوظة بطريقة هرمية للتوسط في تكوين البلعمة الذاتية. عند تحريض المنبع ، تتلامس آلية الالتهام الذاتي مع غشاء العزل / البلعمة. لا تزال الأصول المبكرة والشبكة الإندوبلازمية للمصدر المعقد (ER) ، ومركب جولجي ، والداخلية ، والميتوكوندريا] لغشاء العزل الناشئ محل نقاش [64]. أكدت دراسة البنية التحتية التي تضمنت تجارب المجهر الإلكتروني أن مجالًا فرعيًا متخصصًا من ER يساهم في توليد phagophore [65]. تم تحديد حوالي 40 بروتينًا مرتبطًا بالالتهام الذاتي (ATG) على أنها متورطة في هذه العملية الديناميكية ، وهي منظمة بشكل هرمي ، بدءًا من بدء العملية وتتقدم حتى نضوج البلعمة الذاتية. تعمل هذه البروتينات معًا في العديد من المجمعات الوظيفية ، لا سيما (1) Unc -51- مثل kinase 1 (ULK1) / ATG1 kinase complex؛ (2) مركب فوسفاتيلينوسيتول من الفئة الثانية (PI) 3- كيناز ؛ (2) مجمع PI (3) ATG18 للربط PI 2- ؛ (4) نظاما الاقتران (ATG12 نظام الاقتران و البروتين المرتبط بالأنابيب الدقيقة 1A / 1B-light chain 3 (MAP1LC3) / نظام اقتران ATG8) ؛ و (5) آلية الاندماج (الشكل 2).

في الواقع ، العديد من بروتينات ATG المزعومة لها وظائف بديلة تتجاوز الالتهام الذاتي [66]. وهكذا ، على سبيل المثال ، فإن دهون MAP1LC3 (وهي آلية تستخدم منذ فترة طويلة لتقييم نشاط البلعمة الذاتية [67،68]) تشارك أيضًا في الآليات الخلوية غير البلعمة مثل البلعمة أو LAP أو كثرة الخلايا الصغرى أو العدوى الفيروسية. تُعرف هذه العمليات بعمليات البلعمة الذاتية غير الكنسية [69]. في هذه العمليات غير المتعارف عليها ، والتي لا تزال وظائفها غير مكتملة التوصيف [70،71] يقترن MAP1LC3 بأغشية مفردة (اقتران غشاء واحد ATG8 ، SMAC) ، ولا يتم تسليم مكونات العصارة الخلوية إلى الجسيم الحال [72].
3.2 يساهم الالتهام الذاتي العصبي في علم وظائف الأعضاء العصبية
هناك أدلة دامغة تدعم فكرة أن الالتهام الذاتي للعصبونات يلعب دورًا حاسمًا في العديد من جوانب تطور الخلايا العصبية وفي الحفاظ على نشاط الخلايا العصبية [73-75]. في خلايا ما بعد الانقسام الخيطي مثل الخلايا العصبية ، يعد الالتهام الذاتي مهمًا بشكل خاص للبقاء والتوازن ، لأن هذه الخلايا لا يمكنها التخلص من المواد السامة المتراكمة والعضيات التالفة أثناء انقسام الخلايا. يعد الالتهام الذاتي ، بالإضافة إلى نظام البروتوزوم [76] ، أحد آليات مراقبة الجودة الحيوية التي تضمن طول عمر الخلايا العصبية. الالتهام الذاتي قبل المشبكي في الطرف المحوري ضروري أيضًا لصيانة المشبك واللدونة [77].
من بين الخلايا العصبية ، يمكن فقط للخلايا العصبية القشرية وخلايا بركنجي والخلايا العصبية الوطائية زيادة محتوى البلعمة الذاتية عند التحفيز. الأسباب الدقيقة لهذه الآلية المتخصصة غير معروفة حاليًا [62،78]. أحد التفسيرات المحتملة تافهة وتتعلق بحقيقة أنه ، كما هو الحال بالنسبة لبعض أنواع الخلايا الأخرى ، يظل قياس الالتهام الذاتي في الخلايا العصبية ، وخاصة في الدماغ ، يمثل تحديًا [79 ، 80]. بدلاً من ذلك ، نظرًا لأن الخلايا العصبية متمايزة نهائيًا - مع قدرة تجدد أقل من الخلايا الأخرى - فهي أقل تلقائية. ومع ذلك ، قدمت الدراسات التي أُجريت على أدمغة الفئران التي تعاني من نقص الالتهام الذاتي دليلًا على أن البروتين والبروتينات متعددة التكثيف تتراكم في معظم الخلايا العصبية [81]. في المقابل ، لا يؤدي نقص SQSTM1 إلى نقص كامل في الالتهام الذاتي. لذلك يبدو أن محتوى البلعمة الذاتية يعتمد على نوع الخلايا ونوع الإجهاد.
3.3 أمراض الالتهام الذاتي والتنكس العصبي
كما تم تقديمه أعلاه ، لمنع الخلل الوظيفي العصبي والمتشابك ، طورت الخلايا العصبية آليات لإزالة المكونات والعضيات السامة والمعيبة. هذه الآليات ضرورية للحفاظ على درجة عالية من النقل العصبي وسلامة البروتين الوظيفي في الخلايا العصبية. الالتهام الذاتي هو محور هذا النظام الوقائي. يؤدي فقدان الالتهام الذاتي المرتبط بالعمر إلى جعل الخلايا العصبية أكثر عرضة للإجهاد ويمكن أن يؤدي إلى موت الخلايا [82]. يمكن أن يؤدي الاضطراب الباثولوجي لمسارات الالتهام الذاتي أيضًا إلى اضطرابات تنكسية عصبية قد تكون مرتبطة أو غير مرتبطة بالشيخوخة.
تم توثيق الالتهام الذاتي المُخترق في العديد من الأمراض العصبية التنكسية ، بما في ذلك شلل الرعاش ، ومرض الزهايمر (AD) ، ومرض هنتنغتون (HD) ، والتصلب الجانبي الضموري (ALS) (للمراجعات الشاملة ، انظر [63.84]). عند التحقيق في الآليات التي تربط الالتهام الذاتي بهذه الأمراض ، فقد لوحظ ، على سبيل المثال ، أن الفئران التي تعاني من نقص Atg5 على وجه التحديد في الخلايا العصبية تصاب بعجز تدريجي في الوظيفة الحركية بينما تتراكم أيضًا أجسام متضمنة السيتوبلازم في الخلايا العصبية [85]. وبالمثل ، في الفئران التي تعاني من نقص Atg7 أو Atg5 أو Ambral ، وجد أن اليوبيكويتين يتراكم في الجهاز العصبي المركزي ، كما ارتبطت التضمينات السيتوبلازمية بالخلل الوظيفي الحركي وعيوب الأنبوب العصبي في أجنة الفئران [86]. إن تحور الجينات المرتبطة بعمليات البلعمة الذاتية - على سبيل المثال ، SQSTM1 ، أوبتينيورين / OPTN ، E3 يوبيكويتين ليغاز باركين / PRKN ، PINK1 ، TBK1 - متورط أيضًا في العديد من أمراض التنكس العصبي. على وجه الخصوص ، تم توثيق العيوب في التفتيت والتي تظهر أيضًا في الأمراض الالتهابية الخاصة بالأعضاء والجهازية ، في الأمراض التنكسية العصبية [87]. بالإضافة إلى هذه الطفرات الجينية ، تم ربط التغيرات الكبيرة في تعبير البروتين بالأمراض التنكسية العصبية. على سبيل المثال ، ارتبط التعبير غير الطبيعي للخلية الظهارية الغدية للبروتين 1 (GABARAPL1 / GEC1) بالأمراض التنكسية العصبية [88]. 3.4. الالتهام الذاتي ومرض باركنسون
من بين السمات المرضية للـ PD هي LBs التي تحتوي على بروتين سين متجمع بشكل غير طبيعي. تعد الطفرات أو تضاعف ثلاث مرات في الترميز الجيني سين (SNCA) أمرًا نادرًا ولكن من الواضح أنها تشارك في بدء وتقدم PD. ومن المثير للاهتمام ، أن أي فشل يؤثر على أحد مكونات عملية التدهور ، سواء بشكل مباشر أو غير مباشر ، يضعف عمليات الالتهام الذاتي الأخرى. من المعروف أن نظام يوبيكويتين-بروتيازوم (UPS) هو المسار التدريجي الأولي للسين أحادي الفكهة ، بينما يتحلل مسار الالتهاب الكلي المزمن [89،90]. في PD ، لذلك ، تلعب كل من الميتوكوندريا والليزوزومات أدوارًا حاسمة (الشكل 3). 3.4.1 دور الميتوفاجي في PD
باعتبارها عضية منتجة للطاقة ، تعتبر الميتوكوندريا مركزية للعديد من الأمراض العصبية التنكسية ، بما في ذلك PD [91-95]. كشفت التحقيقات المتعددة أن الطفرات الجينية المرتبطة بالـ PD (على سبيل المثال ، PRKN ، PINK1 ، وغيرها) ترتبط أيضًا ارتباطًا وثيقًا بعيوب الميتوكوندريا ، بما في ذلك العيوب في الميتوفاجي (الجدول 2) [9]. يعتمد نوع الضرر الذي يلحق بالميتوكوندريا بشكل طبيعي على نوع المزامنة (تشكيل الركام أم لا ، الناتج من أشكال طفرة أو أصلية من SNCA). أكدت دراسات أخرى أن o-syn يؤثر على تفاعل الغشاء المرتبط بالميتوكوندريا مع ER. يلعب هذا التفاعل دورًا محوريًا في تنظيم إشارات Ca4 بالإضافة إلى موت الخلايا المبرمج. بالإضافة إلى ذلك ، يتداخل o-syn غير الطبيعي مع عامل تنشيط مستقبلات جاما البيروكسيسوم المُنشّط بتكاثر البيروكسيسوم 1- ألفا ، والذي يلعب دورًا مهمًا في التكوّن الحيوي للميتوكوندريا وفي موت الخلايا المبرمج. تمت مناقشة الخلل الوظيفي في الميتوكوندريا مع مشاركة العوامل المتعلقة بـ a-syn بشكل شامل في مكان آخر [9،97،98].

الشكل 3. ضعف الالتهام الذاتي في PD. لوحظ اختلال أشكال الالتهام الذاتي في شلل الرعاش. ترتبط الطفرات الجينية لـ -syn بضعف عملية الالتهام الذاتي. العديد من العوامل ، مثل العوامل الوراثية ، والاتجار المعيب في الميتوكوندريا ، والإجهاد التأكسدي ، ودورة ATP المختلة وظيفيًا ، وديناميات الميتوكوندريا غير المنظمة ، وتغيير الانقسام ، تزعج الميتوكوندريا الصحية. تسمح الميتوكوندريا التالفة / المختلة وظيفيًا لـ PINK1 بتجنيد PRKN ، والذي بدوره ينشط البروتينات الأساسية الأخرى ، مثل OPTN و ubiquitin و Rab7 وغيرها مما يؤدي إلى بدء عملية مراقبة الجودة ، أي ميتوفاجي. يتم تنظيم وظيفة Rab7 من خلال TBC1D15 / 17 (تنتمي إلى عائلة TBC مع وظائف Rab-GAP) ، والتي تنظم أيضًا وظائف التشكيل والهدف لغشاء العزل عن طريق الربط المتبادل مع Fis1 و MAP1LC3B. الخطوات المتسلسلة للتلوث هي تشكيل البلعمة ، والنضج في جسيم الميتو ، واندماج جسيم الميتو مع الجسيم الحال. تلعب الالتهام الذاتي التقليدي أيضًا دورًا أساسيًا في تدهور النفس (الساذج والمجمع). ترتبط x-syn بشكل انتقائي بمستقبل التعرف على العوامل الممرضة ، TLR -4 ، الذي ينشط مسار إشارات المصب بعد تنشيط NF-kB ، لتحفيز إنتاج SQSTM1 / p62. أنتج SQSTM1 روابط إلى التزامن الداخلي ويبدأ عملية الالتهام الذاتي. يؤدي عدم تنظيم عملية الالتهام الذاتي إلى تراكم -syn جنبًا إلى جنب مع SQSTM1. بصرف النظر عن التخفيف والتلوث الكلي ، يحلل CMA أيضًا بشكل انتقائي -syn ، والذي يحتوي على شكل يشبه KFERQ. يؤثر تثبيط CMA الانتقائي أو أداء CMA المتغير على تدهور الحالة. الاختصارات غير الموصوفة في النص: Fill، Mitochondrial fission 1 protein؛ GAP ، بروتينات تنشيط GTPase ؛ IKK ، IkB كيناز ؛ MyD88 ، بروتين التمايز النخاعي 88 ؛ Rab ، عائلة Ras من بروتينات G الصغيرة ؛ TBC ، Tre -2 / Bub2 / Cdc16 ؛ TIRAP ، بروتين محول مستقبل Toll-interleukin 1.

تم اقتراح العيوب في مسار التخفيف ، وخاصة PARK2 (طفرات PRKN) و PARK6 (طفرات PINK1) ، كسبب رئيسي للـ PD العائلي. في الظروف الصحية ، يتم نقل PINK1 ، الذي يترجم إلى الميتوكوندريا ، إلى الغشاء الداخلي للميتوكوندريا حيث يتحلل. في ظل ظروف معينة غير معروفة ، تتلف الميتوكوندريا وتفقد إمكانات الغشاء (الشكل 3). يؤدي هذا إلى تنشيط PINK1 وتوظيفه لـ PRKN ، مما يساعد على إحداث التخفيف أثناء العمل على بروتينات غشاء الميتوكوندريا الأخرى OPTN وبروتين النقطة النووية 52- كيلو دالتون (NDP52)] [62 ، 119-124]. تعد طفرات PRKN هي السبب الأكثر شيوعًا ل YOPD المتنحية ، تليها الطفرات في PINK1. إلى جانب دوره في التخفيف ، يلعب PRKN دورًا أساسيًا في معالجة الدهون وانتشار GTPase Rab7 ، الذي ينظم الديناميكيات الليزوزومية [125-128]. ينتج عن نقص PRKN تنكس الخلايا العصبية DA في الفئران ، وتظهر الأرومات الليفية الجنينية المشتقة من الفئران الناقصة PINK 1- خللًا في الوظيفة الليزوزومية [129]. بالإضافة إلى ذلك ، تؤدي الطفرات في PINK1 و PRKN إلى عيوب في عملية التخفيف [62]. ومع ذلك ، لا يزال يتعين على الدراسات أن تشرح سبب عدم تجنيد PRKN للميتوكوندريا في الخلايا العصبية DA في ظل ظروف نزع الاستقطاب [130]. نتيجة لاختلالات التفتيت في الخلايا العصبية هو الإجهاد غير المنضبط (أي توليد أنواع الأكسجين التفاعلية) ، مما يؤدي إلى موت الخلايا العصبية. تماشياً مع هذا التأثير ، قد يكون استهداف عيوب التخفيف مفيدًا في شلل الرعاش. لقد تم إثبات ، على سبيل المثال ، أن مثبطًا للميتوكوندريا deubiquitinase USP30 ، والذي ينظم بشكل سلبي الوساطة بوساطة PRKN ، يزيد بشكل انتقائي من تدفق الميتوفاغي ، وبالتالي يمكن أن يكون ذا فائدة لتطوير طرق علاجية جديدة [131،132].
بالإضافة إلى التأثير الرئيسي لطفرات PINK1 و PRKN ، تمت دراسة طفرات SNCA في سياق التخفيف. يتفاعل -syn مع بروتينات ميرو (بروتينات مهايئ غشاء الميتوكوندريا الخارجي ، مفيدة في حركة الميتوكوندريا) ويتداخل مع عملية تحلل ميرو ، وهي خطوة أساسية في عملية التخفيف [133]. أكدت الدراسات التي أجريت على الفئران والطفرات التي تؤوي الخميرة في SCNA دور -syn في موت الخلايا العصبية ، عن طريق اختلال وظائف الميتوكوندريا [134،135].
عامل النسخ المحسن للخلية العضلية 2D (MEF2D) هو منظم أساسي آخر للميتوكوندريا (الجدول 2). إنه عامل مركزي في نقل الإشارات خارج الخلية وتفعيل البرامج الجينية استجابة لمجموعة واسعة من المحفزات في العديد من أنواع الخلايا ، بما في ذلك الخلايا العصبية. MEF2D هو منظم مهم للتعبير الجيني لـ IL -10 ، وهو يشارك في التحكم السلبي في الاستجابة الالتهابية الدبقية الصغيرة ، ويمنع السمية الخلوية بوساطة الالتهاب [136]. تم ربط تعبير MEF2D المنخفض بشكل مباشر بمستويات منخفضة من نازعة هيدروجين الأدينين ثنائي النوكليوتيد النيكوتيناميد (NADH) وهو مكون من مركب الميتوكوندريا I. أظهر تحليل ما بعد الوفاة لعينات الدماغ من مرضى PD انخفاض مستويات كل من MEF2D و NADH [137].
هناك عدد من الطفرات الجينية الأخرى ، بما في ذلك أوجه القصور في عامل تحفيز موت الخلايا المبرمج للميتوكوندريا (AF) وعامل نسخ الميتوكوندريا A (TFAM ؛ [138] الذي يزعج المسارات الداخلية الليزوزومية ، ويؤثر أيضًا على وظائف ووظائف الميتوكوندريا ، مما يؤدي على سبيل المثال إلى اختلال ميتوفاجي ، الفسفرة المؤكسدة المختلة وظيفيًا ، ديناميات الميتوكوندريا غير المنظمة ، الانقسام المتغير ، اختلال توازن الكالسيوم ، تهريب الميتوكوندريا المتغير ، وتحريض الإجهاد التأكسدي (الجدول 2). مسارات يوبيكويتين بوساطة ليجاز [97،139،140]. ليس معروفًا حاليًا إلى أي مدى ترتبط هذه المسارات بـ PD.
تم استخراج هذه المقالة من الخلايا 2021 ، 10 ، 3547. https://doi.org/10.3390/cells10123547 https://www.mdpi.com/journal/cells






