الاكتشاف النوعي القائم على التحفيز وتثبيط التيروزيناز وتطبيقه الجزء الأول
May 09, 2023
خلاصة
التيروزيناز هو إنزيم مهم في التحكم في تكوين الميلانين في الميلانوزومات ويلعب دورًا رئيسيًا في تصبغ الشعر والجلد. يرتبط التعبير أو التنشيط غير الطبيعي للتيروزيناز بالعديد من الأمراض مثل المهق والبهاق وسرطان الجلد ومرض باركنسون. يمكن أن يسبب الترسب المفرط للميلانين أمراضًا مثل النمش والبقع البنية في جسم الإنسان ، كما أنه يرتبط ارتباطًا وثيقًا بتحول الفواكه والخضروات إلى اللون البني وسقوط الحشرات. إن الكشف عن نشاط التيروزيناز وتثبيطه له قيمة غير عادية في تقدم تشخيص وعلاج هذه الأمراض. لذلك ، تم تطوير العديد من مجسات الكشف البصري الانتقائي والمثبطات الجزيئية الصغيرة ، وقدمت مساهمات كبيرة في البحوث الأساسية والسريرية حول هذه الأمراض. في هذا البحث ، تتم مراجعة الكشف عن التيروزيناز وتثبيطه وتطبيقه في منتجات التبييض ، مع التركيز بشكل خاص على تطوير مجسات ومثبطات الفلورسنت. نأمل أن تساعد هذه المراجعة في تصميم مجسات ومثبطات التيروزيناز الأكثر كفاءة وحساسية ، بالإضافة إلى تسليط الضوء على علاجات جديدة لأمراض مثل سرطان الجلد.
وفقًا للدراسات ذات الصلة ،cistancheهو عشب شائع يعرف باسم "عشب معجزة يطيل الحياة". مكونه الرئيسي هوالسيستانوسيد، والتي لها تأثيرات مختلفة مثلمضادات الأكسدة,مضاد التهاب، وتعزيز وظيفة المناعة. الآلية بين cistanche وجلدتبييضيكمن في التأثير المضاد للأكسدة من cistanche glycosides. ينتج الميلانين في جلد الإنسان عن طريق أكسدة التيروزين المحفزالتيروزيناز، ويتطلب تفاعل الأكسدة مشاركة الأكسجين ، لذلك تصبح الجذور الخالية من الأكسجين في الجسم عاملاً مهمًاتؤثر الميلانينإنتاج. يحتوي Cistanche على السيستانوزيد ، وهو مضاد للأكسدة ويمكن أن يقلل من توليد الجذور الحرة في الجسم ، وبالتاليمثبطالميلانينإنتاج.

انقر فوق ملحق Cistanche Tubulosa
لمزيد من المعلومات:
david.deng@wecistanche.com WhatApp: 86 13632399501
الكلمات الدالة:
1 المقدمة
يعتبر التيروزيناز (EC 1.14.18.1 ؛ كاتيكول أوكسيديز ؛ بوليفينول أوكسيديز [1] أو ديفينولاز) أهم إنزيم يحتوي على النحاس في تكوين الميلانين. يمكن أن يحفز التيروزيناز الهيدروكسيل والأكسدة اللاحقة لوحدة مونوفينول إلى أورثوكينون تحت تأثير الأكسجين الجزيئي. يوجد في الميلانوسومات ، موقع تخليق وتخزين ونقل الميلانين. قيم الأس الهيدروجيني للميلانوسومات الخفيفة والشديدة الميلان حوالي 4.5 و 3 ، على التوالي. درجة الحموضة المثلى لنشاط التيروزيناز هي 6.8 [2]. كان Raper [3] و Mason [4] أول من أوضح مسارات التخليق الحيوي لتكوين الميلانين في الكائنات الحية المختلفة ، والتي تم تزيينها مؤخرًا بواسطة Schallreuter et al. [5] وكوكسي وآخرون. (الشكل 1) [6].
يوجد التيروزيناز على نطاق واسع في النباتات والحيوانات والكائنات الحية الدقيقة. نظرًا لتورط التيروزيناز في التسبب في الورم الميلانيني ، فإن مراقبة نشاطه وتنظيمه دوائيًا سيساعد في تشخيص المرض وعلاجه [7]. تم تطوير مجسات لاكتشاف نشاط التيروزيناز على وجه التحديد في البيئات الفسيولوجية. كما تم تطوير مثبطات يمكن أن تجعل التيروزيناز غير نشط ، واستخدم بعضها سريريًا لعلاج الأمراض. على سبيل المثال ، تم استخدام حمض الكوجيك والأربوتين [8] ، كمثبطات محددة للتيروزيناز ، سريريًا كمنتجات مبيضة. مع التقدم في اكتشاف الأدوية ، تم مؤخرًا تصميم وتصنيع عدد متزايد من المركبات الفعالة التي يمكنها اكتشاف / تثبيط نشاط التيروزيناز. هذا من شأنه أن يسهل إلى حد كبير التقدم في تشخيص وعلاج تلك الأمراض الناتجة عن إنتاج الميلانين الشاذ. في هذه المراجعة ، سنناقش التقدم المحرز في تطوير تحقيقات ومثبطات تعتمد على جزيء صغير لنشاط التيروزيناز الداخلي. نأمل أن يساعدنا ذلك في معرفة المزيد عن التيروزيناز والعثور على المزيد من المركبات الوظيفية التي تستهدف / تنظم التيروزيناز.

2. هيكل التيروزيناز
يقدم الموقع النشط للتيروزيناز بنية مركزية نحاسية ثنائية النواة تتكون من أيوني نحاسي (الشكل 2) ، والتي ترتبط ببقايا الهيستيدين في البروتين. يتم توصيل مركزي أيون النحاس بواسطة جسر تنسيق داخلي. يترابط التيروزين ومواد أخرى مع الإنزيم ، من خلال الرابطة بين المركز النشط للإنزيم ومجموعة الهيدروكسيل. في عملية التفاعل التحفيزي للميلانين ، يتم تصنيف الموقع التحفيزي إلى ثلاثة أشكال: حالة الأكسدة (Eoxy) ، حالة الاختزال (Emet) ، حالة إزالة الأكسجين (Edeoxy) ، يكمن الاختلاف في بنية مركز أيون النحاس ثنائي النواة النشط (الصورة 2).
يتكون الايبوكسي من ذرتين مربعيتين من النحاس (II) ؛ تتكون كل ذرة من خطي استواء قويين والرابط هو محوري واحد أضعف NH [9]. يربط جزيء الأكسجين الخارجي ويربط بين مركزي النحاس في شكل بيروكسيدات. يبلغ طول رابطة CueCu حوالي 0. 35 نانومتر. يؤدي الجمع بين جزيئات الأكسجين إلى تكوين بنية (m-h2: h 2 - بيروكسو) [10] ، لذلك يمكن كتابة مركز Eoxy النشط كـ [Cu (II) eO2eCu (II)]. يلعب التركيب الإلكتروني للبيروكسيدات دورًا مهمًا في الوظائف البيولوجية لـ Eoxy. بسبب عمل المستقبِل القوي * ، يكون للبيروكسيد شحنة سالبة أقل ، بينما يتفاعل متقبل الإلكترون p مع الإلكترونات في مدار s * للبيروكسيد ، مما يضعف بشكل كبير قوة رابطة الأكسجين والأكسجين ، مما يجعل النواة من مركز التيروزيناز النشط قابل للكسر بسهولة [9]. يشبه Mettyrosinase (Emet) Eoxy ويحتوي أيضًا على ذرتين من النحاس رباعي الزوايا (II) مقترنة عبر جسر داخلي. الفرق هو أن رابط الجسر بين أيونات النحاس هو هيدروكسيد بدلاً من بيروكسيد [2]. من حيث الخصائص المؤكسدة ، يختلف Emet و Eoxy أيضًا قليلاً. Emet غير قادر على أكسدة المركبات الفينولية الأحادية. في حالة عدم وجود ركائز ، يوجد Emet كشكل رئيسي في الكائنات الحية. يحتوي Deoxytyrosinase (Edeoxy) ، على غرار deoxy hemocyanin ، على بنية متناظرة [(Cu (I) eCu (I)]. لا يوجد رابط ليجند مثل البيروكسيد أو الهيدروكسيد بين النحاس ثنائي النواة ؛ وبالتالي فإن الهيدروكسيد الموجود في الماء هو عامل تجسير أساسي ليجند.
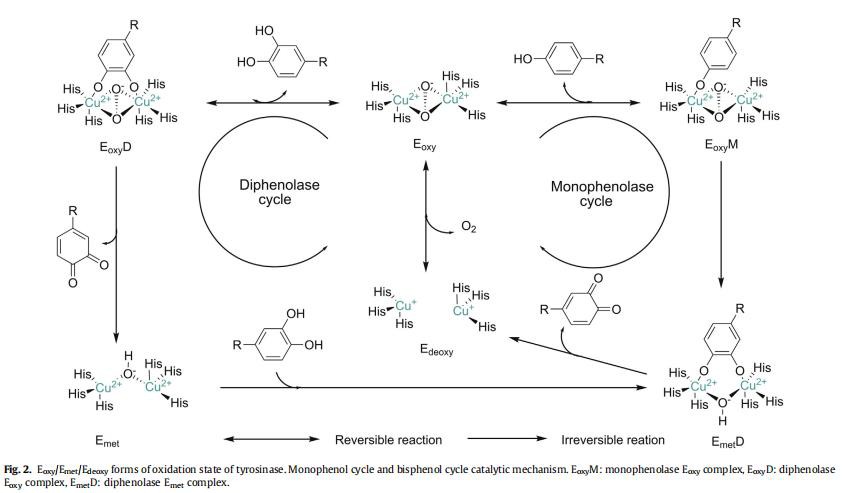
3. آلية عمل التيروزيناز
على الرغم من أن الباحثين قد أجروا دراسات متعمقة حول التيروزيناز والبروتينات المرتبطة به ، إلا أن آلية تفاعله التحفيزي لا تزال مثيرة للجدل. على سبيل المثال ، يختلف النشاط التحفيزي في نفس الموقع النشط للتيروزيناز. يحتوي المركز التحفيزي للتيروزيناز على مركز نحاسي ثنائي النواة يسمى Cu (A) و Cu (B) على التوالي. يتم تنسيق كل أيون نحاسي في المركز النشط مع ثلاث بقايا هيستيدين مختلفة. هناك فرق كبير بين نشاط mycophenolate ونشاط diphenolase ، كما أن انخفاض التيروزيناز له مرحلة تأخر عند التفاعل مع monophenol. هذه موضوعات مهمة يجب استكشافها ودراستها باستمرار [11].
يتم التفاعل بين التيروزيناز والركائز ذات الصلة بشكل أساسي من خلال تكوين رابطة تنسيق فعالة بين مجموعة الهيدروكسيل على الركيزة ومركز التيروزيناز النشط. أوليفاريس وآخرون. [12] اقترح أن Eoxy وركائز مناسبة في الثدييات تؤدي إلى نشاط mycophenolate ونشاط diphenolase. أثناء نشاط mycophenolate ، تتأكسد monophenols (L-Tyrosine) لتكوين o-quinones (o-dopaquinone) ، وهي مقدمة مهمة للميلانين ، و Edeoxy. أثناء نشاط diphenolase ، يمكن لـ Eoxy و Emet أيضًا أكسدة o-diphenols (L-DOPA) لإنتاج o-dopaquinone [13]. يتم قبول هذه الآلية بشكل عام من قبل الباحثين لأنها يمكن أن تعكس بدقة الخصائص الحركية للتيروزيناز ، حيث تكون خطوة تحديد المعدل في إنتاج الميلانين هي دورة مونوفينول [14].
3.1. آلية نشاط mycophenolate
أثناء تخليق الميلانين ، تتمثل الوظيفة الرئيسية للإنزيم في أكسدة ركائز المونوفينول إلى o-quinone بواسطة Eoxy. هذه العملية هي سمة مهمة تميز التيروزيناز عن غيرها من الأكسدة أوكسيديز مثل كاتيكول أوكسيديز. أثناء دورة مونوفينول (الشكل 2) ، يتم تنسيق ذرة الأكسجين الموجودة على الفينول المنزوع البروتونات مع أيون النحاس لمركز التيروزيناز المؤكسد النشط لتكوين مركب إيكسي فينولات ميكوفينولات (EoxyM) ، ومن ثم يتم استبدال الفينول أورثو-إلكتروفيليالي إلى ديفينولياز إيميت مركب (EmetD). يخضع EmetD لعملية انشقاق لتوليد o-quinone و Edeoxy مباشرة. يتحد Edeoxy مباشرة مع جزيئات الأكسجين لإعادة تكوين Eoxy. هذه هي العملية الدورية لنشاط المايكوفينولات. لا تنتهي هذه العملية حتى يكتمل تفاعل الركيزة. في عملية تفاعل دورة monophenol ، إذا التقى Emet في الحالة الطبيعية مع ركيزة monophenol ، فسوف يخضع لتفاعل أكسدة بطيء للغاية ويعيق التقدم الطبيعي لتفاعل monophenol. لذلك ، تسمى هذه الفترة "فترة التأخر" لأن Emet نفسها لا يمكنها ربط جزيئات الأكسجين [12].

3.2 آلية نشاط ديفينولاز
4. وظيفة التيروزيناز
يعتبر Tyrosinase جزءًا من عائلة النحاس من النوع 3 ويوجد في عملية تكوين الميلانين المبكرة. وهي تشارك بشكل رئيسي في عمليتي التفاعل التاليتين [17]: (1) الهيدروكسيل من L-tyrosine إلى L-DOPA ؛ (2) أكسدة L-DOPA لتشكيل dopaquinone. سيشكل Dopaquinone في النهاية الميلانين من خلال سلسلة من التفاعلات. أفراد الأسرة الآخرون من عائلة النحاس من النوع 3 هما أوكسيديز الكاتيكول والهيموسيانين. لا يُظهر أوكسيديز الكاتيكول إلا نشاط ديفينولاز والهيموسيانين على الليمفاوية للعديد من الرخويات ومفصليات الأرجل الحاملة للأكسجين. على الرغم من أن المراكز النشطة لبروتينات الأسرة النحاسية من النوع 3 محفوظة من حيث الهيكل الكلي والقدرة على توصيل جزيئات الأكسجين ، فإن أنشطتها المحتملة للأنزيمية متميزة قليلاً بسبب تباين ارتباط الركيزة بمركز الإنزيم أو عدم القدرة على التحكم في أن الركيزة يمكن أن تصل.

بالإضافة إلى المشاركة في عملية إنتاج الميلانين ، فإن للتيروزيناز أيضًا وظائف فسيولوجية مهمة أخرى. في الإسفنج والنباتات وبعض اللافقاريات ، يشارك التيروزيناز بشكل أساسي في عملية التئام الجروح والاستجابة المناعية الأولية [18]. في المفصليات ، يمكن أن يعزز التيروزيناز عملية تصلب الطبقة القرنية للحيوانات بعد طرح الريش. يمكن إفراز التيروزيناز البكتيري في التربة والمشاركة في عملية الاقتران العشوائي للمركبات العطرية المختلفة لتكوين الدبال. وقد تم اكتشاف أن التيروزيناز يمكن أن يكون أيضًا ترياقًا محتملاً للمواد السامة للبنزين [13 ، 19]. بالإضافة إلى ذلك ، يلعب دورًا لا غنى عنه في قتل النباتات الطفيلية ضد البكتيريا التكافلية الفينولية ، وإنتاج أصباغ طبيعية ، وتخليق المضادات الحيوية من الأحماض الأمينية مثل لينكومايسين. لا يمكن فصل النقطة المشتركة لهذه التأثيرات عن التيروزيناز باستخدام تفاعلات الأكسدة والاختزال مع جزيئات الأكسجين [11].
5. الأمراض المرتبطة بالتيروزيناز
يرتبط توزيع التيروزيناز ارتباطًا وثيقًا بالوظائف الفسيولوجية للنباتات والحيوانات. من المعتقد بشكل عام أن ألوان الريش والشعر والعينين وبشرة الحشرات والبذور والأصباغ الأخرى هي نتيجة التيروزيناز [10]. يحتوي Tyrosinase على وظائف مختلفة ولكنها مهمة في الكائنات الحية المختلفة. في معظم الحشرات في ظل الظروف الفسيولوجية العادية ، يوجد التيروزيناز في شكل الزيموجين ، وتوجد أنواع مختلفة من التيروزيناز في أجزاء معينة من الحشرات لإكمال وظائف فسيولوجية محددة [20]. بالإضافة إلى المشاركة في إنتاج الميلانين ، فإن إنزيم التيروزيناز الحشري هو الإنزيم الوحيد المتورط في التقرن. يمكن للكيراتين المقوى بالحشرات أن يمنع غزو الكائنات الحية الدقيقة والأجسام الغريبة ويحمي جسم اللافقاريات اللين. في المفصليات ، يشارك التيروزيناز أيضًا في عمليتين فسيولوجيتين مهمتين أخريين ، وهما الاستجابة الدفاعية والتئام الجروح. يتم إفراز الميلانين الناتج عن التيروزيناز في الثدييات في الخلايا الكيراتينية للبشرة والشعر ، مما يؤدي إلى تغيير لون سطح الجسم ، وبالتالي حماية الجلد والعينين ، ومقاومة الأشعة فوق البنفسجية ، ومنع ارتفاع درجة حرارة الأنسجة الداخلية [10]. يتم اكتشاف التيروزيناز الموجود في الثدييات بشكل شائع في الخلايا الصباغية ، وهي خلايا محددة للغاية توجد في الجلد وبصيلات الشعر والعينين لإنتاج أصباغ [4،21]. عندما يتم تقليل أو فقدان وظيفة التيروزيناز ، فإنه سيؤثر على استقلاب الميلانين ويسبب أمراضًا مثل الصرع والمهق. ترتبط الأمراض الصبغية المتنحية في الحيوانات والبشر أيضًا بفقدان إنزيم التيروزيناز أو انخفاض النشاط [22].
6. مجسات التيروزيناز
المجسات عبارة عن مواد تتعرف على الهدف على وجه التحديد وتطلق إشارات قابلة للكشف تعكس وجود الهدف ونشاطه. كانت الطريقة اللونية التقليدية لتحليل التيروزينيز محدودة بسبب حساسيتها المنخفضة [23]. في البداية ، تم الإبلاغ عن العديد من طرق الكشف الأخرى القائمة على الكيمياء الكهربائية والجسيمات النانوية الذهبية من قبل مجموعة ويلنر [24e27] ، والتي لا تزيد من تعدد استخدامات الاكتشاف فحسب ، بل تعمل أيضًا على تحديث قياس الألوان بشكل كبير من حيث الحساسية. كما تم تقديم إستراتيجية الفلورسنت لتصميم مجسات التيروزيناز شديدة الحساسية كما هو موضح في الشكل 3. يمكن تطبيق النقاط الكمومية المطورة مبدئيًا ومجسات الفلورسنت البوليمر المترافق لمراقبة نشاط التيروزيناز [28]. ومع ذلك ، فإن مجسات الفلورسنت ذات الجزيئات الصغيرة جذابة بشكل خاص بسبب مزاياها الخاصة مثل الحساسية والنوعية والتوافق. في عام 2008 ، قام فريق Zhu بتصنيع oligo جديد قابل للذوبان في الماء (phenylenevinylene) (Pr1) باعتباره فلوروفور يحتوي على رأس حربي التيروزين (WH) كمسبار فلورسنت للتيروزيناز. تم إثبات أن Pr1 مناسب للكشف عن نشاط التيروزيناز حتى الآن في محلول منظم مائي حتى في هلام الاغاروز [29]. أولاً ، تم استخدام مسبار الفلورسنت القريب من الأشعة تحت الحمراء (NIR) السيانين (Pr2) لمراقبة نشاط التيروزيناز في عام 2010 بواسطة Ma et al. [30]. يمكن اكتشاف التغير الكبير في اللون قبل وبعد التفاعل بالعين المجردة. ومع ذلك ، تُظهر هذه المجسات أيضًا وضع إيقاف ناتج عن جزء الكينون الناتج عن الأكسدة المحفزة بالتيروزيناز. ومع ذلك ، بالنسبة للاستخدام الوظيفي ، فإن أفضل نهج هو تنفيذ اختبار حيوي في وضع التشغيل نظرًا لحساسيته ومدى ملاءمته للتصوير الحيوي للتيروزيناز في الأنظمة الحية. في عام 2010 ، Kim et al. [31] اقترح مسبارًا فلوروجينيًا قائمًا على BODIPY للكشف عن نشاط التيروزيناز الداخلي في خلايا الورم الميلانيني الحية (Pr3 ، الشكل 4). استنادًا إلى بحث سابق عن التيروزيناز المطبق لإزالة مجموعات الأمينات الحامية [32] ، يان وآخرون. [33] مسبار التيروزيناز المُعد ، Pr4 و Pr5 ، حيث تم ربط مجموعة الفينول ومجموعة النفثيلامين من خلال رابط اليوريا في عام 2012. والأهم من ذلك ، كان Pr4 أول مسبار فلوروجينيك يعمل بالفوتونين مصمم لاكتشاف نشاط التيروزيناز في العازلة المائية والخلايا الحية. في عام 2013 ، قام Wang et al. [34] أظهر أن المسبار الفلوري المعتمد على NBD-NH 2- (Pr6 و Pr7) الذي يحتوي على شقوق الفينول (WH) يمكن استخدامه لاكتشاف نشاط التيروزيناز وشاشة مثبطات التيروزيناز المحتملة من خلال "تشغيل" إستراتيجية. ومع ذلك ، لا توجد تجربة بيولوجية متعلقة بتصوير الخلايا في هذا العمل. في عام 2016 ، صمم لي وزملاؤه مجموعة من المجسات الجديدة استنادًا إلى 7- أمينو -4- (ثلاثي فلوروميثيل) - الكومارين باعتباره فلور فلوروفور وقاموا بتصنيعها ، Pr 8-11 ، بمسافات متفاوتة بين FL الفلوروفور والفينولات. تم العثور على Pr9 ليكون مسبار فلوروجينيك "تشغيل" حساس للغاية وانتقائي لتصوير خلايا الورم الميلانيني الحية [35]. في عام 2018 ، كان فريق Wu أول من استخدم مسبار الفلورسنت FL (Pr12) لتشخيص سرطان الجلد المبكر في نماذج الفئران القوارض (الشكلان 4 و 5 أ). يمكن تنشيط المسبار عن طريق أكسدة التيروزيناز بوساطة ثم تحلل روابط اليوريا بالماء لإنتاج إشارة مضان. في الوقت نفسه ، يمكنه أيضًا مراقبة مستوى التيروزيناز الداخلي في الخلايا الحية وسمك الزرد بحساسية وانتقائية (الشكل 5 ب / ج) [36].

في عام 2016 ، طورت مجموعة Ma [37] مسبارًا فلوروجينيًا جديدًا يسمى Mela-TYR (Pr13 ، الشكل 4) لاستهداف الميلانوزومات للكشف عن نشاط التيروزيناز. تم تصميم Pr13 من خلال دمج الفثاليميد مع المورفالين و 4- اليوريا المشتقة من الأمينية الفينول. يُظهر المسبار استجابة تشغيل انتقائية وحساسة للغاية للتيروزيناز من خلال تفاعل الأكسدة والانقسام. تحتوي مجسات التألق الموصوفة أعلاه بشكل أساسي على مجموعة هيدروكسيفينيل 4- باعتبارها جزء التعرف (WH) وأظهرت استجابة مضان موازية للعديد من أنواع الأكسجين التفاعلية (ROS) والتيروزيناز ، وبالتالي تتداخل معها ROS. اكتشفت مجموعة Ma مجموعة جديدة للتعرف على التيروزيناز ، 3- هيدروكسي بنزيلوكسي (WH) ، والتي أظهرت آليات تفاعل متنوعة للتيروزيناز و ROS [38]. تم تطوير مسبار مضان NIR (Pr14 ، الشكل 4) عن طريق تثبيت 3- hydroxy benzyloxy في NIR fluorophore (HXPI) ، وأظهر استجابة غير نشطة للغاية للتيروزيناز بدلاً من ROS ، وبالتالي التغلب على التداخل. يسهل وجود مجموعة الهيدروكسيل 3- عملية التحلل بالهيدروكسيل بواسطة التيروزيناز في 4- الوظيفة الشاغرة ولكن ليس بواسطة ROS ، وسيخضع الوسيط لعملية إعادة ترتيب تلقائية 1 ، 6- ، مما يؤدي إلى إطلاق فلوروفور مجاني. تم إثبات الخصوصية العالية للمسبار المطور من خلال التصوير والكشف عن نشاط التيروزيناز الداخلي في الخلايا الحية وأسماك الزرد ، كما تم التحقق من الخصوصية العالية للمسبار عن طريق مقايسة الممتز المناعي المرتبط بالإنزيم (الشكلان 4 و 6). طورت مجموعة Ma بعد ذلك مسبارًا فلوروجينيًا آخر قيد التشغيل (Pr15 ، الشكل 4) يعتمد على resorufin مدمج مع 3- مجموعة هيدروكسيفينيل [39]. تم استخدامه لاكتشاف وتصوير نشاط التيروزيناز الداخلي في مجموعة متنوعة من الخلايا الحية. مستوحى من التصميم أعلاه ، اقترح Zhang وزملاؤه [40] مسبارًا فلوروجينيًا للتيروزيناز (Pr16 ، الشكل 4) مع resorufin باعتباره حامض الفلور ، وإستر البيناكول m-tolyl boronic acid (WH) كتعرف جديد على التيروزيناز شاردة. أظهر المسبار انتقائية عالية للتيروزيناز على المواد البيولوجية الأخرى ، بما في ذلك ROS. ومع ذلك ، فقد تداخلت معه بشدة بواسطة H2O2. في عام 2019 ، قام Hu et al. [41] أبلغ عن مسبار فلوروجينيك جديد ذو انتقائية كيميائية عالية يعتمد على الفلورسين (Pr17 ، الشكل 4) ، والذي يمكنه تتبع التيروزيناز في المختبر وفي الجسم الحي ، وتحقيق الاكتشاف الكيميائي الانتقائي العالي للتيروزيناز. بالإضافة إلى ذلك ، تفاعل المسبار في محلول مائي وأظهر تعزيزًا مضانًا لأكثر من 24 مرة في وجود التيروزيناز. بالإضافة إلى ذلك ، أظهر Pr17 خصائص غشاء الخلية ونفاذية الأنسجة الرائعة ، مما ساعد على نجاحه في متابعة نشاط التيروزيناز الداخلي في الخلايا الحية ونماذج الزرد. قامت مجموعة Ding ببناء مسبار مضان NIR جديد قابل للذوبان في الماء (Pr18 ، الشكل 4) يمكنه التعرف على التيروزيناز على وجه التحديد ، وهو مستقر للغاية في درجة الحرارة الفسيولوجية ودرجة الحموضة ويمكنه اكتشاف التيروزيناز بدقة في الأنظمة البيولوجية دون أن ينزعج من الكيانات المنتشرة في كل مكان. يمكن استخدامه لتصوير التيروزيناز في الخلايا الحية ، وسمك الزرد ، ونماذج الفئران ذات الصبغة الغريبة [42].

Sidhu وآخرون. ابتكر وصنع مسبارًا مضيئًا لقياس النسب (Pr19 ، الشكل 4) يعتمد على النفثاليميد. يحتوي Pr19 على انتقائية وحساسية عالية للتيروزيناز ، كما أن حد الكشف (LOD) منخفض جدًا [43]. يحدث التحوّل في طيف الانبعاث أو الإثارة بعد دمج المسبار مع المواد المتفاعلة. يمكن تسجيله باستخدام نسبة شدة التألق المقاسة عند طولين موجيين مختلفين ، وهو ما يسمى قياس النسبة. تظهر مجسات الفلورسنت Ratiometric القائمة على هذا المبدأ حساسيتها وانتقائيتها ويمكن استخدامها لدراسة وظيفة الإنزيم في الأنظمة الحية [44]. اقترح فريق Guo مسبارًا جديدًا لقياس المعدل وتشغيل الفلورسنت NIR (Pr2 0 ، الشكل 4) للكشف في الوقت الفعلي عن نشاط إنزيم التيروزيناز الداخلي. هذه الخصائص الخاصة لـ Pr20 ، جنبًا إلى جنب مع السمية الخلوية النادرة ، والخصائص الفيزيائية الضوئية الفائقة ، ونفاذية غشاء الخلية ، تجعله مثاليًا للكشف الكمي عن نشاط التيروزيناز الداخلي [45]. يمكن التحكم في مشتقات السيانين ، مثل الأصباغ الفلورية NIR النموذجية ، في المحاليل المائية ، وبالتالي تظهر العديد من الخصائص الطيفية المختلفة بشكل كبير. يمكن بسهولة استبدال ذرة الكلور الموجودة في وسط الهيكل العظمي للسيانين بمجموعات وظيفية أخرى. بناءً على هذه الوظيفة ، قام Zhang et al. [46] طور مسبار الفلورسنت الجديد القائم على السيانين (Pr21 ، الشكل 4) لاكتشاف مضان قياس النسب لنشاط التيروزيناز (الشكل 7). حصل تحديد النسبة على نسبة إشارة إلى ضوضاء جيدة ، وكانت قيمة LOD لنشاط التيروزيناز 0.02 وحدة / مل. بالإضافة إلى ذلك ، تم استخدام Pr21 بنجاح في تصوير نشاط التيروزيناز الداخلي المنشأ في خلايا B16 وتمييزه نوعياً عن الخلايا السرطانية / الطبيعية الأخرى في غياب التيروزيناز (الشكل 7).
7. مثبطات التيروزيناز
تنقسم المثبطات عمومًا إلى مثبطات عكوسة ومثبطات لا رجعة فيها بناءً على ما إذا كانت المثبطات التي تتفاعل مع الإنزيمات تسبب تثبيطًا دائمًا للإنزيم. إن خاصية التثبيط التي يتميز بها التيروزيناز هي تثبيط قابل للعكس. بالنسبة للتثبيط الذي يتميز بالتثبيط القابل للعكس ، فإن الجمع بين المانع والإنزيم هو عملية توازن ديناميكي عكسي [47e49]. ستؤدي زيادة تركيز المثبط إلى انخفاض نشاط الإنزيم ولكن المثبط يثبط فقط نشاط الإنزيم بدلاً من تثبيط الإنزيم بشكل دائم. عندما ينخفض تركيز المثبط ، سيزداد نشاط التيروزيناز. وفي الوقت نفسه ، فإن التثبيط الذي لا رجعة فيه سيكون التثبيط الدائم للتيروزيناز. وفقًا للمواقع والأساليب المختلفة لتفاعل مثبطات التيروزيناز مع الإنزيم ، يمكن تقسيمها إلى أربعة أشكال: ارتباط تنافسي ، وغير تنافسي ، ومختلط ، وبطيء.


مركبات الفلافونويد هي مجموعة من المركبات تتكون من حلقتين بنزين متصلتين بسلسلة من ثلاثة كربون. نظرًا لأن مجموعات السلسلة الجانبية للهيدروكسيل والميثوكسي والجليكوزيد موجودة في حلقات البنزين ، يمكن تقسيم الترتيب إلى مركبات الفلافونول والكالكون وثنائي هيدروفلافون والبرتقالي (الشكل 8) [56]. يتم توزيع الفلافونويد على نطاق واسع في الأوراق والبذور والجلود وأتباع النباتات ، وقد تحقق الباحثون من أكثر من 4000 فلافونويد. بالنسبة لبعض النباتات ، تتمتع مركبات الفلافونويد ومشتقاتها بحماية ضد الأشعة فوق البنفسجية ومسببات الأمراض والحيوانات العاشبة [57]. يُظهر تحليل بنية مستخلص جذر عرق السوس أن القدرة التثبيطية للتيروزيناز لكل من الجليسيررهيزين الجديد ، والجليسرهيزين ، والإيزليكويريتجينين ، والجليسريهيزين مرتبطة بقدرتها على التثبيط للدهون. من بينها ، يكون تثبيط المونوفينول أكثر فعالية من تثبيط الديفينول ، مما يشير إلى أنه تفاعل يحد من المعدل في الخطوة الأولى من تفاعل الأكسدة [58].
يمكن لبعض مركبات الفلافونات التي تحتوي على {0} بنية هيدروكسي -4- أن تثبط نشاط الإنزيم بشكل تنافسي عن طريق مخلب النحاس في الموقع النشط للتيروزيناز ، مما يؤدي إلى تعطيل لا رجعة فيه لإنزيم التيروزيناز. بعد مخلب التيروزيناز ، يفقد الجزيء نظريًا هيكله المستوي ويصبح مشوهًا. عادة ما تكون المثبطات التنافسية متوازية في هيكلها مع الركيزة ، لذلك يدخل الجزيء بسهولة إلى موقع التيروزيناز النشط ويمنع دخول L-DOPA [59،60]. Jeong et al. استخراج اثنين من الفلافونول من أوراق Zanthoxylum piperitum. يمكن أن تمنع مركبات الفلافونول نشاط التيروزيناز في الفطر ، وهو تثبيط تنافسي ، لكنه لا يمكن أن يمنع إنتاج الميلانين من Streptomyces bikiniensis. في وقت لاحق ، وجد أن مركب الفلافونويد المعزول من فورموزا الفلبينية يمكنه أيضًا تثبيط التيروزيناز ، والتأثير المثبط أفضل من تأثير حمض الكوجيك [62]. Liang et al. وجد أن الصباغ الأصفر القرطم يمكن أن يمنع أيضًا نشاط التيروزيناز في الفطر ، بتركيز مثبط نصف أقصى (IC50) بقيمة 1.01 مجم / مل. يبدو أن علاقة التثبيط هذه تعتمد على الجرعة [63]. (2R ، 3R) - (þ) - البيبورين المستخرج من Shuiliao يثبط 70 بالمائة من نشاط التيروزيناز والتركيز 0.50 ملي مولار. القدرة التثبيطية أفضل من حمض الكوجيك والأربوتين [64].
7،8 ، 40 - ثلاثي هيدروكسي فلافون هو أحد مشتقات الفلافونويد الذي يثبط نشاط التيروزيناز ديفينولاز بطريقة غير تنافسية مع قيمة IC5 0 1 0. 31 ± 0.41 ملي مولار وكي من 9.50 ± 0.40 ملم. آلية عمل هذا المركب مع التيروزينيز هي آلية ثابتة وتوضح موقع ربط واحد مع ثابت ربط (7.05 ± 1.20) × 104 م -1 عند 298 ك. توضح المعلمات الديناميكية الحرارية أن عملية الترابط مرتبطة إلى الترابط الهيدروجيني وقوى فان دير فالس [51].

3 ، 8- هيدروكسي كينولين (In1 ، الشكل 9 [65]) المنفصل عن إعانات Scolopendra mutilans يمكن أن تمنع إنتاج وأكسدة الميلانين في خلايا الميلان أ. يُظهر In1 تأثيرًا مضادًا للأكسدة متطورًا بالتركيز ويثبط بشكل كبير نشاط التيروزيناز في الفطر من خلال التثبيط غير التنافسي. في الوقت نفسه ، وجد أن In1 غير سام للخلايا في الدراسة كما هو موضح في الجدول 1 [65]. يمكن لجزء أسيتات الإيثيل من مستخلص زهرة Nymphaea nuchal (NNFE) (1 0 0 مجم / مل) أن يقلل بشكل فعال من إنتاج الميلانين ويثبط نشاط التيروزيناز في الفطر. تتضمن الآلية الأساسية التدخل في عوامل النسخ ومسارات الإشارات العامة في تخليق الميلانين [66]. يمكن أن يثبط الكابسيسين (In2 ، الشكل 9 [67]) و dihydrocapsaicin (In3 ، الشكل 9) المستخلص من الفلفل نشاط التيروزيناز. تظهر النتيجة أن قيمة IC50 لـ In2 أصغر 1.73 مرة من قيمة In3. يدعم ثابت التثبيط (Ki) أيضًا النشاط المثبط لـ In3 (0.39 ملي مولار ، الجدول 1) على التيروزينازيسلاسر من مثيله في In2 (0.30 ملي مولار ، الجدول 1) [67]. لقد وجد أن الكافيين (In4 ، الشكل 9 [68]) المستخرج من حبوب لقاح الكاميليا يظهر نشاطًا مثبطًا قويًا تجاه التيروزيناز الفطر في نموذج غير تنافسي كما هو موضح في الجدول 1. يغير In4 موقع الربط لـ L-tyrosine والحلقة التشكل المجاور للمركز النشط من خلال الارتباط بالتيروزيناز. أظهرت النتائج التجريبية أن In4 له تأثير مثبط واضح على نشاط التيروزيناز في الخلايا وأن إنتاج الميلانين لخلايا سرطان الجلد B16F10 مرتبط بالتركيز [68]. يمكن لحمض الكفتاريك (In5 ، الشكل 9) المستخرج من العنب أن يثبط بشكل تنافسي التيروزيناز ، وقيمة IC50 (الجدول 1) أقل من تلك الخاصة بالمركبات العلائقية وأحماض الكافيين والكلوروجينيك [47]. يمكن أن يرتبط Phloretin (In6 ، الشكل 9) بالتيروزيناز من خلال عملية ثابتة ، مما يؤدي إلى تغيير شكل التيروزيناز ، وبالتالي تثبيط نشاطه. في نفس الوقت ، In6 لديه قدرة قوية مضادة للأكسدة والقدرة على تقليل o-dopaquinone إلى LDOPA [48].

قام الباحثون بتقييم اثنين من أكريدين سبيرو (AMTAC -01 ، In7 ، الشكل 9) و (AMTAC -02 ، In8 ، الشكل 9) كمثبطات لإنزيم التيروزيناز. أظهرت النتائج أن مشتقات الأكريدين تتفاعل بقوة مع فطر التيروزيناز. يعتبر In8 أكثر فعالية في تثبيط نشاط الإنزيم من In7 كما هو موضح في الجدول 1 ، مما يشير إلى أن مجموعة methoxy من In8 مرتبطة ارتباطًا وثيقًا بالنشاط المثبط [49]. تم تصنيع العديد من 21 ثيوسيميكاربازون المهلجن (TSCs) والتحقيق فيها. وجد أن TSCs 6 و 12 و 21 (In9 / 10/11 ، الشكل 9 [69]) تظهر خصائص مثبطة قوية مع IC مختلفة ، على التوالي (الجدول 1). لقد أظهروا آلية قابلة للعكس بشكل متبادل وتنافسية لتثبيط إنزيم التيروزيناز. من بين المركبات التي تمت دراستها ، فإن مشتقات الأسيتوفينون شبه المستبدلة من ثيوسيميكاربازونات لها أعلى صلة بالإنزيم [69]. البنسلين V (في 12 ، الشكل 9) هو مضاد حيوي مضاد للجراثيم ب لاكتام. لقد وجدت الدراسات أن In12 يمكن أن يثبط نشاط mycophenolate و diphenolase. لقد أظهرت دراسات التبريد بالفلورة والالتحام الجزيئي أن In12 يمكن أن يشكل تفاعلًا ثابتًا بالقرب من الجيب التحفيزي للإنزيم ، مما يعيق نقل الركيزة إلى الموقع النشط ويقلل من ليونة النحاس للتحفيز [70]. في الآونة الأخيرة ، Raza et al. درس الإمكانات المثبطة لـ N- (استبدال فينيل) -4- {(4- [(E) -3- فينيل -2- بروبينيل] -1- بيبرازينيل) بيوتاناميدات ( 5a-e) على التيروزيناز. تم العثور على جميع المركبات لتكون نشطة بيولوجيا ، مع 5 ب (في 13 ، الشكل 9) تظهر أعلى قدرة تثبيط [71]. Mahajan et al. تم تصميم وتصنيع كينازولينون بن أميدات 4a-h (In14e21 ، الشكل 9). من خلال دراسة التأثير المثبط للمركبات على نشاط التيروزيناز ، وجد أن جميع المركبات تظهر قيم IC أقل من حمض الكوجيك القياسي كما هو موضح في الجدول 1 [72]. شين وآخرون. وجد مثبطًا جديدًا للتيروزيناز ، وهو الببتيد ECGYF (EF -5 ، In22) كما هو موضح في الشكل 9. يعتمد الارتباط بين In22 والتيروزيناز بشكل أساسي على الترابط الهيدروجيني والتفاعلات الكارهة للماء ، وتأثير تثبيط التيروزيناز أقوى من أن أربوتين والجلوتاثيون [73]. هو وآخرون. عزل ثلاثة تاماريسينول 1/2/3 (في 23/24/25) واثنين من الفينول 4 و 5 (في 26 و 27) كما هو موضح في الشكل 9. أظهرت التجارب أن جميع العزلات لها تأثيرات مثبطة على تيروزيناز الفطر ، مع كون In23 هو الأكثر فعالية (الجدول 1) [74].

لمزيد من المعلومات: david.deng@wecistanche.com WhatApp: 86 13632399501






