تقييم خصائص مضادات الأكسدة والتبييض ومكافحة الشيخوخة لبروتين الأرز
Mar 27, 2022
اتصال:joanna.jia@wecistanche.com/ واتساب: 008618081934791
Hui-Ju Chen1،2، Fan-Jhen Dai 2، Cheng-You Chen 3، Siao-Ling Fan 2، Ji-Hong Zheng 4، Yu-Chun Huang 2، Chi-Fai Chau 1، Yung-Sheng Lin3،4 ، 5 ، * و Chin-Shuh Chen1 ، *
قسم علوم الأغذية والتكنولوجيا الحيوية ، جامعة تشونغ شينغ الوطنية ، تايشونغ 402204 ، تايوان ؛ d103043004@mail.nchu.edu.tw (H.-JC) ؛ chaucf@nchu.edu.tw (C.-FC)
شركة Healthmate المحدودة ، مدينة تشانغهوا 500016 ، تايوان ؛ jane@healthmate.com.tw (F.-JD) ؛ eileen@healthmate.com.tw (S.-LF) ، tina@healthmate.com.tw (Y.-CH)
دكتوراه. برنامج في المواد والهندسة الكيميائية ، الجامعة الوطنية المتحدة ، مياولي 360001 ، تايوان ؛ D0612002@smail.nuu.edu.tw
قسم الهندسة الكيميائية ، الجامعة الوطنية المتحدة ، مياولي 360001 ، تايوان ؛ U0714049@smail.nuu.edu.tw
معهد تقييم مخاطر سلامة الأغذية والصحة ، جامعة يانغ مينج الوطنية ، تايبيه 112304 ، مراسلات تايوان: linys@nuu.edu.tw (Y.-SL) ؛ cschen@mail.nchu.edu.tw (C.-SC)
الخلاصة: تحلل البروتينات المشتقة من النباتات لها تطبيقات محتملة في التغذية. جذبت تحلل بروتين الأرز (RPHs) ، وهي مصدر ممتاز للبروتينات ، الانتباه لتطوير مستحضرات التجميل. ومع ذلك ، فقد أبلغت دراسات قليلة عن التطبيق المحتمل لـ RPH في التحليل ، وفحصت هذه الدراسةمضادات الأكسدةالأنشطة والأنشطة المثبطة لأنزيمات شيخوخة الجلد. أشارت النتائج إلى أن تركيزات الفينول الكلية والفونويد كانت 2. 0 6 士 0. ، على التوالى. أظهرت RPHs نشاطًا يعتمد على الجرعة للتخلص من الجذور الحرة من 1 و 1- diphenyl -2- picrylhydrazyl [تركيز مثبط نصف الحد الأقصى (IC50)=42. 58 士 2.1 مجم / جم RPHs] و 2 ، 2 ′-and-bis (3- ethylbenzothiazoline -6- sulfonic acid) (IC 50=2. 11 士 0.88 mg / g RPHs) ، قدرة التخفيض المعتمدة على الجرعة (6.95 1.40 مجم فيتامين مكافئ C / جم RPHs) وسعة امتصاص جذور الأكسجين (473 ميكرو مول من مكافئ ترولوكس / جم RPHs). تراكيز محلول RPH المطلوبة لتحقيق 50٪ من تثبيط الهيالورونيداز والتيروزينازتم تحديد الأنشطة لتكون 8.91 و 107.6 مجم / مل على التوالي. أظهرت هذه الدراسة أن RPHs لديهامضادات الأكسدة، ومضادات الهيالورونيداز ، ومضادات-التيروزينازأنشطة لتطبيقات التجميل في المستقبل.
الكلمات الرئيسية: تحلل بروتين الأرز ؛ مضادات الأكسدة. هيالورونيداز. التيروزيناز. مستحضرات التجميل

لدى Cistanche امتدادمضادات الأكسدةوالعناية التبييضتأثير
1 المقدمة
التعرض للأشعة فوق البنفسجية مسؤول عن الشيخوخة الضوئية (أو الشيخوخة الخارجية) ؛ على النقيض من ذلك ، فإن أنواع الأكسجين التفاعلية المنتجة في استقلاب الخلية وتدهور الوظائف البيولوجية هي المسؤولة عن الشيخوخة الذاتية [1،2]. غالبًا ما تحتوي الأطعمة المصنعة على مواد طبيعيةمضادات الأكسدةمثل الكاتيكين وحمض الأسكوربيك والتوكوفيرول وحمض روزمارينيك والمستخلصات الفينولية من نباتات مختلفة. أجريت البحوث في الطبيعةمضادات الأكسدةتعتبر الآن إثباتات غير تقليدية. من مصادر طبيعيةمضادات الأكسدةمرغوبة أكثر من المنتجات الكيميائيةمضادات الأكسدةحيث تم الإبلاغ عن بعض مضادات الأكسدة الاصطناعية لتكون مسببة للسرطان [3]. الأرز (Oryza sativa) هو عنصر غذائي رئيسي للناس في جميع أنحاء العالم ، وخاصة أولئك الذين يعيشون في آسيا. يبلغ إنتاج العالم السنوي من الأرز حوالي 741 مليون طن [4]. في البلدان الآسيوية ، يُقال إن الأرز هو مصدر 75٪ من الطاقة المستهلكة لأكثر من 2 مليار شخص [5]. ينتج عن إنتاج الأرز المكثف كمية مماثلة من إنتاج المنتج الثانوي. يحتوي المنتج المتبقي من عملية إنتاج الأرز على غالبية بروتين الحبوب (~ 60-85 بالمائة) ولكن يتم التخلص منه أو استخدامه لتغذية الحيوانات [6-8]. يقال إن الببتيدات التي تم الحصول عليها من محللات بروتين مختلفة تعمل كإمكاناتمضادات الأكسدة[9]. لذلك يمكن استخلاص مضادات الأكسدة الطبيعية وغير السامة من محللات البروتين الغذائي. استخدم العديد من العلماء نماذج غنية بالدهون وأبلغوا عن تحلل البروتين وكذلك الحليب والزين وببتيدات بروتين الصويا لتكون حاسمة.مضادات الأكسدةالخصائص ، بما في ذلك إزالة الجذور الحرة ، وتثبيط الطعام ، وبيروكسيد الدهون في المختبر ، واستخلاب المعادن الانتقالية [١٠-١٢].
يساعد حمض الهيالورونيك (HA) على تجديد شباب الجلد لأنه يزيد من اللزوجة ، ويحتوي على الرطوبة ، ويجعل السوائل خارج الخلية أقل نفاذية. بسبب قدرته الممتازة على الاحتفاظ بالماء ، يزيد حمض الهيالورونيك من نضارة البشرة وترطيبها ونعومتها ويقلل من درجة التجاعيد [13 ، 14]. لسوء الحظ ، ينخفض مستوى HA في الجلد بشكل طبيعي مع تقدم العمر. Hyaluronidase هو إنزيم يدمر HA ، مما يتسبب في فقدان قوة الجلد ، والمرونة ، والرطوبة ، والتي بدورها تؤدي إلى شيخوخة الجلد. لذلك ، يمكن معالجة التجاعيد عن طريق تثبيط الهيالورونيداز والحفاظ على محتوى HA في الجلد [15،16]. الإنزيم المنتج للميلانينالتيروزينازيساهم بشكل حيوي في خطوة تحديد معدل العملية التي يتم من خلالها إنتاج الميلانين. لذلك ، يتم علاج اضطرابات التصبغ بشكل شائع ويتم تحقيق تفتيح البشرة عن طريق تثبيط أو تقليل التنظيمالتيروزينازنشاط [17 ، 18].
في العديد من الدراسات ، تم اكتشاف تحلل بروتين الحبوب والببتيدات التي يمكن الحصول عليها منهامضادات الأكسدة، الأنشطة الخافضة للضغط ، والأورام [19 ، 20]. يتم التعرف تدريجياً على المساهمات الإيجابية للببتيدات والبروتينات التي تنتج عن الغذاء في صحة الإنسان [21]. يطالب المستهلكون بشكل متزايد بأن تستخدم صناعات مستحضرات التجميل والرعاية الصحية مركبات طبيعية نشطة بيولوجيًا. جذبت تحلل بروتين الأرز (RPHs) الانتباه كمصدر ممتاز للبروتينات. ومع ذلك ، فقد أبلغت دراسات قليلة عن توصيف وتحليل وظيفي لـ RPHs. لذلك ، قيمت هذه الدراسةمضادات الأكسدةالنشاط والهيالورونيداز والتيروزيناز-منع
أنشطة RPHs.
2. النتائج والمناقشة
2.1. إجمالي تركيز الفينول (TPC) ومحتوى الفلافونويد الكلي (TFC)
كان المعيار في مقايسة TPC هو حمض الغال بتركيزات عديدة. يشير الامتصاص العالي إلى ارتفاع TPC. تم الحصول على TPC لعينات RPH عن طريق إدخال قيم الامتصاص البصري لعينات RPH في منحنى معايرة حمض الغال. من خلال رسم تركيز RPH مقابل تركيز الفينول (الشكل 1 أ) ، تم الحصول على متوسط TPC من 2. 0 6 士 0. 13 مجم GAE / g RPHs. تم الحصول على TFC من 25.96 士 0. 52 ميكروغرام QE / g RPHs باتباع إجراء مماثل (الشكل 1 ب). يرتبط الشكل 1 ج كذلك بـ TPC و TFC لعينات RPHs. يكشف أن العلاقة بين TPC و TFC يمكن التعبير عنها بالصيغة y=0. 0121x زائد 0.0659 ، حيث x و y هما TPC و TFC ، على التوالي.
تضمن TPC لـ RPHs تركيزات الأحماض الأمينية الفينولية والمركبات الفينولية من الببتيدات. يتضمن التفاعل المركب بين البروتين والفينول عمومًا الترابط التساهمي وغير التساهمي. يتم إطلاق المركبات الفينولية أثناء التحلل المائي الأنزيمي. قد تكون إنزيمات معينة أكثر قدرة على تدمير معقدات البروتين والبوليفينول. ينتج عن هذا عدد أكبر من المركبات الفينولية والببتيدات مع المجموعات الفينولية ، مثل التيروزين ، التي يتم إطلاقها [22]. تم الإبلاغ عن ارتباط قوي بين محتوى الحبوب الكلي من مادة البوليفينول ونشاطها البيولوجي. من المعروف أن البوليفينول قويمضادات الأكسدةالأنشطة [23]. على الرغم من وجودها بكميات أقل ، إلا أن التربينات [24] أو سيسكيتيربينز [25] في الأرز يمكن أن تساهم أيضًا فيمضادات الأكسدةأنشطة.
2.2. نشاط مضادات الأكسدة
2.2.1. نشاط الكسح الجذري للجذور الحرة DPPH
يصور الشكل 2 نشاط إزالة الجذور الحرة DPPH في محلول RPH. تم اكتشاف تركيز أعلى من المحلول لينتج عنه نشاط أعلى. كان تركيز المثبط نصف الأقصى (IC50) ، وهو تركيز المستخلص الذي يمكن تنظيف نصف جميع الجذور الحرة DPPH ، 42.58 × 2.1 مجم / مل من ببتيدات الأرز.



2.2.2. نشاط الكسح للجذور الحرة ABTS
كان نشاط إزالة الجذور الحرة ABTS من RPHs ، الموضح في الشكل 3 ، أعلى عندما تم استخدام تركيز أكبر للمستخلص. كان IC5 0 2.11 0.88 مجم / مل من ببتيدات الأرز. أشارت هذه النتيجة إلى أن RPHs لها نشاط قوي في إزالة الجذور الحرة من ABTS. الأحماض الأمينية المحتوية على الكبريت ، بما في ذلك Met و Cys ، والأحماض الأمينية الكارهة للماء ، بما في ذلك Ala و Val و Ile و Leu و Met و Cys و Tyr و Phe و Try and Pro ، قد تكون عوامل مهمة فيما يتعلق بنسح الجذور الحرة ABTS نشاط [26]. علاوة على ذلك ، فإن الأحماض الأمينية العطرية ، بما في ذلك Phe و Tyr ، تعزز أيضًا نشاط إزالة الجذور الحرة ABTS بسبب حلقات البنزين التي تتبرع بالبروتونات إلى الجذور المعينة للإلكترون [27].

الشكل 3. تأثير تركيز RPH على قدرة الكسح لـ 2،2 ′ -azino-bis (3- ethylbenz- othiazoline -6- sulfonic acid) (ABTS).
في هذه الدراسة ، كانت قيمة IC50 لنشاط إزالة الجذور الحرة ABTS أقل من نشاط إزالة الجذور الحرة DPPH ، بما يتفق مع نتائج قشرة بذور Jatropha curcas L. ونواة البذور [28] وبذور فاكهة العناب ولب قشرها [29]. تتوافق هذه النتيجة أيضًا مع تقرير التحليل المائي لبروتين نخالة الأرز مع عينة 43.98-66.25 ميكرولتر ترولوكس مكافئ / جم وعينة 403.28-430.12 ميكروجرام ترولوكس مكافئ / جم لنشاط إزالة الجذور الحرة DPPH ونشاط إزالة الجذور الحرة ABTS ، على التوالي [27].
أحد الأسباب المحتملة هو الاختلاف في قابلية الذوبان بين الجذور الحرة DPPH (القابل للذوبان في الزيت) والجذور الحرة ABTS (قابل للذوبان في الزيت / الماء) [30،31]. المضادات الأكسدةتأثرت إمكانات محللات بروتين نخالة الأرز من خلال وزنها الجزيئي وتكوينها من الأحماض الأمينية والكارهة للماء [32].
2.2.3. قدرة التخفيض
يتم عرض نتائج مقايسة قدرة التخفيض لـ RPHs في الشكل 4. وزادت قدرة الإنجاز مع تركيز RPHs. كانت سعة الاختزال 6.95 × 1.40 مجم VCE / جم RPHs ، مما يشير إلى أن RPHs فعالةمضادات الأكسدة.

الشكل 4. تأثير تركيز RPH على قدرة الخفض.
2.2.4. قدرة امتصاص الأكسجين الجذري (ORAC)
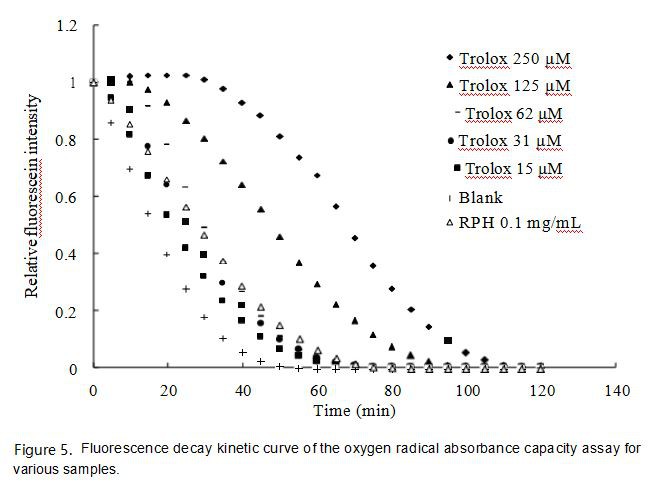
يتميز اختبار ORAC بمزايا مقارنة بالطرق الأخرىمضادات الأكسدةتحديد النشاط ، بما في ذلك المواد المتفاعلة المستخدمة باعتبارها جذور بيروكسي مع آلية مماثلة للتفاعل وإمكانية الأكسدة والاختزال للمؤكسدات الفسيولوجية ؛ حالة الشحن الكلي والبروتون التي بهامضادات الأكسدةتتفاعل مثل تلك الموجودة في جسم الإنسان [33]. طريقة ORAC لها أيضًا صلة بيولوجية بكفاءةمضادات الأكسدةفي جسم الإنسان. يوضح الشكل 5 نتائج تحليل ORAC لـ RPHs ومعيار Trolox بتركيزات مختلفة. تم اشتقاق ORAC من معادلة الانحدار لمنحنى المعايرة المتعلق بـ AUC الصافي لتركيز Trolox. أشارت النتائج إلى أن RPHs كان لها ORAC من 473 ميكرو مول من TE / جم RPHs.
مضادات الأكسدةيمكن الحصول على الببتيدات أو الأحماض الأمينية عن طريق التحلل المائي للبروتين الإنزيمي ، مما يؤدي إلى نشاط عالي ضد المؤكسدات [34]. إن عملية إزالة معدن ثقيل من أيونات المعدن ، وتثبيط بيروكسيد الدهون ، وكسح الجذور الحرة للببتيدات النشطة بيولوجيًا هي المسؤولة عن نشاطها المضاد للأكسدة. يمكن إخماد الجذور الحرة وتنظيم التعبير عن البروتينات والإنزيمات التي تقلل الإجهاد التأكسدي بواسطةمضادات الأكسدةالببتيدات. يقال إن فعالية مضادات الأكسدة في تحلل البروتين والببتيدات تعتمد على تسلسل الأحماض الأمينية وحجم الببتيد ، والتي تتأثر بظروف التحلل المائي ومصدر البروتين ونوع البروتياز [35]. وفقًا لـ Adebiyi et al. [36] ، أكبر بروتين قابل للهضم في نخالة الأرز يمكن تكسيره إلى قطع أصغر بواسطة السبيتيليزين ، مما يؤدي إلى زيادة إنتاجية البروتين ومحتواه. مادة TPC ومضادات الأكسدةقد يتأثر النشاط بمدينة معينة من الإنزيمات. لذلك ، قد يتأثر نشاط الببتيد المضاد للأكسدة بخصائص مصدر البروتين ، ومدينة الإنزيم المحددة ، ومستوى التحلل المائي [37].
هناك العديد من التقارير التي تستخدم البروتياز (مثل Alcalase ، وهو الاسم التجاري لمادة subtilisin A من أنواع العصيات) لتحليل البروتينات المشتقة من النبات للحصول علىمضادات الأكسدةالببتيدات. في هذا الصدد ، يعتبر بروتين الصويا أحد أكثر البروتينات التي تم الإبلاغ عنها [38]. علاوة على ذلك ، تم العثور أيضًا على التحلل المائي Alcalase لبروتين نخالة الأرز. في ظل الظروف المثلى ، أنتج التحلل المائي Alcalase لنخالة الأرز الدبق تحلل بروتيني بقيمة IC5 0 بقيمة 0. 87 士 0.02 مجم / مل في إزالة الجذور الحرة DPPH [39]. في دراستنا ، كانت قيمة IC50 لـ RPHs 42.58 × 2.1 مجم / مل. على الرغم من أن قيمة IC50 في كاسح الجذور الحرة DPPH في هذه الدراسة لم تكن فعالة مثل تلك الموجودة في بروتين نخالة الأرز ، إلا أن تفكيك الجذور الحرة ABTS (IC 50=2. 11 مجم / مل) كان أكثر فعالية من التحلل المائي لبروتين الصويا الذي تم الحصول عليه بواسطة Alcalase التحلل المائي (IC 50=2. 93 مجم / مل) [40].
2.3 نشاط تثبيط الهيالورونيداز
تم العثور على إنزيم حل للبروتين ، هيالورونيداز ، في الأدمة ويحفز تحلل HA في المصفوفة خارج الخلية [41]. استخدمت هذه الدراسة حمض التانيك كعنصر تحكم إيجابي لأغراض المقارنة. يوضح الشكل 6 أن حمض التانيك كان له تأثير أعلى في تثبيط نشاط الهيالورونيداز ؛ كان IC5 0 0. 14 مجم / مل ، على غرار القيمة التي حصل عليها Nishida et al. (0.121 مجم / مل ، 71.1 مم) [42]. على النقيض من ذلك ، تم حساب تركيز IC بقيمة 8.91 مجم / مل لمحلول RPH. تتوافق نتيجة محلول RPH مع قيمة IC50 السابقة ، 7.61 مجم / مل [43]. تعد البروتينات والسكريات والمركبات النباتية والمخلقة من بين مجموعة المركبات التي توجد فيها مثبطات الهيالورونيداز. تساعد هذه المثبطات في الحفاظ على توازن تحلل تخليق HA [44]. يؤدي انخفاض تركيز حمض الهيالورونيك في الجلد إلى الجفاف والتجاعيد. لذلك ، فإن تثبيط نشاط الهيالورونيداز هو الطريق الذي يمكن من خلاله تحسين شكل الجلد وتأخير الشيخوخة.

2.4 نشاط التيروزيناز المثبط
تحلل البروتينات من المصادر الطبيعية لديها القدرة على التثبيطالتيروزينازنشاط. عادة ما يستخدم اختبار تثبيط التيروزيناز في المختبر لتقييم كيفية تأثير عوامل تبييض الجلد بشكل مباشر على نشاط التيروزيناز [45]. من خلال المشاركة في خطوة الحد من معدل تخليق الميلانين ،التيروزينازيحفز L-tyrosine hydroxylation إلى L-DOPA ثم أكسدة الأخير إلى o-dopaquinone. عندما يكون من المرغوب فيه منع التخليق الحيوي للميلانين ، يمكن أن يكون تثبيط نشاط L-tyrosinase أمرًا بالغ الأهمية. هنا،التيروزينازتم استخدامه لقياس نشاط أنتيتروزيناز RPH. كما هو مبين في الشكل 7 ، حقق التركيز 1 0 7.6 مجم / مل 50 بالمائة من تثبيط نشاط التيروزيناز. أظهر حمض الأسكوربيك نشاطًا عاليًا لمثبطات التيروزيناز (IC 50=0. 098 مجم / مل) ، والذي كان مشابهًا لـ 0.102 مجم / مل الذي أظهره Seo et al. ذكرت [46].

الشكل 7. تأثير تركيز RPH علىالتيروزيناز- نشاط مانع. الوسائل التي لا تشترك في نص مرتفع مشترك تختلف اختلافًا كبيرًا (ص <0.>
أظهرت التحلل المائي لبروتين نخالة الأرز ارتفاعًا ملحوظًاالتيروزيناز- نشاط مانع [47 ، 48]. قد ينتج النشاط المثبط للتيروزيناز لمحلول RPH من بروزات الأحماض الأمينية للببتيدات. شورينك وآخرون. وصفها بأنها فعالةالتيروزيناز- الببتيدات المثبطة تتكون من بقايا أرجينين و فينيل ألانين [49]. يمكن تحسين النشاط المثبط للتيروزيناز عن طريق بقايا الأحماض الأمينية الكارهة للماء (على سبيل المثال ، ألانين) ، ويمكن تعطيل إنتاج الميلانين بواسطة الألانين [50]. الى جانب ذلك ، Zhang et al. ذكرت أيضًا أن تحلل بروتين الأرز يمكن أن يقلل من محتوى الميلانين والتيروزينازالنشاط في نموذج الخلية التي يسببها UVB [51].
2.5 الأحماض الأمينية Pro les و MWs من RPHs
كان محتوى بروتين الأرز بعد إزالة النشا في الدراسة الحالية 23.56٪ بالوزن ، ودرجة التحلل المائي للعينة المتحللة بواسطة البروتياز كانت 9.36٪. يوضح الجدول 1 تكوين الأحماض الأمينية في RPHs. في العينة ، احتوى كل 100 جم على 5.18 جم من الأحماض الأمينية. فيما يتعلق بمكونات الأحماض الأمينية ، كانت RPHs غنية بالألانين ، والليوسين ، والأرجينين ، وحمض الجلوتاميك ، وحمض الأسبارتيك. احتوت كل 100 جم من العينة على 1.73 جم من الأحماض الأمينية الطاردة للماء (ألانين ، فالين ، ليسين ، آيزولوسين ، برولين ، فينيل ألانين وسيستين) إجمالاً. كانت هذه النتيجة مختلفة تمامًا عن تقريرنا السابق [43] في محلول الأميليز ودرجة حرارة معالجته لإزالة النشا. كان محتوى الأحماض الأمينية الكارهة للماء أعلى 1.90 مرة من تقريرنا السابق. قد تمنع درجة حرارة المعالجة المنخفضة (60 درجة مئوية) في هذه الدراسة تمسخ البروتينات بكميات كبيرة ، بحيث يمكن الحفاظ على نشاط الأحماض الأمينية بشكل أفضل. بالإضافة إلى ذلك ، تم الحصول على النتيجة المماثلة أيضًا من الأميليز الفطري وجلوكومايلاز لتسكير النشا في نخالة الأرز الأبيض [52].
الجدول 1. بروتوكولات الأحماض الأمينية لعينات تحلل بروتين الأرز (RPH).
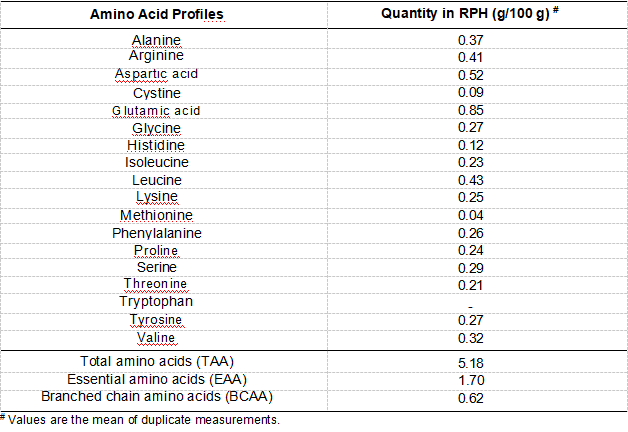
وجدت الأبحاث أن الأحماض الأمينية الكارهة للماء تشبهمضادات الأكسدةعن طريق رفع قابلية الذوبان القائمة على الدهون في تحلل البروتين والببتيدات من مصادر البروتين المختلفة ، وبالتالي تعزيز التفاعل مع الجذور الحرة [38،53]. تم الإبلاغ عن بعض الأحماض الأمينية بواسطة Chen et al. [54] لتكون مضادات الأكسدة بشكل عام. وتشمل الأحماض المذكورة التربتوفان ، والسيستين ، والميثيونين ، والتيروزين ، والهيستيدين. في هذه الدراسة ، تتكون الأحماض الأمينية العطرية (فينيل ألانين ، التيروزين ، والتربتوفان) من 0. 53 جم / 100 جم من RPHs. لذلك ، من المحتمل أن تكون هذه الأحماض الأمينية الناشئة عن الببتيد مسؤولة عن RPHsمضادات الأكسدةنشاط.
بالإضافة إلى ذلك ، فإن البروتينات التي يتم تحللها إلى ببتيدات أقصر لها توزيع ميغاواط مختلف ، وبعض المجموعات الكارهة للماء المطوية في الجزء الداخلي من جزيئات البروتين الطبيعي الكامل عادة ما تتعرض للمرحلة المائية. يرتبط هذا بإعادة ترتيب جزيئات البروتين هيكليًا وبالتالي بالخصائص الوظيفية للبروتين [55،56]. أشارت بيانات tricine-SDS-PAGE إلى أن MW لـ RPHs كان في النطاق 5-35 كيلو دالتون (الشكل 8 أ).

الشكل 8. تحديد الوزن الجزيئي (MW) لـ RPHs من خلال كبريتات دوديسيل الصوديوم - هلام البولي أكريلاميد الكهربائي - الرحلان التروبوري (SDS-PAGE): (أ) أنماط tricine-SDS-PAGE لعلامة MW (السطر 1) و RPHs (السطر 2) و (ب) المحتوى النسبي (نسبة مئوية) لكل ميغاواط من RPHs.
يوضح الشكل 8 ب المحتوى النسبي لمختلف MWs في RPHs. بشكل عام ، كان 45.24 في المائة من كل البروتين في النطاق الرئيسي (MW 2.4 كيلو دالتون). تم الحصول على نتائج مماثلة فيما يتعلق بببتيد بروتين نخالة الأرز المائي. الاعلىمضادات الأكسدةالنشاط التي حصل عليها ثامناراتيب وآخرون. [37] كان ذلك للببتيدات من ميغاواط=6 - 50 كيلو دالتون. بالإضافة إلى ذلك ، توجد علاقات بين وظيفة تحلل البروتين وتوزيع MW وتكوين الأحماض الأمينية [57]. هذا ما يفسرمضادات الأكسدةلوحظ نشاط RPHs في هذه الدراسة.
2.6. اختبار سمية الخلية
مطلوب سمية الخلايا المنخفضة للتطبيقات المستقبلية. لتقييم السمية الخلوية والتوافق الحيوي لـ RPHs ، تم قياس قابلية بقاء الخلية لـ 264.7 خلية خام في محلول RPH عبر طريقة MTT. كما هو موضح في الشكل 9 ، كانت صلاحية الخلية أعلى من 100 في المائة عند معالجتها بـ 25-2000 ميكروغرام / مل من RPH لمدة 24 ساعة و 48 ساعة. تشير النتائج إلى السمية الخلوية المنخفضة بشكل ملحوظ لـ RPHs. لذلك ، يمكن استخدام RPHs كتطبيقات تجميلية ذات سمية خلوية منخفضة جدًا.

الشكل 9. مقايسة MTT للسمية الخلوية لـ 264.7 خلية خام معالجة بتركيزات مختلفة من RPH لمدة 24 و 48 ساعة.
3. المواد والطرق
3.1. الكواشف
كلوريد الحديد (III) ، 2،2 ′ -azino-bis (3- ethylbenzothiazoline -6- sulfonic acid) (ABTS) ، Trolox (6- hydroxy -2 ، 5،7 ، 8- tetramethylchroman -2- carboxylic acid)، l -3، 4- dihydroxyphenylalanine (L-DOPA)، 1، 1- diphenyl -2- picrylhydrazyl ( DPPH) ، وحمض الخليك ثلاثي الكلور من Alfa Aesar (Tewksbury ، MA ، الولايات المتحدة الأمريكية). 2،2 ′ -AZOBIS (2- methylpropionamidine) dihydrochlo- ركوب (AAPH) ، كاشف الفينول من Folin-ciocalteu ، وحمض الغال ، وحمض الأسكوربيك ، و ty- ty- rosinase لويس ، ميزوري ، الولايات المتحدة الأمريكية). تم الحصول على كربونات الصوديوم من Riedel-de Haën (Seelze ، ألمانيا). أخيرًا ، تم الحصول على البوتاسيوم فيري سيانيد وفوسفات هيدروجين الصوديوم وفوسفات ثنائي هيدروجين الصوديوم من Showa Chemical (طوكيو ، اليابان).
3.2 تحضير RPHs
تم تحضير RPHs كما هو موضح سابقًا ، باستثناء أن الأميليز الفطري تم اعتماده لإلغاء النشا في الأرز ، وتجنب الأضرار التي لحقت الأحماض الأمينية الناتجة عن التحلل المائي للأميليز البكتيري في درجات حرارة عالية [43،58]. مائة جرام من الأرز - تم نقعنا في 1 0 0 0 مل من الماء المقطر الذي يحتوي على 0.5 بالمائة من الأميليز الفطري (جينينكور ، نيويورك ، الولايات المتحدة الأمريكية) ؛ يسخن الخليط بعد ذلك لمدة 24 ساعة إلى 60 درجة مئوية (الرقم الهيدروجيني 4.2) ، وبعد ذلك يُترك ليبرد إلى درجة حرارة الغرفة. تم إجراء الطرد المركزي لمدة 10 دقائق عند 1968 × جم لإزالة المادة الطافية المتبقية. بعد إضافة 20- الماء و 2 مل من 0.1 بالمائة من البروتياز المائي (Healthmate ، Changhua ، تايوان) إلى الجزء غير القابل للذوبان ، تم رج المحلول واحتضانه لمدة 4 ساعات عند 55 درجة مئوية. يتم استخدامه للحفاظ على درجة الحموضة للمحلول عند المستوى الأمثل ، ثم تم إجراء تسخين 85 درجة مئوية لمدة 10 دقائق لتعطيل الإنزيم. تمت إزالة الجزء غير القابل للذوبان المتبقي من خلال الطرد المركزي لمدة 15 دقيقة عند 3075 × جم. تم إجراء عملية التجفيف على المادة الطافية ، والتي تم تخزينها بعد ذلك في درجة حرارة _20 درجة مئوية قبل الاستخدام.
3.3 الأنشطة المضادة للأكسدة من RPHs
3.3.1. إجمالي تركيز الفينول (TPC)
تم استخدام طريقة Folin-Ciocalteu لاكتشاف TPC لـ RPHs [59]. أولاً ، تم خلط 2 0 0 ميكرولتر من كاشف الفينول الخاص بـ Folin – Ciocalteu (0.3M) بشكل موحد خلال 5- دقيقة اهتزاز مع 200 ميكرولتر من محلول RPH ، وإلى هذا الخليط ، 400 ميكرولتر من منزوع الأيونات (DI) تمت إضافة الماء و 200 ميكرولتر من محلول كربونات الصوديوم بنسبة 10 بالمائة (وزن / حجم). خضع المحلول المختلط لمدة 60 دقيقة من الحضانة في الظلام عند درجة حرارة الغرفة. ثم تم الطرد المركزي لمدة 15 دقيقة عند 3000 دورة في الدقيقة. استخدم القياس 100 ميكرولتر من المادة الطافية. لتحديد TPC (الوحدة: mg) مكافئ حمض الغال (GAE) لكل جرام من عينة RPH الجافة (الوحدة: mg GAE / g RPHs) ، تم إدخال بيانات الامتصاص البصري إلى منحنى قياسي يمثل حمض الغال. تم الحصول على الامتصاصية عند 700 نانومتر باستخدام مقياس الطيف الضوئي Epoch Microplate (BioTek ، VT ، الولايات المتحدة الأمريكية).
3.3.2. إجمالي محتوى الفلافونويد (TFC)
تم الحصول على TFC باتباع نهج Wathoni et al. مع تعديلات طفيفة [60]. أولاً ، تم خلط 500 ميكرولتر من كل عينة و 2 بالمائة (وزن / حجم) من محلول كلوريد الألومنيوم. تم خلط محلول التفاعل جيدًا وتركه لمدة 10 دقائق ، وتم تقييم الامتصاص عند 415 نانومتر. تم الإبلاغ عن النتيجة بالميكروجرام من مكافئ كيرسيتين (QE) لكل جرام من عينة RPH الجافة (ميكروغرام QE / g RPHs).
3.3.3. نشاط إزالة الجذور الحرة DPPH
أولاً ، تم خلط 198 ميكرومتر من محلول الإيثانول DPPH (5 0 ميكرولتر) ومحلول RPH أو ماء DI (0.5 ميكرولتر ؛ العينة والتحكم ، على التوالي) ثم تركه للوقوف لمدة 30 دقيقة في الظلام عند درجة حرارة الغرفة. تم الحصول على امتصاص المحلول عند 517 نانومتر لاحقًا. تم حساب نشاط الكسح النسبي عن طريق تحديد فرق الامتصاصية بين العينة والمجموعة الضابطة. تم إعادة تأثر النشاط المرتفع لكسح الجذور الحرة DPPH عن طريق الامتصاص البصري المنخفض. في تقييم نشاط إزالة الجذور الحرة لمحلول RPH ، كان المعيار المستخدم هو فيتامين سي [61-63].

3.3.4. نشاط الكسح للجذور الحرة ABTS
النهج الذي أبلغ عنه Wu et al. تم توظيفه لتقييم محلول RPHمضادات الأكسدةنشاط [64]. أولاً ، تم تفاعل 7 ملي مولار من محلول مخزون ABTS (25 0 ميكرولتر) مع 2.45 ملي مولار من بيرسلفات البوتاسيوم (25 0 ميكرولتر) لإنتاج الجذور الحرة ABTS (ABTS ● plus) ، مع الاحتفاظ بالخليط لمدة 16 ساعة عند 4 درجات مئوية في الظلام قبل استخدامه. بعد التوازن في الظلام عند درجة حرارة الغرفة ، تم استخدام 1 مولار من محلول ملحي مخزّن بالفوسفات (PBS ، الرقم الهيدروجيني 7.4) لتخفيف المحلول إلى 0.70 × 0.02 امتصاص عند 734 نانومتر. بعد ذلك ، إلى 180 ميكرولتر من محلول ABTS المخفف ، تمت إضافة 20 ميكرولتر من Trolox (تحكم إيجابي) أو محلول RPH (عينة). ثم تم تعريض الخليط إلى 10 دقائق من التحضين في درجة حرارة الغرفة. حددت هذه الدراسة الامتصاص البصري عند 734 نانومتر ؛ يتوافق الامتصاص المنخفض مع نشاط إزالة الجذور الحرة ABTS العالي. كان المعيار المستخدم لتقييم نشاط إزالة الجذور الحرة لمحلول RPH هو Trolox المضاد للأكسدة.


3.3.5. قدرة التخفيض
تم استخدام مقايسة الطاقة المضادة للأكسدة لخفض الحديديك لتحديد إجمالي محلول RPHمضادات الأكسدةنشاط. كما ذكرت من قبل لين وآخرون. [29] ، تم خلط محلول RPH (2 0 0 ميكرولتر) بشكل موحد مع 1 بالمائة (وزن / حجم) K3Fe (CN) 6 و 0.2 M PBS عازلة (الرقم الهيدروجيني 6.6 ؛ 100 ميكرولتر لكل منهما) . لمدة 20 دقيقة ، تم استخدام حمام مائي 50 درجة مئوية لتسخين الخليط ؛ بعد إزالة الخليط من الحمام ، تم تبريده بسرعة لمدة 3 دقائق. بعد ذلك ، تم إجراء إضافة 10 بالمائة (وزن / حجم) حمض ثلاثي كلورو أسيتيك (100 ميكرولتر) و 10- دقيقة للطرد المركزي عند 3000 دورة في الدقيقة. تبع ذلك استخلاص المادة الطافية (400 ميكرولتر) وخلطها المنتظم مع 0.1 بالمائة (وزن / حجم) FeCl3 (100 ميكرولتر) وماء DI (400 ميكرولتر). تم الحصول على Fe4 [Fe (CN) 6] 3 من خلال تفاعل 10- دقيقة من هذا الخليط في الظلام. بعد ذلك ، يشير الامتصاص البصري العالي (المقاس عند 700 نانومتر) إلى قدرة تخفيض أعلى. تم استخدام فيتامين ج القياسي لتحديد محتوى فيتامين ج المكافئ (VCE) لكل جرام من RPHs.
3.3.6. قدرة امتصاص الأكسجين الجذري (ORAC)
حصلت هذه الدراسة على ORAC عن طريق تعديل طريقة تم الإبلاغ عنها مسبقًا [65]. بعد حل عينة RPH في الماء المقطر ، تم خلط محلول RPH (50 ميكرولتر) مع uoressein (10 ميكرون) في لوحة microtiter جيدًا. خضع المحلول 15- دقيقة من الحضانة عند 37 درجة مئوية متبوعة بإضافة 50 ميكرولتر من AAPH (500 ملي مولار). كل 5 دقائق وأكثر من 120 دقيقة ، تم تسجيل التألق (λex و λem=485 و 528 نانومتر ، على التوالي). المضادات الأكسدةتم اكتشاف قدرة RPHs من حركية تسوس التألق عن طريق حساب المنطقة الواقعة تحت المنحنى (AUC). في حساب RPH ORAC ، كان المعيار 15-250 ميكرومتر ترولوكس. تم الإبلاغ عن ORAC على أنها ميكرومول من مكافئ ترولوكس (TE) لكل جرام من عينة RPH الجافة (µmol TE / g RPHs).
3.4. نشاط تثبيط الهيالورونيداز
تم إجراء اختبار تثبيط الهيالورونيداز باستخدام {0} صفيحة دقيقة جيدة وطريقة تم الإبلاغ عنها مسبقًا مع تعديلات طفيفة [4 0]. تم إطلاق N-acetylglucosamine عن طريق تفاعل الهيالورونيداز مع ركيزة HA. في حالة وجود أي مثبط ، تم تقليل إطلاق N-acetylglucosamine ، مع اكتشاف هذا الإطلاق عن طريق الحصول على امتصاص 600- نانومتر. تم ترسيب HA بمحلول ألبومين حمضي مكون من 0 محلول أسيتات 1 مولار (درجة الحموضة 3.9) وألبومين مصل البقر (1 مجم / مل). خضع محلول العينة و 5 مجم / مل هيالورونيداز 20- دقيقة من الحضانة عند 37 درجة مئوية. إلى خليط الحضانة ، HA (1 {{2 0} 0 ميكرولتر ؛ 5.0 مجم / مل في 0.1 م تمت إضافة المخزن المؤقت للأسيتات) لاحقًا. تم إجراء مزيد من الحضانة عند 37 درجة مئوية لمدة 40 دقيقة. تمت إضافة 0.1 مل 0.4 مولار محلول بورات قلوي لوقف التفاعل الإنزيمي.
3.5 نشاط التيروزيناز المثبط
قيمت الدراسة الحاليةأنتيتروزينازنشاط RPHs باستخدام بروتوكول تم الإبلاغ عنه مسبقًا مع تعديلات [66]. تم تحضير محلول إنزيم (135 وحدة / مل) عن طريق التذويبالتيروزينازفي محلول فوسفات 20 ملي مولار (الرقم الهيدروجيني 6.8). بالإضافة إلى ذلك ، تم استخدام ماء DI لإعداد محلول L-DOPA 1.25 ملي مولار. بعد ذلك ، تم خلط 40 ميكرولتر من تركيزات مختلفة من محلول RPH مع 40 ميكرولتر من محلول التيروزيناز و 120 ميكرولتر من محلول L-DOPA. لمدة 30 دقيقة ، تم الاحتفاظ بهذا الخليط عند 37 درجة مئوية في اختبار تثبيط RPHsالتيروزينازنشاط. تم استخدام مقياس الطيف الضوئي (FLUOstar Omega Microplate Reader ، BMG Labtech GmbH ، ألمانيا) للحصول على امتصاص 475- نانومتر. تم إجراء جميع القياسات ثلاث مرات. عند امتصاص المجموعة المقابلةالتيروزينازلم يكن حاضرا تم طرحه. تم تحديد معدل تثبيط الإنزيم على أنه
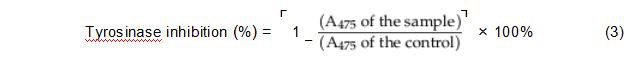
3.6 توصيف RPHs
3.6.1. برو الأحماض الأمينية
اكتشفت هذه الدراسة تكوين الأحماض الأمينية لـ RPHs. أولاً ، لمدة 24 ساعة وعند 115 درجة مئوية ، تم استخدام 4 مولار من حمض الميثان سلفونيك لتحليل العينات في الأنابيب المختومة المفرغة. تم استخدام نظامي توصيل مذيب من Waters 51 0 ومحلل الأحماض الأمينية (L - 8900 ؛ Hitachi ، طوكيو ، اليابان) لفصل الأحماض الأمينية المشتقة على عمود Spherisorb ODS2 بقياس 25 م × 64.6 مم. استخدمت هذه الدراسة المذيبات التالية: (أ) أسيتات الصوديوم (0. 14 م) وثلاثي إيثيل أمين (85 0 ميكرولتر / لتر ؛ الأس الهيدروجيني 5.6) و (ب) 60 في المائة أسيتونتريل ، والتي يكون التدرج اللوني لها كان 0 في المائة لمدة دقيقتين ؛ 0-42 بالمائة لمدة 15.5 دقيقة (منحنى محدب) ؛ و 100 بالمائة لمدة 4 دقائق. تم أخذ عينات مكررة لقياس مقادير الأحماض الأمينية عند 254 نانومتر [67،68].
3.6.2. الوزن الجزيئي (MW) للبروتين
وفقًا لطريقة Schägger [69] وتحت ظروف الاختزال ، حصلت هذه الدراسة على توزيع MW من خلال الرحلان الكهربي للهلام التريسين - الصوديوم دوديسيل (SDS) - بولي أكريلاميد الكهربي (PAGE) مع تعديلات طفيفة. نموذج مخزن مؤقت (3 0 g / L SDS ، 0. 375 M Tris-HCl ، 0. 125 جم / لتر Coomassie Brilliant Blue G -250 ، و 75 جم / لتر الجلسرين ؛ الرقم الهيدروجيني 7) لتفريق العينة المجففة بالتجميد ، مع الطرد المركزي ثم إجراء قبل التحميل. تمت إضافة ما مجموعه 20 ميكرولتر 2- مركابتوإيثانول إلى 1 مل من عينة tricine-SDS-PAGE. تم تسخين العينة عند 100 درجة مئوية لمدة 90 ثانية. تم تحميل عينة بئر بكل عينة ومعيار واسع النطاق للبروتين غير الملوث (مختبرات Bio-Rad ، ألمانيا) باستخدام microsyringe. تم بعد ذلك إجراء الرحلان الكهربي - أولاً عند 30 مللي فولت ثابت حتى تم احتواء العينة بأكملها داخل هلام التراص وبعد ذلك حتى اكتمالها عند 100 مللي فولت ثابت. بعد ذلك ، تم تطبيق 0.02 بالمائة من محلول Coomassie Brilliant Blue R -250 لتلطيخ الجل. تم إجراء إزالة المواد الهلامية المطلقة للخلفية عن طريق هز المواد الهلامية بنسبة 10 في المائة من حمض الأسيتيك طوال الليل. أخيرًا ، تم تحليل صورة الهلام لتحديد نطاقات البروتين في الممرات ؛ تم إجراء هذا التحليل في ImageJ (المعاهد الوطنية الأمريكية للصحة ، بيثيسدا ، دكتوراه في الطب ، الولايات المتحدة الأمريكية). تم استخدام علامات قياسية للحصول على منحنى معايرة تم من خلاله تقدير MW. كانت الخطوة الأولى هي تحديد طول كل نطاق للهجرة (RF) من الجزء العلوي من الهلام المنفصل. كانت الخطوة الثانية هي حساب منحنى المعايرة باستخدام Rf و log (MW) لعلامة قياسية مع MW معينة. تم إجراء تحديد MW باستخدام التردد الراديوي لعصابات البروتين في RPHs.

3.7 فحص السمية الخلوية
تمت زراعة 264.7 خلية خام في Modi ed Eagle Medium (DMEM) من Dulbecco الذي يحتوي على 1 0 بالمائة من مصل بقري جنيني (FBS) ، 4.5 جم / لتر جلوكوز ، 1 بالمائة محلول مضاد حيوي (1 0 0 وحدة / مل البنسلين و 100 ميكروغرام / مل من الستربتومايسين) ، 4 ملي L-Glutamin و 1.5 جم / لتر بيكربونات الصوديوم عند 37 درجة مئوية و 5 في المائة من ثاني أكسيد الكربون. تم قياس سمية الخلية لـ 264.7 خلية خام لـ RPHs عن طريق مقايسة انتشار 3- (4 ، 5- ثنائي ميثيلثيازول -2- yl) -2 ، 5 بروميد ثنائي فينيل تترازوليوم (MTT) طريقة. تم طلاء حوالي 1 × 104 خلية لكل بئر في 96- أطباق جيدة. بعد 24 ساعة ، تمت إضافة تركيزات مختلفة من RPHs (0-2000 ميكروغرام / مل) في الخلايا. بعد 24 و 48 ساعة من الحضانة ، تمت إضافة 100 ميكرولتر من محلول MTT (0.5 مجم / مل). لوحظت بلورات فورمازان الزرقاء عند فحصها تحت المجهر. تمت إزالة DMEM وتمت إضافة 100 ميكرولتر من ثنائي ميثيل سلفوكسيد (DMSO) لكل بئر. تم قياس الامتصاصية باستخدام قارئ لوحة ميكروتيتر. تم حساب صلاحية الخلية (النسبة المئوية) على أنها [A570 (الخلايا المعالجة) _ A570 (خلفية)] / [A570 (خلايا غير معالجة) _ A570 (خلفية)] × 100 بالمائة [70].
3.8 تحليل احصائي
كان التقرير الخاص بكل عينة من التحلل المائي هو متوسط القيمة من ثلاث تجارب وقرارات متكررة مستقلة. تم تحليل النتائج المعبر عنها بالمتوسط 士 الانحراف المعياري (SD) عن طريق ANOVA أحادي الاتجاه واختبار Duncan اللاحق باستخدام نظام التحليل الإحصائي (الإصدار 2 0. 0 ؛ SPSS ، أرمونك ، نيويورك ، الولايات المتحدة الأمريكية) . اعتبرت قيم p <0.05 ذات="" دلالة="">
4 - نتائج
فحصت هذه الدراسة وظائف RPHs. أظهرت النتائج التجريبية أن RPHs تحتوي على مركبات فينولية و avonoids وعرضت مجموعة منمضادات الأكسدةالأنشطة ، مثل أنشطة الكسح DPPH و ABTS ، وسعة التخفيض ، و ORAC. بالإضافة إلى ذلك ، تم تثبيط RPHs بشكل فعالالتيروزينازوأنشطة الهيالورونيداز. كان البروتياز عاملاً حاسماً يؤثر على أنماط MW من RPHs. يشير تحليل RPHs إلى إمكانية استخدامها كعنصر في مستحضرات التجميل.
مساهمات المؤلف: تم وضع تصور للدراسة بواسطة Y.-SL ؛ تم إجراء التحليل الرسمي بواسطة Y.-SL و C.-SC ؛ تم إجراء معالجة البيانات بواسطة H.-JC و F.-JD و C.-YC و J.-HZ و Y.-CH ؛ تمت صياغة المخطوطة الأصلية بواسطة H.-JC و F.-JD و S.-LF ؛ أخيرًا ، تمت مراجعة المسودة وتحريرها بواسطة C.-FC و Y.-SL و C.-SC لقد قرأ جميع المؤلفين النسخة المنشورة من المخطوطة ووافقوا عليها.
التمويل: قدمت وزارة العلوم والتكنولوجيا التمويل لهذه الدراسة. بيان مجلس المراجعة المؤسسية: لا ينطبق.
بيان الموافقة المستنيرة: لا ينطبق.
بيان توافر البيانات: البيانات المقدمة في هذه الدراسة متاحة عند الطلب من المؤلف المقابل.
تضارب المصالح: يعلن المؤلفون أنه لا توجد تضارب في المصالح. توفر العينة: غير متوفر.

