تفاعل الخلايا المناعية والكلى المقيمة في تكوين الهياكل الليمفاوية الثالثة في التهاب الكلية الذئبي
Mar 14, 2022
لمزيد من المعلومات: ali.ma@wecistanche.com
سيمين جمالي وآخرون
نبذة مختصرة
الكلىيؤدي التورط إلى حدوث مراضة ووفيات كبيرة في مرضى الذئبة الحمامية الجهازية (SLE). يتضمن التسبب في التهاب الكلية الذئبي (LN) آليات متنوعة تحرضها عناصر استجابة المناعة الذاتية التي تغير بيولوجياالكلىالخلايا المقيمة. قد تستمر العمليات في الكبيبات والنسيج الخلالي بشكل مستقل وإن كان الحديث المتبادل بين الاثنين أمر لا مفر منه. بودوسيتيس ، ميسانجيال ، الخلايا الظهارية الأنبوبية ،الكلىالضامة المقيمة ، والخلايا اللحمية مع مدخلات من السيتوكينات والأجسام المضادة الموجودة في الدورة الدموية تغير التعبير عن الإنزيمات ، وتنتج السيتوكينات والكيموكينات التي تؤدي إلى إصابتها وتلفها.الكلى. يمكن استهداف العديد من هذه الجزيئات بشكل مستقل لمنع الفشل الكلوي وعكس مساره. توجد هياكل ليمفاوية من الدرجة الثالثة مع مراكز جرثومية حقيقية في كليتي مرضى التهاب الكلية الذئبي وقد تم التعرف عليها بشكل متزايد على ارتباطها بالأفقركلويالنتائج. تنتج الخلايا اللحمية ، والخلايا الظهارية الأنبوبية ، والأوعية البطانية العالية ، وخلايا الأوردة اللمفاوية مواد كيميائية تمكن من تكوين هياكل تتكون من منطقة غنية بالخلايا التائية مع خلايا متغصنة ناضجة بجوار جريب الخلية البائية بخصائص المركز الجرثومي محاطة بخلايا البلازما. بعد نظرة عامة على تفاعل الخلايا المناعية مع الخلايا المقيمة في الكلى ، نناقش الأحداث الخلوية والجزيئية التي تؤدي إلى تكوين الهياكل اللمفاوية الثالثة في خلاليالكلىمن الفئران والمرضى الذين يعانون من التهاب الكلية الذئبي. بالتوازي ، يتم عرض الجزيئات والعمليات التي يمكن استهدافها علاجيًا.

انقر فوق Cistanche DHT لمرض الكلى
مقدمة
الذئبة الحمامية الجهازية (SLE) هي أحد أمراض المناعة الذاتية مع عدم تجانس سريري مثير للإعجاب والذي يظهر مع مظاهر من أعضاء متعددة. تم تحديد العديد من المسارات المُمْرِضة الناشئة عن عوامل وراثية ، وعوامل فوق جينية ، وهرمونية ، وبيئية ، وتنظيم مناعي ، وكلها تتلاقى في التسبب في التهاب الأنسجة وتلف الأعضاء [1،2]. تم الإبلاغ عن كل جانب من جوانب الاستجابة المناعية الفطرية والتكيفية في المرضى الذين يعانون من مرض الذئبة الحمراء ويساهمون في التعبير عن المرض في مجموعات فرعية متميزة من المرضى. إن وجود عدد كبير من الأجسام المضادة الذاتية قد ميز المرض في حين أن إنتاج تلك الموجهة ضد المستضدات النووية ، والبروتينات النووية الصغيرة ، والحمض النووي المزدوج (dsDNA) ، والنيوكليوزومات تمثل السمة المميزة للمرض [1،3]. الأجسام المضادة من المركبات المناعية القابلة للذوبان (IC) مع المستضدات الذاتية (مثل النيوكليوزومات) التي يتم إطلاقها بكثرة في الدورة الدموية لمرضى الذئبة الحمراء ، قد تترسب في الأغشية القاعدية في الأعضاء المختلفة بما في ذلكالكلى، وبدء الالتهاب. قد ترتبط الأجسام المضادة الذاتية مباشرة بـالكلىالمستضدات وتشكل IC في الموقع كما هو محدد بواسطة الأجسام المضادة الكاتيونية المضادة لـ dsDNA التي ترتبط بالغشاء القاعدي الكبيبي [4-6]. بالتوازي مع ذلك ، فإن الإنتاج المفرط للسيتوكينات بما في ذلك النوع الأول من الإنترفيرون (IFN) والإنترلوكين (IL) -17 والإنترلوكين -23 يزيد من تشوهات الخلايا المناعية أو يعمل بشكل مباشر علىالكلىالخلايا المقيمة لإحداث ضرر [7]. أخيرًا وليس آخرًا ، تتسلل الخلايا التائية ذاتية التنشيط إلىالكلىحيث قد تشكل بنية ليمفاوية ثلاثية (TLS) وتسبب تلفًا في الأعضاء.
الأجسام المضادة أو ترسب IC داخلالكلىجنبا إلى جنب مع عمل السيتوكينات وتسلل الخلايا المناعية تساهم في تطور التهاب الكلى في المرضى الذين يعانون من مرض الذئبة الحمراء والذي يظهر على شكل التهاب الكلية الذئبي (LN) مع معدلات الاعتلال والوفيات [8،9]. بعد تحديث تفاعل خلايا الكلى المقيمة والمناعة ، سنناقش بالتفصيل تكوين TLS فيكلويالخلالي وتأثيره على وظائف الكلى.
الخلايا المقيمة في الكلى
2.1. بودوسيتس
Podocytes هي خلايا متخصصة على الجانب الحشوي من كبسولة بومان التي تحيط بالشعيرات الدموية الكبيبية. إنها جزء من آلة الترشيح الكبيبي وهي ضرورية للصيانةكلويوظيفة [10]. إنها تعبر عن بروتينات فريدة بما في ذلك سينابتوبودين ، ونيفرين [11] ، بودوسين [12] ، وبروتين ورم ويلمز [13] ، وكلها ضرورية للحفاظ على هيكلها ووظيفتها [14]. تؤدي العيوب الوراثية أو المكتسبة في التعبير عن جزيئات خلية البودوسيت الرئيسية دائمًا إلى انفصالها وتطورها.كلويفشل [15]. إصابة خلايا بودوسيت ملحوظة في الأشخاص الذين يعانون من LN وتسبب في تطور البيلة البروتينية والضرر الكبيبي [16،17].
من المعروف أن Podocytes تنتج وتعبِّر عن مكونات المسار التكميلي الذي يساهم جنبًا إلى جنب مع ترسيب وتنشيط المكمل من الدورة الدموية في إصابة خلايا podocyte. تم إجراء تثبيط للمسار التكميلي في التجارب السريرية لعلاج الأشخاص المصابين بالتهاب الكبد LN [18]. علاوة على ذلك ، تعبر الخلايا البودية عن جميع المستقبلات الشبيهة بالرصد (TLR) وبروتين المستقبل الشبيه بالعقد -3 (NLRP3) وكاسبيز 1 [19]. ينشط الهوموسيستين الجراثيم الالتهابية NLRP3 في الخلايا البادئة للفئران المعرضة لمرض الذئبة والمرضى الذين يعانون من LN [20] ويقلل تثبيطه من البيلة البروتينية والنسيجيةكلويالآفات ، ومحو عملية القدم podocyte [16] مما يشير إلى أنه يمكن استهداف NLRP3 علاجيًا.
تعبر خلايا Podocytes من الفئران المعرضة لمرض الذئبة والأشخاص الذين يعانون من LN عن مستويات متزايدة من جزيئات التوافق النسيجي الرئيسية جنبًا إلى جنب مع جزيئات costimulation CD80 و CD 86 والتي تعتبر علامات على إصابة الخلية ولكنها في الوقت نفسه قد تنشط الخلايا الليمفاوية المارة وتساهم في تراكمها في الكلويحمة. بشكل عكسي ، فإن الاختراقات في كبسولة بومان ، في التهاب كبيبات الكلى الهلالي البشري قد تسمح لخلايا CD8 + T بالوصول إلى الخصل الكبيبي والخلايا البادئة وتسبب تدميرها [21].
تعبر خلايا Podocytes عن مستقبل Fc الوليدي (FcRn) الذي يتيح نقل IgG من الشعيرات الدموية إلى حيز البول. IgG من المرضى الذين يعانون من LN يدخل الخلايا البودوسية باستخدام FcRn ويسبب زيادة تنظيم بروتين كيناز IV المعتمد على الكالسيوم / كالودولين (CaMK4) الذي يفسفوريلات 14 - 3-3 ، وهو بروتين سقالة سينابتوبودين ، والذي يتحلل عند إطلاقه. سينابتوبودين مهم في الحفاظ على بنية بودوسيت [22]. في موازاة ذلك ، ينشط CaMK4 NFkB الذي يقمع التعبير عن النيفرين ، وهو بروتين مهم في الحجاب الحاجز المنقسم ، من خلال تعزيز وظيفة مثبط النسخ SNAIL [23]. يسبب IgG من المرضى الذين يعانون من LN النشط انتفاخ CaMK4 تحت كونه تحت الجالاكتوزيلات [23]. الحذف الشامل لـ Camk4 في الفئران المعرضة لمرض الذئبة MRLlpr يقمع بشكل فعال LN [24]. والأهم من ذلك ، أن توصيل مثبط CaMK4 الذي يستهدف خلية البودوسيت يمنع جميع عناصر LN ويمنع ترسب IC [22] ، مما يشير إلى أن الحفاظ على بنية ووظيفة الخلايا البودوسية عن طريق قمع نشاط CaMK4 IC لا يتم ترسيبها. يوضح هذا الخط من المعلومات أهمية العوامل المحلية في تطوير تلف الأعضاء وقيمة توصيل الأدوية الخاصة بالخلية / الأعضاء للحد من تلف الأعضاء في المناعة الذاتية.

Cistanche جيد لالكلى
2.2. خلايا ميسانجيل
تجعل الخلايا ميسانجيل ومصفوفة ميسانجيلكلويالقطب الوعائي للجسم مهم في إزالة البروتينات المتجمعة و IC الصغيرة من الغشاء القاعدي [19]. يشاركون في التسبب في LN حيث أن تكاثر الخلايا ميسانجيل ومصفوفة ميسانجيل موجودة دائمًا في LNالكلى[25]. تعبر الخلايا ميسانجيل عن مستقبلات شبيهة بالرصاص (TLRs) [25،26] ، وعندما يتم تحفيزها باستخدام رابط TLR3 (dsRNA) فإنها تنتج النوع I IFN [25] - وهو سيتوكين يُزعم أنه مهم في التسبب في مرض الذئبة الحمراء [25] ، 27].
ترتبط الأجسام المضادة لـ dsDNA بالخلايا المسراقية وتنشط المسارات الالتهابية والتليفية ، لا سيما تلك التي تتضمن مسارات إشارات بروتين كيناز المنشط بالميتوجين (MAPK) وبروتين كيناز سي (PKC) ، مما يؤدي إلى إنتاج السيتوكينات المسببة للالتهاب [27 ، 28]. تفرز الخلايا الميزانجيّة الإنترلوكين (IL) -6 ، والذي بمفرده يمكن أن يقود تطور التهاب كبيبات الكلى [29]. CaMK4 ضروري لتكاثر خلايا ميسانجيل وإنتاج السيتوكينات. على وجه التحديد ، لا تتكاثر خلايا ميسانجيل من الفئران المعرضة للذئبة MRLlpr والتي تفتقر إلى CaMK4 وراثيًا ، استجابةً لعوامل النمو المشتقة من الصفائح الدموية ولا تنتج IL -6 [30].
2.3 الخلايا الظهارية الأنبوبية الكلوية
كلويوتشارك الخلايا الظهارية الأنبوبية في الفيزيولوجيا المرضية لـ LN. يفرزون السيتوكينات المسببة للأمراض ، بما في ذلك النوع الأول IFN [31] وعامل تنشيط الخلايا B (BAFF) [32] ، وكلاهما له دور مهم في تطوير مرض الذئبة الحمراء (الشكل 1). بالإضافة إلى،كلويتعبر الخلايا الظهارية الأنبوبية المأخوذة من مرضى LN عن جزيء التكلفة B 7- H4 ، مما يوحي بإمكانية تنشيط الخلايا التائية. تؤدي إضافة الأجسام المضادة لـ dsDNA إلى الخلايا الطلائية الأنبوبية الكلوية في المزرعة إلى التنظيم المتسلسل لعامل نخر الورم (TNF) و IL -1 و IL -6 [33] ، مما يشير إلى مساهمة الخلايا للعمليات الالتهابية في tubulointerstitium في LN [34].الكلىتعبر الخلايا الظهارية الأنبوبية عن نوكليازات داخلية موت الخلايا المبرمج [35] والتي على ما يبدو عند تنشيطها من خلال آليات غير معروفة حتى الآن ، يمكن أن تسبب موت الخلية [36]. في الآونة الأخيرة ، تبين أن الخلايا الظهارية الأنبوبية يمكن أن تنتج CXCL12 استجابة لـ IL -23 لتعزيز الخلالي وحذفها الجيني فقط في هذه الخلايا مما حد من التهاب كبيبات الكلى في الفئران المعرضة لمرض الذئبة [7].

BAFF ، هو عامل نمو وتمايز لخلايا B راسخ يساعد الخلايا البائية ذاتية التفاعل على البقاء والهروب من التسامح المحيطي [37 ، 38]. تمت الموافقة على حصار BAFF بجسم مضاد (Benlysta) لعلاج مرض الذئبة الحمراء [39] و LN [40]. يتم التعبير عن BAFF أيضًا بواسطة الخلايا الظهارية الأنبوبية للأشخاص الذين يعانون من LN التكاثري وترتبط مستويات التعبير بمؤشر النشاط المحدد في التشريح المرضي [32]. قد يعزز BAFF مزيدًا من التمايز للخلايا البائية الموجودة في الفضاء الخلالي لـالكلىمن المرضى الذين يعانون من LN [41]. علاوة على ذلك ، يُزعم أن BAFF يروج لتشكيل TLS فيالكلىعن طريق زيادة عدد الخلايا التائية الموضوعة داخل الكبيبات وزيادة الالتهاب في الفئران [42] مما قد يفسر التأثير العلاجي لبينليستا في مرضى LN [40]. يستهدف Benlysta نضج الخلايا البائية والإشارات عن طريق تثبيط بقاء الخلايا البائية ، وتقليل التمايز إلى خلايا البلازما المنتجة للغلوبولين المناعي في المرضى الذين يعانون من LN [43].
2.4 الخلايا الجذعية الوسيطة
الخلايا الجذعية الوسيطة (MSCs) هي خلايا مناعية سلفية متعددة القدرات موجودة في جميع الأنسجة [44]. يبدو أن لها دورًا في كبت الخلايا التغصنية والخلايا التائية [45]. أظهرت الدراسات السابقة أنه عندما تكون تركيزات السيتوكينات المنشطة للالتهابات منخفضة ، فقد يكون للخلايا الجذعية الوسيطة إمكانات تحفيز مناعي [45 ، 46]. يمكن اكتشاف الخلايا الجذعية السرطانية داخل جدار الحوض و TLS فيالكلىمن الفئران المعرضة لمرض الذئبة [47]. يؤدي تحفيز الخلايا الجذعية السرطانية باستخدام السيتوكينات الالتهابية إلى التعبير عن TNF- و IL -1 و CCL19 و ICAM [47]. على الرغم من عدم وضوحه ، يبدو أن الخلايا الجذعية السرطانية تلعب دورًا مشابهًا لدور الخلايا المنظمة للأنسجة اللمفاوية (LTo) وأن الخلايا MSCs الخاصة بالأنسجة تعمل مثل خلايا محفز الأنسجة اللمفاوية (LTi). يمكنهم إعادة البرمجة وبدء سلسلة التهابية مبكرة من خلال التفاعل مع الخلايا التائية [47]. يتسبب تمايز MSC وتراكم الخلايا المناعية في توسع الأوعية اللمفاوية وبالتالي تكوين TLS [48].

Cistanche جيد لالكلى
2.5 البلاعم
الضامة المقيمة فيالكلىعادة ما تُرى في النسيج الخلالي المحيط بالكبيبات [49]. حيدات المحيطية بعد الدخول إلىالكلىالأنسجة والتمايز إلى البلاعم تلعب دورًا رئيسيًا في الالتهاب والإصابة والتليف في اضطرابات الكلى الحادة والمزمنة [50]. يتم تجنيد CD16 plus أو CD14 plus الضامة للإصابةالكلىفي وجود السيتوكينات والكيموكينات [50]. تم تسجيل عدة أنواع فرعية من الضامة (M1 ، M2a-c) [51] موجودة في أنسجة LN ذات الأصل والوظيفة غير المعروفين [49،50،52]. بشكل عام ، يبدو أنه إذا تعرضت البلاعم المقيمة لرابطات TLR الداخلية وجزيئات النمط الجزيئي المرتبطة بالتلف (DAMPs) [53] ، فإنها تنتقل من مرحلة الاستبانة إلى مرحلة الالتهاب. خلال مرحلة الالتهاب ، تحول الضامة نمطها الظاهري إلى M1 وتعبر عن Ly6C / Gr1 والسيتوكينات السرية المؤيدة للالتهابات [54،55]. في المقابل ، أثناء مرحلة الإصلاح أو الحل ، فإنها تستقطب في النمط الظاهري M2 [56،57]. لذلك ، يبدو أن البلاعم لها وظيفة مزدوجة وتظهر مرونة عالية أثناء مرض الكلى.
3. الهياكل الليمفاوية الثلاثية
تم تقديم مصطلح "الليمفاوية الثلاثية" بواسطة Picker and Butcher [58] لشرح المواقع اللمفاوية الإضافية في الأنسجة غير اللمفاوية. تمت الإشارة إلى TLS بعدة طرق ، بما في ذلك الأعضاء الليمفاوية من الدرجة الثالثة ، والأنسجة الليمفاوية من الدرجة الثالثة ، والتركيبات اللمفاوية المنتبذة. يختلف تراكم الخلايا الليمفاوية في الأنسجة المحيطية غير اللمفاوية ، ودرجة تنظيمها ، وفقًا لنوع ومدة المنبهات الالتهابية المستضدية [59]. نتيجة لذلك ، تتراوح الكتل اللمفاوية من مجموعات فضفاضة ، تضم عددًا قليلاً من الخلايا التائية أو البائية ، إلى الأنسجة المنظمة التي تعرض السمات المميزة لـ TLS [60-63].
يتكون TLS من منطقة غنية بالخلايا التائية مع DCs ناضجة بجوار جريب الخلية B مع خصائص مركز جرثومي محاط بخلايا البلازما. الحد الأدنى من السمات اللازمة لتشكيل TLS وظيفي غير معروف ، ولكن يتم تعريف TLS على أنه تكتل ليمفاوي مع مكونات انسجة منظمة تتكون من خلايا شجيرية جرابية (FDCs) وخلايا شبكية ليفية (FRCs) ، وبشكل مميز ، مع أوردة بطانية عالية (HEVs) والأوعية اللمفاوية (LVs) [64،65]. التعريف القائم على هذه المعايير يستبعد تكتلات الخلايا البائية أو التائية استجابةً للالتهاب الذي يفتقر إلى الأجزاء اللحمية المتمايزة (الإطار 1).
تطوير TLS في مختلفالكلىالأمراض ، بما في ذلك اعتلال الكلية بالجلوبيولين المناعي (IgA) [66] ، ومرحلة مبكرة من IgG 4- المرتبطة بالتهاب الكلية النُبيبي الخلالي [67] ، الحادالكلىالإصابة [68،69] ، السرطان [70] ، التهاب الحويضة والكلية [71] ، الزرع و LN [41،72،73]. في الفئران المعرضة لمرض الذئبة ، تم العثور على TLS بالقرب من جدار الحوض ، بجانب الشرايين والأوردة الكبيرة [74]. في أمراض المناعة الذاتية مثل التهاب المفاصل الروماتويدي ، ومتلازمة سجوجرن ، والتصلب المتعدد ، والسكري ، والتهاب الغدة الدرقية هاشيموتو ، والتهاب الأقنية الصفراوية المصلب الأولي والتليف الصفراوي الأولي ، والوهن العضلي الوبيل ، قد تمكن TLS الأجيال الموجودة في الموقع من الخلايا التائية والبائية النشطة ذاتيًا وإنتاج الأجسام المضادة الذاتية التي إدامة العملية المسببة للأمراض [63،70،75،76].
3.1. تداخل الخلايا المناعية في الكلى مع الهياكل الليمفاوية من الدرجة الثالثة
تحافظ الخلايا التائية على التوازن المناعي في ظل الظروف الفسيولوجية وتعزز التسامح ضد المستضدات الذاتية. في المناعة الذاتيةالكلىيمكن أن يؤدي خلل في تحمل الخلايا التائية للمضادات الذاتية إلى تكوين الأجسام المضادة والالتهابات وتسلل الخلايا المناعية وتطور أنواع مختلفة من التهاب الكلية [77،78].
قد تتسلل الخلايا التائية إلىالكلىالنسيج إما لأنه تم تنشيطه في المحيط ويعبر عن جزيئات الالتصاق أو قد يكون ساذجًا ويتم تنشيطه بعد دخولهالكلىparenchyma بواسطة podocytes أو الخلايا الظهارية الأنبوبية كما نوقش أعلاه. تعبر الخلايا المنشطة عن جزيئات الالتصاق مثل CD44 والتي ، عندما تترافق مع ESRIN / إعادة التصميم / moesin الفسفوري [79] ، ترتبط بحمض الهيالورونيك المرتبط برباط ، والذي يزداد تركيبه في كليتي الفئران المعرضة لمرض الذئبة [80]. نظرًا لأن esrin / إعادة التصميم / moesin يتم فسفرته بواسطة Rho-kinase ، فإن تثبيط نشاطه يحد من دخول الخلايا التائية إلىالكلى[81]. وبالمثل ، فإن تثبيط تخليق حمض الهيالورونيك يقلل من دخول الخلايا التائية إلى كليتي الفئران المعرضة لمرض الذئبة [80] ومن المثير للاهتمام أن عدد خلايا CD3 بالإضافة إلى CD44 plus في الدم المحيطي للأشخاص المصابين بمرض الذئبة الحمراء ترتبط بنشاط أمراض الكلى [82] .
غالبية الخلايا في TLS هي CD3 بالإضافة إلى الخلايا التائية [74] وهي تشتمل على خلايا CD8 بالإضافة إلى الخلايا التائية السامة للخلايا وخلايا CD4 بالإضافة إلى الخلايا التائية التي تعرض النمط الظاهري لخلية TH1 وخلايا CD4 بالإضافة إلى خلايا Treg [83 - 86 ]. من المفترض أن الخلايا التغصنية الناضجة (DC) تقدم مستضدًا لخلايا CD4 بالإضافة إلى الخلايا التائية في منطقة الخلايا التائية في TLS [87] ، ولكن تم أيضًا اكتشاف DC-LAMP بالإضافة إلى DCs في المراكز الجرثومية ، مما يشير إلى أن لها دورًا في عرض مستضد للخلايا البائية [88]. تنتظم الخلايا البائية في مراكز جرثومية بخلايا بلازما. تحتوي مناطق الخلايا B على CD21 بالإضافة إلى FDCs بينما تحتوي مناطق الخلايا T على MIDC -8 بالإضافة إلى DCs [74].
يتم تعريف الخلايا التائية المزدوجة السلبية (DN) من خلال وجود مستقبلات الخلايا التائية (TCR) بالإضافة إلى عدم وجود جزيئات CD4 و CD8. يتم توسيعها في الدم المحيطي لمرضى الذئبة الحمراء ، وتوفر المساعدة للخلايا البائية لإنتاج الأجسام المضادة [89] ، وتنتج IL -17 [90]. يبدو أنها مشتقة من CD8 بالإضافة إلى الخلايا التائية [91،92] استجابةً للتنبيه باستخدام المستضد الذاتي ووجود IL -23 [93]. ميكانيكيًا ، يتم إغلاق موضع CD8 من خلال التعديلات اللاجينية التي يفرضها مغير عنصر استجابة cAMP (CREM) [94]. الأكثر إثارة للاهتمام ، أن خلايا DN T موجودة فيالكلىمن المرضى الذين يعانون من LN وينتجون IL -17 [90] مما يشير إلى مساهمتهم المباشرة فيالكلىاشتعال.
يتم تعريف المجموعة الفرعية TH17 من الخلية T من خلال التعبير عن النسب الذي يحدد عامل النسخ ROR t. إنها تعزز استجابة المناعة الذاتية لدى البشر والفئران من خلال إنتاج عامل تحفيز مستعمرة الخلايا المحببة (GM-CSF) و IFN و IL -17 و - 21 و - 22 [95،96]. تعبر خلايا TH17 عن نوع مستقبلات كيميائية C-C لعزر C-C 6 (CCR6) ويتم تجنيدها فيالكلىبواسطة C – C motif chemokine 20 (CCL20) ، والذي يتم إنتاجه بواسطة خلايا ميسانجيل بعد التحفيز بواسطة IL -17 (تنتج أيضًا العدلات أو الخلايا δT) [97] وعن طريق TEC المعرض لـ IL -23 [ 7]. خلايا TH17 الموجودة فيالكلىسري {0}} ويعزز الالتهاب عن طريق توليد TLS [98] ، وتعزيز تنشيط الخلايا البائية وفقدان التسامح [99،100].
خلايا T-helper (TFH) المسامية هي خلايا CD4 بالإضافة إلى T التي تعبر عن عامل النسخ BCL6 و CXC من النوع 5 (CXCR5). تهاجر هذه الخلايا إلى المراكز الجرثومية استجابةً لعزر CXC الكيميائي 13 (CXCL13). كما أنها تعبر عن مستقبلات الأسطح الثلاثة ، بما في ذلك تكلفة الخلايا التائية المحفزة ، CD40L ، PD -1 ، وتنتج IL -21 لتعزيز تنشيط الخلايا البائية وتمايز الخلايا البائية في خلايا الذاكرة ب والبلازما [ 101-103].
تزداد مستويات خلايا TFH المنتشرة في الأشخاص المصابين بأمراض المناعة الذاتية بما في ذلك مرض الذئبة الحمراء وقد أكدت الدراسات التي أجريت على الفئران المعرضة لمرض الذئبة دورها الممرض [102]. في مرضى الذئبة الحمراء ، يرتبط تواتر مجموعة فرعية من هذه الخلايا - خلايا TH خارج الجريبات - بمستويات الأجسام المضادة لـ dsDNA وكمية الخلايا البائية البلازمية. تحدد خلايا TH المسامية الإضافية مجموعة فرعية من CCR6 plus ، والتي تعبر عن CXCR5 ولكن ليس BCL6 ويمكنها إفراز IL -17 وتسهيل إنتاج الغلوبولين المناعي بواسطة الخلايا البائية [103،104].
الخلايا Treg هي خلايا TCR بالإضافة إلى Foxp3 بالإضافة إلى CD4 بالإضافة إلى الخلايا التائية التي تتطور في الغدة الصعترية أو المحيط. إنها تظهر نشاطًا قمعيًا وتتحكم في معظم الاستجابات المناعية من خلال آليات مختلفة [105]. أحد أشهر أدوارهم فيالكلىهو إفراز سيتوكين IL المضاد للالتهابات -10 [106]. تم توضيح بعض الأحداث الجزيئية التي تؤدي إلى خلل وظيفي في خلايا Treg. تشتمل الجزيئات المعنية على بروتين فوسفاتيز 2A (PP2A) ، وهدف الثدييات لمركب رابامايسين 1 (mTORC1) ، وفوسفاتيديلينوسيتول 3،4 ، و 5- ثلاثي فوسفات 3- فوسفاتيز ، وفوسفاتاز بروتين ثنائي الخصوصية (PTEN) ، وكالسيوم / بروتين كيناز الرابع المعتمد على الكالودولين (CaMK4). قد يؤدي استهداف هذه العناصر إلى إنقاذ وظيفة الخلايا Treg وتعديلهاالكلىالتهاب [107].
تحليل الأنماط المستنسخة للخلايا التائية من أنسجة مختلفة من الفئران LN ، وكذلك من الدم المحيطي أوالكلىمن المرضى الذين يعانون من مرض الذئبة الحمراء ، قد كشفوا عن توسع في مجموعة فرعية مقيدة من ذخيرة TCR ، مما يشير إلى استجابة لعدد محدد من المستضدات الذاتية [93]. تظل هذه المجموعة الموسيقية مستقرة لأشهر أو سنوات [108،109]. في مرضى الذئبة الحمراء ، تختلف الحيوانات المستنسخة في الدم المحيط عن تلك الموجودة في الكلى [110] ، مما يشير إلى أن الخلايا التائية الساذجة يتم تنشيطها بشكل مستقل في المحيط والكلى.
يعد الإنتاج المحلي للأجسام المضادة أمرًا بالغ الأهمية في تكوين TLS. ومن المثير للاهتمام أنالكلىيشبه المظهر الجيني TLS المرتبط بجهاز المناعة في الفئران المعرضة لمرض الذئبة مثيله في العقد الليمفاوية أثناء المراحل النشطة من LN [74]. يوفر TLS عوامل بقاء الخلايا التائية والخلايا البائية IL -7 و BAFF اللذان يجندان الخلايا الليمفاوية ويفضلان التفاعل بين الخلايا التائية والخلايا البائية في بيئة محصورة [111]. تم إثبات تنشيط خلايا B المحلية في TLS من خلال التعبير عن تنشيط Cytidine Deaminase (AICDA) ، وهو إنزيم مسؤول عن إعادة تركيب مفتاح الفصل والطفرة الجسدية المفرطة [112] والانتشار النشط. كما لوحظ تمايز محلي لخلايا البلازما ذاتية النشاط [113].
في نموذج من الذئبة الحمامية المجموعية الفأرية التي يسببها البرستان ، تتكاثر الخلايا البائية وتتحول إلى فئة داخل TLS ، وتنتج خلايا البلازما والبلازما المنتجة للأجسام المضادة لـ Sm / RNA أجسامًا مضادة ذاتية محليًا [114،115]. علاوة على ذلك،الكلىمن مرضى LN تحتوي على هياكل شبيهة بالمركز الجرثومي تحتوي على FDCs. قد يكون لهذه المراكز دور في الاستجابات المناعية النشطة الخاصة بالأنسجة المحلية [41]. يجب أن يؤدي تحديد الأحداث التي تبدأ في تكوين TLS إلى تعزيز فهمنا لهاالكلىالضرر في المرضى الذين يعانون من LN. ترتبط مستويات الجسم المضاد الذاتي BAFF والمصل بتشكيل TLS فيالكلى[42]. خفض مستويات BAFF خفض عدد الخلايا التائية في الكبيبات ومنع LN وتكوين أو الحفاظ على TLS [42].
علاوة على ذلك ، قد يوفر وجود FDCs ، أو ارتباط IgG-ICs بـ Fc RIIB ، مصدرًا لمستضد سليم [41،116،117] لتوسيع وتنشيط الخلايا البائية ، وإنتاج السموم اللمفاوية 1 2 ، والتي قد تزيد تعزيز تطوير TLS [118،119]. بدلاً من ذلك ، تفرز CD11b بالإضافة إلى الخلايا النخاعية مستوى عالٍ من BAFF وتعزز القدرة الكيميائية للخلايا B عن طريق تعديل الإشارات التي يسببها الكيماوي [120] ، مما يؤدي إلى تجميع الخلايا وتقسيم TLS. نظرًا لأن المستويات المتزايدة من BAFF تضخم تنشيط الخلايا التائية المحلية [121] ، فقد تعزز نشاط TFH وتطيل استجابات المركز الجرثومي في الموقع لـالكلىTLS. علاوة على ذلك ، في المرضى الذين يعانون من LN ، تؤدي التفاعلات من خلية إلى خلية فقط بين خلايا TFH والخلايا البائية إلى إحداث مستويات عالية من Bcl -6 و IL -21 في الخلالي [122]. قد يمثل هذا تأثير BAFF الذي يعزز التعبير عن ICOSL على الخلايا البائية المنشطة [123] ويحث على تكوين خلايا TFH [124،125]. هكذا،كلويقد يتشكل TLS في LN بسبب تسلل الخلايا المكونة للدم إلىالكلى، ولكن يلزم وجود مستويات عالية من BAFF لتشكيل TLS المقسمة بشكل صحيح أو الحفاظ عليها. يشير هذا إلى أن المستوى العالي أو الإنتاج المطول لـ BAFF قد يكون حدثًا رئيسيًا في تكوين TLS المجزأة.

Cistanche جيد لالكلى
3.2 الإشارات الجزيئية لتشكيل الهياكل الليمفاوية من الدرجة الثالثة
CXCL13 الذي تنتجه الخلايا اللحمية الليفية هو مادة كيميائية مهمة لخلايا B وخلايا محفز الأنسجة اللمفاوية (LTi). الفئران التي تفتقر إلى CXCL13 لا تشكل العقد الليمفاوية باستثناء العقد الوجهية وعنق الرحم والمساريقي [126]. يمكن تحقيق تحريض تكوين TLS في الفئران عن طريق الإفراط في التعبير عن CXCL13 مدفوعًا بمحفز أنسولين الجرذ (RIP) ، والذي ينشط في البنكرياس والبنكرياس.الكلى. يؤدي هذا إلى تكوين TLS التي تتميز بمناطق الخلايا B و T المنفصلة ، ووجود DCs التقليدية ، وشبكة كثيفة من الخلايا اللحمية والأوردة البطانية العالية (HEV) من نوع الأوعية الدموية [128]. يتم التعبير عن CXCL12 (أو العامل 1 المشتق من الخلايا اللحمية (SDF1)) بواسطة الخلايا اللحمية للنخاع العظمي وهو أمر بالغ الأهمية في تكوين الدم في نخاع العظم وتطور الخلايا البائية [129]. يتم التعبير عن CXCL12 بواسطة HEVs في الأعضاء الليمفاوية الثانوية (SLO) ويعمل بمثابة كيموكين أساسي لتجنيد الخلايا B ، في حين أن الخلايا التائية لا تستجيب في الغالب [130] (الجدول 1).
يمكن للخلايا الطلائية الأنبوبية من الفئران المعرضة لمرض الذئبة أن تعبر عن مستقبلات IL -23 وتنتج chemokine CCL20 الذي يمكنه جذب الخلايا الليمفاوية إلىالكلىالخلالي (الشكل 1) [7]. علاوة على ذلك ، يمكن لـ IL -23 العمل على الخلايا الظهارية الأنبوبية أن يثبط إنتاج الأرجيناز 1 الذي يقوّض الأرجينين وبالتالي يؤدي إلى زيادة تركيزات الأرجينين الضرورية للنمو المحلي للخلايا الليمفاوية [7]. من خلال الآلية الأولى ، تكون الخلايا الظهارية الأنبوبية قادرة على إنتاج مواد كيميائية مسببة للالتهابات لجذب الخلايا الليمفاوية التي يمكن تنشيطها محليًا. من خلال الآلية الثانية ، يمكن للخلايا الظهارية الأنبوبية إظهار القدرات المثبطة للمناعة والتي يمكن تجنبها في وجود الإنترلوكين -23 وربما المنشطات الأخرى.
يتم التعبير عن CCL19 و CCL21 بواسطة HEVs وبعض الخلايا اللحمية. وهي الروابط الخاصة بـ CCR7 الموجودة على الخلايا التائية والـ DC وخلايا LTi. كشفت الفئران PLT التي تفتقر إلى جين CCL19 و CCL21 المعبر عنها بالأنسجة اللمفاوية في الأوعية اللمفاوية عن دور حاسم لـ CCR7 و CCL19 / CCL21 في توجيه الخلايا التائية. في نموذج RIP-overexpression ، أثبت CCL21 أنه أكثر فعالية من CCL19 في إحداث تكوين TLS [131،132]. ومع ذلك ، حتى مع الإفراط في التعبير CCL21 ، لا يوجد تشكيل واضح لبصيلات الخلايا البائية 131. CCL28 له دور في تجنيد وتوجيه الخلايا البائية والتائية ويعزز الاستجابات المناعية التكيفية [١٣٣-١٣٥]. تدفع الإشارات من التفاعل بين CCL28 و CCR3 / CCR10 هذه العمليات وتجذب خلايا مناعية مختلفة من الجوار المحلي [135،136]. في الآونة الأخيرة ، لوحظ تجنيد خلايا Treg بواسطة CCL28 ، مما يدل على أن لها دورًا في تعديل جهاز المناعة ، والحفاظ على تحمل المستضدات الذاتية ، ومنع تطور أمراض المناعة الذاتية [137،138] (الجدول 1).

تم اقتراح أعضاء عائلة TNF الفائقة (TNFSF) ، وهي TNF و lymphotoxin (LT) ومستقبلات الإشارة الخاصة بهم TNFRI / II و LT R ، لتعزيز تكوين TLS. أيضًا ، أدى التعبير خارج الرحم عن TNF أو LT ، ولكن ليس LT ، تحت سيطرة RIP إلى تكوين TLS [139140]. لوحظ التأثير الأكثر أهمية عندما تم التعبير عن LT و LT معًا ، مما أدى إلى تراكم كريات الدم البيضاء الغازية في جزر البنكرياس ، و TLS أكبر بكثير من تلك التي تشكلت في الفئران المعدلة وراثيا LT [139]. TNFR-I هو المنظم الأساسي لتكوين الأنسجة اللمفاوية وتكوين المركز الجرثومي ، بدلاً من TNFR-II [141] ، وهو يتوسط TLS البنكرياس الناجم عن LT [142]. تم أيضًا تورط تنشيط TNFR-I و LT R في الأبهر TLS ، حيث يؤدي انحراف إشارة LT R إلى قمع تعبير CCL21 و CXCL13 ، نتيجة لانخفاض تكوين HEV وتعطل تطور TLS [143،144] (الشكل 1 ب). 2).

في حين أن تأثير LT ، بمفرده أو مع LT ، يبدو واضحًا ، فإن دور TNF متنازع عليه. في بعض الأمراض الالتهابية ، بما في ذلك تلك التي تنطوي على TLS ، يكون لعامل نخر الورم نشاط مضاد للالتهابات [144]. يتحسن التهاب الأنسولين في الفئران NOD والذئبة في الفئران النيوزيلندية بعد حقن عامل نخر الورم [144145].
يؤدي الإفراط في التعبير الجيني عن IL -6 و IL -6 R إلى التراكم حول الأوعية الدموية للخلايا B وخلايا البلازما B الناضجة [146]. يتم التعبير عن IL -1 الذي تنتجه MSCs بشكل مفرط في الفئران المعرضة لمرض الذئبة وقد يساهم في تكوين TLS [47]. تحفيز الخلايا التائية باستخدام IL -4 أو التعبير المستحث IL -7 عن LT ؛ كان IL -7 أكثر فاعلية بالنسبة لخلايا CD4 بالإضافة إلى الخلايا التائية [131]. تعد عائلة جين IL -17 أمرًا حيويًا في الدفاع ضد مسببات الأمراض وقد تورطت في العديد من سيناريوهات الالتهابات المزمنة. مثل أعضاء TNFRSF ، يتم تحفيز إشارات مستقبلات IL -17 عبر الخلايا التائية NF-κB و IL -17 بواسطة IL -6 و TGF و IL -23 ، ولكن يتم تثبيتها بواسطة إيل -27. لذلك ، فإن IL -17 هو وسيط أساسي في عملية تحفيز عديد السكاريد الدهني حول [147]. يتم التعبير عن IL -7 R بواسطة خلايا LTi جنبًا إلى جنب مع CXCR5) يعزز IL -7 تكوينها في SLOs [126].
قد يعزز BAFF إصابة الأنسجة من خلال التأثير على جودة وكمية السيتوكينات التي تحركها الخلايا التائية مثل IL -17 و IL -4 و IFN. زيادة مستويات BAFF فيالكلىقد يؤدي إلى تلف الكبيبات عن طريق غزو الخلايا التائية داخل الكبيبات ، أو عن طريق تحفيز تكوين خلايا TH17. من غير الواضح ما إذا كان موضع الخلايا التائية عملية موازية أو معتمدة تعزز التهاب كبيبات الكلى والتهاب الكلية الخلالي النبيبي. لقد ثبت أن منع التحفيز المشترك للخلايا التائية [148] أو تحييد IFN و IL -4 [149،150] ، يؤدي إلى تحسن أو تأخير فيكلويعلم الأمراض. وبالمقارنة ، تم العثور على تسلل الخلايا التائية وتجميعها فيالكلىخزعات من مرضى الذئبة الحمراء [151]. ارتشاح الخلايا المناعية في المناطق الخلالي الأنبوبية في SLE يرتبط مع LN [41] ، مما يشير إلى أن موضع الخلايا التائية داخل الكلى أمر حيوي في المرض.
3.3 الأوعية في الهياكل اللمفاوية من الدرجة الثالثة
يشبه TLS العقد الليمفاوية من حيث الهيكل والأوعية الدموية والتكوين الخلوي والملف الجانبي الكيميائي. تشمل الخلايا المناعية مناطق الخلايا التائية والخلايا البائية والخلايا العارضة للمستضد ، بما في ذلك الخلايا الجذعية الجنينية والخلايا الناضجة. تنقسم الأوعية في TLS بشكل أساسي إلى أوعية لمفاوية ودموية (الشكل 3).
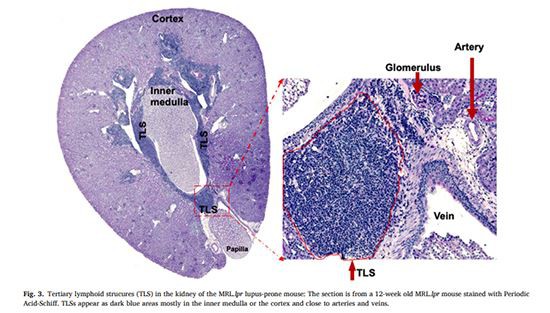
كلويتعتبر الأوعية اللمفاوية (LVs) جزءًا من النسيج الخلالي لأنها لا تحتوي على غشاء قاعدي ، كما أنها ذات نهايات عمياء وتفتقر إلى الخلايا الحبيبية [152]. الشعيرات الدموية اللمفاوية تعبر عن PROX -1 و LYVE -1 و CCL21 و podoplanin و VEGFR -2 و VEGFR -3 [153]. تعبر الأوعية اللمفاوية في TLS عن العلامات اللمفاوية مثل LYVE -1 و PROX -1 والبودوبلانين (في كل من الفئران والبشر) و D2-40 (في البشر) [154] ، كما ورد في دراسات مختلفة من المزمنةالكلىالرفض [155156] ، الطعم الخيفي للقلب [157] ، نماذج الفئران المعدلة وراثيًا [158] ونموذج فأر لمرض شوغرن الأولي الشبيه بالعمر [159]. ومع ذلك ، لا يزال هناك الكثير لتوضيحه.
من غير المعروف ما إذا كانت أوعية TLS تؤدي نفس الوظائف الموجودة في العقد الليمفاوية. يبدو أنها تساهم في تصريف السوائل ، لكن هذا لم يتم استكشافه بالكامل. من غير المعروف أيضًا ما إذا كانت LVs تحمل مستضدًا وخلايا داخل TLS والخلايا بعيدًا عن TLS ، مثل الأوعية الواردة والصادرة في العقد الليمفاوية. يشير احتواء TLS LVs بشكل متكرر على الخلايا [159،160] ، إلى أن لها دورًا كناقلات من خلال تعبير CCL21 ، الذي يتفاعل مع الخلايا التي تعبر عن CCR 7-. ومع ذلك ، فإن LVs في بعض TLSs تتراكم الخلايا ، مما يشير إلى أنها لا تسهل التصريف الخلوي ولديها ضعف في الوظيفة الصادرة.
تعبر الخلايا المقيمة في العقدة الليمفاوية عن سفينجوزين -1 فوسفات (S1P) وتفاعلها مع مستقبلات S1P1 على الخلايا الليمفاوية مهم لخروجها من العقد الليمفاوية. FTY720 (فينجوليمود) هو ناهض S1P1 الذي يتسبب في استيعابها وتراكم الخلايا الليمفاوية في الغدد الليمفاوية [161] ، وبالتالي تعمل كمثبط للمناعة. عندما يتم علاج الفئران NOD المصابة بـ TLS البنكرياس بـ FTY720 ، فإنها لا تستمر في تطوير تدمير الجزر ومرض السكري [162]. يثبط FTY720 تطور المرض فقط في الوقت الذي تظهر فيه الفئران TLS [163]. ارتبط TLS البنكرياس مع درجات عالية من التهاب الأنسجة بعد علاج FTY720 ، مما يشير إلى أن الخلايا محاصرة داخلها. حدث تدمير الجزر ومرض السكري في غضون أيام من توقف العلاج FTY720 [162،164]. وبالتالي ، يبدو أن التدرج S1P يؤثر على تهريب الخلايا الليمفاوية في TLS LVs. قد يجبر فينجوليمود TLS على الذوبان في المرضى والفئران المصابة بمرض الذئبة.
تنقل LVs مستضدات قابلة للذوبان أو مرتبطة بالخلايا إلى العقد الليمفاوية. يتم التعبير عن البروتين المرتبط بحويصلة البلازما (PLVAP) بواسطة الخلايا البطانية اللمفاوية في الجيوب الأنفية اللمفاوية في الغدد الليمفاوية. تساهم الخلايا البطانية اللمفاوية الإيجابية PLVAP في غربلة الخلايا الليمفاوية ومستضدات الوزن الجزيئي المرتفع التي تدخل الغدد الليمفاوية [165]. نظرًا لأن TLS تحتوي على نظام قناة [166] ، فمن المنطقي التساؤل عما إذا كانت LVs في TLS والعقد الليمفاوية تعمل بشكل مشابه. قد يكون نقل المستضد أقل أهمية مما هو عليه في SLO لأن المستضد هو مكون فعلي لـ TLS. ومع ذلك ، نظرًا لأن الخلايا العارضة للمستضد موجودة عادةً في TLS ، فإن هذا أمر قابل للنقاش.
كما هو مذكور أعلاه ، فإن LVs في العقد الليمفاوية تقدم مستضدات ذاتية [167-169] إما مباشرة من خلال التعبير عن جزيئات معقد التوافق النسيجي الرئيسي (MHC) أو مستضد على الخلايا العارضة للمستضد "الكلاسيكية". قد يسهل عرض المستضد الذاتي بواسطة LVs [167] تحريض التسامح أو تنشيط الخلايا التائية في العقد الليمفاوية أو TLS. لم يتم إجراء الدراسات التي تبحث في قدرة TLS LVs على تقديم مستضد وتحفيز أي من هذه النتائج.
HEVs هي عبارة عن أوعية دموية موجبة ذات بنية مميزة. يبدو أن HEVs لها دور في نقل الخلايا الليمفاوية المنقولة بالدم إلى TLS. هذه الظاهرة هي نوع من التسلل المتخصص الذي يمكن لخلايا الذاكرة التائية ذات التعبير المنخفض من L-selectin (ربما بسبب التعبير عن PNAd) أن تدخلالكلى[139]. وجدت دراسة تجريبية أجريت على الفئران التي تعاني من نقص في LT أو LT LN أن تطوير HEV المعبّر عن PNAd متوقف ، مما يؤدي إلى انخفاض حجم وخلوية التسربات اللمفاوية [139]. وبالتالي ، قد تكون إشارة LT R مطلوبة للتجميع اللمفاوي المنظم وتشكيل HEV.
4. الاستنتاجات والأسئلة المفتوحة
على الرغم من أن الاستجابات المناعية المتولدة في SLO يمكن أن تولد الحماية ضد مسببات الأمراض ، فإن استجابات المناعة الذاتية في TLS قد تكون مدمرة. المراكز الجرثومية في TLS لها خصائص مماثلة للمراكز الجرثومية في SLOs وتوفر أرضية للتوسع النسيلي للخلايا المناعية وفرط التحول الجسدي [41]. على الرغم من أن وجود المجمعات المناعية يعتبر مهمًا في تكوين TLS ، فإن المزيد من الأدلة الحديثة تشير إلى أنه تحت تأثير السيتوكينات يمكن أن تنتج الخلايا الظهارية الأنبوبية السيتوكينات القادرة على جذب الخلايا التائية [7].
لقد ثبت أن الخلايا البائية الموجودة في TLS خضعت لفرط تحور جسدي [41] وبالتالي فإن الإنتاج المحلي للأجسام المضادة الذاتية والتشكيل المحتمل للدوائر المتكاملة في الموقع أمر مؤكد. توجد خلايا Th17 فيالكلىمن الأشخاص والفئران المصابة بالذئبة تشير إلى المساهمة المباشرة لهذه الخلايا في الاستجابة الالتهابية والكلىالضرر [101.170 - 172]. حقيقة أن ذخيرة TCR منالكلىارتشاح الخلايا في الفئران والأشخاص المصابين بمرض الذئبة مقيد [93] يشير إلى أنه يتم التعرف على مستضدات خاصة بالكلى ، لا تزال طليقة. تعتبر خلايا Th17 حيوية في تكوين TLS في انتشار الالتهاب في الجهاز العصبي المركزي ورئتي الأطفال حديثي الولادة [173-175]. يمكن توقع دور مماثل للخلايا في إنشاء والحفاظ على الالتهاب في العصبة الليفية.
وجود خلايا Treg فيالكلىTLS ووظيفتها المحتملة غير معروفة. من الممكن أن يتم استبعادهم من خلال آليات غير معروفة أو في حالة وجودهم يصبحون محرومين من وظيفتهم المتوقعة. من المعروف أن خلايا Treg في وجود بيئة التهابية تفقد وظيفتها التنظيمية [78].
على الرغم من الادعاء بأن شدة الالتهاب الخلالي تمثل علامة مشؤومة علىكلويلا تزال وظيفة TLS غير معروفةالكلىتلف. قد تدمر الخلايا التائيةالكلىتم عرض الخلايا المقيمة مثل الخلايا البادوسية [21] ، من خلال السمية الخلوية المباشرة أو عن طريق الإضرار بوظيفة خلايا الكلى من خلال عمل السيتوكينات كما هو موضح في IL -23 [7] و BAFF [123].
إن مجال مساهمة TLS في تطويرالكلىالتليف الذي لا رجعة فيه ويحدد نهاية الوظيفة. قد تؤدي السيتوكينات التي تنتجها الخلايا المتسللة إلى جانب مساهمة العوامل الأخرى التي تنتجها الخلايا المقيمة في الكلى إلى تعزيز إنتاج الكولاجين بواسطة الخلايا الليفية.
ستمكن التقنيات القادمة بما في ذلك تسلسل الحمض النووي الريبي أحادي الخلية [176] ونسخ النسخ المكانية من توصيف التفاعلات بين الخلايا التي تتألف من TLS والكلىالخلايا المقيمة. قد تسمح أيضًا بتوصيف مجموعات فرعية بين مرضى LN ، حيث من المؤكد أن LN غير متجانس سريريًا وممرضًا. الجهود المبذولة لعكس أمراض الكلى عن طريق توصيل الأدوية إلىالكلىيجب أن تسمح الخلايا المقيمة (الخلايا الحجرية [22] ، الخلايا الظهارية الأنبوبية [7]) باستعادة أكثر فعالية لوظيفة خلايا الكلى بينما يتم تجنب الآثار الجانبية الناتجة عن الإعطاء الجهازي.
شكر وتقدير
بدعم من هيئة الصحة الإقليمية لشمال النرويج ، منحة بحثية HNF 1427-18.
من: 'التفاعل المناعي والكلىالخلايا المقيمة في تكوين الهياكل اللمفاوية الثالثة في التهاب الكلية الذئبيسيمين جمالي وآخرون
---1568-9972 / © 2021 المؤلفون. تم النشر بواسطة Elsevier BV. هذه مقالة مفتوحة الوصول بموجب ترخيص CC BY.

