يتم تعديل التواقيع العصبية لتشفير الذاكرة في مرض انفصام الشخصية عن طريق العلاج المضاد للذهان
Mar 17, 2022
للمزيد من المعلومات:ali.ma@wecistanche.com
الملخص
لا يوجد علاج دوائي لعلاج ضعف الإدراك في مرض انفصام الشخصية (SZ). من الضروري توصيف الأمراض الكامنة وراء معالجة الذاكرة لتطوير علاجات جديدة بشكل فعال.
في هذه الدراسة الطولية ، قمنا بدمج التصوير بالرنين المغناطيسي الوظيفي أثناء مهمة تشفير الذاكرة مع التحليل الطيفي للبروتون بالرنين المغناطيسي لقياس الجلوتامات الحصينية بالإضافة إلى الجلوتامين (Glx). تم فحص سبعة عشر SZ بدون علاج وبعد 6 أسابيع من العلاج باستخدام ريسبيريدون ومقارنتها بمجموعة من الضوابط الصحية المتطابقة (HC) التي تم فحصها لمدة 6 أسابيع.

انقر لمعرفة الفوائد والآثار الجانبية للذاكرة
أظهر المرضى غير المعالجين استجابة منخفضة تعتمد على مستوى الأكسجين في الدم (BOLD) في عدة مناطق ، بما في ذلك الحُصين ، واستجابة BOLD أكبر في مناطق شبكة الوضع الافتراضي (DMN) أثناء تشفير الذاكرة الصحيح. أشارت التناقضات اللاحقة من التفاعلات المهمة للمجموعة بمرور الوقت إلى انخفاض استجابة قرن آمون BOLD عند خط الأساس مع زيادة لاحقة بعد العلاج. لم يكن Hippocampal Glx مختلفًا بين المجموعات عند خط الأساس ، ولكن في الأسبوع 6 ، كان Hippocampal Glx أقل بشكل ملحوظ في SZ مقارنة بـ HC. أخيرًا ، في SZ أعلى من الحصين Glx تنبأ بإلغاء تنشيط أقل لاستجابة BOLD في مناطق DMN.

سمح لنا استخدام طريقتين لتصوير الدماغ بالتحقيق في الآليات المختلفة المتضمنة في اختلال وظيفي في ترميز الذاكرة في مرض انفصام الشخصية. تنبع أمراض الحصين أثناء تشفير الذاكرة من انخفاض تجنيد الحصين وإلغاء تنشيط خلل لشبكة DMN ، ويمكن تعديل تجنيد الحصين أثناء التشفير عن طريق العلاج بمضادات الذهان. توقع ارتفاع Glx في المرضى غير المعالجين انخفاضًا في إلغاء تنشيط DMN ؛ تشير هذه النتائج إلى آلية يتم من خلالها تحقيق التعطيل الخاطئ لشبكة DMN ، وهي السمة المميزة للنتائج المرضية في SZ.

ديميت غورلير 1 ، ديفيد ماثيو وايت 1 ، نينا فانيسا كراجولجاك 1 ، لورانس فير هوف 2 ،
كلينتون مارتن 1 ، بليك تينانت 1 ، أدريان كارول لاهتي 1 ، *
1 قسم الطب النفسي والبيولوجيا العصبية السلوكية ، جامعة ألاباما في برمنغهام
2 قسم الأعصاب بجامعة ألاباما في برمنغهام
الكلمات الدالة:
التشفير؛ استرجاع؛ قرن آمون؛ شبكة الوضع الافتراضي (DMN) ؛ الغلوتامات. العلاج المضاد للذهان. التصوير بالرنين المغناطيسي الوظيفي مطيافية الرنين المغناطيسي (MRS)
مقدمة
يظهر ما يقرب من 75-85 بالمائة من مرضى الفصام ضعفًا في الإدراك مع قصور انتقائي في التعلم والذاكرة (1). الأهم من ذلك ، أن الضعف في الذاكرة العرضية لا يتم تفسيره حصريًا من خلال الضعف العام في معدل الذكاء أو الأداء التنفيذي (2). في الآونة الأخيرة ، أصبح مزيج من تقنيات تصوير الدماغ ممارسة شائعة في البحث للاستفادة من المعلومات المتقاطعة وتحسين تحديد العلامات المرضية للأمراض (3). يمكن دراسة الارتباطات العصبية لمعالجة الذاكرة العرضية في مرضى الفصام (SZ) باستخدام النماذج السلوكية المناسبة جنبًا إلى جنب مع التصوير بالرنين المغناطيسي الوظيفي (fMRI) (4 ، 5). يسمح التحليل الطيفي بالرنين المغناطيسي للبروتون (1H-MRS) بالقياس في الجسم الحي لمستقلبات الدماغ مثل الجلوتامات ، وهو حمض أميني يشارك في النقل العصبي الاستثاري (6) والتمثيل الغذائي (7 ، 8). بالنظر إلى دور الغلوتامات باعتباره الناقل العصبي الرئيسي المثير للمشارك في الإدراك (9) ودور الحُصين في عمليات التعلم والذاكرة ، فإن قياس الغلوتامات في الحُصين يمكن أن يوفر نظرة ثاقبة في علم أمراض التعلم وضعف الذاكرة في SZ. الأهم من ذلك ، أبلغت عدة مجموعات الآن عن مستويات مرتفعة من الغلوتامات في الأدوية الساذجة أو غير المعالجة من SZ في مناطق الدماغ المختلفة (10 ، 11) ، بما في ذلك في قرن آمون (12).

تشير الأدلة التراكمية إلى أن عجز الذاكرة في SZ قد يكون مرتبطًا بضعف في التشفير المتعمد (13 ، 14). أظهرت الدراسات السابقة وجود علاقة إيجابية بين نجاح التشفير والاستجابة المعتمدة على مستوى الأكسجين في الدم في قرن آمون (BOLD) ، مشيرة إلى دور الحُصين في تكامل المعلومات من مناطق قشرية مختلفة (15-17). لقد ثبت أن تنشيط الحُصين والتلفيف المجاور للحصين أثناء التشفير يُنبئ بنجاح الاسترجاع اللاحق (18 ، 19). أبلغت العديد من دراسات التصوير العصبي عن تشوهات إشارة BOLD في الحُصين والتلفيف المجاور للحصين في كل من SZ (20) والأقارب غير المتأثرين (21-24). ومع ذلك ، فقد أسفرت هذه الدراسات عن نتائج متناقضة ، مما يدل على زيادة وانخفاض استجابة BOLD في SZ أثناء مهام الذاكرة (25).

يلعب منع مناطق شبكة الوضع الافتراضي (DMN) أثناء تشفير الذاكرة دورًا مهمًا في تحقيق الأداء الأمثل للذاكرة (26). يتم قمع DMN أثناء المطالب المعرفية ولكنها تعمل أثناء الراحة (27). في SZ ، تم الإبلاغ على نطاق واسع عن فرط نشاط DMN أثناء المهام المعرفية (28 ، 29). تمشيا مع دور الجلوتامات في علم الطاقة العصبية (30) ، Hu et al. (31) عن وجود علاقة إيجابية بين تركيز الغلوتامات العالي في DMN الخلفي وتقليل تعطيل DMN أثناء مهمة الذاكرة العاملة. بالإضافة إلى ذلك ، Kapogiannis et al. حددت العلاقة بين الغلوتامات الخلفية DMN (القشرة الخلفية الخلفية) والاتصال الوظيفي الجوهري لـ DMN (32). حددت دراستان الآن وجود علاقة بين الغلوتامات في القشرة الحزامية الأمامية (ACC) والاستجابة الجريئة في DMN الخلفي في الضوابط الصحية ، ووجد أن هذه العلاقة معاكسة في SZ (33 ، 34). هناك حاجة لتوضيح الكيمياء العصبية لفرط نشاط DMN في SZ.

قامت الغالبية العظمى من دراسات التصوير الخاصة بوظيفة الذاكرة بتسجيل SZ الدوائي ، ومع ذلك ، فقد ثبت أن الأدوية المضادة للذهان لها تأثيرات تعديل على وظائف المخ أثناء الراحة (35 ، 36) ، وأثناء المهام الإدراكية (37). لذلك ، من غير الواضح إلى أي مدى ترتبط هذه النتائج بالعلاج بمضادات الذهان بدلاً من الخصائص الجوهرية للمرض. بالإضافة إلى ذلك ، على الرغم من أن الدور الحاسم للأدوية المضادة للذهان في تخفيف الأعراض ، مثل الهلوسة أو الأوهام ، راسخ جيدًا ، إلا أن فوائدها على الوظائف المعرفية أكثر إثارة للجدل (38). ومع ذلك ، فقد أظهرت الدراسات التي شملت عددًا كبيرًا من الموضوعات مثل CATIE (39) و EUFEST (40) أن العلاج بمجموعة متنوعة من مضادات الذهان من الجيل الأول والثاني يرتبط بتحسينات معتدلة في الاختبارات المعرفية. فيما يتعلق بأهدافنا ، أفادت الدراسات الحديثة أن الأدوية المضادة للذهان تقلل من مستويات الجلوتامات (41-43).
كان الغرض من الدراسة الحالية هو فحص استجابة BOLD ذات الصلة بالتشفير ومستويات الغلوتامات في الحصين في حالة الراحة في SZ باستخدام تصميم طولي (قبل العلاج المضاد للذهان ، أثناء عدم تلقيه للعلاج ، وبعد 6 أسابيع) لمقارنة عناصر التحكم الصحية واستجابة SZ دون التأثير. من الدواء كعامل مربك والتحقيق في تأثير الدواء على استجابات الدماغ في SZ. افترضنا أنه في SZ سنقوم بتكرار نتائج استجابة BOLD المنخفضة في المناطق التي تم العثور عليها سابقًا المرتبطة بمعالجة الذاكرة ، وزيادة استجابة BOLD في مناطق DMN ، بالإضافة إلى التغييرات نتيجة العلاج. بناءً على النتائج السابقة ، افترضنا أن مستويات الغلوتامات في الحصين سترتفع قبل العلاج وتنخفض بعد العلاج. بالإضافة إلى ذلك ، استكشفنا العلاقة بين الغلوتامات الحصينية والاستجابة الجريئة في DMN قبل العلاج وبعده.

المواد والأساليب
مشاركون
تم تجنيد الأشخاص المصابين بالفصام والاضطراب الفصامي العاطفي (SZ) من عيادات الطب النفسي الخارجية وغرفة الطوارئ في جامعة ألاباما في برمنغهام للمشاركة في الدراسة بناءً على التوقف عن تناول الأدوية المضادة للذهان لمدة 10 أيام على الأقل (لم يتم إيقاف الدواء لتلبية هذا معيار). من بينهم ، أكمل 17 مريضًا كلاً من جلسات التشفير والاسترجاع لنموذج الذاكرة في نقطتين زمنيتين (خط الأساس / غير المعالج والأسبوع 6). تم تجنيد سبعة عشر موضوعًا صحيًا (HC) ، بدون تاريخ شخصي أو عائلي في قريب من الدرجة الأولى لاضطرابات كبيرة في DSM-IV-TR Axis I ، باستخدام الإعلانات في النشرات وصحيفة الجامعة. كانت معايير الاستبعاد هي الحالات الطبية الرئيسية ، وتعاطي المخدرات أو الاعتماد عليها (باستثناء النيكوتين) في غضون ستة أشهر من التصوير ، وإصابة سابقة في الرأس ، واضطراب عصبي ، وفقدان الوعي لأكثر من دقيقتين ، والحمل. قدم مجلس المراجعة المؤسسية بجامعة ألاباما في برمنغهام الموافقة على الدراسة وأعطت جميع المواد موافقة خطية مستنيرة قبل المشاركة. تم إجراء التشخيصات باستخدام السجلات الطبية للأشخاص والمقابلة التشخيصية للدراسات الجينية (DIGS) (44). تميزت الوظيفة المعرفية العامة لكل موضوع بالبطارية القابلة للتكرار لتقييم الحالة العصبية النفسية (RBANS) (45).
تم فحص المرضى وهم دون علاج ثم دخلوا في تجربة لمدة {{0} أسبوع باستخدام ريسبيريدون (نظام جرعات مرن) ، وفي نهاية الأمر تلقوا فحصًا ثانيًا. تم تقييم شدة الأعراض باستخدام مقياس التقييم النفسي الموجز (BPRS) (46) والمقاييس الفرعية الإيجابية والسلبية. تمت مراقبة الامتثال للأدوية من خلال عدد حبوب منع الحمل. تم فحص HC مرتين كل 6- أسبوع. قبل كل جلسة مسح ، خضع جميع الأشخاص لفحص دواء البول.
تصميم المهمة والتحليل السلوكي
تتكون مهمة الذاكرة العرضية (انظر في (4 ، 47) للحصول على التفاصيل) من مرحلة تشفير متعمدة ، تليها مرحلة ذاكرة التعرف بعد تأخير دقيقة 15-. لتعظيم أداء الاسترداد ، تم استخدام نموذج تشفير عميق باستخدام قرار الرسوم المتحركة. أثناء مهمة التشفير ، شاهد المشاركون سلسلة من 60 كلمة ، مقدمة واحدة في كل مرة لمدة 300 مللي ثانية متبوعة بشاشة تثبيت. أشارت إشارة التحفيز الثانية 2- ("Alive؟") إلى أن المشارك يجب أن يجيب عن طريق الضغط على الزر ما إذا كانت الكلمة القادمة حية أم لا. بعد فاصل زمني مدته 15 دقيقة ، أجرى المشاركون مهمة الاسترجاع ، حيث رأوا 60 كلمة ، بما في ذلك 30 كلمة شوهدت سابقًا (كلمات قديمة) و 30 كلمة جديدة ، مقدمة واحدة تلو الأخرى لمدة 300 مللي ثانية. أشار 2- منبه التحذير الثاني ("جاهز؟") إلى أن المشارك يجب أن يجيب عن طريق الضغط على الزر سواء كانت الكلمة التالية "قديمة" أو "جديدة". اعتمادًا على ردود المشاركين ، تم تصنيف هذه العناصر على أنها نقرات ، وأخطاء ، ورفض صحيح ، وإنذارات كاذبة. نظام IFIS-SA (في Vivo Corp. ، أورلاندو ، فلوريدا) يقوم بتشغيل برنامج E- Prime (الإصدار 1.2 ؛ Psychology Software Tools ، Inc. ، Pittsburgh ، Pennsylvania) يتحكم في تسليم التحفيز وتسجيل الاستجابات وأوقات رد الفعل.
تم اعتبار الكلمة مشفرة بشكل صحيح إذا تم استرجاعها بنجاح في جلسة الاسترجاع اللاحقة. تم حساب مشاركة المهام باستخدام الضغط على الأزرار أثناء تجارب التشفير. استخدمنا d-prime (d ') ، محسوبًا على أساس المعلومات أثناء جلسات الاسترجاع ، كمقياس أساسي لأداء الذاكرة. d 'مقياس الحساسية عن طريق حساب المسافة بين الإشارة والضوضاء في وحدات الانحراف المعياري (d ′=z (HITS) - z (FALSE ALARMS)) (48)
معلمات التصوير
تم الحصول على جميع بيانات التصوير في جلستين على ماسح ضوئي للرأس فقط 3T (Siemens Allegra ، Erlangen ، ألمانيا) ، مزود بملف رأس إرسال / استقبال مستقطب دائريًا. تم الحصول على بيانات الرنين المغناطيسي الوظيفي باستخدام تسلسل التصوير المتدرج المستوي (EPI) (وقت التكرار / وقت الصدى [TR / TE]=2100 / 30 مللي ثانية ، زاوية الانقلاب=70 درجة ، مجال الرؤية {{6 }} × 24 سم 2 ، 64 × 64 مصفوفة ، سمك شريحة 4 مم ، فجوة 1 مم ، 26 شريحة محورية). تم الحصول على مسح هيكلي عالي الدقة باستخدام T 1- المغناطيسية المرجحة المعدة للحصول على تسلسل التدرج والصدى السريع (MPRAGE) (TR / TE / وقت الانعكاس [TI]=2300 / 3.93 / 1100 مللي ثانية ، زاوية انعكاس=12 درجة ، مصفوفة 256 × 256 ، وحدات بكسل متجانسة 1 مم). تم الحصول على سلسلة من عمليات المسح التشريحي الموزونة السهمية والإكليلية والمحورية 1- والتي تعمل كمؤشرات MRS لوضع فوكسل الطيفي. تم محاذاة الشرائح إلى خط الوسط التشريحي للتحكم في إمالة الرأس. لتسهيل وضع فوكسل ، تم الحصول على الصور المحورية على طول المحور الطويل للحصين ، كما يتم عرضها من الصور السهمية. تم وضع فوكسل في الحصين الأيسر بحيث تم تكبير كمية المادة الرمادية (حجم فوكسل 2.7 × 1.5 × 1 سم 3). تم إجراء الملء اليدوي لتحسين تجانس المجال عبر فوكسل ، واستخدمت نبضات انتقائية التحول الكيميائي (CHESS) لقمع إشارة الماء. تم الحصول على الأطياف باستخدام تسلسل التحليل الطيفي ذي النقاط (PRESS ؛ TR / TE=2000 / 80 مللي ثانية لتحسين إشارة الغلوتامات (49) وتقليل مساهمة الجزيء الكبير ؛ عرض النطاق الترددي الطيفي 1200 هرتز ؛ 1024 نقطة ؛ 640 متوسطًا).
التحليل الإحصائي
السلوك والديموغرافيات. - تم إجراء التحليلات باستخدام SPSS 20 (IBM SPSS Inc. ، شيكاغو ، إلينوي). تم إجراء مقارنات المجموعة باستخدام مربع كاي أو تحليل التباين ، حسب الاقتضاء. تم تحليل تحليلات الاستجابة على تجارب التشفير ، ووقت رد الفعل (RT) للتجارب الصحيحة ، والنسبة المئوية للكلمات المشفرة بشكل صحيح ، وقيم d 'باستخدام نماذج مختلطة خطية تقارن التأثيرات الثابتة للمجموعة (HC مقابل SZ) ، والوقت (غير المعالج مقابل الأسبوع 6) ) والتفاعلات. تم إجراء التحليلات اللاحقة عند الاقتضاء باستخدام تصحيح Bonferroni.
تحليل MRS. - بعد إزالة ذروة الماء المتبقية ، تم تحديد كمية بيانات MRS في المجال الزمني باستخدام خوارزمية AMARES (5 0) في jMRUI (الإصدار 3.0). تم تضمين المعرفة السابقة المستمدة من أطياف المستقلب في المختبر وفي الجسم الحي في النموذج (51) ، والذي يتكون من قمم لـ N-acetyl-aspartate (NAA) ، والكولين (Cho) ، والكرياتين (Cr) ، وثلاث قمم للجلوتامات زائد. الجلوتامين (Glx). تم تحسين السعة وعرض الخط والتحول الكيميائي لكل قمة. تم حساب الحدود السفلية كرامر-راو (CRLB) (52) لكل قمة. كانت معايير الاستبعاد CRLB أكبر من 25 بالمائة. لم يتم استبعاد أي بيانات بناء على هذه المعايير. تم تحديد كمية Glx فيما يتعلق Cr. كانت بيانات MRS مفقودة لـ 1 SZ ، في كل من خط الأساس والأسبوع 6 ، و 2 HC في الأساس و 3 HC في الأسبوع 6. تم اختبار الاختلافات بين المجموعات باستخدام عينة مستقلة اختبار t في الأساس والأسبوع 6. كان مستوى ألفا. تعيين في .05.
تحليل الرنين المغناطيسي الوظيفي. - تم تنفيذ تحليلات البيانات في SPM12 الذي يعمل في MATLAB (الإصدار R2013b). تضمنت المعالجة المسبقة لبيانات الرنين المغناطيسي الوظيفي تصحيح توقيت الشريحة ، وإعادة المحاذاة ، وإعادة التوزيع إلى الحجم الوظيفي المتوسط ، وتصحيح القطع الأثرية / الحركة (الحركة> 1 مم) باستخدام ArtRepair ، والتسجيل في الفحص الهيكلي ، والتطبيع لمساحة MNI باستخدام DARTEL (53) مع { {4}} تجانس FWHM Gaussian kernel. تم استبعاد المشاركين من مزيد من التحليلات إذا تم إصلاح 33 في المائة أو أكثر من بياناتهم أثناء تصحيح القطع الأثرية والحركة.
يتكون التحليل الإحصائي على مستوى الموضوع من GLM مرتبط بالحدث مع عوامل الانحدار التالية: ترميز التأثير الرئيسي ، وتشفير التجارب غير الصحيحة وترميزها بشكل صحيح. تم اعتبار الكلمة مشفرة بشكل صحيح إذا تم استرجاعها بنجاح في جلسة الاسترجاع اللاحقة. تم تصميم جميع الأحداث باستخدام دالة استجابة الدورة الدموية المتعارف عليها ، وتمت تصفية البيانات بمرور عالي (حد القطع=256 ثانية). على مستوى المجموعة ، تم إنشاء خرائط معلمية إحصائية لإشارة BOLD أثناء التشفير وأجريت مقارنات بين المجموعات باستخدام اختبارات t ذات عينتين. بالنسبة لتصحيحات المقارنة المتعددة ، تم تحديد عتبة حجم الكتلة داخل SPM12 ، بناءً على نظرية المجال العشوائي الغاوسي ، مثل عدد وحدات البكسل المتجاورة مع p< .05="" (uncorrected)="" to="" accept="" the="" false="" discovery="" rate="" (fdr)="" of="" 0.05="">
لتحديد الاختلافات بين المجموعات الخاصة بشبكة DMN ، قمنا ببناء منطقة اهتمام مشتركة (ROI) ، بما في ذلك التلفيف الأمامي الإنسي ، والحزامية الخلفية ، والحصين ، والتلافيف الجداري السفلي ، باستخدام أطلس AAL داخل جامعة ويك فورست بيك أطلس الإصدار 2.4 (55). استندت الارتباطات التشريحية لقناع الشبكة الافتراضي إلى Buckner وزملائه (56). تصحيح الحجم الصغير (SVC) ص< .05="" was="" used="" to="" correct="" for="" multiple="">
لتقييم تأثير الدواء ، أجرينا تحليلًا عامليًا كاملًا ، وحددنا مناطق الدماغ الحساسة لتفاعل المجموعة × الوقت أثناء تشفير التجارب الصحيحة. تم إدخال تقديرات الموضوع والمعلمة لتشفير التجارب الصحيحة في تحليل التأثير العشوائي باستخدام "نموذج العوامل الكامل" الخاص بـ SPM. كانت العوامل هي الوقت (خط الأساس / غير المعالج ، الأسبوع 6) والمجموعة (HC ، SZ). بالنسبة إلى تحليل الدماغ بالكامل هذا ، تم تحديد عتبة حجم الكتلة للمقارنات المتعددة بواسطة محاكاة مونت كارلو باستخدام عتبة مستوى فوكسل عند p=.05 مع 1000 محاكاة. لأغراض التوضيح ، تم استخراج الإشارة من مناطق مهمة باستخدام REX (CIBSR Stanford University ، CA) بعائد استثمار 6 مم ، ثم تم رسم إشارة المتغير الذاتي الأولى المستخرجة في كل نقطة زمنية ولكل مجموعة. بالإضافة إلى ذلك ، لاستكشاف العلاقة بين المناطق التي تم فيها تحديد تفاعلات المجموعة × الوقت وأداء الذاكرة ، تم رسم المتغير الذاتي الأول المستخرج مقابل القيمة الأولية المرتبطة بكل مشارك.
لاستكشاف العلاقة بين DMN BOLD و hippocampal Glx ، تم استخراج المتغير الذاتي الأول للتباين "الصحيح للترميز" في DMN ROI باستخدام REX وقمنا بإجراء ارتباط ثنائي المتغير بين البيانات المستخرجة وتدابير الحصين Glx باستخدام SPSS. تم تحليل العلاقات بين Glx و BOLD بواسطة ارتباط بيرسون وتمت مقارنتها باستخدام تحويل Fisher من r إلى Z.
نتائج
السلوك والحصين الجلوتامات
كانت المجموعات متطابقة جيدًا من حيث العمر والجنس والحالة الاجتماعية والاقتصادية للوالدين والتدخين (الجدول 1).
استجاب كل من HC و SZ لمعظم تجارب التشفير دون اختلافات كبيرة بين المجموعات (F1 ، 32= 2. 778 ؛ ص=.105) ، الوقت (F1 ، 32= 0. 001 ؛ ص {{ 8}} .98) أو تفاعل مجموعة حسب الوقت (F1، 32= 0. 001 ؛ ص=98.). كان متوسط أوقات التفاعل أطول بالنسبة لـ SZ مقارنةً بـ HC (HC ، 1100 مللي ثانية ؛ SZ ، 1459 مللي ثانية ؛ F1 ، 29=11. 141 ؛ ص=.002) ولكن له تأثير كبير للوقت ، أو مجموعة تلو الأخرى التفاعل الزمني (خط الأساس HC ، 1103 مللي ثانية ، الأسبوع 6 ، 1096 مللي ثانية ؛ خط الأساس SZ ، 1530 مللي ثانية ، الأسبوع 6 ، 1389 مللي ثانية ؛ F1 ، 29=2. 294 ؛ ص=.141) لم يتم ملاحظته. كان هناك اختلاف كبير بين المجموعات في النسبة المئوية للكلمات المشفرة بشكل صحيح (HC، 85٪؛ SZ، 67٪؛ F1، 32=11. 141؛ p=.002) بدون أي فرق كبير في الوقت أو التفاعل الجماعي حسب الوقت (خط الأساس HC ، 86 بالمائة ، الأسبوع 6 ، 84 بالمائة ؛ خط الأساس SZ ، 66 بالمائة ، الأسبوع 6 ، 67 بالمائة ؛ F1 ، 32= 0. 306 ؛ ص {{ 55}} 584). كشفت مقارنة قيم d 'عبر المجموعة والوقت عن تأثيرات رئيسية مهمة للمجموعة (HC، 2.1؛ SZ، 1.44؛ F1، 32=7. 02؛ p=.012) ولكن ليس الوقت ، أو التفاعل الجماعي حسب الوقت (خط الأساس HC ، 2.14 ، الأسبوع 6 ، 2.07 ؛ خط الأساس SZ ، 1.43 ، الأسبوع 6 ، 1.44 ؛ F1 ، 32=0. 152 ؛ ص=.699 ).
لم تختلف مستويات Hippocampal Glx بشكل كبير بين المجموعات عند خط الأساس ، ولكن في الأسبوع 6 ، كانت مستويات HC hippocampal Glx أعلى بكثير من SZ (خط الأساس ، t=0. 425 ، nHC=15 ، nSZ {4} } ، الصفحة=0. 675 ؛ week6، z=2. 46، nHC=14، nSZ=16، p=0. 02).
نتائج الرنين المغناطيسي الوظيفي
مقارنات خط الأساس وتأثيرات الدواء
أظهرت تحليلات الدماغ الكامل أن كلاً من HC و SZ أظهران استجابة BOLD كبيرة على المستوى الثنائي في القشرة الجزرية والظهرية والبطنية قبل الجبهية والقشرة الجدارية والقشرة الصدغية العلوية والوسطى والمهاد والبوتامين أثناء التجارب الصحيحة. مقارنةً بـ HC ، كشفت SZ غير المعالجة عن انخفاض استجابة BOLD في الجزيرة اليمنى ، والحصين ، والقشرة الأمامية السفلية ، والقشرة الزمنية (الجدول 2 ، الشكل 1 ، اللوحة العلوية). باستخدام قناع DMN ، استجابات BOLD أكبر (الشكل 1 ، اللوحة السفلية) في الطليعة (إحداثيات MNI على مستوى voxel الذروة: x=0 ، y=−63 ، z=27 ، z=3. 07) والحزامية الخلفية (ذروة إحداثيات MNI على مستوى فوكسل x=−3، y=−51 z=24، z=2. 89) في SZ مقارنة بـ HC.
أظهر التحليل العاملي الكامل تفاعلًا كبيرًا بين المجموعة والوقت في نصف الكرة الأيسر في القشرة الصدغية العلوية والوسطى ، تلفيف هيشل والجزيرة. في نصف الكرة الأيمن ، في التلفيف المجاور للحصين ، الحصين ، اللوزة ، والقشرة الصدغية الوسطى (الجدول 3 ، الشكل 2). في تلك المناطق ، كشفت التناقضات اللاحقة عن انخفاض استجابة BOLD عند خط الأساس ، وزيادة لاحقة في الأسبوع 6 في SZ (الشكل 3 أ).
لفحص ما إذا كانت هذه الأنماط قد أثرت على الأداء ، استكشفنا العلاقة بين المناطق التي تم فيها تحديد تفاعلات كبيرة بين المجموعة والوقت وأداء الذاكرة. في HC ، ولكن ليس في SZ ، تم ربط المزيد من التنشيط في هذه المناطق بتحسين الأداء. كان تحليل الارتباط بين التنشيط في هذه المناطق و d 'مختلفًا بشكل كبير بين HC و SZ في الأساس ولكن ليس في الأسبوع 6 في اللوزة (خط الأساس ، z=1. 75 ، nHC=17 ، nSZ {{ 4}} ، ص=0. 0 4 ؛ الأسبوع 6 ، ض=−1.36 ، nHC=17 ، nSZ=17 ، ص = 0. 1) ، وعلى مستوى الاتجاه ، في التلفيف المجاور للحصين (baseline، z=1. 54، nHC=17، nSZ=17، p =0. 06؛ week 6، z=−0.43، nHC=17، nSZ=17، p =0. 33؛ الشكل 3 ب).
العلاقة بين الغلوتامات والإشارة الجريئة
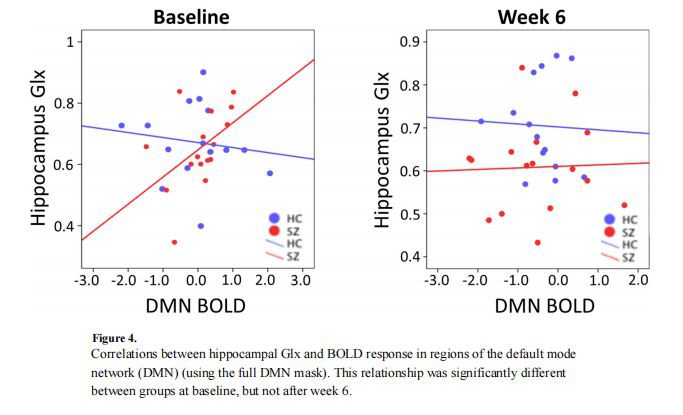
لاستكشاف العلاقة بين استجابة Hippocampal Glx و DMN BOLD ، أجرينا تحليل الارتباط بين هذه المتغيرات. في الأساس ، في SZ ولكن ليس في HC ، كان هناك ارتباط كبير بين استجابة الحصين Glx و BOLD المقاسة في منطقة DMN الخلفية حيث أظهرت SZ تنشيطًا متزايدًا (ص {0}} .49 ، ن { {2}} ، ص=0. 03). كانت العلاقة بين إشارة BOLD في مناطق DMN (باستخدام قناع DMN الكامل) و hippocampal Glx مختلفة بشكل كبير بين المجموعات (z=−1.62، nHC=15، nSZ=16 ، ص=0. 05) في الأساس (الشكل 4). وهكذا في هذه المناطق ، ارتبطت مستويات الغلوتامات المرتفعة بزيادة تنشيط DMN في SZ. في الأسبوع السادس ، لم يكن الارتباط بين مستويات Glx الحصين وشبكة الوضع الافتراضي كبيرًا ولم يكن مختلفًا بشكل كبير عن HC (z=−0.19، nHC=14، nSZ=16، p { {19}} .42) (الشكل 4).
مناقشة
على حد علمنا ، هذه هي الدراسة الأولى التي تستخدم تصميمًا طوليًا جنبًا إلى جنب مع مجموعة تحكم لتقييم استجابة BOLD أثناء تشفير الذاكرة وعلاقاتها مع الغلوتامات الحصين في مرضى الفصام قبل (بدون علاج) وبعد دورة تدريبية مدتها 6- أسبوع من العلاج مع ريسبيريدون. النتائج التي توصلنا إليها هي 1) في المرضى غير المعالجين ، وجود استجابة BOLD منخفضة في عدة مناطق ، بما في ذلك في قرن آمون ، واستجابة BOLD أكبر في مناطق DMN أثناء تشفير الذاكرة الصحيح ؛ 2) مجموعة استجابة BOLD كبيرة حسب التفاعل الزمني في القشرة الزمنية ، على المستوى الثنائي ، بما في ذلك في الحُصين الأيمن ؛ ولكن ليس في مناطق شبكة DMN ؛ 3) تعديل غير طبيعي للحصين عند خط الأساس الذي يبدو أنه طبيعي في الأسبوع 6 ؛ بالإضافة إلى ذلك ، هناك فرق كبير في العلاقة بين الحُصين BOLD والأداء عند خط الأساس ، ولكن ليس في الأسبوع 6. 3) لم يكن Hippocampal Glx مختلفًا بشكل كبير بين المجموعات عند خط الأساس ، ولكن في الأسبوع 6 ، كان Hippocampal Glx أقل بشكل ملحوظ في SZ مقارنة إلى HC ؛ 4) في الأساس ، توقعت Glx الحصين الأعلى تنشيطًا أكبر (أو تعطيل أقل) لاستجابة BOLD في مناطق DMN في SZ ، ولكن ليس في HC ؛ لم يكن هناك اختلاف جماعي في هذه العلاقة في الأسبوع 6.
الأنماط غير الطبية وتأثير الأدوية على BOLD
تم التحقيق في أداء الحصين في SZ باستخدام تقنيات التصوير المختلفة ، مثل PET و SPECT ووسم الدوران الشرياني و fMRI. تم الإبلاغ باستمرار عن شذوذ في تدفق الدم الدماغي الإقليمي (57-59) ، والحجم (60-63) ، وإشارة BOLD (64 ، 65). بالنظر إلى أن غالبية الدراسات شملت المرضى المعالجين ، كان من المهم تقييم الموضوعات غير المعالجة. فيما يلي مجموعة من المرضى غير المعالجين ، نلاحظ نقص تنشيط الحُصين أثناء تشفير الذاكرة الصحيح والعلاقة بين الحُصين BOLD والأداء الذي كان مختلفًا بشكل كبير عن الضوابط الصحية. تتوافق هذه النتائج مع غالبية الدراسات التي أبلغت عن انخفاض تجنيد الحُصين أثناء أداء الذاكرة في الفصام (65-67) ، بما في ذلك ذهان الحلقة الأولى (68). تم تحديد هذا الخلل الوظيفي أيضًا في الأشقاء الأصحاء (23 ، 24) ، مما يشير إلى أنه سمة وراثية ومرشح جيد لنمط ظاهري متوسط. تتوافق نتائجنا في HC أيضًا مع دراسات أخرى تُظهر أن تنشيط الحُصين والباراهيبوكامبوس أثناء التشفير ينبئ بنجاح الاسترجاع اللاحق (18 ، 19). في مجموعة من المرضى غير المعالجين الذين يتداخلون مع المجموعة الحالية ، أبلغنا عن وجود خلل وظيفي كبير بين الحصين والمناطق القشرية الأخرى أثناء حالة الراحة (69) ، بالإضافة إلى اتصال فعال غير طبيعي ، تم قياسه باستخدام طرق سببية جرانجر ، بين الحصين الثنائي والجبهي. مناطق أثناء مهمة استرجاع الذاكرة (4).
تم الإبلاغ أيضًا عن استجابات BOLD غير طبيعية في المناطق الأمامية والزمنية الأخرى في SZ مقارنة بـ HC (64 ، 65). في الأساس ، لوحظ استجابة أكبر لـ DMN BOLD في SZ مقارنةً بـ HC في القشرة الحزامية الخلفية والقشرة الحزامية. تتوافق نتائجنا مع النتائج السابقة للتنشيط المفرط لـ DMN في SZ عبر مجموعة متنوعة من المهام المعرفية (70-73).
حددنا مجموعة استجابة BOLD كبيرة من خلال التفاعل الزمني في منطقة تشمل الحُصين ، والحصين ، واللوزة. في تلك المناطق ، تكشف التناقضات اللاحقة عن انخفاض استجابة BOLD عند خط الأساس مع زيادة لاحقة في الأسبوع 6 ، مما يشير إلى نمط طبيعي مع العلاج. بالإضافة إلى ذلك ، مما يدل على وجود تأثير دوائي في هذه المنطقة ، لم تعد العلاقة بين استجابة BOLD والأداء مختلفة بشكل كبير عن تلك الخاصة بعناصر التحكم الصحية ، كما كانت في الأساس. تتوافق هذه النتائج مع نتائج دراسة PET سابقة حيث أظهرنا تعديلاً هامًا في الحصين rCBF عن طريق العلاج المضاد للذهان أثناء حالة الراحة وأداء المهام (58). بالإضافة إلى ذلك ، بعد أسبوع واحد من العلاج بمضادات الذهان ، أبلغنا عن تطبيع الاتصال الفعال غير الطبيعي بين منطقة الحصين ومناطق الفص الجبهي التي لوحظت عندما كان المرضى بدون علاج (4).
على الرغم من ملاحظة تعديل استجابة BOLD في قرن آمون ، لم نلاحظ تحسنًا كبيرًا في درجات الذاكرة بمرور الوقت لدى المرضى. أبلغ آخرون عن تحسن في كل من استجابة BOLD والإدراك باستخدام الأدوية المضادة للذهان. خلال مهمة التحكم الإدراكي ، أظهر المرضى المعالجون تنشيطًا أعلى لقشرة الفص الجبهي الظهراني بالإضافة إلى أداء سلوكي أفضل مقارنة بالمرضى غير المعالجين (74). على الرغم من أن الوقت حسب التفاعل الجماعي في دراستنا لم يشر إلى تأثير الدواء في مناطق شبكة DMN ، في دراسة طولية ، تم العثور على 8 أسابيع من العلاج المضاد للذهان لتحسين الأداء السلوكي وتعديل الاتصال الوظيفي لـ DMN في SZ خلال مهمة الذاكرة العاملة (75). سيكون من المهم تحديد ما إذا كانت التغييرات التي لوحظت في هذه الدراسة مرتبطة بتحسين عمليات الذاكرة ، لأنها يمكن أن توفر مؤشرات حيوية يحتمل أن تؤدي إلى تحديد عوامل جديدة لعلاج ضعف الذاكرة في مرض انفصام الشخصية.
كيف يمكن للأدوية المضادة للذهان تحسين وظيفة الحُصين؟ تم العثور على الأدوية المضادة للذهان اللانمطية لزيادة مستويات البروتينات المشبكية وتعزيز النمو التغصني (76). أحد هذه البروتينات ، عامل التغذية العصبية المشتق من الدماغ (BDNF) والذي يتم تخزينه وإطلاقه بواسطة الخلايا العصبية الجلوتاماتيكية ، هو منظم مهم للانتقال التشابكي. BDNF ضروري أيضًا لللدونة المشبكية ويساعد على الحماية من موت الخلايا المبرمج (77 ، 78). يوضح مزيد من الأدلة أن BDNF يرتبط بزيادة مستويات كثافة العمود الفقري (79). تحليل تلوي كبير شمل أكثر من 7000 موضوع بواسطة فرنانديز وآخرون. يوضح أن SZ يرتبط بمستويات منخفضة من BDNF وأن هذه المستويات تزداد مع العلاج بمضادات الذهان (80). هناك أسبقية أن مضادات الذهان غير التقليدية تساعد على وجه الخصوص في عكس أو على الأقل التخفيف من موت الخلايا المبرمج التغصني للطبقات الخارجية من القشرة (81).
الجلوتامات
في الأساس ، لم يكن هناك فرق كبير في مجموعة مستويات Glx. لقد أظهرنا سابقًا مستويات مرتفعة من الحصين Glx في مجموعة من 27 مريضًا غير خاضعين للعلاج مقارنة بمجموعة متطابقة من الضوابط الصحية (12). وبالتالي من الممكن أن تكون دراستنا ضعيفة لإظهار اختلاف المجموعة. بعد 6 أسابيع من العلاج ، لاحظنا انخفاضًا ملحوظًا في الحصين Glx في المرضى المعالجين مقارنةً بـ HC ، ولكن ليس مقارنة بخط الأساس غير المعالج. هناك عدد محدود من الدراسات الطولية التي تقيم تأثير العلاج قصير الأمد بمضادات الذهان على نواتج الجلوتامات. في المرضى المزمنين الذين تم غسلهم من الأدوية ، أبلغ Szulc عن انخفاض في الفص الصدغي Glx بعد أربعة أسابيع من العلاج بمجموعة متنوعة من الأدوية المضادة للذهان (43). في مرضى الذهان من النوبة الأولى الذين يعانون من السذاجة / الحد الأدنى من العلاج ، أبلغ Egerton عن انخفاض في الغلوتامات القشرة الحزامية الأمامية بعد أربعة أسابيع من العلاج باستخدام الأميسولبرايد (41). في حالات ذهان الحلقة الأولى الساذجة من الأدوية مقارنةً بالضوابط الصحية ، لاحظ دي لا فوينتي ساندوفال وجود غلوتامات خطي قاعدي أعلى وانخفاض كبير في الغلوتامات المخطط بعد أربعة أسابيع من العلاج باستخدام ريسبيريدون (42). وبالتالي هناك مؤشرات قوية على أن مستويات الغلوتامات يتم تعديلها بواسطة الأدوية المضادة للذهان. نحن نقر بأن حجم العينة كان محدودًا وهناك حاجة لمعالجة هذه الأسئلة بحجم عينة أكبر.
إشارة الغلوتامات / جريئة
في الأساس ، توقعت Glx الأعلى تعطيلًا أقل لاستجابة BOLD في مناطق DMN في SZ ، ولكن ليس في HC ؛ هذه العلاقة لم تكن موجودة في الأسبوع 6. في الضوابط الصحية ، Hu et al. أبلغ عن وجود علاقة إيجابية بين تركيز الغلوتامات العالي في DMN الخلفي وتقليل تعطيل DMN أثناء مهمة الذاكرة العاملة (31). أيضًا في الضوابط الصحية ، وجد Kapogiannis علاقة بين الغلوتامات DMN الخلفي (القشرة الخلفية الخلفية) والاتصال الوظيفي الجوهري لـ DMN (32). وجدنا هنا ارتباطًا بين استجابة الحصين Glx و BOLD في منطقة DMN ، وهي منطقة خارج المنطقة التي يتم قياس Glx منها. في حين أن التركيزات الكيميائية العصبية المحلية لا بد أن تؤثر على النشاط العصبي المحلي ، يمكن القول أيضًا أنها من المحتمل أن تساهم في نشاط مناطق الإسقاطات البعيدة ؛ من المحتمل أن يتضمن هذا انتقالًا متشابكًا معقدًا. توجد الآن العديد من الدراسات التي توضح الارتباطات بين الغلوتامات وإشارة BOLD في المناطق البعيدة عن حيث تم قياس الغلوتامات (33 ، 47 ، 82-84).
نظرًا لوجود مستويات أعلى من الغلوتامات باستمرار في الأدوية الساذجة أو غير المعالجة SZ (10-12) ، يمكن للمرء أن يتكهن بأن المستويات الأعلى من Glx في المرضى غير المعالجين تمثل حالة مرضية تغير النسبة المحلية للإثارة على التثبيط وضبط الإسقاطات العصبية مع تأثير كبير على إشارة BOLD في مناطق العرض. بشكل مثير للاهتمام ، على غرار الدراسات السابقة (82 ، 85) ، لوحظ الارتباط غير الطبيعي بين استجابة BOLD و Glx في SZ في DMN الخلفي. ارتبطت DMN اللاحق باستمرار بالتذكر الناجح (Vincent et al. ، 2006) ؛ بالإضافة إلى ذلك ، فهي منطقة مركزية رئيسية مترابطة بشكل مكثف مع مناطق محور أخرى ، وتشكل معًا ناديًا غنيًا (86). في الأسبوع السادس ، في مواجهة انخفاض مستويات Glx في SZ ، لم يعد هذا الارتباط مهمًا بعد الآن.
الاستنتاجات
ضعف الإدراك في مرض انفصام الشخصية ، وحتى يومنا هذا لا يوجد علاج دوائي لعلاجه. من الضروري توصيف الأمراض الكامنة الكامنة وراء معالجة الذاكرة في المرض لتطوير علاج جديد بشكل فعال. سمح لنا استخدام طريقتين لتصوير الدماغ بالتحقيق في الآليات المفترضة المختلفة المتضمنة في اختلال وظيفي في ترميز الذاكرة في مرض انفصام الشخصية. أكدنا أن علم أمراض الحصين أثناء تشفير الذاكرة ينبع من انخفاض تجنيد الحصين والتعطيل الخاطئ لشبكة DMN وأن تجنيد الحصين أثناء تشفير الذاكرة يتم تعديله عن طريق العلاج المضاد للذهان مع التطبيع اللاحق للعلاقة بين BOLD وأداء المهمة. أخيرًا ، أظهرنا أن ارتفاع Glx في المرضى غير المعالجين يتنبأ بإلغاء تنشيط أقل لـ DMN ؛ تشير هذه النتائج التي تحتاج إلى تكرارها مع مجموعات أكبر إلى آلية يتم من خلالها تحقيق التعطيل الخاطئ لشبكة DMN ، وهي السمة المميزة للنتائج المرضية في SZ.
المرجعي
1. Saykin AJ و Gur RC و Gur RE و Mozley PD و Mozley LH و Resnick SM et al. الوظيفة العصبية النفسية في مرض انفصام الشخصية. ضعف انتقائي في الذاكرة والتعلم. قوس جنرال للطب النفسي. 1991 ؛ 48 (7): 618-24. [PubMed: 2069492]
2. Kopald BE، Mirra KM، Egan MF، Weinberger DR، Goldberg TE. حجم تأثير الأداء التنفيذي ومعدل الذكاء على الذاكرة العرضية في الفصام. بيول للطب النفسي. 2012 ؛ 71 (6): 545-51. [PubMed: 22265665]
3. Sui J، Yu Q، He H، Pearlson GD، Calhoun VD. مراجعة انتقائية لطرق الاندماج متعدد الوسائط في مرض انفصام الشخصية. همهمة عصبية أمامية. 2012 ؛ 6:27. [PubMed: 22375114]
4. Hutcheson NL ، Sreenivasan KR ، Deshpande G ، Reid MA ، Hadley J ، White DM ، وآخرون. الاتصال الفعال أثناء استرجاع الذاكرة العرضية في مرضى الفصام قبل وبعد تناول الأدوية المضادة للذهان. همهمة الدماغ خريطة. 2015 ؛ 36 (4): 1442–57. [PubMed: 25504918]
5. Ragland JD ، Gur RC ، Valdez J ، Turetsky BI ، Elliott M ، Kohler C ، et al. التصوير بالرنين المغناطيسي الوظيفي المرتبط بالحدث للنشاط الجبهي الصدغي أثناء ترميز الكلمات والتعرف في مرض انفصام الشخصية. أنا ي الطب النفسي. 2004 ؛ 161 (6): 1004-15. [PubMed: 15169688]
6. Petroff OA. GABA والغلوتامات في الدماغ البشري. الأعصاب. 2002 ؛ 8 (6): 562-73. [PubMed: 12467378]
7. Magistretti PJ ، Pellerin L. الآليات الخلوية لاستقلاب طاقة الدماغ. الصلة بالتصوير الوظيفي للدماغ والاضطرابات التنكسية العصبية. آن نيويورك أكاد علوم. 1996 ؛ 777: 380-7. [PubMed: 8624117]
8. موفيت جونيور ، روس ب ، أرون بي ، مادهافاراو سي إن ، نامبوديري آم. N-Acetylaspartate في الجهاز العصبي المركزي: من التشخيص العصبي إلى علم الأعصاب. بروغ نيوروبيول. 2007 ؛ 81 (2): 89-131. [PubMed: 17275978]
9. روبينز تي دبليو ، ميرفي إير. علم العقاقير السلوكي: 40 عامًا زائدًا من التقدم ، مع التركيز على مستقبلات الجلوتامات والإدراك. اتجاهات علوم فارماكول. 2006 ؛ 27 (3): 141-8. [PubMed: 16490260]
10. de la Fuente-Sandoval C و Leon-Ortiz P و Favila R و Stephano S و Mamo D و Ramirez-Bermudez J وآخرون. مستويات أعلى من الغلوتامات في المخطط الترابطي للأشخاص الذين يعانون من الأعراض البادرية لمرض انفصام الشخصية والمرضى الذين يعانون من ذهان الحلقة الأولى. علم الادوية النفسية والعصبية. 2011 ؛ 36 (9): 1781–91. [PubMed: 21508933]
11. Kegeles LS ، Mao X ، Stanford AD ، Girgis R ، Ojeil N ، Xu X ، et al. تم قياس ارتفاع مستويات حمض جاما-أمينوبوتيريك والقشرة الجبهية المرتفعة في الفصام في الجسم الحي باستخدام التحليل الطيفي بالرنين المغناطيسي بالبروتون. قوس جنرال للطب النفسي. 2012 ؛ 69 (5): 449-59. [في النشر: 22213769]
12. Kraguljac NV، White DM، Reid MA، Lahti AC. زيادة الغلوتامات في الحصين والعجز الحجمي في المرضى غير المعالجين بالفصام. جاما للطب النفسي. 2013 ؛ 70 (12): 1294-302. [PubMed: 24108440]
13. كايرو تا ، وودوارد تى إس ، نجان إت. انخفاض كفاءة التشفير في مرض انفصام الشخصية. بيول للطب النفسي. 2006 ؛ 59 (8): 740-6. [PubMed: 16229823]
14. Cirillo MA ، Seidman LJ. ضعف الذاكرة التصريحية اللفظية في مرض انفصام الشخصية: من التقييم السريري إلى علم الوراثة وآليات الدماغ. نيوروبسيكول ريف .2003 ؛ 13 (2): 43-77. [في النشر: 12887039]
15. بريستون إيه آر ، إيشنباوم هـ. تفاعل الحصين وقشرة الفص الجبهي في الذاكرة. كور بيول. 2013 ؛ 23 (17): R764-73. [PubMed: 24028960]
16. بريستون أر ، شوهامي د ، تاممينجا كاليفورنيا ، واجنر إيه دي. وظيفة الحصين والذاكرة التقريرية وانفصام الشخصية: اعتبارات تشريحية ووظيفية للتصوير العصبي. مندوب نيوروسسي بالكور .2005 ؛ 5 (4): 249-56. [PubMed: 15987607]
17. شهمي د ، فاغنر AD. دمج الذكريات في الدماغ البشري: ترميز الحُصين - الدماغ المتوسط للأحداث المتداخلة. عصبون. 2008 ؛ 60 (2): 378-89. [PubMed: 18957228]
18. Brewer JB، Zhao Z، Desmond JE، Glover GH، Gabrieli JD. صنع الذكريات: نشاط الدماغ الذي يتنبأ بمدى تذكر التجربة البصرية. علوم. 1998 ؛ 281 (5380): 1185-117. [PubMed: 9712581]
19. جاكسون يا ثالث ، شاكتر DL. يدعم نشاط الترميز في الفص الصدغي الإنسي الأمامي التعرف الترابطي اللاحق. التصوير العصبي. 2004 ؛ 21 (1): 456-62. [في النشر: 14741683]
20. Jessen F ، Scheef L ، Germeshausen L ، Two Y ، Kockler M ، Kuhn KU ، et al. انخفاض تنشيط الحصين أثناء التشفير والتعرف على الكلمات في مرضى الفصام. أنا ي الطب النفسي. 2003 ؛ 160 (7): 1305-12. [في النشر: 12832246]
21. أكيم إيه إم ، برتراند إم سي ، ساتون إتش ، مونتويا إيه ، تشيكوسكا واي ، مالا إيه كيه ، وآخرون. تعديل انتقائي غير طبيعي لنشاط الحصين أثناء تكوين الذاكرة في ذهان الحلقة الأولى. قوس جنرال للطب النفسي. 2007 ؛ 64 (9): 999-1014. [في النشر: 17768265]
22. Goldberg TE ، Torrey EF ، Gold JM ، Bigelow LB ، Ragland RD ، Taylor E ، وآخرون. الخطر الوراثي للضعف العصبي النفسي في مرض انفصام الشخصية: دراسة التوائم أحادية الزيجوت المتنافرة والمتوافقة مع الاضطراب. Schizophr Res.1995 ؛ 17 (1): 77-84 [PubMed: 8541253]
23. Pirnia T ، Woods RP ، Hamilton LS ، Lyden H ، Joshi SH ، Asarnow RF ، et al. ضعف الحصين أثناء ترميز الذاكرة التقريرية في مرض انفصام الشخصية وآثار المسؤولية الوراثية. Schizophr Res.2015؛ 161 (2-3): 357-66. [PubMed: 25497222]
24. Rasetti R، Mattay VS، White MG، Sambataro F، Podell JE، Zoltick B، et al. تغيير وظيفة الحصين المجاورة للحصين أثناء تشفير التحفيز: مؤشر محتمل للمسؤولية الوراثية للفصام. JAMA Psychiatry.2014 ؛ 71 (3): 236-47. [PubMed: 24382711]
25.Kraguljac NV، Srivastava A، Lahti AC. عجز الذاكرة في مرض انفصام الشخصية: مراجعة انتقائية لدراسات التصوير بالرنين المغناطيسي الوظيفي (FMRI). Behay Sci (بازل). 2013: 3 (3): 330-47. [PubMed: 25379242]
26- Anticevic A و Repovs G و Shulman GL و Barch DM. عندما يكون القليل أكثر: إلغاء تنشيط TPJ والشبكة الافتراضية أثناء التشفير يتنبأ بأداء الذاكرة العاملة. التصوير العصبي. 2010 ؛ 49 (3): 2638-48. [PubMed: 19913622]
27. Raichle ME. شبكة الوضع الافتراضي للدماغ. Annu Rev Neurosci.2015؛ 38: 433-47. [PubMed: 25938726]
28. Anticevic A، Repovs G، Barch DM. ترميز الذاكرة العاملة ونقص الصيانة في مرض انفصام الشخصية: دليل عصبي على تشوهات التنشيط والتعطيل. شيزوفر بول 2013 ؛ 39 (1): 168-78. [في النشر: 21914644]
29. Whitfield-Gabrieli S. Thermenos HW. ميلانوفيتش إس تسوانغ إم تي. فاروني إس في. مكارلي RW وآخرون. فرط النشاط والاتصال المفرط للشبكة الافتراضية في مرض انفصام الشخصية وأقارب الدرجة الأولى للأشخاص المصابين بالفصام. Proc Natl Acad Sci US A.2009؛ 106 (4): 1279-84. [PubMed: 19164577]
30. Shulman RG ، Rothman DL ، Behar KL ، Hyder F. الأساس النشط لنشاط الدماغ: الآثار المترتبة على التصوير العصبي. مؤشرات Neurosci.2004 ، 27 (8): 489-95. [في النشر: 15271497]
31. Hu Y و Chen X و Gu H و Yang Y. تتنبأ تركيزات الغلوتامات في الحالة المستقرة و GABA بإلغاء التنشيط الناجم عن المهام في شبكة الوضع الافتراضي. J Neurosci.2013 ، 33 (47): 18566-73. [PubMed: 24259578]
32. Kapogiannis D، Reiter DA، Wiltte AA، Mattson MP. يتنبأ غلوتامات القشرة الخلفية الخلفية و GABA باتصال وظيفي جوهري لشبكة الوضع الافتراضي. Neuroimage.2013: 64: 112-9. [PubMed: 23000786]
33- Falkenberg LE و Westerhausen R و Craven AR و Johnsen E و Kroken RA.EM LB وآخرون تأثير مستويات الغلوتامات على الاستجابة العصبية والقدرات المعرفية في مرض انفصام الشخصية. نيورويماج كلين. 2014 ؛ 4: 576-84. [PubMed: 24749064]
34. Overbeek G العلاقة بين الغلوتامات وتأثير BOLD Stroop في الفصام من الحلقة الأولى. مخطوطة مقدمة 2018.
35. لاهتي إيه سي ، ويلر إم إتش هولكومب إتش إتش ، تاممينجا سي إيه ، كروبسي ك.ل.تعديل الدوائر الحوفية يتنبأ باستجابة العلاج للأدوية المضادة للذهان. دراسة تصويرية وظيفية لمرض انفصام الشخصية. علم الأدوية النفسية والعصبية 2009 ؛ 34 (13): 2675-90. [PubMed: 19675535]
36. Kraguljac NV، White DM، Hadley JA، Visscher K، Knight D، ver Hoef L، et al. شذوذ في الشبكات الوظيفية واسعة النطاق في المرضى غير المعالجين بالفصام وتأثيرات ريسبيريدون. Neuroimage Clin.2016 ؛ 10: 146-58. [في النشر: 26793436]
. بروك Natl Acad Sci US A. 1999 ؛ 96 (23): 13432-7. [PubMed: 10557338]
38. Minzenberg MJ. كارتر سي إس. تطوير علاجات لضعف الإدراك في مرض انفصام الشخصية. Trends Cogn Sci.2012 ؛ 16 (1): 35-42. [PubMed: 22178120]
39، Keefe RS.Bilder RM، Davis SM، Harvey PD، Palmer BW، Gold M، et al. التأثيرات العصبية المعرفية للأدوية المضادة للذهان في مرضى الفصام المزمن في تجربة CATIE. {4}}. [PubMed: 17548746]
40. Davidson M ، Galderisi S ، Weiser M ، Werbeloff N ، Fleischhacker WW ، Keefe RS ، et al. التأثيرات المعرفية للأدوية المضادة للذهان في حالة الفصام والاضطراب الفصامي من الحلقة الأولى: أ
