يثبط مستحضر الألبومين المصل البشري الجديد S-sulfhydrated تخليق الميلانين
Jan 30, 2022
اتصال:jaslyn.ji@wecistanche.com
مايومي إيكيداa,1يو إيشيماa,⁎,1، ريو كينوشيتاb، فيكتور تي جي تشوانغcنانامي تاساكاaنانا ماتسوa، هيروشي واتانابيb، تارو شيميزوa، تاتسوهيرو إيشيداa، ماساكي أوتاجيريd، تورو ماروياماb,⁎
نبذة مختصرة
تحفز منتجات الأشعة فوق البنفسجية (UV) مثل أنواع الأكسجين التفاعلية (ROS) وأكسيد النيتريك (NO) تخليق الميلانين. لقد ثبت أن أنواع الكبريت التفاعلية (RSS) لها تأثيرات ROS قوية و NO تأثيرات الكسح. ومع ذلك ، فإن عدم الاستقرار وانخفاض الاحتفاظ بـ RSS يحد من استخدامها كمثبطات لتخليق الميلانين. يعتبر الثيول الحر الموجود في Cys34 على ألبومين المصل البشري (HSA) مستقرًا للغاية ، وله احتفاظ طويل الأمد وله تفاعل عالي مع RSS. نُبلغ هنا عن تطوير نظام توصيل RSS قائم على HSA. مشتقات الكبريت الكبريتية المنبعثة من polysulfides الصوديوم (Na2Sn) تتفاعل بسهولة مع HSA. أظهر اختبار لتقدير التخلص من الكبريتيد من polysulfide أن جميع الكبريت تقريبًا المنطلق من Na2Sn المرتبط بـ HSA. تم العثور على HSA المعالج Na2Sn بكفاءة في تنظيف ROS و NO الناتج من الكواشف الكيميائية. وجد أيضًا أن HSA المعالج بـ Na2Sn يثبط تخليق الميلانين في خلايا سرطان الجلد B16 وكان هذا التثبيط مستقلاً عن عدد ذرات الكبريت المضافة. في خلايا سرطان الجلد B16 ، تثبط HSA المعالج بـ Na2Sn أيضًا مستويات ROS و NO الناجم عن الأشعة فوق البنفسجية. أخيرًا ، منع HSA المعالج بـ Na2Sn تخليق الميلانين من L-DOPA وتيروزيناز الفطر وقمع مدى تراكم أصباغ الميلانين. تشير هذه البيانات إلى أن HSA المعالج بـ Na2Sn يثبط نشاط التيروزيناز لتخليق الميلانين عبر مسارين ؛ عن طريق تثبيط إشارات ROS مباشرة وكسح NO. تشير هذه النتائج إلى أن HSA المعالج بـ Na2Sn لديه القدرة على أن يكون مرشحًا جذابًا وفعالًا للاستخدام كعامل تبييض للبشرة.

Cistanche هو عامل مبيض للجلد.
1 المقدمة
ينتج عن الإشعاع فوق البنفسجي (UV) أنواع الأكسجين التفاعلية (ROS) التي تتسبب في النهاية في موت الخلايا [1]. لحماية الجلد من أضرار الأشعة فوق البنفسجية ، يتم إنتاج الميلانين ، وهو صبغة داكنة اللون ، بواسطة الخلايا الصباغية [2]. في حين أن الميلانين ضروري لصحة الجلد ، إلا أن هناك طلبًا على مستحضرات تنظيف الميلانين. الكلف (الكلف) هي حالة يتطور فيها الجلد إلى مناطق متغيرة اللون ناتجة عن الإفراط في إنتاج الميلانين ، ويُنظر إليها أحيانًا على أنها استعارة للشيخوخة. بالإضافة إلى ذلك ، تعتبر مثبطات تخليق الميلانين من مستحضرات التجميل الشعبية لتفتيح البشرة ، خاصة في الدول الآسيوية [3].
يحفز Tyrosinase إنتاج الميلانين من التيروزين عبر DOPA و dopaquinone في الخلايا الصباغية [4]. يتم تنظيم نشاطها من خلال مجموعة متنوعة من العوامل مثل إشارات ERK1 / 2 و Akt [5]. ROS مثل
ينتج بيروكسيد الهيدروجين عن طريق الإشعاع فوق البنفسجي ، وينشط التيروزيناز ويعزز تخليق الميلانين في الخلايا الصباغية [2]. تسبب الأشعة فوق البنفسجية أيضًا إنتاج أكسيد النيتريك (NO) وتحفز نشاط التيروزيناز عبر cGMP [6] ، وهو مرسال ثان لـ NO.
من ناحية أخرى ، تم استخدام مركبات الثيول ذات التأثير المضاد للأكسدة على نطاق واسع كمكملات وعوامل حماية من الإشعاع وعوامل تجعيد [7]. تخضع المركبات المحتوية على ثيول للأكسدة الذاتية لتكوين حمض السلفونيك وحمض السلفونيك وحمض السلفونيك [8]. يقوم Thiol أيضًا بكسح NO عن طريق S-nitrosation [8]. بسبب هذه التأثيرات ، غالبًا ما تستخدم المركبات المحتوية على الثيول في علاج الكلف [7،9]. ومع ذلك ، فإن تأثير تبييض الجلد للثيول ضعيف للغاية ، وهناك حاجة إلى وجود عوامل تنظيف أكثر فعالية من نوع ROS و NO.
تم الإبلاغ مؤخرًا عن أن أنواع الكبريت التفاعلية (RSS) بما في ذلك بيرسلفيد السيستين لها تأثيرات أقوى من مضادات الأكسدة من الثيول. يحتوي RSS على مجموعة thiol التفاعلية [10] و pKa لمعظم RSS أقل بكثير من تلك الخاصة بالثيول [11]. لذلك ، يمكن أن تتفاعل RSS بشكل فعال مع كل من ROS و NO ويتوقع أن تقلل من مدى إنتاج الميلانين. تُستخدم عديد كبريتيدات الصوديوم (Na2Sn) ، وديليلتريسولفيد (DATS) وثنائي ميثيل تريسولفيد (DMTS) بشكل شائع كمانحين لـ RSS [12]. ومع ذلك ، فإن Na2Sn لديها احتباس منخفض في درجة الحموضة المحايدة ولها رائحة كريهة. بالإضافة إلى ذلك ، فإن DATS و DMTS ، اللذين ينتجانهما الثوم والبصل ، لهما رائحة أيضًا ، كما أن إمكاناتهما لمثل هذه العلاجات محدودة [13]. علاوة على ذلك ، فإن عمر النصف لـ Na2Sn قصير جدًا في المصل ، وبناءً على النماذج الموجودة في الجسم الحي ، هناك حاجة إلى حقن متعددة حتى تكون فعالة. وبالتالي ، فإن تطوير أنظمة توصيل RSS الجديدة أمر مرغوب فيه للغاية.
الزلال البشري (HSA) هو البروتين الأكثر وفرة في المصل ويستخدم على نطاق واسع كناقل للأدوية بسبب توافقه الحيوي وخصائصه الطويلة في الاحتفاظ بالبلازما [14 ، 15]. تحتوي HSA على ما مجموعه 35 من مخلفات Cys وواحدة منها ، Cys34 ، موجودة في شكل مجموعة ثيول حرة [16]. يكون Cys34 أحيانًا هدفًا لموقع ربط دواء ، بسبب مجموعة ثيول التفاعلية [17 ، 18]. على سبيل المثال ، في ظل وجود أكسيد النيتريك (NO) ، فإن مجموعة Cys34 thiol تكون نيتروسية. لقد حددنا سابقًا أن HSA (SNO-HSA) S-nitrosated HSA يسمح بالاحتفاظ بـ NO لفترات طويلة في المصل [19]. يحتوي SNO-HSA على وظائف بيولوجية مختلفة ، بما في ذلك تأثير وقائي للكبد ضد نقص التروية / ضخه [20] وتأثيرات تثبيط الورم [21].
وبالتالي ، افترضنا أنه يمكن استخدام HSA كناقل RSS (مثل SNO-HSA) عبر S-sulfhydration لـ Cys 34- SH. كمصدر للكبريت المتعدد ، فإن DATS و DMTS محدودة بسبب قوتها وتقلبها. وبالتالي ، تم استخدام Na2Sn المتاح تجاريًا (Na2S و Na2S2 و Na2S3 و Na2S4) في هذه الدراسة. أوغاساوارا وآخرون. تفاعل الألبومين المصل المرتبط بالكبريت المحضر مسبقًا مع كبريتيد الصوديوم (NaHS) عن طريق خلط بسيط من الكواشف [22]. تمت إضافة الكبريت من NaHS إلى Cys34 وحمى المستحضر الناتج تلف الكبد الناجم عن بيروكسيد الدهون. لقد اعتمدنا هذه الطريقة لتقسيم RSS-added-HSA باستخدام Na2Sn لتسليم RSS.
في هذا العمل ، أبلغنا عن إعداد HSA المعالج بـ Na2Sn واستخدامه كنظام توصيل جديد لـ RSS. تم تحليل الكبريت المضاف بواسطة مسبار كبريت الكبريت [23] وإزالة الكبريتيد من عديد الكبريتيد [24]. لتقييم تأثير HSA المعالج بـ Na2Sn على تبييض الجلد ، تمت دراسة تأثير HSA المعالج بـ Na2Sn على تخليق الميلانين باستخدام خط خلية سرطان الجلد B16.
2. المواد والأساليب
2.1. المواد
تم شراء ألبومين المصل البشري (HSA) من KAKETSUKEN (كوماموتو ، اليابان) وتم إزالة الدهن من جميع عينات HSA بمعالجة الفحم. تم شراء كبريتيد الصوديوم ورابع كبريتيد الصوديوم من مختبر DOJINDO (كوماموتو ، اليابان). تم تحضير مسبار كبريت السلفان 4 (SSP4) كما هو موصوف سابقًا [23]. تم شراء L-DOPA و glu-tathione و (DTNB) وحمض الأسكوربيك وكاشف Griess الساخر للصوديوم (sulfanilamide ، naphthylethylenediamine-HCl) من Nakarai Chemicals (كيوتو ، اليابان). تم شراء عمود إزالة الملوحة Sephadex G -25 (φ 1.6 × 2.5 سم) من GE Healthcare (كيوتو ، اليابان). تم الحصول على وسيط النسر المعدل Dulbecco (DMEM) و 2 ، 2- diphenyl -1- pi- crylhydrazyl (DPPH) من Wako Pure Chemical (أوساكا ، اليابان). تم شراء الفطر تيروزيناز من سيجما الدريش. كانت جميع المواد الكيميائية الأخرى من أفضل درجة متوفرة تجارياً ، وتم تحضير جميع المحاليل في الماء المقطر منزوع الأيونات.

استخراج cistanche
2.2. فحص بروتين BCA
تم قياس تركيزات البروتين باستخدام اختبار بروتين BCA. تم تحضين 10 ميكرولتر من العينات ومعايير الألبومين المصل البقري (BSA) في 100 ميكرولتر من المخزن المؤقت للتفاعل عند 25 درجة لمدة 30 دقيقة. بعد التفاعل ، تم استخدام قارئ الصفيحة الدقيقة لقياس الامتصاصية البالغة 540 نانومتر. تم استخدام BSA لبناء منحنى قياسي.
2.3 توليف Na2Sn المعالج- HSA
تم تحضين HSA (300 ميكرومتر) مع 1 ملي مولار من polysulfides الصوديوم (Na2Sn) في PBS (الرقم الهيدروجيني 7.4) لمدة ساعة عند 37 درجة. بعد التفاعل ، تمت إزالة عديد كبريتيدات الصوديوم الزائدة عن طريق الترشيح الهلامي باستخدام عمود Sephadex G -25.
2.4 تحديد معدل ارتباط الكبريت بطريقة التخلص من الكبريتيد من عديد الكبريتيد (EMSP)
تم تحضير EMSP كما هو موصوف سابقًا (3 × EMSP بإضافة 792 مجم من حمض L-ascorbic إلى 5 مل من 3 N من NaOH) [24]. تم تحضين العينات (7.5 ميكرومتر ، 133 ميكرولتر) مع 66.7 ميكرولتر من 3 × EMSP لمدة 3 ساعات عند 37 درجة. ثم تمت إضافة محلول أسيتات الزنك بنسبة 1 بالمائة (600 ميكرولتر) إلى محلول إعادة العمل ، متبوعًا بالدوامة على الفور. تم طرد العينات عند 8 ، 000 × جم لمدة 5 دقائق وغسلها بمحلول ملحي بالفوسفات (PBS) مرتين. بعد إزالة المواد الطافية ، تمت إضافة الماء المقطر منزوع الأيونات (200 ميكرولتر) إلى الرواسب. بعد إضافة 1 في المائة من أسيتات الزنك (300 ميكرولتر) ، و 50 ميكرولتر من 20 ملي مولار ، و N-dimethyl-p-phenylenedia- منجم و 20 ملي مولار FeCl3 في 7.2 N HCl ، تم تحضين المحلول لمدة 30 دقيقة عند 25 درجة. تم الطرد المركزي للعينات عند 8000 × جم لمدة دقيقة واحدة وتم نقلها إلى 96- من ألواح البئر وقياس OD عند 665 نانومتر. تم استخدام Na2S لبناء منحنى قياسي.
2.5 الكشف عن كبريت الكبريت باستخدام SSP4
تم تحضين كل عينة (20 ميكرومتر) بـ 5 ميكرومتر من SSP4 في 1 ملي مولار من Cetyltrimethylammonium Bromide / PBS (الرقم الهيدروجيني 7.4) لمدة 10 دقائق عند 25 درجة. بعد الحضانة ، تم قياس التألق بمقياس الطيف الضوئي (JASCO Corporation) مع الإثارة عند 457 نانومتر ، والانبعاث عند 490-535 نانومتر.
2.6. اختبارات DPPH الجذرية
تم خلط DPPH (250 ميكرومتر) في الإيثانول بنفس المقدار من المخزن المؤقت MES (50 ملي مولار ، الرقم الهيدروجيني 7.4). تمت إضافة HSA المعالج بـ Na2Sn (40 ميكرومتر) إلى محلول DPPH هذا ، والذي تم تحضينه بعد ذلك لمدة 30 دقيقة عند 25 درجة وتم قياس امتصاص جذور DPPH عند 540 نانومتر. تم تحويل معدلات الجذور الكسح باستخدام الصيغة التالية ؛
جذرية مكسوبة (نسبة مئوية)=(Abssample-Abspbs) / Abspbs × 100
2.7. تحليل NO و SNO
تم تحضين HSA المعالج بـ Na2Sn (5 0 ميكرومتر) مع مانح NO ، NOC7 (2 0 0 ميكرومتر) ، لمدة 30 دقيقة عند 25 درجة. بعد التفاعل ، تم قياس تركيز NO و SNO بواسطة مقايسة Griess مع تعديلات طفيفة [25]. تم تحضير محلول كاشف Griess بخلط 0.1٪ N -1- Naphtylethylene-Diamide dihydrochloride و 1٪ sulfanilamide في 2٪ حمض فوسفوريك. يتكون محلول التفاعل من 0.1 مولار كلوريد الصوديوم و 0.5 ملي مولار DTPA و 10 ملي مولار AcONa - AcOH (درجة الحموضة 5.5). تم تفاعل العينات (20 ميكرومتر) مع محلول كاشف Griess (60 ميكرولتر) في محلول التفاعل (110 ميكرولتر) مع 3 ملي مولار HgCl في 10 ملي مولار من خلات الصوديوم (درجة الحموضة 5.5). بعد فترة حضانة لمدة 15 دقيقة ، تم قياس امتصاص 540 نانومتر بواسطة قارئ صفيحة ميكروسكوبية. تم حساب نسبة NO / SNO المتبقية (النسبة المئوية) ومقارنتها بقيم PBS للعينات.
2.8. زراعة الخلايا
تم توفير خلايا سرطان الجلد B16 من قبل بنك موارد أبحاث السرطان الياباني (JCRB ، طوكيو ، اليابان) ، وتم زراعتها في DMEM الذي يحتوي على 10 بالمائة من مصل بقري جنيني ومحلول مضاد حيوي. نمت الخلايا مع الحفاظ عليها عند 37 درجة في الهواء المرطب المحتوي على 5 في المائة من ثاني أكسيد الكربون في الحاضنة (رقم الممر 10-20).
2.9 إنتاج الميلانين
تم زرع خلايا سرطان الجلد B16 في 24 طبقًا جيدًا بتركيز 2.5 × 1 0 4 خلايا / بئر وزُرعت تحت 5 بالمائة من ثاني أكسيد الكربون عند 37 درجة لمدة 24 ساعة. عولجت العينات باستخدام 0.4 ملي مولار من التيروزين و 10 ملي مولار NH4Cl في DMEM الذي يحتوي على 10 بالمائة من FBS ثم حضنت تحت 5 بالمائة من ثاني أكسيد الكربون عند 37 درجة لمدة 72 ساعة. بعد الحضانة ، تم غسل الخلايا مرتين باستخدام PBS وتم إذابتها في 1 N هيدروكسيد الصوديوم (200 ميكرولتر). بعد حضانة لمدة ساعتين على 60 درجة ، تم قياس الامتصاص (405 نانومتر) عن طريق قارئ لوحة ميكروية.

يمنع Cistanche إنتاج الميلانين.
2.10. الأشعة فوق البنفسجية
تم استخدام مصباح يدوي للأشعة فوق البنفسجية لتشعيع العينات على مسافة 5 سم من لوحة البئر. يوفر مصباح الأشعة فوق البنفسجية هذا كثافة من الأشعة فوق البنفسجية تبلغ 614 أو 743 ميكرو وات / سم 2 على التوالي مع إشعاع 254 نانومتر أو 365 نانومتر من مسافة 5 سم.
2.11. عالج نشاط الكسح لـ Na2S 4- HSA مقابل ROS داخل الخلايا ، لا ، RSS
تم قياس ROS و NO في خلايا سرطان الجلد B16 بواسطة كل من مجسات التألق CM-H2DCF-DA و DAF-FM-DA على التوالي. تم زرع خلايا سرطان الجلد B16 في 96- أطباق جيدة بتركيز 1 × 104 خلية / بئر وزرعت في 37 درجة ، 5 في المائة من ثاني أكسيد الكربون لمدة 24 ساعة. بعد الثقافة ، تمت إزالة الوسائط واستبدالها بـ CM-H2DCF-DA (5 ميكرومتر) أو DAF-FM-DA (10 ميكرومتر) في برنامج تلفزيوني. تم أخذ المجسات بواسطة الخلايا باحتضانها عند 37 درجة لمدة 30 دقيقة. بعد التفاعل ، تمت إزالة المواد الطافية ، وتم تخفيف العينات في برنامج تلفزيوني وقياس التألق على الفور. تم إشعاع الخلايا بواسطة مصباح UV لمدة 15 دقيقة. بعد التشعيع ، تم قياس شدة التألق (مثال. 485 نانومتر ، إم. 535 نانومتر) عن طريق قارئ لوحة دقيقة مضان.
2.12. نشاط الفطر التيروزينيز وتجمع الميلانين
تم تحضير محاليل Tyrosinase و L-DOPA في PBS (الرقم الهيدروجيني 7.4) مباشرة قبل الفحص. تم استخدام Tyrosinase ، المعزول من الفطر ، لفحص النشاط المثبط لـ HSA المعالج بـ Na2Sn. تم خلط جزء 20 ميكرولتر من تيروزيناز الفطر (537 وحدة / مل) و 100 ميكرولتر من HSA المعالج بـ Na2Sn (40 ميكرومتر) جيدًا مع PBS (60 ميكرولتر) في 96 طبقًا جيدًا و 20 ميكرولتر من L-DOPA (5 ملي مول) كان ثم أضاف. بعد فترة حضانة لمدة 30 دقيقة ، تم تحليل مستوى الميلانين المركب عن طريق قياس OD 490 نانومتر. لمعايرة تراكم الميلانين ، تم طرد الخليط عند 20 ، 000 جم ، 15 دقيقة لمدة 3 ساعات. يظهر السهم الأبيض المواد المجمعة. تم قياس الميلانين غير المتجمع في المادة الطافية عند OD من 490 نانومتر.
2.13. اختبارات السلامة
تم تحضير الكريم الموضعي المستخدم في هذه الدراسة عن طريق خلط الماء (30 مل) زيت الجوجوبا (15 مل) و 5 جرام من شمع الاستحلاب عند 60 درجة. بعد التبريد ، تم خلط HSA المعالجة بـ Na2S 4- (20 ميكرومتر) والمعلق الناتج جيدًا. تم إجراء اختبار تهيج الجلد باتباع إرشادات اختبار منظمة التعاون والتنمية في الميدان الاقتصادي رقم 439 باستخدام نموذج LabCyte Epi-Model (نموذج ثلاثي الأبعاد لجلد الإنسان).
2.14. تحليل احصائي
تم تقييم الأهمية الإحصائية للبيانات التي تم جمعها من خلال تحليل ANOVA متبوعًا بطريقة نيومان-كيلس لأكثر من وسيلتين. تم تقييم الفروق بين المجموعات عن طريق اختبار الطالب. تم اعتبار P <0. 05="" ذات="" دلالة="">
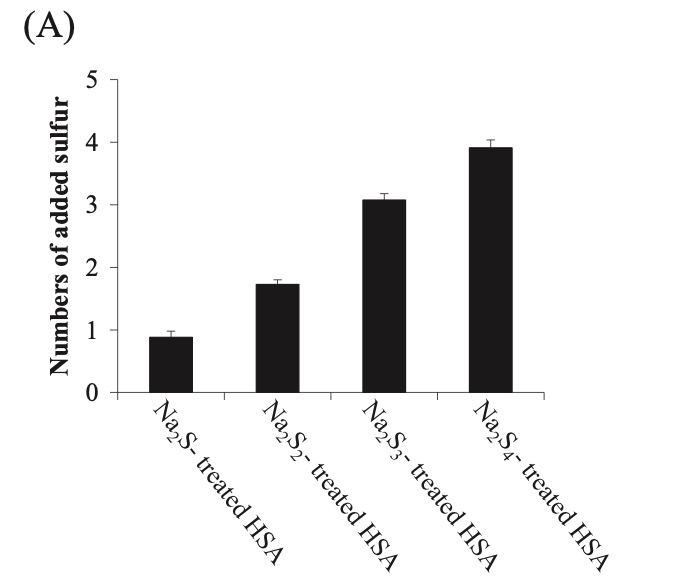

رسم بياني 1.يرتبط عديد الكبريت بـ HSA عن طريق الحضانة مع polysul الصوديومفايدي.
3. النتائج
3.1. تحضير حمض كبريتيد الصوديوم
تم تحضير HSA المعالج بـ Na2Sn من HSA الذي تم تحضينه باستخدام Na2Sn وتعريضه لترشيح الهلام بعد التفاعل. لتقييم كمية كبريت الكبريت في العينة ، تم استخدام طريقة EMSP ، وهي طريقة كمية جديدة قمنا بتطويرها سابقًا [24]. ومن ثم ، تم تحضير HSA المعالج Na2S 4- من HSA و Na2Sn بالسماح للعوامل بالتفاعل لمدة ساعة عند 37 درجة. تم السماح بكميات مختلفة من بولي كبريتيد الصوديوم للتفاعل مع HSA. بعد ذلك ، تم تحضين عينات HSA بمحلول EMSP ، الذي تم تحضيره في وقت الاستخدام ، لمدة 3 ساعات عند 37 درجة. بناءً على تحليلات EMSP ، زاد مستوى الكبريتيد S بشكل مستقل عن كمية الكبريت (الشكل 1 أ). من ناحية أخرى ، كما هو موضح في الشكل 1 ب ، عززت معالجة Na2S 3- أو Na2S 4- كثافة التألق SSP4 (مسبار مضان لكبريت السلفان) مقارنةً بـ Na2S- أو Na2S {{24 }} ، مما يشير إلى أن SSP4 ربما تفاعل مع polysulfide للبروتين بطريقة غير خطية (الشكل 1 ب).
3.2 مضادات الأكسدة ولا يوجد تأثير قمعي لـ HSA المعالج بـ Na2S
افترضنا أن HSA المعالج بـ Na2Sn سيثبط إنتاج الميلانين بسبب نشاطه المضاد للأكسدة. ومن ثم ، تم إجراء اختبار جذري DPPH لتحليل نشاط مضادات الأكسدة في المختبر. نتيجة لذلك ، كان HSA المعالج بـ Na2Sn يحتوي على تركيز أعلى بكثير من الكبريت المضاف (الشكل 2 أ). لتوضيح تأثير NO ، تم احتضان NOC7 (مانح NO) مع Na2S 4- معالج HSA عند 25 درجة. بعد فترة 30 دقيقة من الحضانة ، تم تحديد كمية تركيز NO المتبقية بواسطة مقايسة Griess. كما رأينا في الأشرطة المغلقة في الشكل 2 ب ، فإن حمض HSA المعالج Na2S 4- قد قام بتجميع NO أكثر بشكل ملحوظ مقارنة مع عنصر التحكم و HSA (الشكل 2 ب). من المعروف أن الزئبق الأولي (Hg) يقلل من SNO ويطلق NO 2-. عندما تمت إضافة Hg إلى محلول Na2S 4- معالج HSA ، تم إطلاق NO 2- ، مما يشير إلى أن HSA المعالج Na2S 4- قد تم تنظيفه عبر نيتروز S.

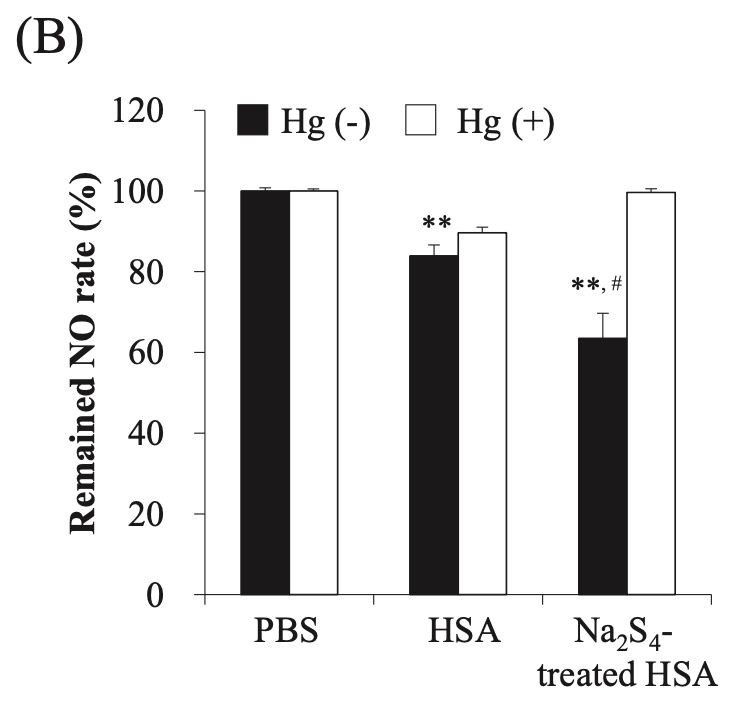
الصورة 2.الخصائص المضادة للأكسدة لـ Na2Sn-علاج هائل سعيد أنعم.
3.3 الميلانين يقمع تأثير HSA المعالج Na2Sn
تمت زراعة خلايا سرطان الجلد في الفئران B16 وتم تعزيز تخليق الميلانين عن طريق إضافة التيروزين إلى الوسائط. كما هو مبين في الشكل 3 ، فإن حمض HSA المعالج بـ Na2Sn يثبط تخليق الميلانين ويعتمد التثبيط على محتوى الكبريت. أظهرت الصور الخلوية لخلايا سرطان الجلد B16 بعد تطبيق HSA المعالج بـ Na2Sn أيضًا أن HSA المعالج بـ Na2Sn قلل من نسبة إنتاج الميلانين.الخلايا الإيجابية (الشكل 3).
3.4. التأثير المضاد للأكسدة لـ Na2S 4- يعالج HSA بإشعاع الأشعة فوق البنفسجية
لفحص ما إذا كان HSA المعالج بـ Na2Sn قد كبح تكوين ROS المستحث بالأشعة فوق البنفسجية أو NO ، تم إجراء اختبار الإجهاد التأكسدي باستخدام خلايا سرطان الجلد B16 كنماذج. تم قياس إنتاج ROS بواسطة Na2S 4- المعالج HSA في خلايا سرطان الجلد B16 عن طريق التشعيع بجهازي UV مختلفين لمدة 15 دقيقة بواسطة CMH 2- DCF-DA. تشير النتائج إلى أن HSA المعالج Na2S 4- تسبب في انخفاض كبير في مضان CMH 2- DCF-DA إلى PBS و HSA عن طريق التشعيع عند 254 نانومتر و 365 نانومتر (الشكل 4AB). على العكس من ذلك ، فإن HSA المعالج Na2S 4- يثبط أيضًا إنتاج أكسيد النيتروجين في خلايا سرطان الجلد B16 عن طريق التشعيع باستخدام 254 نانومتر من الأشعة فوق البنفسجية (الشكل 4CD). تشير هذه النتائج إلى أن HSA المعالج بـ Na2Sn يثبط تخليق الميلانين عن طريق تثبيط ROS و NO الناتج عن الإشعاع فوق البنفسجي.
3.5 قمع مباشر لتراكم التيروزيناز والميلانين بواسطة HSA المعالج بـ Na2Sn
من المعروف أن بعض العوامل التجارية المضادة للميلانين تثبط نشاط التيروزيناز بشكل مباشر. وهكذا ، قمنا باختبار ما إذا كان HSA المعالج Na2Sn قد غير نشاط التيروزيناز. أشارت النتائج إلى أن HSA المعالج Na2Sn يثبط التيروزيناز الفطر إلى حد أكبر من HSA غير المعالج (الشكل 5 أ). بعد أن يتولد الميلانين ، يتجمع بسهولة ويحث على تكوين النخاع [28]. لذلك ، تناولنا بعد ذلك مسألة ما إذا كان HSA المعالج بـ Na2Sn يمنع تراكم الميلانين. وبالتالي ، عندما تم تحضين التيروزيناز و L-DOPA معًا لمدة 3 ساعات ، أصبحت أصباغ الميلانين مجمعة ، لكن HSA المعالج بـ Na2Sn منع التجميع (الشكل 5 ب). من ناحية أخرى ، تم العثور على HSA أيضًا لمنع التجميع ، مما يشير إلى أن HSA نفسها يمكن أن تمنع ارتباط L-DOPA بالتيروزيناز.
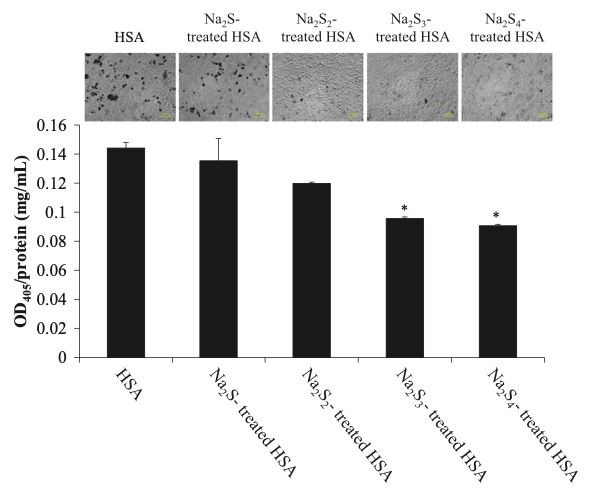
تين. 3.Eوما يليهاإلخ من نا2Sn-علاج HSA على تخليق الميلانين في خلايا سرطان الجلد B16.
3.6 اختبار سلامة HSA المعالج بـ Na2Sn باستخدام جلد بشري مثقف ثلاثي الأبعاد
تم إجراء اختبارات تهيج الجلد لـ HSA المعالج Na2S 4- باستخدام خلايا جلد بشرية مستنبتة ثلاثية الأبعاد وفقًا لإرشادات منظمة التعاون الاقتصادي والتنمية. نتيجة لذلك ، لم يتم تقليل عدد الخلايا الباقية بواسطة HSA المعالجة بـ Na2S 4- مع / بدون استخدام كريم موضعي (الشكل 6 أ). أظهر استخدام مجموعة اكتشاف السمية الخلوية LDH أيضًا أن خلايا الجلد لم تتضرر بسبب HSA المعالج بـ Na2S 4- (الشكل 6 ب). أشارت هذه البيانات إلى أن HSA المعالج بـ Na2Sn آمن جدًا للاستخدام ضد جلد الإنسان تحت التركيزات التي تم فحصها في هذه الدراسة.
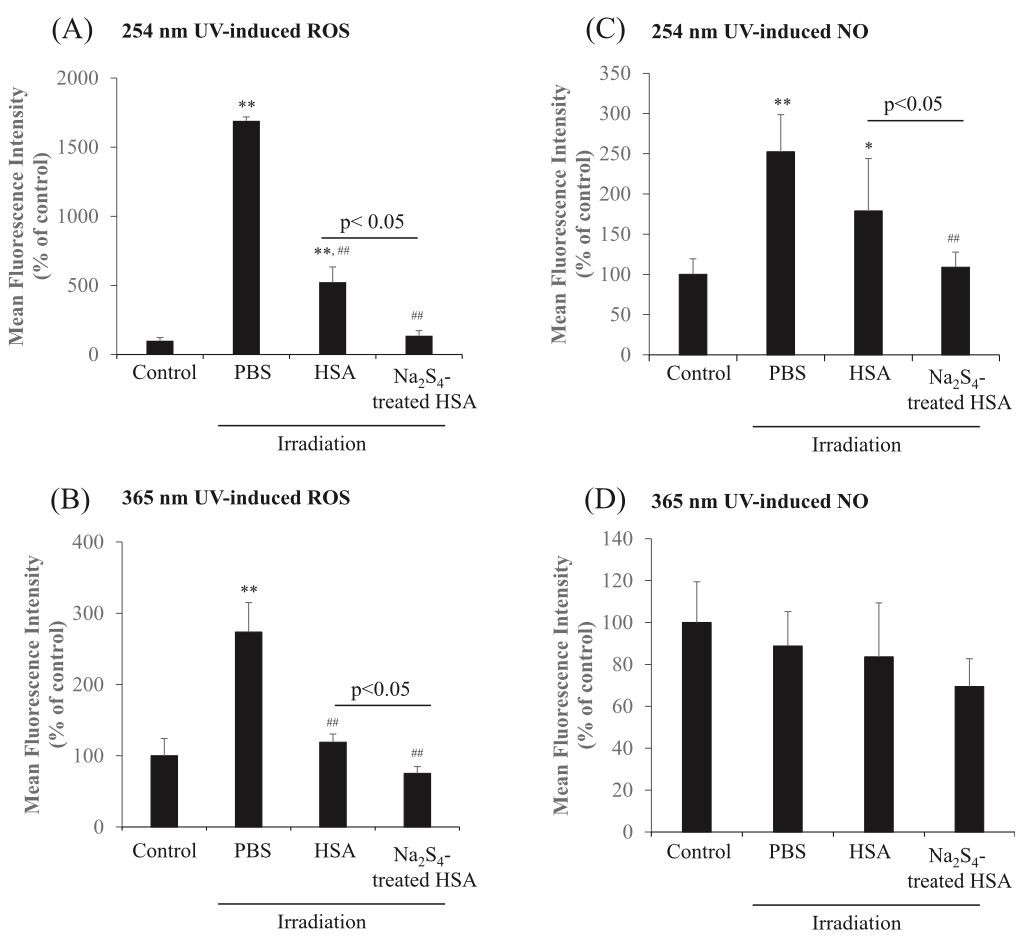
الشكل 4.ROS و NO الكسح هـوما يليهاآثار نا2S4- HSA المعالجة تحت إشعاع فوق البنفسجي.
4. مناقشة
يتم تصنيع الميلانين عن طريق أكسدة التيروزين. يتأكسد التيروزين إلى L-DOPA ، ثم يتأكسد dopaquinone بفعل التيروزيناز. يتأكسد الدوباكينون تلقائيًا إلى الميلانين. يحفز الميلانين على تكوين أصباغ سوداء ونمش ، ولكنه يلعب أيضًا دورًا في حماية الجلد من التلف الناتج عن الأشعة فوق البنفسجية. في جلد الإنسان ، تنتج الخلايا الصباغية أنواع الأكسجين التفاعلية وأكسيد النيتروجين عندما يتم تحفيزها عن طريق الإشعاع فوق البنفسجي [2،29،30]. يعزز ROS تخليق الميلانين عن طريق تنشيط tyr- osinase من خلال عمل سينسيز ATP ، هيدروكسيلاز فينيل ألانين ، وفسفرة MAPKs [31،32]. لا ينشط التيروزيناز عن طريق زيادة المستوى الخلوي لـ cGMP [6]. لذلك ، تعتبر ROS و NO sca vengers من العوامل المضادة لتكوين الميلانين. هنا ، اكتشفنا تأثير التوليف المضاد للميلانين لـ HSA المعالج بـ Na2Sn. قمع HSA المعالج بـ Na2Sn بشدة المستويات الخلوية لـ ROS و NO الناتجة عن الأشعة فوق البنفسجية (الشكل 4). علاوة على ذلك ، كان لـ HSA المعالج بـ Na2Sn تأثير مباشر على تثبيط عمل التيروزيناز (الشكل 5 أ) وتراكم الميلانين (الشكل 5 ب). لم نكن قادرين على توضيح آلية كيفية نقل كبريت الكبريت من HSA المعالج بـ Na2Sn إلى خلية. لذلك ، تظل طبيعة كيفية التأثيرات المباشرة لوظيفة HSA المعالجة بـ Na2Sn غير واضحة. ياماشيتا وآخرون أوضح أن الدوباكوينون يرتبط ببروتينات الثيول عبر بقايا السيستين [33]. مجتمعة ، قد يشتمل تثبيط تراكم الميلانين بواسطة HSA و HSA المعالج بـ Na2Sn أيضًا على تكوين روابط ثاني كبريتيد مع الدوباكوينون أو الميلانين. من ناحية أخرى ، كان تثبيط التيروزيناز يعتمد على محتوى الكبريت المضاف (الشكل 5 أ). من المعروف أن GSH يربط التيروزيناز ويقلل من نشاطه [34]. لأن السيستين الكبريتيد S له تفاعل أقوى من السيستين العادي [11] ، قد يثبط الجلوتاثيون بيرسلفيد (GSSH) عمل التيروزيناز أكثر من GSH. هناك حاجة إلى مزيد من الدراسات بشأن مسألة ما إذا كان HSA المعالج بـ Na2Sn يزيد من GSSH داخل الخلايا في المستقبل.
يتم إنتاج أنواع الأكسجين التفاعلية عن طريق الإشعاع فوق البنفسجي أو الإجهاد الخارجي الذي يسبب ظهور علامات الشيخوخة ، ليس فقط في شكل تكوين الميلانين ولكن أيضًا عن طريق ظهور التجاعيد وترهل الجلد ، الناجم عن تلف الحمض النووي وتكوين الكولاجين المتقاطع. ومن المعروف أيضًا أن أنواع الأكسجين التفاعلية هي عامل تفاقم لأنواع مختلفة من الالتهابات مثل البثور والصدفية. تم تصميم العديد من عوامل تبييض البشرة ، مثل حمض الترانيكساميك [35] وأربوتين [36] ، لمعالجة هذه المشكلات. ومع ذلك ، فإن هذه المركبات تمنع فقط تخليق الميلانين وليس لها تأثير على الإجهاد التأكسدي. وهكذا ، ظلت مخاطر السمية الناجمة عن أنواع الأكسجين التفاعلية قائمة. ميزة استخدام HSA المعالج بـ Na2Sn هو أنه يقوم بكسح ROS بكفاءة (الشكلان 2 و 4).
تمت دراسة كبريتيد الهيدروجين كجزيء أساسي ثالث بعد أكسيد النيتريك وأول أكسيد الكربون. ثبت أن التأثيرات العلاجية لكبريتيد الهيدروجين قابلة للتطبيق في علاج نقص التروية / ضخه [37] وتصلب الشرايين [38] والإنتان [39] والسمية التي يسببها النظام الغذائي عالية الدهون [40]. بالإضافة إلى ذلك ، يحتوي كبريتيد الهيدروجين على نشاط أعلى من كبريتيد الهيدروجين. على سبيل المثال ، يقوم Na2S4 بإزالة سموم ميثيل الزئبق بشكل فعال ويمنع تمايز خلايا الورم الأرومي العصبي ، بينما لا يفعل Na2S [12،41]. لذلك ، ليس فقط تأثير تبييض الجلد ولكن أيضًا التأثيرات الإيجابية الأخرى لـ HSA المعالج بـ Na2Sn ممكنة.
في الختام ، أبلغنا عن تطوير نظام جديد لتقديم خدمة RSS باستخدام ألبومين المصل كناقل مستقر. عندما يقترن الكبريت التفاعلي مع HSA ، يكون له تأثير مضاد للأكسدة أقوى من HSA ويثبط تخليق الميلانين في خلايا الورم الميلانيني. آلية مكافحة تكون الميلانين لا تشمل فقط الكسح ROS و NO ، ولكن أيضًا قمع نشاط التيروزيناز وتراكم الميلانين. ومن ثم ، فإن HSA المعالج بـ Na2Sn لديه إمكانات كبيرة لاستخدامه كعامل تبييض آمن للبشرة.
هذا هو منتجنا.
لمزيد من المعلومات ، الرجاء الضغط على الصورة.

