الكيستانش وإصابة الكلى الحادة في الحالات الحرجة: مراجعة محدثة عن الفيزيولوجيا المرضية والإدارة
Mar 15, 2022
Cistanche وإصابة الكلى الحادة في الحالات الحرجة: مراجعة محدثة على الفيزيولوجيا المرضية والإدارة
اتصال:joanna.jia@wecistanche.com/ واتساب: 008618081934791
الملخص
التأثير الرئيسي للطب الصيني التقليديسيستانشهو حماية الكلى وعلاجها بمختلف أنواعهاأمراض الكلى، مثلفشل كلوي مزمن,التهاب الكلية وسرطان الكلى. هذه الآثارسيستانشتم تسجيله في الطب التقليدي منذ ألفي عام. قام الطب الحديث أيضًا بالعديد من الأبحاث حول التأثيرات الوقائية لـسيستانشعلى الكلى. الأوساط الأكاديمية تعتقد أن تأثيرسيستانشفي حماية وظائف الكلى يأتي من إجمالي جليكوسيداتcistanche، فيرباسكوسايد ، إشنكوسايد ، وفلافونويد. تُعرف إصابة الكلى الحادة (AK) الآن على أنها متلازمة غير متجانسة لا تؤثر فقط على المراضة والوفيات الحادة ، بل تؤثر أيضًا على تشخيص المريض على المدى الطويل. في هذه المراجعة السردية ، سيتم توفير تحديث حول جوانب مختلفة من القصور الكلوي الحاد في المرضى ذوي الحالات الحرجة. سيكون التركيز على التنبؤ والاكتشاف المبكر لـ AKI (على سبيل المثال ، دور المؤشرات الحيوية في تحديد المرضى المعرضين لمخاطر عالية واستخدام التعلم الآلي للتنبؤ بمرض AK) ، وجوانب الفيزيولوجيا المرضية ، والتقدم في التعرف على الأنماط الظاهرية المختلفة لـ AK ، بالإضافة إلى تحديث حول السمية الكلوية والتحدث المتبادل للأعضاء. بالإضافة إلى ذلك ، تتم مناقشة الوقاية من AK (مع التركيز على إدارة السوائل ، وضغط نضح الكلى ، واختيار مقبس الأوعية) والعلاج الداعم لمرض AK. أخيرًا ، مخاطر ما بعد AK من العواقب طويلة الأجل بما في ذلك الحادث أو تطورفشل كلوي مزمنوالأحداث القلبية الوعائية والوفيات.
الكلمات الدالة:بَصِيرالكلىإصابة، التشخيص ، المؤشرات الحيوية ، التعلم الآلي ، عدم التجانس ، الأنماط الظاهرية ، الفيزيولوجيا المرضية ، السمية الكلوية ، الحديث المتبادل للأعضاء ، العلاج بالسوائل ، إدارة ضغط الدم ، ضغط الأوعية ، العواقب طويلة المدى ،سيستانش, مرض كلوي

سيستانشtubulosa يمنعالكلىالمرض ، انقر هنا للحصول على العينة
مقدمة
كان توافر تعريف متفق عليه لإصابة الكلى الحادة (AKI) [1] خطوة مهمة في إنشاء وبائيات القصور الكلوي الحاد. يصيب القصور الكلوي الحاد 30-60 بالمائة من المرضى ذوي الحالات الحرجة ويرتبط بالمراضة والوفيات الحادة [2]. تتراكم الأدلة أيضًا على أن عبء القصور الكلوي الحاد يمتد إلى ما بعد المرحلة الحادة مع التقدم إلىفشل كلوي مزمن(كد) ، زيادة خطر حدوث مضاعفات القلب والأوعية الدموية ، نوبات متكررة من القصور الكلوي الحاد ، والوفيات طويلة الأجل [3]. تقتصر الوقاية من التطور و / أو التقدم حاليًا على تحسين حالة الدورة الدموية والسوائل وتجنب السموم الكلوية. البحث عن علاج دوائي محدد يعوقه التشخيص المتأخر والفيزيولوجيا المرضية المعقدة وغير الموضحة بشكل كامل. من المتوقع حدوث تقدم في إدارة القصور الكلوي الحاد من خلال الاعتراف بأن القصور الكلوي الحاد هو متلازمة غير متجانسة للغاية مع مسببات متغيرة ، وعلم وظائف الأعضاء ، وعرض سريري [4].
من خلال استنبات الخلايا الظهارية الأنبوبية الكلوية للأرنب في المختبر ، وتأثير H2O2 على تكاثر الخلايا وتأثيرسيستانشتمت دراسة مستخلص الصحراوية على تلف الخلايا الطلائية الأنبوبية الكلوية التي يسببها H2O2. من خلال مراقبة مورفولوجيا الخلية ، تم استخدام طريقة MTT لتحديد تأثير H O على تكاثر الخلايا الظهارية الأنبوبية الكلوية الأرانب والتأثير الوقائي لمجموعات الجرعات الثلاث منسيستانشمستخلص مائي وخلاصة كحول 2 و 20 و 200 مجم! L -1 ، وتم تحديد إصدار الخلية LDH. . أظهرت النتائج أنه مع زيادة تركيز H2O2 ، زاد عدد الخلايا المتغيرة شكليًا بشكل تدريجي ، وانخفض عدد الخلايا الملتصقة تدريجياً. كلما زاد معدل تثبيط تكاثر الخلايا ، زاد LDH المنطلق من الخلايا ، والذي كان يعتمد على التركيز. يمكن لمجموعة مستخلصات الماء عالية التركيز أن تقلل بشكل كبير من التأثير المثبط لـ H2O2 على تكاثر الخلايا الظهارية الأنبوبية الكلوية في الأرانب (P<0.01). the="" high,="" medium,="" and="" low-dose="" groups="" of="" the="" alcohol="" extract="" and="" water="" extract="" of="" cistanche="" can="" make="" h2o2="" after="" the="" action="" the="" ldh="" release="" of="" rabbit="" renal="" tubular="" epithelial="" cells="" was="" extremely="" significantly="" lower="" than="" that="" of="" the="" model="" group="" (p=""><0.01), and="" the="" results="" were="" concentration-dependent.="" h2o2="" has="" varying="" degrees="" of="" effects="" on="" the="" proliferation="" of="" rabbit="" renal="" tubular="" epithelial="" cells.="" cistanche="" has="" a="" protective="" effect="" on="" h2o2-induced="" damage="" to="" rabbit="" renal="" tubular="" epithelial="">
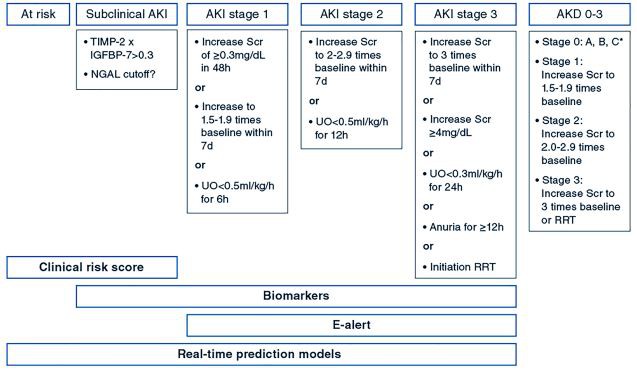
الشكل 1 مراحل مختلفة من تطور القصور الكلوي الحاد وتقدمها والاختبارات التشخيصية المرتبطة بها. إصابة الكلى الحادة AKI ، مثبط أنسجة TIMP للبروتينات المعدنية ، بروتين رابط عامل النمو الشبيه بالأنسولين IGFBP ، ليبوكسين العدلات NGAL المرتبط بالجيلاتيناز ، إخراج البول UO
نحو تشخيص أفضل للـ AKI؟
على الرغم من أن الكلى لها وظائف عديدة ، يتم تعريف AKI في الغالب على أنها انخفاض في معدل الترشيح الكبيبي (GFR).
اقترحت مجموعة عمل KDIGO تعريفًا جماعيًا ونظامًا للتدريج للممارسة السريرية (تعريف KDIGO) الذي يعتمد على زيادة كرياتينين المصل (Scr) في غضون 7 أيام و / أو وجود قلة البول (الشكل 1) ، وكلاهما علامات بديلة لـ GFR [1]. مكن هذا التعريف من تبسيط البحث في هذا المجال. ومع ذلك ، قد يتأثر كل من Scr ومخرجات البول أيضًا بالعوامل غير الكلوية وغير المرتبطة بـ GFR ، وبالتالي فهي علامات ناقصة لخفض معدل الترشيح الكبيبي (GFR) [5]. وبالتالي ، يجب تفسير تشخيص AKI بواسطة معايير KDIGO في السياق السريري. الجدل حول كيفية تحديد وظيفة الكلى الأساسية هو عيب آخر لتعريف الإجماع. على الرغم من المخاوف بشأن قلة البول كعلامة لوظيفة الكلى ، هناك دليل على أن قلة البول تحدد المرضى الذين يعانون من نتائج أسوأ [6،7]. بالإضافة إلى ذلك ، بسبب العمر النصفي الطويل للكرياتينين ووجود احتياطي وظيفي كلوي (احتياطي كلوي السعة التي يمكن تجنيدها قبل أن يبدأ تحديد GFR القاعدية [8]) ، يتطلب Scr وقتًا ليعكس بدقة GFR مما يؤدي إلى تأخر التعرف على ضعف الكلى. يمكن أن تتمثل الحلول المحتملة للكشف في الوقت المناسب عن معدل الترشيح الكبيبي المنخفض في قياس تصفية الكرياتينين على مدار ساعتين أو 4 ساعات ، أو قياس معدل الترشيح الكبيبي الحركي المحسوب من قياسين متسلسل للكرياتينين [9] ، أو استخدام اختفاء البلازما لمركب محقون مثل iohexol الذي يعتمد على إزالة الكلوي. لم يتم التحقيق في هذه الأساليب على نطاق واسع أو استخدامها في إعداد وحدة العناية المركزة. قياسات GFR في الوقت الحقيقي بجانب السرير باستخدام حقن صبغة ومسبار الفلورسنت وتمكين التشخيص المبكر لخلل وظائف الكلى قيد التحقيق ولكن لم تحصل بعد على الموافقة التنظيمية [10]. قد يكون Cystatin-C ، وهو علامة أخرى على الترشيح الكبيبي ، مفيدًا في ظروف الهزال العضلي ولكنه يتأثر أيضًا بالاعتلال المشترك.

الجدول 1 نظرة عامة على المؤشرات الحيوية واختبارات AKI الحالية ؛ الآليات والتطبيقات السريرية
Late AKI diagnosis has been implicated for the lack of efficacy success in drug trials. This explains the interest in biomarkers to predict KDIGO AKI(with 1700 publications over the past 5 years). Ideally, increased biomarker levels indicate kidney injury before the KDIGO criteria for AKI are met (so-called"subclinical AKI"), and thus might trigger early diagnostic and preventive measures [11]. The most widely investigated markers are neutrophil gelatinase-associated lipocalin (NGAL), kidney injury molecule-1(KIM-1), liver fatty acid-binding protein (LFABP), and the product of and tissue inhibitor of metalloproteinase 2 and insulin-like growth factor-binding protein 7(TIMP-2IGFBP7; Nephrocheck)(Fig,1)(Table 1). Only NGAL and TIMP-2*IGFBP7 are available for clinical use. TIMP-2*IGFBP7 is a urinary marker of cell cycle arrest, reflecting cellular stress that precedes tissue damage (Fig.1). It has FDA and EMEA approval for the prediction of AKI stage2and 3 within 12 hin critically ill patients with cardiac and respiratory failure [12]. High sensitivity (>0.3) and high specificity(>2. 0) تم تحديد الانقطاعات ، مما يسمح بتقسيم المخاطر إلى طبقات [13]. أظهر تحليلان تلويان حديثان AUROC 0. 83 للتنبؤ بـ AKI في غضون 24 ساعة في جراحة القلب [14] و 0. 74 للتنبؤ بالمرحلة 2 و 3 في غضون 12 ساعة في الحالات الحرجة مريض [15]. أظهر التحليل التلوي على دقة NGAL البولية AUROC من 0. 75 لالتهاب المفاصل الروماتويدي الحاد مع انقطاع قدره 12 نانوغرام / مل لحساسية 95 في المائة و 580 نانوغرام / مل لخصوصية 95 في المائة [16]. ومع ذلك ، تم الإبلاغ عن عدم تجانس كبير فيما يتعلق بمجتمع الدراسة (احتمالية الاختبار المسبق) ، وتوقيت أخذ العينات ، ونافذة التنبؤ ، وشدة AKI المتوقعة. يجب أيضًا الاعتراف بأن التعريف القياسي الذهبي (معايير KDIGO) يشير إلى وظائف الكلى ، وليس الضرر. وقد تعكس "الإيجابيات الكاذبة" إصابة "تحت الإكلينيكي" وقد تعكس السلبيات الكاذبة "الدورة الدموية" (التي كانت تسمى سابقًا) AKI. قد يؤدي الجمع بين المؤشرات الحيوية للضرر ومعايير KDIGO الوظيفية إلى توصيف أفضل للأنماط الظاهرية لـ AKI وتحسين دقة التشخيص [11]. لذلك ، تم اقتراح دمج المرقمات الحيوية في تعريف AKI [11].
على الرغم من البحث المكثف ، فإن الإرشادات حول كيفية استخدام المؤشرات الحيوية AKI في الممارسة السريرية غير متوفرة. حاليًا ، نجحت هذه المؤشرات الحيوية في تحديد المرضى المعرضين لمخاطر عالية للتجارب السريرية التي تحقق في استراتيجيات الوقاية المبكرة [17 ، 18]. ومع ذلك ، فإن إظهار المنفعة / الفعالية في بيئة العالم الحقيقي يتطلب مقارنة بين استراتيجيتين حيث يكون لدى الأطباء أو لا يمكنهم الوصول إلى نتيجة المرقم الحيوي. تعتبر التكاليف ، والتوافر ، وندرة الخيارات العلاجية من العوائق الأخرى التي تحول دون الاستخدام السريري على نطاق واسع.
تم اقتراح مؤشّر آخر للـ AKI وهو فقدان الاحتياطي الوظيفي الكلوي (يُقاس بحمل بروتيني فموي مرتفع) ، والذي ثبت أنه يتنبأ بالـ AKI بعد الجراحة في جراحة القلب [19] وقد يكون علامة على الشفاء غير الكامل [20]. ومع ذلك ، لا يزال هذا الاستخدام السريري لهذه المعلمة أيضًا بحاجة إلى التقييم.
تم اقتراح التنبيهات الإلكترونية (التنبيهات الإلكترونية) كحلول للتشخيص المبكر لـ AKI [21]. وهي تستند إلى معايير KDIGO السائدة وتتمثل ميزتها الرئيسية في توقع الإعداد الأقل مراقبة غير الخاص بوحدة العناية المركزة وفقط عند ربطها بمجموعة أوامر و / أو إجراء [22]. الأدلة على الاستفادة في وحدة العناية المركزة محدودة [23].

يلخص الجدول 2 خصائص نماذج التعلم الآلي المتاحة لتنبؤ AKI في وحدة العناية المركزة
المزيد من نماذج التنبؤ الواعدة إما على أساس الانحدار اللوجستي أو منهجيات التعلم الآلي التي تستفيد من كمية كبيرة من البيانات المتاحة في السجلات الصحية الإلكترونية (EHR). شهدت السنوات الماضية انتشارًا لنماذج التنبؤ بالـ AKI القائمة على الذكاء الاصطناعي [24 ، 25]. ركز عدد قليل فقط على مرضى وحدة العناية المركزة (الجدول 2). تم تطوير معظم النماذج بأثر رجعي في مجموعة بيانات مُجهزة مسبقًا (مجموعة بيانات بحثية أو سجلات صحية إلكترونية) وتستخدم معايير الكرياتينين فقط. يظهر Tey بدقة متكافئة إلى ممتازة (AUC 0. 75– 0. 90) ومعايرة جيدة. تكون الدقة أعلى بشكل عام مع وجود نافذة تنبؤ أقصر (مهلة زمنية) وأكثر شدة AKI. توفر هذه النماذج إما نتائج اللقطة المفاجئة [26] ، أو النوافذ المتحركة [27] ، أو توقع AKI المستمر [28]. واحد فقط من نماذج وحدة العناية المركزة هذه قد خضع لعملية تحقق خارجية تؤكد الدقة الجيدة في مجموعة بيانات مستقلة متعددة المراكز [29]. الخطوة الأخيرة في عملية التحقق من صحة نماذج التنبؤ هذه ، والتي لا يزال يتعين اتخاذها ، هي الترجمة إلى أداة تنبؤ في الوقت الفعلي بجانب السرير (باستخدام السجلات الصحية الإلكترونية "غير النظيفة") توفر احتمالية AKI المحدثة باستمرار مع مستويات عدم اليقين. يجب بعد ذلك تقييم هذا النموذج في اختبار RCT لتأثير استخدامه على النتائج التي تركز على المريض عند دمجه في سير العمل السريري في العالم الحقيقي ، وفي النهاية مرتبطًا بنظام دعم القرار السريري ("تحويل التنبؤات إلى عمل"). مثل هذه التجربة جارية حاليًا (NCT03590028) (الجدول 3).

الجدول 3 اقتراحات لبحوث AKI المستقبلية
الأنماط الظاهرية السريرية
على مدى العقد الماضي ، تم الاعتراف بشكل متزايد بأن القصور الكلوي الحاد هو متلازمة غير متجانسة ليس فقط فيما يتعلق بالتعرض (انخفاض النتاج القلبي ، والإنتان ، والجراحة الكبرى ، والسمية ، وما إلى ذلك) والفيزيولوجيا المرضية (نقص تدفق الدم ، والالتهاب ، وما إلى ذلك) ولكن أيضًا فيما يتعلق إلى العرض السريري (الخطورة والتطور). تتمثل إحدى الطرق المحتملة لتمييز الأنماط الظاهرية السريرية في تطبيق تحليل الفئة الكامنة على مجموعة من المتغيرات السريرية والبيولوجية لتحديد المجموعات الفرعية ذات النتائج والاستجابات العلاجية المختلفة [30 ، 31]. تم إثبات الأهمية التنبؤية لمدة AKI ونمط الاسترداد في العديد من التحليلات. حدد مؤتمر ADQI الأخير AKI العابر و AKI المستمر بناءً على مدة تزيد أو تقل عن 48 ساعة [32]. يمكن للتنبؤ بمسار القصور الكلوي الحاد أن يمكّن من تحديد أنماط ظاهرية مختلفة تتطلب إدارة مختلفة. تؤدي الكيمياء الحيوية البولية التقليدية [33] ومؤشر المقاومة الكلوية [34] أداءً ضعيفًا في هذا الصدد ، لا سيما في حالة تعفن الدم. قد تكون المؤشرات الحيوية مفيدة [35 ، 36] على الرغم من أن النتائج ليست إيجابية بشكل موحد [37 ، 38]. تم مؤخرًا تحديد علامة حيوية جديدة ، ليجند chemokine chemokine عزر C-C البولي -14 (CCL14) كمؤشر دقيق للغاية (يتفوق على جميع المؤشرات الحيوية الأخرى) للمرحلة الثالثة من AKI المستمرة في مرضى وحدة العناية المركزة الذين يعانون من القصور الكلوي الحاد الشديد [39]. تشير البيانات المحدودة إلى أن معدل الترشيح الكبيبي الحركي يتنبأ بشكل أفضل بتطور القصور الكلوي الحاد بشكل أفضل من بعض المؤشرات الحيوية [40] وينطبق الشيء نفسه على اختبار إجهاد فوروسيميد (FST) الذي كان أداؤه أفضل من المؤشرات الحيوية الكيميائية الحيوية في التنبؤ بالتقدم إلى المرحلة الثالثة من القصور الكلوي الحاد [41 ، 42]. من المؤكد أن التطورات المستقبلية في قياس معدل الترشيح الكبيبي في الوقت الحقيقي أو استخدام نماذج توقع AKI في الوقت الحقيقي ستساهم بالتأكيد في هذا المجال.

سيستانشيمكن أن يخففمرض كلوي
مرض الكلى الحاد: حديث الكيان
أمراض الكلى الحادة(AKD) يُعرَّف بأنه نوبة AKI تدوم أكثر من 7 أيام ولكن أقل من 90 يومًا تم اقتراحها مؤخرًا كمفهوم (الشكل 1) [32]. يهدف إلى سد الفجوة بين AKI و CKD (والتي تتطلب 3 أشهر ليتم تشخيصها). يستخدم AKD معايير الكرياتينين لتعريف KDIGO. من المهم أن نلاحظ أن تشخيص AKD (شدة) أو الشفاء الظاهر قد يتأثر بانخفاض سكر الدم المرتبط بفقدان كتلة العضلات المرتبط بمرض خطير مزمن [5]. تتطلب العلاقة بين AKI المستمر و AKD و CKD بالإضافة إلى التدخلات التي قد تتداخل مع هذا التطور مزيدًا من الدراسة (الشكل 2).
الفيزيولوجيا المرضية لمتلازمة غير متجانسة
لم يتم توضيح الفيزيولوجيا المرضية لـ AKI بشكل كافٍ ليس على الأقل لأن الكلى أعضاء معقدة ولا يمكن الوصول إليها إلى حد ما. تعكس النماذج الحيوانية بشكل سيء الفيزيولوجيا المرضية للإنسان (حيث تلعب الأمراض المصاحبة دورًا مهمًا) ومتلازمة AKI غير متجانسة [43] ، كما يتضح من الدراسات الحديثة التي توضح الاستجابات الجينية المختلفة في استنفاد الحجم ، ونماذج الحيوانات الإقفارية والتفسخية لـ AKI [44 ، 45]. في الممارسة السريرية ، من المحتمل وجود نماذج فسيولوجية مرضية متميزة ولكنها متداخلة لـ AKI والتي قد تتطلب علاجات فردية [4] ، مما يفسر جزئيًا فشل العديد من التدخلات في التجارب السريرية. باستثناء مرض كلوي داخلي محدد ، يمكن أن تتراوح أمراض القصور الكلوي الحاد من انخفاض معدل الترشيح الكبيبي ، بوساطة تغيرات الدورة الدموية النظامية أو المحلية من خلال الإجهاد / الإصابة الأنبوبية القابلة للعكس إلى النخر الأنبوبي الصريح. تعتبر التغيرات النسيجية في القصور الكلوي الحاد من الأمراض الخطيرة بؤرية ومتواضعة بشكل عام [46]. ضمن هذا الفيزيولوجيا المرضية المعقدة ، يظهر عدد من الموضوعات المشتركة مع أنماط من إصابات الكلى الالتهابية ، الإقفارية ، والسمية الكلوية التي يمكن أن تحدث بشكل متتابع ومتزامن وقد تتأثر بشكل مختلف بالأمراض الكامنة (الشكل 3).
يعد تحديد الأنماط الظاهرية السريرية ذات الفيزيولوجيا المرضية والنتائج أمرًا ضروريًا لتحديد أهداف علاجية جديدة [4]. تتضح أهمية السياق السريري في متلازمة القلب الكلوي بسبب عدم المعاوضة الحادة لفشل القلب المزمن ، حيث يكون الاحتقان الكلوي هو المحرك الرئيسي لتدهور وظائف الكلى. على الرغم من أن الحل الناجح للحمل الزائد للسوائل باستخدام مدرات البول أو الترشيح الفائق قد يؤدي إلى زيادة SCR ، إلا أنه يرتبط بتحسين وظائف الكلى على المدى الطويل [47] ، حتى في المرضى الذين يعانون من ارتفاع علامات الإصابة الكلوية [48]. يشير هذا إلى أن فائدة إزالة الاحتقان تفوق الزيادة المتواضعة في سكر الدم ، وعلى سبيل المثال ، قد تكون NT-proBNP علامة بيولوجية تنبؤية أكثر فائدة من علامات تلف الكلى في هذا الوضع المحدد [49]. من المهم أن نلاحظ ، مع ذلك ، أنه غالبًا ما تتعايش العديد من عوامل خطر الإصابة بالتهاب المفاصل الروماتويدي والإعدادات السريرية أو تتبعها بشكل متسلسل بحيث يصعب استخلاص الاستدلالات السريرية الواضحة ، مما يؤكد على أهمية إجراء مزيد من البحث لتحديد أنماط AKI السائدة الأساسية لتوجيه العلاج. تدخل قضائي.

يظهر التفاعل بين المسارات الفيزيولوجية المرضية المختلفة أكثر وضوحًا في تعفن الدم ، وهو السبب الأكثر شيوعًا لـ AKI في الحالات الحرجة [2]. بشكل عام ، لا يبدو أن المكون الإقفاري ناتج عن انخفاض تدفق الدم الكلي في الكلى. بدلاً من ذلك ، قد يقلل التحويل المحيط بالكبيبات من تدفق الدم الكبيبي ويؤدي الخلل الوظيفي البطاني الناجم عن الالتهاب إلى اضطرابات الأوعية الدموية الدقيقة وتشكيل الجسيمات الدقيقة [50 ، 51]. يعتبر التضيق الوعائي الناتج بسبب التغذية المرتدة الأنبوبية الكبيبية نتيجة وليس سببًا للخلل الأنبوبي [51]. ينتج المكون الالتهابي عن الأنماط الجزيئية المرتبطة بالتلف (DAMPs) والأنماط الجزيئية المرتبطة بالعوامل الممرضة (PAMPs) الموجودة في الشعيرات الدموية حول الأنبوب والتي تخضع للترشيح الكبيبي وتتفاعل لاحقًا مع المستقبلات الشبيهة بالفرشاة الموجودة على غشاء حدود الفرشاة للخلايا الظهارية في النبيبات القريبة [50 ، 51]. يساهم تجنيد الخلايا المناعية أيضًا في الاستجابة الفيزيولوجية المرضية المناعية والضرر المناعي [52]. إلى جانب الضرر الالتهابي ، أشارت البيانات التجريبية الحديثة إلى أن توقف الدورة الخلوية ، والالتهام الذاتي الناقص ، والتطعيم الحديدي ، واختلال وظائف الميتوكوندريا ، وإعادة البرمجة الأيضية هي آليات تساهم في الخلل الأنبوبي في القصور الكلوي الحاد الإنتاني [50].
أدت بعض هذه المسارات بالفعل إلى استكشاف التدخلات المحتملة في المرضى. تعتبر الكلى عضوًا نشطًا للغاية في عملية التمثيل الغذائي ، أحد المسارات التي حظيت باهتمام كبير مؤخرًا هو الخلل الوظيفي في الميتوكوندريا وضعف استقلاب الطاقة بسبب نقص نيكوتيناميد الأدينين ثنائي النوكليوتيد (NAD plus) وإعادة البرمجة الأيضية [50 ، 51]. يتميز AKI التجريبي بنقص PPAR gamma-coactivator 1a (PGC -1 a) ، وهو منظم مهم للتكوين الحيوي للميتوكوندريا. يرتبط نقص PGC -1 أ بضعف تخليق NAD plus ، وهو عامل أساسي في استقلاب الطاقة الخلوية (بشكل أساسي أكسدة الأحماض الدهنية وتحلل السكر). تم إثبات علامات انخفاض NAD plus في المرضى الذين يعانون من القصور الكلوي الحاد بعد جراحة القلب. بالإضافة إلى ذلك ، فإن النيكوتيناميد ، وهو مقدمة لـ NAD بالإضافة إلى انخفاض مستويات الكرياتينين بعد الجراحة في المرحلة الأولى من المضبوطة. تجري حاليًا مجموعة أكبر من المعشاة ذات الشواهد (NCT04342975). تشير إعادة البرمجة الأيضية إلى التحول من الفسفرة المؤكسدة إلى إنتاج طاقة أقل كفاءة من خلال تحلل السكر استجابةً لانخفاض الأكسجين وإمدادات الركيزة. إنه يقلل من إنتاج أنواع الأكسجين التفاعلية (ROS) وهو آلية بقاء مع تقليل الوظائف غير الحيوية مما يدفع ثمن الحفاظ على السلامة الخلوية ، مما قد يفسر التفكك بين الهيكل والوظيفة التي تميز AKI. ومع ذلك ، فإن العودة إلى الفسفرة المؤكسدة (بوساطة AMPK) تبدو ضرورية للبقاء على قيد الحياة ولكنها تتطلب استعادة الميتوكوندريا الوظيفية عن طريق التكوُّن الحيوي للميتوفاجي والميتوكوندريا [50 ، 51].
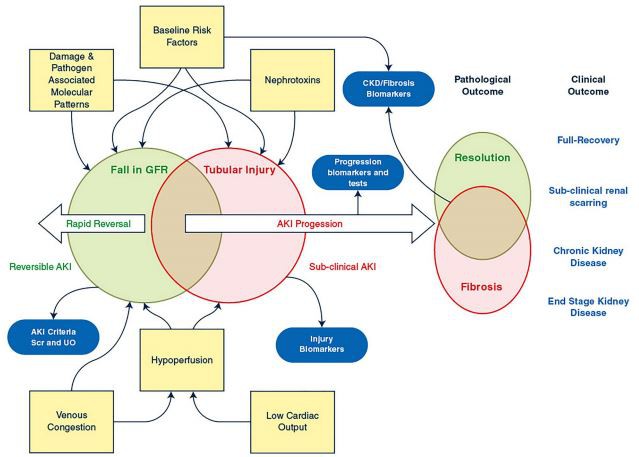
الشكل 3 نظرة عامة مبسطة على الفيزيولوجيا المرضية للـ AKI توضح عدم التجانس في المسببات ، والعرض ، وعلم الأمراض ، والتقدم ، والنتائج وكيف يمكن أن تساعدنا التحقيقات في فهم الأنماط الظاهرية لـ AKI في مراحل مختلفة من المرض. يشير اللون الأخضر إلى العمليات الوظيفية / القابلة للعكس ؛ يشير اللون الأحمر إلى إصابة الأنسجة الحادة والمزمنة. تشير المربعات الصفراء إلى العوامل المسببة في التسبب في أمراض القصور الكلوي الحاد ، والاختبارات التشخيصية للصناديق الزرقاء التي تشير إلى العمليات الفيزيولوجية المرضية الأساسية
ساهمت المؤشرات الحيوية في كشف الفيزيولوجيا المرضية لـ AKI. إلى جانب إعادة البرمجة الأيضية ، يعد توقف دورة الخلية آلية وقائية أخرى تمنع الخلايا التي بها تلف الحمض النووي من الانقسام وتقليل إنفاق الطاقة. ومع ذلك ، كما هو الحال مع إعادة البرمجة الأيضية ، يبدو أنه سيف ذو حدين لأنه مع استمرار توقف دورة الخلية يصبح الإصلاح غير قادر على التكيف مما يؤدي إلى انتقال AKI إلى CKD [54]. تم وصف يجند Chemokine C-C المزخرف -14 (CCL14) مؤخرًا بأنه علامة على ثبات AKI. الآلية المفترضة (والهدف العلاجي المحتمل) هي إطلاق CCL14 بواسطة الخلايا الأنبوبية استجابةً للوسطاء الالتهابيين ، مما يؤدي إلى التسلل والتمايز بين الخلايا الوحيدة والتليف الذي يتوسط الخلايا التائية والانتعاش غير الكامل للكلى [39]. مستقبل منشط البلازمينوجين القابل للذوبان (suPAR) من urokinase القابل للذوبان ، وهو علامة على الالتهاب المزمن ويزداد تنشيط المناعة في عدد من حالات التعرض بما في ذلك زيادة العمر والسكري وأمراض القلب والأوعية الدموية والعدوى والتدخين. كما أنه يتوقع تطور CKD و CKD الحادث. تنبأت مستويات القبول بشكل مستقل بتطور القصور الكلوي الحاد خلال الأيام السبعة الأولى بعد الإجراءات المختلفة [55]. الأهم من ذلك ، يبدو أن استهداف المسارات المؤكسدة suPAR يخفف الضرر في AKI التجريبي [55] مما يشير إلى إمكانية كهدف علاجي. وبالمثل ، فإن جهاز Dickkopf البولي -3 (DKK3) هو بروتين سكري مؤيد للتليف تفرزه الخلايا الأنبوبية الكلوية التي تعدل مسار Wnt / b المتضمن في التليف الأنبوبي الخلالي وتتنبأ بفقدان GFR والتليف الكلوي في مرض الكلى المزمن. وقد تم وصفه مؤخرًا بأنه مؤشر قوي قبل الجراحة لجراحة القصور الكلوي الحاد بعد الجراحة القلبية ، والأهم من ذلك ، تدهور وظيفة الكلى على المدى الطويل بعد القصور الكلوي الحاد [56]. تؤكد هذه النتائج على الفيزيولوجيا المرضية المترابطة لنوبات AKI وتطور CKD. وجدت الدراسة التي سبق ذكرها باستخدام تحليل الفئة الكامنة للكشف عن الأنماط الظاهرية السريرية أن طريقتين فرعيتين (AKI-SP1 و AKI-SP2) مع ملامح مختلفة للعلامات الحيوية (علامات الخلل البطاني مثل مستقبل عامل نخر الورم -1 ، أنجيوبويتين { {23}} و 2) ، نتائج الكلى والمريض والاستجابة للعلاج بالفازوبريسين [57] ، على ما يبدو محددًا وراثيًا [58]. هذه ليست سوى الخطوات الأولى في البحث عن المسارات الفيزيولوجية المرضية التي يمكن أن تؤدي إلى الطب الدقيق والفوائد السريرية.
ما الجديد في السمية الكلوية؟
هناك عقاقير سامة للكلى بشكل مباشر ، وأدوية غير سامة للكلى ولكنها تتداخل مع ديناميكا الدم داخل الكلى (مثل مثبطات الإنزيم المحول للأنجيوتنسين ، ومضادات الالتهاب غير الستيروئيدية) ، والأدوية غير السامة للكلية ، ولكنها تتراكم في الفشل الكلوي ، وبالتالي يجب أن توصف بحذر . الأدوية الأكثر شيوعًا هي عوامل التباين والمضادات الحيوية ولكن قد تكون سمية الأدوية المتعددة هي المشكلة السائدة. عند وصف الأدوية ، يجب على الأطباء أن يفكروا في كيفية تأثيرها على وظائف الكلى وما إذا كان تخليصها يتأثر بوجود القصور الكلوي الحاد. يجب تقليل وصف الأدوية السامة للكلية من حيث التكرار والمدة ، ومع ذلك ، لا ينبغي حجبها في المواقف التي تهدد الحياة بسبب القلق من AKI [59]. يجب أن تستمر الأدوية ذات التأثيرات الواقية للكلية حتى لو كانت مرتبطة بارتفاع طفيف في كرياتينين المصل (أي مثبطات الإنزيم المحول للأنجيوتنسين في اعتلال الكلية السكري).
تاريخياً ، تم اعتبار عوامل التباين من الأسباب المهمة لـ AKI. ومع ذلك ، فإن الدراسات القائمة على الملاحظة الحديثة مع النماذج المعدلة لدرجة الميل لم تجد أي فرق ذي صلة في حدوث AKI بين أولئك المعرضين أو غير المعرضين لعوامل التباين الحديثة ، حتى في مرضى الإنتان ووحدة العناية المركزة [60-62] ، مما يشير إلى أن خطر الإصابة بالتهاب القصور الكلوي الحاد الناجم عن التباين (الارتباط السببي) أقل بكثير مما كان يعتقد سابقًا وهذا التباين المرتبط بـ AKI (الارتباط الزمني) غالبًا ما يكون له أسباب أخرى. يدعم عدم وجود زيادة ما بعد التباين في المؤشرات الحيوية لإصابة الكلى [63] هذا المفهوم. ومن ثم ، لا ينبغي تأجيل التصوير المقطعي المحسن بالتباين إذا لزم الأمر لتشخيص حالة تهدد الحياة. في جميع المواقف الأخرى ، يجب موازنة الخطر غير المؤكد للـ AKI الناجم عن التباين مقابل خطر فقدان تشخيص مهم ، مع الأخذ في الاعتبار إمكانية إجراءات التصوير البديلة [64]. تقترح الدلائل الإرشادية الحديثة استخدام جرعات التباين المعتدلة والترطيب متساوي التوتر الوقائي في المرضى المعرضين للخطر [65] على الرغم من أن الأخير قد تم استجوابه [66]. من الواضح أنه في المرضى ذوي الحالات الحرجة ، يجب أن يراعي الماء حالة حجم المريض الفردي ، مع الموازنة بين مخاطر نقص تدفق الدم في الكلى وخطر زيادة السوائل. أكدت تجربة RCT كبيرة أن الأسيتيل سيستئين ليس له فائدة وأن البيكربونات ليست أفضل من المحلول الملحي في منع اعتلال الكلية المتباين [67].
فيما يتعلق بجرعات المضادات الحيوية ، تؤكد الأدبيات الحديثة بشكل أساسي على خطر التركيزات تحت العلاجية في علاج الكائنات الدقيقة المقاومة للأدوية المتعددة (MDR) ، مما يجعل الجرعات صعبة بالنسبة للمضادات الحيوية ذات المؤشر العلاجي الضيق مثل الفانكومايسين والأمينوغليكوزيدات والبوليميكسين. التجارب جارية للتحقيق في الإدارة والمدة المثلى للمضادات الحيوية.
تمت مناقشة السمية الكلوية للفانكومايسين على مدار سنوات عديدة وربما تكون أقل مما كان يُقترح سابقًا [68]. أظهر تحليل تلوي حديث أن حدوث التهاب المفاصل الروماتويدي يزداد بتركيزات أعلى في الحوض ويكون أعلى بشكل ملحوظ بالنسبة لتركيزات الحوض التي تزيد عن أو تساوي 20 ميكروغرام / مل. واقترح أيضًا أن استراتيجية الرصد التابعة لمفوضية الاتحاد الأفريقي / وزارة الصناعة والتجارة (التي تهدف إلى هدف 400) يمكن أن تؤدي إلى سمية كلوية أقل [69]. في المرضى المعرضين لخطر كبير أو الذين لديهم علامات مبكرة على ضعف وظائف الكلى ، يجب التفكير في التحول إلى بديل أقل سمية. أظهرت العديد من التجارب القائمة على الملاحظة زيادة السمية الكلوية عند دمج فانكومايسين مع البيبراسيلين / تازوباكتام بالمقارنة مع فانكومايسين بمفرده أو بالاشتراك مع بيتا لاكتام آخر [70]. اقترح آخرون أن زيادة Scr لا تعكس AKI الحقيقي (انخفاض GFR) ، ولكن تثبيط الإفراز الأنبوبي للكرياتينين بواسطة piperacillin / tazobactam ولكن هذا قد يكون صالحًا فقط للمراحل الدنيا من AKI [71]. يجب أن توضح التجارب المعشاة ذات الشواهد المستقبلية ذات العلامات غير الكرياتينينية لـ GFR المشكلة. أدى ظهور البكتيريا سالبة الجرام التي يصعب علاجها إلى تجديد الاهتمام بالبوليميكسين والأمينوغليكوزيدات ، وخاصة الأميكاسين. تركز معظم التجارب الحديثة على الأميكاسين على الجرعات المثلى فيما يتعلق بالفعالية ، في حين تمت دراسة السمية الكلوية بشكل سيئ في مرضى وحدة العناية المركزة ، اقترحت دراسة صغيرة قائمة على الميل عدم وجود سمية قصيرة (<3 days)amikacin="" treatment,="" which="" might="" be="" sufficient="" to="" bridge="" the="" waiting="" time="" for="" bacteriological="" results="" [72].="" polymyxins="" are="" nephrotoxic="" [(73]="" with="" colistin="" being="" more="" harmful="" than="" polymyxin="" b="" 74].="" however,="" since="" they="" are="" mostly="" used="" as="" a="" last="" resort,="" kidney="" dysfunction="" is="" often="" an="" unavoidable="" side="" effect.="" a="" combination="" of="" injury="" biomarkers="" and="" therapeutic="" drug="" monitoring="" could="" help="" to="" reduce="" nephrotoxicity,="" although="" evidence="" from="" clinical="" studies="" is="">
عبر الجهاز الحديث
أثناء تطور ووجود AKI في الحالات الحرجة ، تتأثر جميع الأعضاء غير الكلوية تقريبًا. يمكن أن تمثل هذه العملية الجهازية المعممة تأثير المرض الأساسي (الصدمة ، الالتهاب الجهازي) على أنظمة أعضاء متعددة. ومع ذلك ، يشير تفسير بديل إلى أن التأثير المتبادل للأعضاء الفاشلة ، والمعروف باسم الحديث المتبادل للأعضاء ، يمكن أن يلعب دورًا أيضًا. يمكن أن ينتج القصور الكلوي الحاد بالفعل عن فشل أعضاء أخرى ، وأشهر الأمثلة على ذلك هي متلازمة القلب الكلوي ، من فشل القلب ، والمتلازمة الكبدية الكلوية ، من الكبد الفاشل. هناك أيضًا مؤشرات على أن متلازمة الضائقة التنفسية الحادة و (طريقة) التهوية الميكانيكية قد تؤثر على وظائف الكلى [75]. ومع ذلك ، فإن مفهوم الكلام المتبادل يعمل أيضًا في الاتجاه الآخر ويعتبر أمراض القصور الكلوي الحاد مرضًا جهازيًا له تأثير على أعضاء أخرى مثل القلب [76] والرئة [75] والكبد والدماغ [77،78]. بدلاً من أن تكون متفرجًا بريئًا في عملية فشل أعضاء متعددة ، قد تبدأ الكلى بالفعل في إنشاء مسارات استقلابية أو خلطية تؤثر على وظيفة الأعضاء البعيدة. الآليات المحتملة هي عواقب انخفاض وظائف الكلى ، مما يؤدي إلى تراكم السموم البوليسية ، وزيادة السوائل ، واضطرابات الكهارل ، واختلال التوازن الحمضي القاعدي. بدلاً من ذلك ، قد تلعب آلية التهابية تنطوي على هجرة العدلات والوسطاء الالتهابيين الناشئين في الكلى أو الآثار الجانبية للعلاج الداعم بالعلاج الكلوي البديل (RRT) دورًا. يوجد أيضًا تداخل بين الكلى والجهاز المناعي مع الالتهاب باعتباره آلية فسيولوجية مرضية مهمة لـ AKI من ناحية وتثبيط المناعة الناجم عن AKI مما يؤدي إلى زيادة القابلية للإصابة بالعدوى الثانوية من ناحية أخرى. يبدو أن مادة مقاومة التوكسين اليوريمي هي وسيط مهم لضعف المناعة الخلوية [79]. تتضح الأهمية السريرية للشلل المناعي الناجم عن القصور الكلوي الحاد من خلال الملاحظة التي تفيد بأن الخلل الكلوي يزيد من فرص الإصابة بعدوى خطيرة بعد جراحة القلب [80] ويموت ما يقرب من نصف مرضى القصور الكلوي الحاد الذين لا ينجون من الإنتان [81،82] ].
ينتج الدليل المباشر لتأثير القصور الكلوي الحاد على الأعضاء الأخرى في الغالب من التجارب على الحيوانات (تم تلخيصها في [77،78]) نظرًا لأنه من الصعب تمييز تأثير المسببات الشائعة والتحدث المتبادل للأعضاء في الحالة السريرية. على سبيل المثال ، تبين أن المسار المعتمد على الجالكتين -3- متورط في متلازمة القلب الرينو [83]. تشير الدراسات الحديثة التي أجريت على الحيوانات أيضًا إلى أن نقص التروية الكلوي الحاد قد يؤدي إلى حدوث تغيرات وظيفية وتغييرات نسخية في الرئة ، بغض النظر عن التبول في الدم ، ولكنه مرتبط بتهريب الكريات البيض [84].
من الواضح أن الحديث المتبادل بين الكلى والأعضاء الأخرى قد يكون مساهماً مهماً في زيادة معدلات الاعتلال والوفيات المرتبطة بـ AKI [85] وقد يفسر لماذا ، مقارنةً بالضوابط المتطابقة ، يكون المرضى الذين يعانون من القصور الكلوي الحاد أكثر عرضة للوفاة من تعفن الدم والنزيف والهذيان وفشل الجهاز التنفسي [75،76 ، 86].
الوقاية من القصور الكلوي الحاد
مبادئ عامة
يجب تطبيق الإجراءات الوقائية العامة على جميع المرضى المقبولين في وحدة العناية المركزة ، بما في ذلك تصحيح نقص حجم الدم وانخفاض ضغط الدم ، ووقف وتجنب العوامل السامة للكلى ، وتصحيح ارتفاع السكر في الدم [64].
إدارة السوائل
الهدف من إدارة السوائل هو تصحيح نقص حجم الدم داخل الأوعية الدموية دون التسبب في زيادة السوائل والمضاعفات المرتبطة بها ، بما في ذلك التطور الجديد وتطور القصور الكلوي الحاد [87]. تم العثور أيضًا على ارتباط بين ارتفاع الضغط الوريدي المركزي والاحتقان الوريدي الكلوي وتطور القصور الكلوي الحاد ، الذي تم الإبلاغ عنه بشكل رئيسي في قصور القلب الاحتقاني ، في مجموعات مرضى وحدة العناية المركزة الأخرى [88،89]. وجدت تجربة عشوائية أجريت على مرضى متلازمة الضائقة التنفسية الحادة أن الاستراتيجيات المقيدة للسوائل آمنة [90]. في المقابل ، زادت إدارة السوائل المقيدة قبل الجراحة من خطر الإصابة بالتهاب المفاصل الروماتويدي في المرضى الذين يخضعون لعملية جراحية اختيارية في البطن [91]. في AKI المؤسس ، يظل دور تقييد السوائل غير مؤكد ويعتمد على الأرجح على حالة الحجم داخل الأوعية الدموية الموجودة مسبقًا. أظهرت دراسة تجريبية أجريت على مرضى مصابين بأمراض خطيرة مع القصور الكلوي الحاد أن تقييد تناول السوائل بهدف منع الحمل الزائد للسوائل كان مرتبطًا بانخفاض معدل حدوث التأثيرات الضائرة وحاجة أقل إلى العلاج المضاد للفيروسات القهقرية [92]. وبالمثل ، ارتبطت استراتيجية الحد من السوائل النشط بعد الإنعاش الأولي للسوائل في المرضى الذين يعانون من الصدمة الإنتانية بتطور القصور الكلوي الحاد [93] ولكن لا يمكن إعادة إنتاج هذه النتيجة في تجربتين لاحقتين باستخدام نهج مماثل [94،95]. تنتظر نتائج التجارب المعشاة ذات الشواهد المستمرة لفحص فعالية وسلامة تقييد السوائل ودور الإنعاش النشط في المرضى المعرضين لمخاطر عالية [96].
تم أيضًا تقييم نوع السائل البلوري للإنعاش في تجارب معشاة ذات شواهد كبيرة حديثة في المرضى غير الحرجين والمرضى المصابين بأمراض خطيرة. أظهرت دراسة SMART ، التي جمعت المحلول الملحي مع البلورات المخزنة ، انخفاض معدل حدوث الأحداث الضائرة الكبرى في الكلى (MAKE) في أولئك الذين يتلقون البلورات المخزنة مؤقتًا ، ولكن لم يكن هناك فرق كبير في المرحلة القصوى من AKI ، أو الحاجة إلى RRT ، أو نسبة من المرضى الذين يعانون من مضاعفة سكر الدم على الأقل. لم يكن هناك أيضًا اختلاف في متوسط حجم السوائل بين المجموعتين. بين مرضى الإنتان ، ارتبط استخدام البلورات المخزنة مؤقتًا بانخفاض معدل الوفيات داخل المستشفى 30- يوميًا مقارنةً باستخدام المحلول الملحي [97].
Kidney perfusion pressure Conditions with non-fluid-responsive impaired cardiac output (CO) may require inotropes. Interestingly, the intervention arm of the PREV-AKI study, showing a beneficial effect of a care bundle, used more dobutamine [17]. With regards to early AKI, observational evidence suggests a higher CO and oxygen delivery (DO2) may be beneficial to prevent its progression [98], although early goal-direct therapy, in general, does not impact AKI [99]. It is important to note that AKI may also occur in situations of normal or increased kidney perfusion pressure due to the development of intrarenal shunting and microcirculatory disturbances [50]. Every effort should be made to avoid severe hypotension, a definite cause for AKI, especially in situations of disturbed autoregulation. The ideal mean arterial pressure (MAP) to avoid AKI remains to be determined and might need to be tailored to patients' characteristics [100]. In 2463 sepsis patients aged>65 عامًا ، لم يرتبط "انخفاض ضغط الدم المسموح به" (60-65 ملم زئبق) بالحاجة إلى RRT أو زيادة معدل الوفيات النهارية 90- مقارنة بالرعاية المعتادة ؛ لم يتم تقييم AKI الأقل شدة على الرغم من [101]. من ناحية أخرى ، في تجربة معشاة ذات شواهد في مرضى الصدمة الإنتانية ، كان هدف MAP المنخفض مرتبطًا بمضاعفة الكرياتينين أو الحاجة إلى RRT في المجموعة الفرعية من المرضى المصابين بارتفاع ضغط الدم المزمن [102]. وبالمثل ، فإن الحفاظ على ضغط الدم الانقباضي في غرفة العمليات في غضون 10 في المائة من ضغط الدم الانقباضي أثناء الراحة أدى إلى حدوث انخفاض ملحوظ في الإصابة بالتهاب المفاصل الروماتويدي بعد الجراحة مقارنةً بالهدف الثابت (80 ملم زئبقي) في البالغين المعرضين لمخاطر عالية والذين يخضعون لعملية جراحية كبرى [103]. أظهرت دراسة بأثر رجعي لمرضى الصدمة الإنتانية ، مقسمة وفقًا للاختلاف بين MAP قبل المرضية وبعد الإنعاش ، أن حدوث AKI كان أقل بين أولئك الذين كانت MAP بعد الإنعاش الأقرب أو أعلى من MAP المرضية السابقة [ 104]. لذلك ، يبدو من المعقول أن اتباع نهج أكثر تخصيصًا ، يعتمد بشكل أساسي على القيم الموجودة مسبقًا ، ربما يكون الطريقة المثلى لإدارة ضغط الدم. بالإضافة إلى ذلك ، ينبغي إيلاء المزيد من الاهتمام لأهمية ضغط التروية الكلوي (MAP-CVP) [105 ، 106].
يختلف تأثير الأدوية المختلفة النشطة في الأوعية أو المؤثر في التقلص العضلي على وظائف الكلى وقد تعتمد على الحالة الأساسية. إن أكثر مقابض الأوعية الدموية استخدامًا للحفاظ على ضغط التروية الكلوي هو النوربينفرين [1 0 7]. لم يتم التحقيق بشكل جيد في تأثيرات فينيليفرين ، وهو ناهض نقي -1 ، على وظائف الكلى ، ولكن بدون دليل على الفائدة [1 0 8]. قد يكون للكاتيكولامينات آثار جانبية عند الجرعات العالية. الفازوبريسين Vasopressin ، وهو عبارة عن مقبس وعائي داخلي غير كاتيكولامين ، لديه القدرة على تقليص الشرايين الكبيبية الصادرة بشكل تفضيلي ، وبالتالي زيادة ضغط التروية الكبيبي وتوليد البول. أثناء استخدام Vasopressin vs Norepinephrine كعلاج أولي في تجربة الصدمة الإنتانية (VANISH) [1 0 9] ، كان عدد الأيام الخالية من الفشل الكلوي متماثلًا في المرضى الذين تلقوا النورأدرينالين أو الفازوبريسين ، كان المرضى في مجموعة الفازوبريسين انخفاض مستويات Scr وزيادة إنتاج البول في الأيام السبعة الأولى ، مما أدى إلى استخدام أقل لـ RRT (25.4٪ مقابل 35.3٪). خلص تحليل تلوي متضمن 4 تجارب معشاة ذات شواهد إلى أن الفازوبريسين قلل من متطلبات RRT (RR 0. 86 ، 95٪ CI 0.74–0.99) ، لكن هذه النتيجة لم تكن قوية لتحليلات الحساسية [110]. في الآونة الأخيرة ، أظهرت تجربة Vasopressin مقابل Norepinephrine في المرضى الذين يعانون من صدمة الأوعية الدموية بعد جراحة القلب (VANCS) نتيجة مركبة أولية أفضل بكثير في المرضى الذين تم اختيارهم عشوائياً لفازوبريسين مقابل النورإبينفرين ، وهو تأثير مدفوع بشكل أساسي بمعدل منخفض من AKI [111]. تم فحص حقنة أنجيوتنسين 2 مؤخرًا في المرضى الذين يعانون من الصدمة مما يدل على استقرار الدورة الدموية كما هو الحال مع النوربينفرين (ATHOS -3 ، [112]). أظهر تحليل لاحق لهذه التجربة أنه في مجموعة فرعية من المرضى في RRT ، كانت مدة RRT أقصر والبقاء على قيد الحياة أعلى في المرضى الذين تلقوا أنجيوتنسين 2 مقارنة بالنورادرينالين [113] ، وهي نتيجة تستدعي التأكيد. بطبيعة الحال ، يجب دائمًا موازنة التأثير المحتمل على وظائف الكلى مقابل الآثار الضارة المحتملة.

المؤشرات الحيوية لتوجيه الإدارة
اقترحت العديد من الدراسات التي أجريت على مركز واحد في المرضى الذين يخضعون لعملية جراحية كبرى أن بدء حزمة الوقاية من KDIGO في المرضى المعرضين لمخاطر عالية والتي تم تحديدها بواسطة المؤشرات الحيوية يمكن أن تقلل من حدوث وتطور القصور الكلوي الحاد مع ذلك ، دون تأثير مفيد على النتيجة المتمحورة حول المريض [17 ، 18]. كما تمت الدعوة إلى الإدارة الموجهة بالعلامات الحيوية للأدوية السامة للكلية كشكل من أشكال الإشراف على السموم الكلوية [114]. تمنع قوة الأدلة حاليًا الاستخدام الروتيني للواصمات الحيوية لتوجيه عملية صنع القرار بشأن متى يجب بدء RRT [115]. تم اكتشاف مؤشرات حيوية جديدة لعدم تعافي الكلى ، أي CCL14 [39]. يجب تحديد دورها المحتمل في توجيه بدء RRT في الدراسات المستقبلية. أظهرت دراسة أجريت على 162 مريضًا مصابين بالتهاب المفاصل الروماتويدي (AKI) أن اختبار الإجهاد فوروسيميد (FST) يتمتع بقدرة تنبؤية ممتازة للاستخدام اللاحق لـ RRT [116]. ومع ذلك ، لم يكن هناك فرق في النتيجة بين البدء المبكر مقابل البدء المعياري لـ RRT في غير المستجيبين FST.
أدوية جديدة
حتى الآن ، لا توجد أدوية أو علاجات محددة تمنع أو تعالج القصور الكلوي الحاد. أظهر RCT متعدد المراكز مؤخرًا أن الفوسفاتاز القلوي البشري المؤتلف (AP) ، وهو إنزيم يزيل الذيفان الداخلي و ATP ، لم يكن مرتبطًا بتحسن كبير في تصفية الكرياتينين الداخلي خلال الأيام السبعة الأولى. ومع ذلك ، كان تصفية الكرياتينين حتى اليوم 28 أفضل وكانت الوفيات الناجمة عن جميع الأسباب أقل [117]. تشمل العوامل الواعدة الأخرى المركبات الجديدة ، والأدوية المعاد توجيهها ، والعلاجات القائمة على الخلايا التي تستهدف مجموعة متنوعة من المسارات ، بما في ذلك إجهاد الميتوكوندريا ، واستقلاب الخلايا ، والالتهابات ، وتأثيرات مضادات الأكسدة ، وموت الخلايا المبرمج ، وآليات الإصلاح ، وديناميكا الدم الجهازية [118] (الجدول التكميلي 1). بعض هذه المركبات تتقدم من خلال التجارب السريرية المبكرة.
بدء RRT
أربعة من أصل خمسة تجارب معشاة ذات شواهد حديثة [119-124] (الجدول التكميلي 2) فشلت في إثبات فائدة البقاء على قيد الحياة من البدء المبكر في RRT ، في المرضى الذين ليس لديهم مؤشرات عاجلة واضحة. يوجد قلق بشأن الضرر المحتمل من البدء المبكر (انخفاض ضغط الدم ، نقص فوسفات الدم ، الاعتماد المطول لغسيل الكلى) ، ويبدو أن استراتيجية "المراقبة والانتظار" آمنة إلى حد معين [125]. قارنت تجربة AKIKI 2 الأخيرة "المتأخرة" مع البدء "المتأخر جدًا" لـ RRT ولم تظهر أي فرق في عدد الأيام الخالية من RRT بين المجموعتين [124] ولكن معدل الوفيات في اليوم {{7} كان أعلى في "المتأخر جدًا". ' ذراع. تفتقر الأدلة القوية لبدء الاستجابة السريعة الموجَّهة بالعلامات الحيوية [114]. لا يزال دور اختبار الجهد فوروسيميد قيد التحديد. في بعض المرضى ، قد يكون من المناسب اتخاذ قرار فردي أكثر [59].
نتيجة طويلة المدى بعد القصور الكلوي الحاد
أظهرت العديد من الدراسات بأثر رجعي ، والتي تستند في الغالب إلى قواعد البيانات الإدارية ، أن القصور الكلوي الحاد ، حتى بعد التعافي الكامل على ما يبدو ، يرتبط بنتائج غير مواتية طويلة الأجل ، بما في ذلك زيادة خطر الوفاة ، وحدوث أحداث القلب والأوعية الدموية ، وتطور (أو التقدم إلى). ) كد [2 ، 3]. تم تأكيد هذه النتائج مؤخرًا في مجموعة مستقبلية (دراسة ASSESS) بما في ذلك الناجين من المستشفى في عمر 3 أشهر مع أو بدون القصور الكلوي الحاد أثناء الاستشفاء بمتوسط متابعة لمدة 4 7- أعوام [126]. يبدو أن الخطر المتزايد للوفاة يسود على خطر الإصابة بمرض الكلى المزمن الجديد. الأسباب الرئيسية للوفيات هي أمراض القلب والأوعية الدموية والسرطان [3]. إلى جانب عوامل الخطر المتوقعة (على سبيل المثال ، العمر ، والأمراض المصاحبة ، وشدة القصور الكلوي الحاد) ، يبدو أن نمط الشفاء من القصور الكلوي الحاد مرتبط أيضًا بالوفيات طويلة الأجل [127 ، 128].
ما إذا كان ارتباط القصور الكلوي الحاد بأحداث القلب والأوعية الدموية على المدى الطويل مرتبطًا بعوامل الخطر المشتركة (مرض السكري ، ارتفاع ضغط الدم ، قصور القلب ، CKD الموجود مسبقًا) ، زيادة حدوث CKD (عامل خطر معروف لأمراض القلب والأوعية الدموية [76]) ، أو إلى علاقة سببية لم يتم إثباتها بشكل واضح ، لكن الأدلة تتراكم على أن القصور الكلوي الحاد نفسه قد يسرع من الإصابة بأمراض القلب والأوعية الدموية [3 ، 129] ، والتي من المحتمل أن تكون مرتبطة بإصابة أعضاء بعيدة ناجمة عن القصور الكلوي الحاد والتهاب جهازي (الحديث المتبادل للأعضاء). من المحتمل أن تكون الفيزيولوجيا المرضية متعددة العوامل. الجلكتين -3 ، وهي مادة تسبب التهاب القلب وتليف القلب والخلل الوظيفي القلبي قد تساهم في [83]. تم تحديد تنشيط RAAS بعد AKI أيضًا كوسيط لتلف القلب والأوعية الدموية AKI لأن Angiotensin II يؤدي إلى ارتشاح البلاعم والتهاب القلب وتليف عضلة القلب مما يؤدي في النهاية إلى ضعف القلب وفشل القلب [130]. تم توضيح خطر حدوث CKD الحادث والتقدمي في الدراسات بأثر رجعي والمستقبل [3 ، 126] ويمكن أن يسهم في نتائج سيئة على المدى الطويل. القصور الكلوي الحاد هو عامل خطر للبيلة البروتينية اللاحقة [131] ، وهو مؤشر مستقل للنتائج السلبية [126]. تشمل عوامل الخطر الأخرى لانتقال AKI-CKD مدة وشدة إصابة الكلى ، وكبر السن ، والحالات الصحية المزمنة ، بما في ذلك وظائف الكلى الأساسية. أظهرت دراسة ASSESS أن المرضى الذين يعانون من القصور الكلوي الحاد الذي يستمر لأكثر من 72 ساعة لديهم مخاطر أعلى للإصابة بمرض الكلى المزمن من أولئك الذين يعانون من أمراض الكلى المزمنة الحلوة وأن البيلة البروتينية في 3 أشهر كانت مؤشرًا قويًا على مزيد من التدهور في وظائف الكلى [132]. لم يتم توضيح الآليات الكامنة وراء انتقال AKI-CKD بشكل كامل ، ولكن يُعتقد أنها تشمل الإصلاح الأنبوبي غير القادر على التكيف ، وتلف الأوعية الدموية الدقيقة المستمر ، والالتهاب الذي يؤدي إلى التليف [133].
يتزايد الاعتراف بالحاجة إلى متابعة أفضل ورعاية طويلة الأمد للمرضى الذين يتعافون من أمراض القصور الكلوي الحاد أو أمراض القلب الرئوية. وقد طورت العديد من المؤسسات وأنظمة الرعاية الصحية عيادات متابعة القصور الكلوي الحاد [134]. ومع ذلك ، هناك أيضًا حاجة لمؤشرات جودة محددة ومقاييس جودة وتقدير أفضل لتأثير هذه المنظمات على النتائج التي تركز على المريض [135]. ظهرت مؤخرًا استراتيجيات للوقاية من المضاعفات طويلة المدى لمرض القصور الكلوي الحاد. أولاً ، الوقاية من نوبات القصور الكلوي الحاد (على سبيل المثال ، مع تجنب السموم الكلوية) أمر مهم [64 ، 136]. يعتبر التعرف على ارتفاع ضغط الدم أو مرض السكري أو السمنة وعلاجه من العوامل الرئيسية المحتملة لتحسين النتائج على المدى الطويل. في هذا الخط ، أظهرت دراسة قائمة على الملاحظة أن المتابعة من قبل أخصائي أمراض الكلى كانت مرتبطة بانخفاض معدل الوفيات لجميع الأسباب على المدى الطويل بعد القصور الكلوي الحاد [137] ، ولكن التنفيذ في الممارسة السريرية من شأنه أن يفرض عبئًا كبيرًا على مجتمع طب الكلى. هذا يستدعي متابعة طبقية للمخاطر [138] ، مدفوعة بالبروتينية [129] وتقدير GFR عند التفريغ ، يحتمل أن تكون مدعومة بمستويات العلامات الحيوية [11 ، 56 ، 139].
تبشر العديد من الاستراتيجيات الدوائية الواقية للقلب والكلى بتحسين نتائج ما بعد القصور الكلوي الحاد. يبدو أن الحد من عواقب تنشيط RAAS بعد AKI يحسن معدل الوفيات على المدى الطويل في المرضى الذين يتعافون من AKI [140]. ثبت مؤخرًا أن العلاجات بمضادات مستقبلات القشرانيات المعدنية الانتقائية أو مثبطات الناقل المشترك للجلوكوز والصوديوم -2 تحسن النتائج السريرية (معدل الوفيات أو تطور أمراض القلب والأوعية الدموية والأمراض القلبية الوعائية) في مرضى الكلى المزمن [141 ، 142]. يجب استكشاف ما إذا كانت هذه النتائج تترجم إلى نتائج أفضل لما بعد القصور الكلوي الحاد.

استنتاج
AKI هي متلازمة غير متجانسة قد تظهر في أنماط ظاهرية مختلفة ، ولا تنعكس في المعايير الحالية التي تحدد AKI. تعد التطورات الجديدة بما في ذلك العلامات الحيوية والتعلم الآلي بأن تكون أكثر حساسية وتوقعًا لتطور القصور الكلوي الحاد. بالإضافة إلى ذلك ، قد تكشف حركية العلامات الحيوية عن مزيد من التبصر في التسبب في المرض كما لوحظ في مجموعات AKI تحت الإكلينيكية المحددة. ومع ذلك ، هناك حاجة إلى التجارب السريرية لتقييم فائدتها الحقيقية. إذا كان الأمر كذلك ، فإن اتباع نهج أكثر تخصيصًا ، مع الأخذ في الاعتبار الفيزيولوجيا المرضية الأساسية ، قد يغير الطريقة التي ينظر بها إلى القصور الكلوي الحاد وإدارته في المستقبل. في هؤلاء المرضى الذين قد يحتاجون إلى RRI ، تتوفر الآن المزيد من البيانات السريرية المتعلقة بتوقيت البدء لتوضيح أن النهج المحجوز إلى حد ما مقبول. بالإضافة إلى ذلك ، أصبح من الواضح أنه ، بصرف النظر عن العواقب قصيرة المدى لـ AKI ، قد تحدث مضاعفات طويلة المدى في الناجين من AKI ومتابعة هذه المجموعة المحددة من المرضى تتطلب مزيدًا من الاهتمام.
مراجع
1 مرض K (2012) تحسين النتائج العالمية (KDIGO) مجموعة عمل إصابات الكلى الحادة (2012) إرشادات الممارسة السريرية لـ KDIGO: تعريف AKI. مكملات الكلى المركزة 2 (1): 19-36
2. Hoste EAJ، Kellum JA، Selby NM، Zarbock A، Palevsky PM، Bagshaw SM، et al (2018) علم الأوبئة العالمية ونتائج إصابة الكلى الحادة. نات ريف نفرول 14 (10): 607-625
3. James MT، Bhatt M، Pannu N، Tonelli M (2020) النتائج طويلة المدى لإصابة الكلى الحادة واستراتيجيات تحسين الرعاية. نات ريف نفرول 16 (4): 193-205
4. Kellum JA، Prowle JR (2018) نماذج إصابة الكلى الحادة في العناية المركزة. نات ريف نفرول 14 (4): 217-230
5. Schetz M ، Schortgen F (2017) عشرة أوجه قصور في التعريف الحالي لـ AKI. مركز العناية المركزة 43 (6): 911-913
6. Priyanka P ، Zarbock A ، Izawa J ، Gleason TG ، Renfurm RW ، Kellum JA (2020) تأثير إصابة الكلى الحادة بواسطة كرياتينين المصل أو معايير إخراج البول على أحداث الكلى العكسية الكبرى في مرضى جراحة القلب. J ثوراك كارديوفاسك سورج. https://doi.org/10.1016/j.jtcvs.2019. 11.137
7. Kellum JA، Sileanu FE، Murugan R، Lucko N، Shaw AD، Clermont G (2015) تصنيف AKI عن طريق إخراج البول مقابل مستوى كرياتينين المصل. J آم سوك نفرول 26 (9): 2231-2238
8. Ronco C، Bellomo R، Kellum J (2017) فهم احتياطي وظائف الكلى. مركز العناية المركزة 43 (6): 917-920
9. Chen S (2013) إعادة تجهيز معادلة تصفية الكرياتينين لتقدير معدل الترشيح الكبيبي الحركي عندما يتغير كرياتينين البلازما بشكل حاد. J آم سوك نفرول 24 (6): 877-888
10. Schneider AG، Molitoris BA (2020) معدل الترشيح الكبيبي في الوقت الحقيقي: تحسين الحساسية والدقة والقيمة الإنذارية في إصابة الكلى الحادة. العناية الحرجة بالعملات 26 (6): 549-555
11. Ostermann M ، Zarbock A ، Goldstein S ، Kashani K ، ماسيدو E ، Murugan R ، وآخرون. توصيات بشأن المؤشرات الحيوية لإصابة الكلى الحادة من مؤتمر إجماع مبادرة جودة الأمراض الحادة: بيان إجماع. جاما نتو مفتوح. 2020 ؛ 3 (10): e2019209.
12. كاشاني ك ، الخفاجي أ ، أرديليس تي ، أرتيجاس أ ، باجشو إس إم ، بيل إم ، وآخرون (2013) اكتشاف والتحقق من المؤشرات الحيوية لتوقف دورة الخلية في إصابة الكلى الحادة للإنسان. العناية الحرجة (لندن ، إنجلترا) 17 (1): R25
13. Hoste EA ، McCullough PA ، Kashani K ، Chawla LS ، Joannidis M ، Shaw AD ، وآخرون (2014) اشتقاق والتحقق من عمليات القطع للاستخدام السريري للعلامات الحيوية لتوقف دورة الخلية. Nephrol Dial Transpl 29 (11): 2054-2061
14. Su LJ ، Li YM ، Kellum JA ، Peng ZY (2018) القيمة التنبؤية للعلامات الحيوية لتوقف دورة الخلية لإصابة الكلى الحادة المرتبطة بجراحة القلب: التحليل التلوي. Br J Anaesth 121 (2): 350–357
15. Zhang D و Yuan Y و Guo L و Wang Q (2019) مقارنة بين قطع البول TIMP -2 و IGFBP7 للتنبؤ بإصابة الكلى الحادة في المرضى المصابين بأمراض خطيرة: مراجعة منهجية متوافقة مع PRISMA وتحليل تلوي . الطب (بالتيمور) 98 (26): e16232
16. Albert C ، Zapf A ، Haase M ، Rover C ، Pickering JW ، Albert A ، et al. (2020) الليبوكسين المرتبط بالجيلاتيناز العدلات المُقاس على منصات المختبرات السريرية للتنبؤ بإصابة الكلى الحادة والحاجة المرتبطة بها لعلاج غسيل الكلى: مراجعة منهجية وتحليل تلوي. Am J Kidney Dis 76 (6): 826-41 e1.
17. Meersch M ، Schmidt C ، Hofmeier A ، Van Aken H ، Wempe C ، Gerss J ، وآخرون (2017) الوقاية من AKI المرتبط بجراحة القلب من خلال تنفيذ إرشادات KDIGO في المرضى المعرضين لمخاطر عالية التي تم تحديدها بواسطة المؤشرات الحيوية: تم توزيع PrevAKI بشكل عشوائي محاكمة خاضعة للرقابة. مركز العناية المركزة 43 (11): 1551-1561
18. Göcze I ، Jauch D ، Götz M ، Kennedy P ، Jung B ، Zeman F ، وآخرون (2018) التدخل الموجه بالعلامات الحيوية للوقاية من إصابة الكلى الحادة بعد الجراحة الكبرى: دراسة BigpAK العشوائية المرتقبة. آن سورج 267 (6): 1013-1020
19. حسين سيد إف ، فيراري إف ، شارما إيه ، دانيسي تي إتش ، بيزيرا بي ، لوبيز جياكومان إس ، وآخرون (2018) يتنبأ الاحتياطي الوظيفي الكلوي قبل الجراحة بخطر إصابة الكلى الحادة بعد إجراء عملية القلب. آن ثوراك سورج 105 (4): 1094-1101
20. حسين سيد إف ، فيراري إف ، شارما إيه ، هينا دانيسي تي ، بيزيرا بي ، لوبيز جياكومان إس ، وآخرون (2019) الانخفاض المستمر في احتياطي وظائف الكلى لدى المرضى بعد إصابة الكلى الحادة المرتبطة بجراحة القلب على الرغم من التعافي السريري . زرع الكلى لغسيل الكلى 34 (2): 308-317
21. Hoste EA، Kashani K، Gibney N، Wilson FP، Ronco C، Goldstein SL et al (2016) تأثير التنبيه الإلكتروني لإصابة الكلى الحادة: بيانات مجموعة العمل من مؤتمر إجماع ADQI الخامس عشر. Can J Kidney Health Dis 3:10
22. Al-Jaghbeer M، Dealmeida D، Bilderback A، Ambrosino R، Kellum JA (2018) دعم القرار السريري لـ AKI داخل المستشفى. J آم سوك نفرول 29 (2): 654-660
23. Colpaert K، Hoste EA، Steurbaut K، Benoit D، Van Hoecke S، De Turck F et al (2012) تأثير التنبيه الإلكتروني في الوقت الحقيقي لإصابة الكلى الحادة على التدخل العلاجي وتطور فئة RIFLE. Crit Care Med 40 (4): 1164-1170
24. De Vlieger G، Kashani K، Meyfroidt G (2020) الذكاء الاصطناعي لتوجيه إدارة إصابات الكلى الحادة في وحدة العناية المركزة: مراجعة سردية. العناية الحرجة للعملات 26 (6): 563-573
25. Gameiro J ، Branco T ، Lopes JA (2020) الذكاء الاصطناعي في التنبؤ بمخاطر إصابات الكلى الحادة. J كلين ميد. 9 (3): 678.
26. Flechet M ، Guiza F ، Schetz M ، Wouters P ، Vanhorebeek I ، Derese I et al (2017) متنبئ AKI ، آلة حاسبة للتنبؤ على الإنترنت لإصابة الكلى الحادة لدى المرضى البالغين المصابين بأمراض خطيرة: التطوير والتحقق والمقارنة مع جيلاتينيز العدلات المصل - ليبوكالين المرتبط. مركز العناية المركزة 43 (6): 764-773
27. Koyner JL، Carey KA، Edelson DP، Churpek MM (2018) تطوير نموذج التعلم الآلي للتنبؤ بإصابات الكلى الحادة للمرضى الداخليين. Crit Care Med 46 (7): 1070-1077
28. Chiofolo C، Chbat N، Ghosh E، Eshelman L، Kashani K (2019) التنبؤ الآلي المستمر بإصابات الكلى الحادة والمراقبة: نموذج غابة عشوائي. مايو كلين بروك 94 (5): 783-792
29. Churpek MM ، Carey KA ، Edelson DP ، Singh T ، Astor BC ، Gilbert ER ، وآخرون (2020) التحقق الداخلي والخارجي من درجة مخاطر التعلم الآلي لإصابة الكلى الحادة. JAMA Netw Open 3 (8): e2012892
30. Chaudhary K ، Vaid A ، Dufy A ، Paranjpe I ، Jaladanki S ، Paranjpe M ، وآخرون (2020) استخدام التعلم العميق لتحديد النمط الفرعي في إصابة الكلى الحادة المرتبطة بالإنتان. Clin J Am Soc Nephrol 15 (11): 1557-1565
31. Wiersema R ، Jukarainen S ، Vaara ST ، Poukkanen M ، Lakkisto P ، Wong H ، et al (2020) يرتبط نوعان فرعيان من إصابة الكلى الحادة الإنتانية بمختلف 90- الوفيات اليومية والتعافي الكلوي. العناية الحرجة (لندن ، إنجلترا) 24 (1): 150
32. Chawla LS، Bellomo R، Bihorac A، Goldstein SL، Siew ED، Bagshaw SM، et al (2017) أمراض الكلى الحادة والتعافي الكلوي: تقرير إجماع حول مبادرة جودة الأمراض الحادة (ADQI) 16 Workgroup. نات ريف نفرول 13 (4): 241-257
33. Pons B ، Lautrette A ، Oziel J ، Dellamonica J ، Vermesch R ، Ezingeard E ، وآخرون (2013) الدقة التشخيصية للتغيرات المبكرة في مؤشر المسالك البولية في التمييز العابر عن إصابة الكلى الحادة المستمرة في المرضى المصابين بأمراض خطيرة: دراسة جماعية متعددة المراكز. العناية الحرجة (لندن ، إنجلترا) 17 (2): R56
34. Darmon M، Bourmaud A، Reynaud M، Rouleau S، Meziani F، Boivin A، et al (2018) أداء مؤشر المقاومة المعتمد على دوبلر والتروية الكلوية شبه الكمية في توقع استمرار القصور الكلوي الحاد: نتائج دراسة مستقبلية متعددة المراكز. طب العناية المركزة 44 (11): 1904-1913
35. Coca SG ، Nadkarni GN ، Garg AX ، Koyner J ، Thiessen-Philbrook H ، McArthur E ، وآخرون (2016) أول مؤشرات حيوية لإصابة الكلى البولية بعد الجراحة والارتباط بمدة AKI في TRIBE-AKI Cohort. بلوس واحد 11 (8): e0161098
36. ميرش إم ، شميدت سي ، فان أكين إتش ، مارتينز إس ، روسينت جي ، سينغبارتل ك ، وآخرون (2014) Urinary TIMP -2 و IGFBP7 كمؤشرات بيولوجية مبكرة لإصابة الكلى الحادة والتعافي الكلوي بعد جراحة القلب. بلوس واحد 9 (3): e93460
37. Legrand M ، Jacquemod A ، Gayat E ، Collet C ، Giraudeaux V ، Launay JM ، وآخرون (2015) فشل المؤشرات الحيوية الكلوية في التنبؤ بتدهور وظائف الكلى في المرضى المعرضين لمخاطر عالية والذين يعانون من قلة البول. طب العناية المركزة 41 (1): 68-76
38. Titeca-Beauport D ، و Daubin D ، و Van Vong L ، و Belliard G ، و Bruel C ، و Alaya S et al (2020) تميز المؤشرات الحيوية لتوقيف دورة خلية البول بشكل سيء بين AKI العابرة والمستمرة في الصدمة الإنتانية المبكرة: دراسة مستقبلية متعددة المراكز. العناية الحرجة (لندن ، إنجلترا) 24 (1): 280
39. Hoste E، Bihorac A، Al-Khafaji A، Ortega LM، Ostermann M، Haase M، et al (2020) تحديد والتحقق من المؤشرات الحيوية لإصابة الكلى الحادة المستمرة: دراسة RUBY. طب العناية المركزة 46 (5): 943-953
40. Dewitte A، Joannes-Boyau O، Sidobre C، Fleureau C، Bats ML، Derache P، et al (2015) Kinetic eGFR and new AKI Markers للتنبؤ بالشفاء الكلوي. Clin J Am Soc Nephrol 10 (11): 1900-1910
41. Koyner JL ، Davison DL ، Brasha-Mitchell E ، Chalikonda DM ، Arthur JM ، Shaw AD ، et al (2015) اختبار إجهاد فوروسيميد والمؤشرات الحيوية للتنبؤ بشدة القصور الكلوي الحاد. J Am Soc Nephrol 26 (8): 2023-2031
42. Chen JJ، Chang CH، Huang YT، Kuo G (2020) اختبار الإجهاد فوروسيميد كعلامة تنبؤية لتطور إصابة الكلى الحادة أو العلاج بالبدائل الكلوية: مراجعة منهجية وتحليل تلوي. العناية الحرجة (لندن ، إنجلترا) 24 (1): 202
43. Barasch J، Zager R، Bonventre JV (2017) إصابة الكلى الحادة: مشكلة التعريف. لانسيت 389 (10071): 779-781
44. Xu K ، Rosenstiel P ، Paragas N ، Hinze C ، Gao X ، Huai Shen T ، وآخرون (2017) تحدد برامج النسخ الفريدة الأنواع الفرعية من AKI. J Am Soc Nephrol 28 (6): 1729-1740
45. Mar D، Gharib SA، Zager RA، Johnson A، Denisenko O، Bomsztyk K (2015) الكلية الدولية 88 (4): 734-744
46. Garofalo AM ، Lorente-Ros M ، Goncalvez G ، Carriedo D ، Ballén-Barragán A ، Villar-Fernández A et al (2019) التغيرات النسيجية المرضية لخلل الأعضاء في الإنتان. العناية المركزة Med Exp 7 (ملحق 1): 45
47. Ahmad T، Jackson K، Rao VS، Tang WHW، Brisco-Bacik MA، Chen HH et al (2018) لا يرتبط تدهور وظائف الكلى لدى مرضى قصور القلب الحاد الذين يخضعون لإدرار البول بإصابة أنبوبية. التداول 137 (19): 2016-2028
48. Rao VS، Ahmad T، Brisco-Bacik MA، Bonventre JV، Wilson FP، Siew ED، et al (2019) الآثار الكلوية للإزالة المكثفة للحجم في مرضى قصور القلب الذين يعانون مسبقًا من تدهور وظائف الكلى. Circ Heart Fail 2 (6): e005552
49. Yoshioka K، Matsue Y، Okumura T، Kida K، Oishi S، Akiyama E et al (2020) تأثير تقليل الببتيد الناتريوتريك في الدماغ على تدهور وظائف الكلى في المرضى الذين يعانون من قصور القلب الحاد. بلوس ون 15 (6): e0235493
50. Peerapornratana S، Manrique-Caballero CL، Gómez H، Kellum JA (2019) إصابة الكلى الحادة من الإنتان: المفاهيم الحالية ، وعلم الأوبئة ، والفيزيولوجيا المرضية ، والوقاية ، والعلاج. الكلى Int
96 (5): 1083-1099 علم الأوبئة ، الفيزيولوجيا المرضية ، الوقاية والعلاج. الكلى Int
96(5):1083–1099
51. Gomez H و Ince C و De Backer D و Pickkers P و Payen D و Hotchkiss J et al (2014) نظرية موحدة لإصابة الكلى الحادة الناجمة عن الإنتان: الالتهاب واختلال الدورة الدموية الدقيقة والطاقة الحيوية وتكيف الخلايا الأنبوبية مع الإصابة . الصدمة (أوغوستا ، جا) 41 (1): 3-11
52. Radi ZA (2018) الممرض المناعي لإصابة الكلى الحادة. توكسيكول باثول 46 (8): 930-943
53. Poyan Mehr A ، Tran MT ، Ralto KM ، Leaf DE ، Washco V ، Messmer J ، وآخرون (2018) De novo NAD (بالإضافة إلى) ضعف التخليق الحيوي في إصابة الكلى الحادة لدى البشر. نات ميد 24 (9): 1351-1359
54. Kellum JA، Chawla LS (2016) توقف دورة الخلية وإصابة الكلى الحادة: الجوانب المضيئة والمظلمة. زراعة الطلب الكلوي 31 (1): 16-22
55. Hayek SS ، Leaf DE ، Samman Tahhan A ، Raad M ، Sharma S ، Waikar SS et al (2020) مستقبل urokinase القابل للذوبان وإصابة الكلى الحادة. إن إنجل جي ميد 382 (5): 416-426
56. Schunk SJ و Zarbock A و Meersch M و Kullmar M و Kellum JA و Schmit D et al (2019) الرابطة بين dickko pf البولي -3 وإصابة الكلى الحادة وفقدان وظائف الكلى لاحقًا في المرضى الذين يخضعون لجراحة قلبية : دراسة الأتراب القائمة على الملاحظة. لانسيت (لندن ، إنجلترا) 394 (10197): 488-496
57. Bhatraju PK و Zelnick LR و Herting J و Katz R و Mikacenic C و Kosamo S et al (2019) تحديد الأنماط الفرعية لإصابة الكلى الحادة ذات التوقيعات الجزيئية المختلفة والاستجابات للعلاج بالفازوبريسين. Am J Respir Crit Care Med 199 (7): 863 - 872
58. Bhatraju PK، Cohen M، Nagao RJ، Morrell ED، Kosamo S، Chai XY، et al (2020) التباين الجيني يورط أنجيوبويتين البلازما -2 في تطور أنماط فرعية لإصابة الكلى الحادة. BMC Nephrol 21 (1): 284
59. Ostermann M ، Bellomo R ، Burdmann EA ، Doi K ، Endre ZH ، Goldstein SL ، et al. الخلافات في إصابة الكلى الحادة: استنتاجات من مؤتمر أمراض الكلى: تحسين النتائج العالمية (KDIGO). الكلى الدولية. 2020 ؛ 98 (2): 294-309.
60. McDonald JS، McDonald RJ، Williamson EE، Kallmes DF، Kashani K (2017) إصابة الكلى الحادة بعد التباين في مرضى وحدة العناية المركزة: دراسة معدلة درجة الميل. طب العناية المركزة 43 (6): 774-784
61. Hinson JS، Al Jalbout N، Ehmann MR، Klein EY (2019) إصابة الكلى الحادة عقب إعطاء وسائط التباين في المريض الإنتاني: تحليل بأثر رجعي مطابق للميل. J Crit Care 51: 111-116
62. Miyamoto Y، Iwagami M، Aso S، Yasunaga H، Matsui H، Fushimi K، et al (2019) العلاقة بين التعرض لوسائط التباين الوريدي وعدم التعافي من إصابة الكلى الحادة الإنتانية التي تتطلب غسيل الكلى: دراسة رصدية على الصعيد الوطني. طب العناية المركزة 45 (11): 1570-1579
63. Rouve E ، Lakhal K ، Salmon Gandonnière C ، Jouan Y ، Bodet-Contentin L ، Ehrmann S (2018) نقص تأثير وسائط التباين المعالج باليود على المؤشرات الحيوية لتوقف دورة خلايا الكلى في المرضى المصابين بأمراض خطيرة. BMC Nephrol 19 (1): 308
64. Joannidis M، Druml W، Forni LG، Groeneveld ABJ، Honore PM، Hoste E، et al (2017) الوقاية من إصابة الكلى الحادة وحماية وظائف الكلى في وحدة العناية المركزة: تحديث 2017: رأي الخبراء لمجموعة العمل حول الوقاية ، قسم أمراض القصور الكلوي الحاد ، الجمعية الأوروبية لطب العناية المركزة. مركز العناية المركزة 43 (6): 730-749
65. Davenport MS ، Perazella MA ، Yee J ، Dillman JR ، Fine D ، McDonald RJ et al (2020) استخدام وسائط التباين الميودنة عن طريق الوريد في مرضى الكلى: بيانات إجماع من الكلية الأمريكية للأشعة والمؤسسة الوطنية للكلى. الأشعة 294 (3): 660-668
66. Tamil RJ ، Kooiman J ، Sijpkens YWJ ، de Vries JPM ، Verberk-Jonkers I ، Brulez HFH et al (2020) تأثير عدم الترطيب مقابل ترطيب بيكربونات الصوديوم قبل التصوير المقطعي المحوسب المعزز بالتباين في الوقاية من الكلى الحادة بعد التباين إصابة البالغين المصابين المزمنة
أمراض الكلى: تجربة سريرية عشوائية كومباس. JAMA Intern Med 180 (4): 533-541
67. Weisbord SD ، Gallagher M ، Jneid H ، Garcia S ، Cass A ، Thwin SS ، وآخرون (2018) النتائج بعد تصوير الأوعية باستخدام بيكربونات الصوديوم وأسيتيل سيستئين. إن إنجل جي ميد 378 (7): 603-614
68. Arnaud FCS، Libório AB (2020) السمية الكلوية المنسوبة للفانكومايسين في المرضى المصابين بأمراض خطيرة: دراسة نموذجية هيكلية هامشية. ياء أنتيميكروب كيميوثر 75 (4): 1031-1037
69. Tsutsuura M ، Moriyama H ، Kojima N ، Mizukami Y ، Tashiro S ، Osa S et al (2021) الجرعات الموجهة. BMC تصيب ديس 21 (1): 153
