زرع جراثيم البراز في الحد من تراكم السموم اليوريمية في أمراض الكلى: الفهم الحالي والآفاق المستقبلية
Aug 08, 2023
الملخص: خلال العقود الماضية ، ظهر ميكروبيوم الأمعاء كلاعب رئيسي فيمرض كلوي. تعتبر السموم البوليسية المرتبطة بدسباقتريوزس جنبًا إلى جنب مع الوسطاء المؤيدين للالتهابات من العوامل الرئيسية في أتدهور وظائف الكلى. تم توثيق سمية مركبات اليوريمي جيدًا في عدد كبير من الآليات الفيزيولوجية المرضية فيمرض كلوي، مثل إصابة القلب والأوعية الدموية (CVI) والخلل الأيضي والتهاب. دعم البيانات المتراكمة حول التأثير الضار للمذابات اليوريمية في أمراض الكلى تطوير العديد من الاستراتيجيات لاستعادة eubiosis. انتشر زرع جراثيم البراز (FMT) كعلاج مشجع لمختلف الاضطرابات المرتبطة ب dysbiosis. في هذا السيناريو ، تشير الدراسات المزدهرة إلى أن زرع البراز يمكن أن يمثل علاجًا جديدًا لتقليل تراكم السموم البوليسية. هنا ، نقدم أحدث ما توصلت إليه التكنولوجيا فيما يتعلق بتطبيق FMT على أمراض الكلى لاستعادة eubiosis وعكس الاحتفاظ بالسموم البوليسية.
الكلمات المفتاحية: زرع جراثيم البراز. PBUTs ؛فشل كلوي مزمن; إصابة الكلى الحاد; زرع الكلى؛ السموم اليوريمية FMT عن طريق الفم
المساهمة الرئيسية: سموم اليوريميك هي المساهم الرئيسي في تطور مضاعفات اليوريم أثناء الحادة أو المزمنةضعف كلويوتضر بالعديد من الوظائف الفسيولوجية. بناءً على هذا الدليل ، فإن توظيف FMT لـمرض كلوييمكن أن يمثل استراتيجية واعدة للحد من PBUT.

انقر هنا لمعرفة مكملات القسطرة لمرض الكلى
1. ميكروبيوم الأمعاء في الصحة وأمراض الكلى
يتكون النظام البيئي الصحي للميكروبات المعوية من تريليونات من الكائنات الحية الدقيقة التي تلعب وظيفة محورية في الحفاظ على التوازن من خلال التأثير على الحالة الأيضية والأكسدة والمعرفية والدفاع المناعي ضد العدوى المسببة للأمراض. يعرض كل فرد ملفًا ميكروبيًا فريدًا في حياته المبكرة اعتمادًا على تاريخ الحمل ونوع الولادة وطرق تغذية الحليب والجنس والجنس. في مرحلة البلوغ ، تظل هذه الميكروبات الأصلية الصحية مستقرة نسبيًا ، على الرغم من عدة عوامل بما في ذلك مؤشر كتلة الجسم (BMI) ، والتمارين الرياضية ، والعادات الغذائية ، والعلاجات الدوائية (مثل المضادات الحيوية) ، والشيخوخة التي يمكن أن تغير تركيبها [1]. وفقًا لدراسات واسعة النطاق ، يرتبط التنوع الجرثومي العالي والثراء في الشُّعَب والأجناس والأسر بحالة معوية صحية ومفيدة [2،3]. بشكل أكثر تحديدًا ، تم وصف وفرة بعض الأنماط المعوية مثل Bifidobacterium Bififidum أو Lactobacillus acidophilus أو Streptococcus thermophilus على نطاق واسع بأنها مفيدة للاستجابة المناعية الفعالة [4،5]. علاوة على ذلك ، تم العثور على بكتيريا تنتمي إلى فصيلة المطثيات ، Bififidobacteriaceae ، وعائلات Bacteroidaceae في المجتمعات الميكروبية من المعمرين ، مما يشير إلى أن هذه الظاهرة يمكن أن تقلل من ضعف الجهاز المناعي المرتبط بالعمر [6].
في هذا السيناريو ، يمثل dysbiosis كلاً من التغيير الهيكلي والوظيفي للميكروبيوم المرتبط ارتباطًا وثيقًا بمرض معين. الأهم من ذلك ، يوضح التحليل الميتاجينومي المقارن الاختلافات في ملامح ميكروبيوم الأمعاء بين الحالات المرضية وغير المرضية. على سبيل المثال ، تتميز الأمراض المزمنة (مثل التهاب المفاصل الروماتويدي ، ومرض التهاب الأمعاء (IBD) ، والسكري ، وما إلى ذلك) بتنوع وثراء ميكروبيين أقل ، ومستويات أعلى من البكتيريا الضارة ، ونسبة غير طبيعية من العوامل الثابتة / الجراثيم [7-9] . من ناحية أخرى ، تشير هذه الدراسات أيضًا إلى حدوث اختلافات في ملف تعريف الميكروبيوم بين الأمراض.
على مدى العقد الماضي ، أثار الحديث المتبادل بين ميكروبيوم الأمعاء والأمراض البشرية اهتمامًا متزايدًا بالعديد من الأمراض المعوية وخارجها ، مثل الأمراض الالتهابية المزمنة ، والضعف الأيضي ، والاضطراب العصبي ، وأمراض القلب والأوعية الدموية [10]. في سياق مرض الكلى ، لا يزال من الضروري توضيح ما إذا كان خلل التنسج المعوي يمثل سببًا أم نتيجة حيث تم التعرف على دورة ضارة بين بولينا الدم وميكروبيوم الأمعاء [11]. أثبتت مجموعة كبيرة من البيانات أن التغيير في ترتيب الميكروبيوم يمثل نتيجةإصابة في الكلىويؤدي بشدة إلى تفاقمه بسبب تراكم السموم المشتقة من البكتيريا المتشعبة [11 ، 12].

إجمالاً ، يتميز المجتمع المعوي اليوريمي بنسبة عالية من البكتريا الشعاعية ، والبكتيرويد ، والثبات ، والتي نادراً ما توصف في الظروف الصحية [13]. وفقًا للعديد من الدراسات الميتاجينومية ، يُظهر مرضى CKD تغيرات في التعبير عن الرنا الريباسي 16S المرتبط بعائلة Enterobacteriaceae (على سبيل المثال ، Enterobacter و Klebsiella و Escherichia genera) ، مما يشير إلى أن البكتيريا سالبة الجرام تمثل مكونًا أساسيًا للنباتات البوليسية [13 ، 14]. وفرة اليورياز ، وهو اليوريك المصحوب ببكتيريا التربتوفاناز-التيروزين الفينول-لياز الموجبة (على سبيل المثال ، أكتينوميسيتيا ، ميثيلوكوكاسي ، ميكروكوكسينيا ، بسيودوموناداليس ، ألتروموناداليس ، ميكروكوركلس ، هالوموناداسي ، وسودوموناداسيا المعترف بها) نشاطها الحال للبروتين في إنتاج السموم اليوريمية [15،16]. بالإضافة إلى ذلك ، ارتبط النمو المرتفع للبكتريا والمطثيات مع الالتهاب الجهازي [17]. من ناحية أخرى ، يعكس الانخفاض الكبير في النسبة النسبية لكل من العصيات اللبنية وشعبة البكتيريا الشعاعية جنبًا إلى جنب مع انخفاض تكاثر عائلات Prevotellaceae و Bacteroidacee تراجعًا في إنتاج الأحماض الدهنية قصيرة السلسلة (SCFAs) [17 ، 18]. وتجدر الإشارة أيضًا إلى أن الاختلافات في ملامح ميكروبيوم الأمعاء تحدث ليس فقط بين مراحل CKD ولكن أيضًا بينأمراض الكلىتتميز بأنماط ظاهرية مختلفة. على سبيل المثال ، تبين أن مرضى غسيل الكلى (HD) يظهرون عدم تناسق في البكتريا Gammaproteobacteria و Firmicutes عند مقارنتها بمرضى ما قبل غسيل الكلى [13 ، 19]. علاوة على ذلك ، يبدو أن اعتلال الكلية بالجلوبيولين المناعي (IgA) يتميز بكمية كبيرة من العديد من المجموعات الميكروبية ، بما في ذلك Streptococcus و Paraprevotella [20،21]. ومن المثير للاهتمام ، أن العديد من الدراسات أشارت إلى زيادة تخصيب Escherichia-Shigella فيتلف الكلى المرتبط بمرض السكري[22]. من ناحية أخرى ، ارتبط النمو المفرط للبكتيريا اللاهوائية والبلوتية بالاختلالات الأيضية في اعتلال الكلية السكري (DN) [23 ، 24]. ومن المثير للاهتمام ، أن الأدلة الحديثة قد أشارت إلى أن دسباقتريوز الأمعاء يحدث أيضًا فيإصابة الكلى الحاد(آكي) [25]. على سبيل المثال ، Andrianova et al. أظهر من خلال دراسة في الجسم الحي أن التغيرات في تكوين الميكروبيوم حدثت بعد إصابة نقص التروية الكلوية / إعادة التروية (IRI) ، وأن العديد من البكتيريا بما في ذلك Rothia و Staphylococcus كانت مرتبطة بدرجة عالية من الإصابة [26]. تماشياً مع هذا البحث ، أظهر يانغ وزملاؤهم أن البكتيريا المرتبطة بالـ AKI ساهمت في تفاقم التلف الكلوي والالتهاب ونفاذية الأمعاء عند زرعها في حيوانات خالية من الجراثيم [27]. أخيرًا ، أبرزت البيانات الحديثة تورط دسباقتريوز والسموم البوليسية بعد زرع الأعضاء الصلبة ، بما في ذلكزرع الكلى. بالتفصيل ، كشف تحليل 16S لمرضى زرع الكلى عن اضطراب عميق في التنوع الميكروبي المرتبط بإثراء السموم البوليسية المنتجة للبكتيريا المعوية (28 ، 29). بناءً على هذه الأدلة ، يمكن أن تمثل الاستراتيجيات التي تهدف إلى استعادة eubiotics ومستويات المستقلبات المرتبطة بالميكروبيوم علاجًا واعدًا لـمرض كلوي. ومع ذلك ، فإن التغيير في تكوين الميكروبيوم ليس بالضرورة سلبيًا ؛ يمكن تعديل تركيبة الميكروبيوم واستيعابها من خلال تدخلات مثل النظام الغذائي لمنطقة البحر الأبيض المتوسط ، والمكملات (البروبيوتيك ، والبريبايوتكس ، و Ω -3 الأحماض الدهنية) أو التمارين التي تؤثر على الحالة الالتهابية ، والتي يمكن أن تبطئ من تقدم مرض الكلى المزمن [30-32].

المعرفة المتزايدة للتأثير الضار ل dysbiosis فيمرض كلويدعم تطوير العديد من الاستراتيجيات المستهدفة لاستعادة مستوى السموم البوليسية. في المقام الأول ، كانت التدخلات العلاجية القائمة على المكملات الحيوية تهدف إلى منع توليد PBUTs عن طريق إعادة التوازن إلى توازن فلورا الجهاز الهضمي. ومع ذلك ، فإن عددًا كبيرًا من عناصر الخلط ، مثل فترة الإعطاء ، وكمية البكتيريا ، واختيار السلالة يعيق تفسير النتيجة وتوحيد الطريقة. في هذا السيناريو ، يمكن أن يمثل التلاعب بالميكروبات بواسطة FMT علاجًا جديدًا لتقليل سمية اليوريم في مرضى CKD. لذلك ، يسلط هذا الاستعراض الشامل الضوء على المعرفة الحالية لدور زرع البراز في سياقمرض كلوي، مما يوفر نظرة ثاقبة للاستراتيجية القائمة على FMT لتصحيح مستويات السموم البوليسية.
2. محور الأمعاء والكلى
عندما ينخفض معدل الترشيح الكبيبي ، تتراكم كمية كبيرة من مركبات الهدم السامة النيتروجينية (مثل اليوريا والبول) في دم مرضى الكلى المزمن [33]. على هذه الخلفية ، يتم دعم إزالة هذه السموم بواسطة الأمعاء ، مما يؤدي إلى الاحتفاظ بها في تجويف الأمعاء. ونتيجة لذلك ، فإن البيئة اليوريمية تعزز خلل التنسج المستمر الذي يتميز باختلال توازن البكتيريا المحللة للبروتين على حساب المجتمعات المحللة للسكريات. وبالتالي ، فإن نشاط اليورياز القوي جنبًا إلى جنب مع التخمير المكثف للبروتين يعزز تحويل اليوريا والأحماض الأمينية (على سبيل المثال ، التيروزين ، التربتوفان) في المركبات السامة ، المسماة سموم اليوريم [11]. أظهرت العديد من الدراسات أن الاحتفاظ بهذه المركبات يؤثر بشدة على سلامة الغشاء المخاطي في الأمعاء عن طريق تحفيز الأمعاء المتسربة والتهاب الموضعي. تماشياً مع هذا الدليل ، لوحظ ضعف ملحوظ في التقاطعات الظهارية بما في ذلك CLDN و OCLN و Zonula occludens - 1 ، داخل الحاجز المعوي للعديد من النماذج الحيوانية من CKD [34-36]. بالإضافة إلى ذلك ، فإن إزاحة عدد كبير من السموم في الدورة الدموية جنبًا إلى جنب مع تحفيز فرع الاستجابة المناعية يسبب التهابًا مفرطًا جهازيًا ويؤدي إلى تلف العديد من الأعضاء [37] (الشكل 1).

الشكل 1: التأثير الضار لتراكم السموم البوليسية المشتق من الجراثيم والمرتبط بأمراض الكلى.
2.1. السموم اليوريميك في كد
تعتبر سموم اليوريميك المساهم الرئيسي في تطور المضاعفات اليوريمية أثناء ضعف الكلى الحاد أو المزمن وتضر بالعديد من الوظائف الفسيولوجية. وفقًا لوزنها الجزيئي وخصائصها ، يتم تصنيفها عادةً إلى مواد مذابة صغيرة (<0.5 kDa), middle-weight molecules (0.5–60 kDa), and protein-bound uremic toxins (PBUTs) [38]. Small solutes (creatinine, urea) are usually successfully removed by conventional hemodialysis techniques. The second category includes peptides and proteins with middle-molecular weight molecules, such as b2 microglobulin and alfa1-macroglobulin. In patients with وظائف الكلى الطبيعية، التخلص الكلوي يمثل 30-80 في المائة من الإزالة الكلية ، بينما أثناء الإصابة الكلوية ، قد يتم تغيير إزالة هذه المركبات بشكل كبير. تتضمن الفئة الأخيرة من السموم اليوريمية (PBUTs) جزيئات ذات وزن جزيئي منخفض نسبيًا تقدم خصائص أيونية أو كارهة للماء والتي من خلالها ترتبط بشدة بالألبومين في الدم [39 ، 40]. في المرضى الذين يعانون من وظائف الكلى الطبيعية ، يتم التخلص منها عادة بواسطة ناقلات الأنيون العضوية (OATs) في الأنابيب القريبة [41]. على الرغم من أن غسيل الكلى التقليدي هو التقنية الرئيسية المستخدمة لتقليل السموم اليوريمية ، فقد ثبت أنه أكثر فاعلية في التخلص من المركبات الصغيرة القابلة للذوبان في الماء ، في حين أن إزالة أرطال المركبات متوسطة الوزن و PBUTs محدودة للغاية (معدل التخفيض<30–35%), due to the strong protein-bond of such compounds and the usual pores' cutoff of low-efflux (LF) membranes that avoid albumin loss and the consequent hypoalbuminemia [39,42]. Moreover, the increase in the number of HD sessions and/or the treatment time may improve small and middle molecule removal, but not for PBU molecules. Only the unbound portion of PBUTs could be efficiently removed by HD, due to their low molecular weight [39,43,44]. The reduction rate of PBUTs by conventional HD is listed in Table 1. Interestingly, most of the gut-derived uremic toxins including indoxyl sulfate (IS), p-cresyl sulfate (PCS), p-cresyl glucuronide (PCG), indol-3-acetic acid (IAA), and hippuric acid (HA), belong to the PBUTs group. On the other hand, the bacterial metabolite Trimethylamine-N-Oxide (TMAO) is grouped as small water-soluble molecules. The metabolic pathways of the most relevant uremic toxins together with their characteristics are summarized in Table 1. Briefly, phenol-derived PCS and PCG originate from tyrosine metabolism, while IS and IAA derive from tryptophanase-positive bacteria. Notably, tryptophan metabolism was also implicated in the kynurenine pathway [45].
الجدول 1. ملخص للسموم التي تنتجها الميكروبات ، والفئة ، والسلائف ، والممتلكات ، والتأثيرات السامة ذات الصلة.
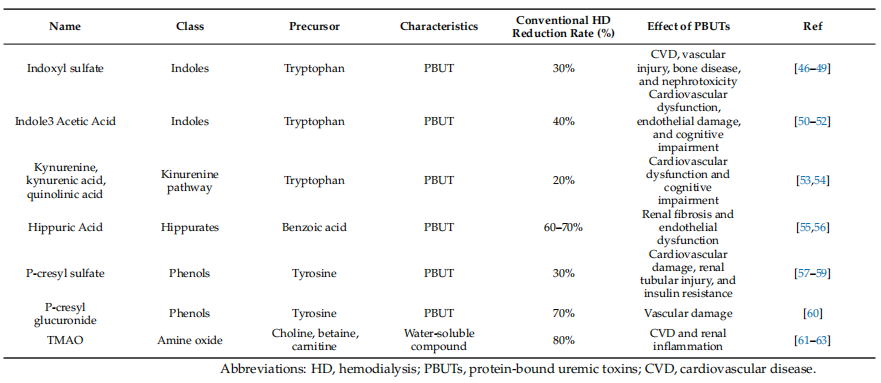
تم توثيق سمية PBUTs جيدًا في عدد كبير من الآليات الفيزيولوجية المرضية في أمراض الكلى ، مثل إصابة القلب والأوعية الدموية (CVI) ، والخلل الأيضي ، والتهاب [64،65].
في السنوات الماضية ، أكدت الدراسات المتزايدة دور PBUTs في ضعف القلب والأوعية الدموية وخلخلة الشعيرات الدموية. على سبيل المثال ، أثبتت التجارب في الجسم الحي وفي المختبر أن الإندولات والفينولات تلعب دورًا في تسرب الأوعية الدموية عن طريق تعزيز موت الخلايا المبرمج والتأثير على سلامة الوصلات الملتصقة في الخلايا البطانية [66،67]. بالإضافة إلى ذلك ، أشارت أدلة أكثر حداثة إلى أن زيادة الإجهاد التأكسدي يمثل أكثر العواقب ذات الصلة لتلف بطانة الأوعية الدموية في المرضى الذين يظهرون أعلى مستوى من السموم البوليسية [68]. على مستوى القلب ، تم تحديد السموم المتعلقة بالأمعاء لتحفيز نشوء أنواع الأكسجين التفاعلية (ROS) عن طريق تنظيم نشاط أوكسيداز NADPH (NOX) [69]. ارتبط هذا الاكتشاف ارتباطًا وثيقًا بتلف فجوة الوصلة في خلايا عضلة القلب مما أدى إلى ضعف عضلة القلب [70]. وفقًا للعديد من الدراسات في المختبر ، تعدل PBUTs شيخوخة الخلايا البطانية عن طريق تقليل تنظيم التعبير عن كلوثو مما يؤدي إلى تضخم الأوعية الدموية عبر الانتقال البطاني / اللحمة المتوسطة [71،72].

قد يكون تأثير العديد من السموم اليوريمية على ضعف الأوعية الدموية أيضًا بسبب قدرتها على تعديل التعبير المصب للعديد من miRNAs داخل الخلايا في الخلايا البطانية [73،74]. إجمالاً ، يسلط هذا الدليل الضوء على أن السموم البوليسية قد تمثل اللاعب المفقود بين تلف البطانة و CVI المرتبط بالبول. من ناحية أخرى ، تسببت PBUTs في عواقب ضارة على الالتهاب الجهازي. على سبيل المثال ، قام إيتو وزملاؤه بتقييم أن الإفراط في التعبير عن E-selectin تم توسطه بواسطة PCS عبر مسارات JNK / NF-kB ، مما أدى إلى تعزيز دوران الكريات البيض على الخلايا البطانية وتسرب الأعضاء [75]. في الآونة الأخيرة ، وجدت عدة مجموعات علاقة سبب-نتيجة بين المواد المذابة اليوريمية والتعبير عن بعض السيتوكينات المؤيدة للالتهابات [76]. على مستوى الكلى ، تم إثبات أن تراكم PBUTs يزيد من مستويات أنواع الأكسجين التفاعلية في الخلايا الظهارية الأنبوبية الكلوية (TEC) والخلايا ميسانجيل عن طريق تنظيم نشاط أكاسيد النيتروجين [77-80]. علاوة على ذلك ، فقد تبين أن تغيير العديد من المسارات الخلوية بما في ذلك AhRs و NF-kB و p53 ، استجابة للمستوى المرتفع من PBUTs ، كان مرتبطًا بالتليف الخلالي وتنشيط نظام الرينين-أنجيوتنسين (RAS) [49 ، 81 ، 82]. علاوة على ذلك ، يمثل تقليل تنظيم klotho السمة المميزة لـ AKI و CKD ويرتبط ارتباطًا وثيقًا بتقدم خلايا الكلى [83]. تشير البيانات المتزايدة إلى أن PBUTs متورطة في فرط ميثيل كلوثو من خلال التأثير على التعبير عن العديد من ناقلات الميثيل ، ربما عبر آلية تتوسط فيها NF-kB [84].
أخيرًا ، وجدت العديد من البيانات التجريبية علاقة قوية بين دسباقتريوزيس اليوريمي ومقاومة الأنسولين المرتبطة بمرض الكلى المزمن (IR) [85]. تم التعرف على الأشعة تحت الحمراء على أنها حالة سريرية مهمة تؤثر على المضاعفات الأيضية ، ضمور الدم ، وإصابات القلب والأوعية الدموية في سكان مرض الكلى المزمن. علاوة على ذلك ، فإن التغييرات في إشارات الأنسولين في CKD تتحول إلى حثل شحمي كلوي ، والذي يتميز بخلل وظيفي في الخلايا الشحمية [85]. وتجدر الإشارة إلى أن الخلايا الشحمية التي تم تحفيزها بدم من مرضى CKD ثبتت النمط الظاهري للأشعة تحت الحمراء التي تتميز بضعف امتصاص الجلوكوز [86]. بالإضافة إلى ذلك ، ستوكر بينتو وآخرون. أظهر أن عدم توازن ROS حدث عندما تم تحفيز الخلايا الشحمية بمحلول اليوريمي [87]. لتوضيح هذه الآلية ، Koppe وآخرون. أظهر أنه تم اكتشاف الأشعة تحت الحمراء مع إعادة توزيع دهون الجسم عندما عولجت الفئران السليمة بـ PCS [59]. إجمالاً ، تشير هذه البيانات إلى أن PBUTs يبدو أنها المفتاح المفقود في تفاقم المضاعفات الأيضية في بولينا الدم. ومن المثير للاهتمام ، أن بعض الوسطاء اليوريمي المتعلقين بتدهور وظائف الكلى يبدو أنهم مرتبطون ارتباطًا مباشرًا بالتدهور المعرفي. على سبيل المثال ، تم العثور على التراكم المرتفع للعديد من المواد المذابة الصغيرة القابلة للذوبان في الماء بما في ذلك حمض اليوريك ، ومركبات الغوانيدينو ، وثنائي ميثيلارجينين غير المتماثل (ADMA) ، ليكون متورطًا في السمية العصبية [88-90]. بالإضافة إلى ذلك ، أشارت العديد من الدراسات إلى أن المستويات المرتفعة من IS و PCS زادت من التهاب الأعصاب ، مما أدى إلى ضعف الإدراك لدى مرضى CKD [91،92]. علاوة على ذلك ، يمكن أن يسبب الإندول والكريسول ضعف BBB عن طريق تنشيط AhR ، مما يؤدي إلى التهاب وضغط الأكسدة [92]. تم ربط Homocysteine (Hcy) ، الذي يتم إنتاجه من خلال التحويل الأيضي المعوي للميثيونين إلى السيستين ، بتلف الخلايا العصبية في العديد من الأمراض العصبية. من المعروف أن المرضى الذين يعانون من مرض الكلى المزمن الذين يظهرون تركيزات عالية من البلازما Hcy يعانون من ضعف الإدراك والحركة [93]. تتضمن الآلية المقترحة التحفيز المفرط لمستقبلات N-methyl-D-aspartate (NMDAR) [94]. يمثل الالتهاب العصبي عاملاً ضارًا آخر في الضعف الإدراكي المرتبط بمرض الكلى المزمن لأن الوسطاء المؤيدين للالتهابات (IL -1 و IL -6 و TNF و TGF-) والخلايا المناعية تؤدي إلى تفاقم التدهور المعرفي لدى مرضى CKD [95] . يسمح اضطراب BBB أثناء الالتهاب بتفاعل السيتوكينات مع عامل التغذية العصبية (BDNF) في الجهاز العصبي المركزي (CNS). في الآونة الأخيرة ، وجد أن مسار kynurenine متورط بقوة في سياق اضطرابات الدماغ. يمكن تقويض العديد من المستقلبات النشطة عصبيًا من التربتوفان ، بما في ذلك kynurenine ، 3- hydroxykynurenine (3HKYN) ، حمض البيكولينيك ، وحمض الكينولينيك (QUIN) [96]. يمكن أن تؤدي حالة الالتهاب إلى زيادة تنظيم مسار الكينورينين ، مما يقلل من قدرة تخليق السيروتونين من التربتوفان. تؤدي المستويات المرتفعة من مادة HKYN المؤيدة للأكسدة 3- في الجهاز العصبي المركزي إلى زيادة موت الخلايا المبرمج للخلايا العصبية ، بسبب مشاركتها في تكوين أنواع الأكسجين التفاعلية (ROS) ، عن طريق توليد الأكسيد الفائق وتوليد H2O2 [97،98]. يتم إنتاج QUIN بواسطة الخلايا الدبقية الصغيرة ويتم اختراقها بواسطة الضامة [99]. يؤدي التوليف المفرط لـ QUIN إلى تكوين ROS عن طريق إثارة مستقبل NMDA [100،101]. هذا يزيد من بيروكسيد الدهون ، ومستويات أكسيد النيتريك ، وتحلل البروتين ، وزعزعة استقرار الهيكل الخلوي [101].
2.2. السموم اليوريميك في القصور الكلوي الحاد
مقارنةً بمرض الكلى المزمن ، كان الاهتمام بسموم اليوريم في القصور الكلوي الحاد في مهده في عام 2009 ، وكثيراً ما نوقش وجود الحديث المتبادل بين القناة الهضمية والكلية في القصور الكلوي الحاد. اليوم ، ثبت جيدًا من خلال مجموعة متنوعة من الدراسات على الحيوانات التجريبية والتجارب السريرية أن التلف الكلوي الحاد يؤثر سلبًا على تكوين الجراثيم [25]. الأهم من ذلك ، أن العلاقة بين AKI و microbiota ثنائية الاتجاه: فمن ناحية ، يمكن أن تسبب AKI dysbiosis. من ناحية أخرى ، فإن التحول الميكروبي يؤثر على شدة الإصابة الكلوية. لتأكيد هذه النظرية ، جانغ وآخرون. أظهر لأول مرة أنه بعد تحريض IRI ، أظهرت القوارض الخالية من الجراثيم أسوأ ضرر الكرياتينين والنسيج مقارنةً بعناصر التحكم [102]. بعد ذلك ، في سياق IRI الكلوي ، يمكن أن يغير نقص الأكسجة نفسه النسبة بين المجموعات الهوائية واللاهوائية [103]. في الآونة الأخيرة ، أندريانوفا وآخرون. أظهر من خلال دراسة في الجسم الحي أن التغيرات في تكوين الميكروبيوم حدثت بعد IRI [26]. تم تعزيز العلاقة بين السموم البوليسية وحدوث القصور الكلوي الحاد من خلال العديد من الدراسات [94]. الإندول والكريسول من السموم المعروفة ، وقد ارتبط مستوى تداولها بـ CVI وضعف معدلات البقاء على قيد الحياة في المرحلة النهائية من مرض الكلى [104105]. ومن المثير للاهتمام ، أن التركيز المتزايد لـ PBUTs في AKI مرتبط بالحدة ، وفقًا لمعايير RIFLE [106]. في قوارض AKI ، أدى استنفاد IS و PCS إلى تخفيف الضرر الكلوي [107]. كما تمت مناقشته سابقًا ، فإن تكوين ميكروبيوتا الأمعاء له أهمية محورية ، ليس فقط بالنسبة للسموم البوليسية ، حيث يمكن أن يؤثر أيضًا على الاستجابات المناعية. بالإضافة إلى ذلك ، أظهرت قوارض AKI الخالية من الجراثيم تنشيطًا أعلى للخلايا القاتلة الطبيعية وخلايا CD -8 الإضافية مقارنةً بالضوابط غير المعقمة. وبشكل أكثر تحديدًا ، أظهرت "المناعة العقيمة" الانتشار المفرط لسكان Th17. تؤثر اللمفاوية Th17 على ضعف الكلى عن طريق إطلاق الإنترلوكين -17 ، مما يؤدي إلى استجابة التهابية قوية في البيئة الكلوية [108]. علاوة على ذلك ، يمكن أيضًا إصابة حاجز القناة الهضمية أثناء التهاب المفاصل الروماتويدي مع زيادة تركيزات السموم البوليسية. بالإضافة إلى ذلك ، تحفز مستويات الذيفان الداخلي المنتشر تأثيرًا منهجيًا والتهابًا. ضد هذا السيناريو ، تم إجراء واحدة من أحدث الدراسات التدخلية التي تهدف إلى تعديل AKI بواسطة السموم البوليسية / تعديل الميكروبيوم بواسطة Dong et al. [109]. أظهر المؤلفون أن العلاج بالمضادات الحيوية كان قادرًا على تخفيف شدة التلف الكلوي الحاد.
في الختام ، في حين أن السموم اليوريمية يمكن أن تمثل العوامل الأساسية لـ AKI ، إلا أنه لا يوجد سوى كمية محدودة من البيانات المتاحة ، حيث أن غالبية النتائج مستمدة من نماذج الحيوانات التجريبية ، والتي لديها قيود شديدة. علاوة على ذلك ، على الرغم من التقدم في تقنيات غسيل الكلى ، فإن التشخيص السيئ لمرضى القصور الكلوي الحاد يمكن أن يكون مرتبطًا بالمركبات المرتبطة بالنباتات الدقيقة ، والتي تؤدي إلى اختلال وظيفي متعدد الأعضاء ، خاصة في الكلى ، حيث يؤدي تراكمها إلى زيادة الإصابة الأنبوبية والأوعية الدموية الموجودة مسبقًا مما يؤدي إلى تأخير الشفاء الكلوي. السموم اليوريمية هي العوامل المركزية في انهيار الأعضاء المتعددة وتؤثر سلبًا على الانتعاش الكلوي بعد الإصابة الحادة. وبالتالي ، فإن البحث عن خرطوشة العلاج الأمثل لاستبدال الكلى القادرة على إزالة السموم المحددة أو العلاجات الدوائية مع تأثير مستقلبات البكتيريا تتطلب بشدة مزيدًا من الاستكشاف.
2.3 السموم اليوريميك في زراعة الكلى
يمثل زرع الكلى أحد أكثر العلاجات فعالية للمرضى الذين يعانون من مرض الكلى في نهاية المرحلة لأنه يحسن بشكل كبير معدل البقاء على قيد الحياة ويحسن نوعية الحياة. علاوة على ذلك ، تبين أن تطبيق العلاجات المثبطة للمناعة يقلل من نوبات الرفض الحادة ويزيد من بقاء الأعضاء. من ناحية أخرى ، فإنه يؤدي إلى زيادة المضاعفات المتعلقة بانخفاض الكفاءة المناعية للمرضى الذين تم زرعهم ، مثل الالتهابات ، مع الحاجة اللاحقة للعلاج بمضادات الميكروبات.زراعة الكلىغالبًا ما ترتبط بمضاعفات معدية ، مما يزيد من معدل وفيات المتلقين. على مدى السنوات الماضية ، ثبت أن زرع الكلى يسبب اضطرابات في الفلورا المعوية التي يمكن أن تلعب دورًا رئيسيًا في العدوى المرتبطة بالزراعة [110]. علاوة على ذلك ، يمكن أن يؤثر دسباقتريوز الأمعاء على الجهاز المناعي للمتلقي ، وقد سلطت الأدلة الحديثة الضوء على وجود علاقة بين التغيرات في مجتمعات الجهاز الهضمي والنتائج السيئة لدى متلقي زراعة الكلى [111]. على الرغم من أنه لا يزال يتعين توضيح ما إذا كانت حالة دسباقتريوز القناة الهضمية مرتبطة ارتباطًا وثيقًازرع الكلىأو هو عنصر شائع لجميع المرضى الذين يعانون من مرض الكلى في نهاية المرحلة ، فقد تم الإبلاغ عن وجود اختلافات جوهرية تميز النمط الجرثومي للمتلقين مقارنة بالأشخاص الأصحاء [29،111]. على وجه الخصوص ، فقد ثبت أن التجمعات الميكروبية في القناة الهضمية لمتلقي زراعة الكلى تتميز بانتشار الثبات ، بينما تم الكشف عن زيادة في البكتيريا المتقلبة في غضون خمسة عشر يومًا بعد الزرع [29]. يمثل دسباقتح القناة الهضمية عامل خطر للأداء الأمثل للكسب غير المشروع الكلوي ويمكن أن يؤثر سلبًا على نتيجة زرع الكلى من خلال التغييرات في كل من الجهاز المناعي للمضيف وإنتاج السيتوكينات الالتهابية [111]. في الواقع ، يمكن أن يترافق دسباقتريوز الأمعاء مع ضعف سلامة الحاجز المعدي المعوي ، والذي يمكن أن يتسبب في إزاحة البكتيريا في الدورة الدموية الجهازية التي تؤدي إلى الاستجابة المؤيدة للالتهابات. يمكن أن تتسبب هذه الحالات في التهاب الكسب غير المشروع ، وفي النهاية ، رفض الكسب غير المشروع عن طريق الخلايا الليمفاوية ذاتية التفاعل والتفاعلية [111،112]. التمثيل الغذائي الميكروبي ضروري في إنتاج مواد مذابة للاحتفاظ اليوريمي ، مثل PBUTs. تم توثيق سمية PBUTs جيدًا في عدد كبير من الآليات الفيزيولوجية المرضية في أمراض الكلى [113-115]. ومع ذلك ، فإن تأثير زراعة الكلى على هذه السموم لم يتم استكشافه بالكامل حتى الآن. ليابوف وآخرون ذكرت أن كمية IS أقل بشكل ملحوظ في المتلقين الذين تم زرعهم بعد 12 شهرًا عنها في موضوعات CKD غير المزروعة ذات معدلات الترشيح الكبيبي المقدرة بالمثل [116]. بالإضافة إلى ذلك ، أدت زراعة الكلى إلى خفض مستويات الدم في كمية كبيرة من PBUTs ، بما في ذلك الفينولات ، وبدرجة أقل ، الإندولات [117]. تم أيضًا وصف العديد من المركبات اليوريمية الأخرى مثل HA و PHS و IAA و kynurenines ، على أنها انخفضت بشكل كبير في الأسبوع الأول بعد الزرع [118] ، على الرغم من أن تقليلها لا يبدو مرتبطًا بتحسين الوظائف الإدراكية العصبية. أظهرت هذه النتائج مجتمعة أن زرع الكلى يمكن أن يؤثر على مستويات السموم البوليسية حيث انخفض تراكمها إلى حد كبير بعد التطعيم الكلوي. وبالتالي ، يمكن التكهن بأن عملية الزرع نفسها قادرة على التأثير على تنوع الميكروبيوم ، والأمعاء المتسربة ، وبالتالي على امتصاص هذه السموم [117]. يمكن أن تعتمد هذه الحالة على كبت المناعة والعلاج الوقائي بمضادات الميكروبات مع ما يترتب على ذلك من تقليل و / أو تغيير في إنتاج PBUT.
قد يكون للمستقلبات المشتقة من الجراثيم تأثير سلبي على نتائج بقاء الكسب غير المشروع ووظيفته ، نظرًا لأن المستويات العالية من PCS و IS يمكن أن تتسبب في إنتاج الجزيئات المؤيدة للليفية والسيتوكينات الالتهابية من الخلايا الأنبوبية الكلوية ، مما يؤدي إلى زيادة التليف النُبيبي الخلالي ، والإصابة الخلوية ، والسمية الكلوية [58119]. Korytowska et al. أظهر في عام 2021 أنه يمكن استخدام IS اللعابي كعلامة تشخيصية غير جراحية من أجل التعرف على فقدان / تدهور وظيفة الكسب غير المشروع (DoGF) بعد أكثر من عام من زرع الكلى [120]. تم إجراء الدراسة على 92 متلقيًا لزراعة الكلى ، وعلى الرغم من أنها تمثل بعض القيود على النموذج المقترح ، فقد قيمت هذه الدراسة دور IS كمؤشر محتمل لـ DoGF وكعلامة مفيدة لمنع فشل الكسب غير المشروع ، وبالتالي توسيع نطاق البقاء على قيد الحياة وعمل الكلى المزروعة [120]. ومع ذلك ، في حالة بعض السموم البوليسية ، تم الإبلاغ عن نتائج مختلفة ومتناقضة ، فيما يتعلق بتلك الموصوفة سابقًا. على سبيل المثال ، تظل مستويات عامل نمو الأرومة الليفية التوكسين اليوريمي الجزيئي رقم 23 (FGF23) مرتفعة حتى بعد زرع الكلى [121] ؛ بدلاً من ذلك ، تزداد مستويات البلازما من جزيء ثنائي ميثيلارجينين غير المتماثل (ADMA) في البلازما مباشرة بعد زرع الكلى ، وتنخفض مستوياتها على مدار الأسابيع دون أن ينعكس ذلك في تحسين وظيفة الكسب غير المشروع الكلوي [122]. لا يزال فهم الآليات البيولوجية الكامنة وراء هذه النتائج جزئيًا ، ويرجع ذلك جزئيًا إلى العدد المحدود للدراسات التي أجريت حتى الآن حول هذا الموضوع. وبالتالي ، من الواضح أن هذه النتائج تسلط الضوء على الحاجة إلى مزيد من التحقيق في كيفية تأثير السموم اليوريمية على زراعة الكلى والعكس صحيح ، بهدف تنفيذ تدخلات علاجية محددة لتحسين نتائج عمليات زرع الكلى.
الخدمة الداعمة:
البريد الإلكتروني: wallence.suen@wecistanche.com
Whatsapp / Tel: plus 86 15292862950
محل:
https٪3a٪2f٪2fwww.xjcistanche.com٪2fcistanche-shop






